EVALUATION OF MELATONIN USE IN REVERSIBLE LIGATION OF THE LEFT ANTERIOR DESCENDING ARTERY IN RATS UNDER EXPERIMENTAL CONDITIONS
EVALUATION OF MELATONIN USE IN REVERSIBLE LIGATION OF THE LEFT ANTERIOR DESCENDING ARTERY IN RATS UNDER EXPERIMENTAL CONDITIONS
Abstract
In this work, we studied the effect of exogenous melatonin on a number of biochemical parameters and histopathological changes during reversible ligation of the left anterior descending artery (LADA) in rats. During LADA, LDH activity in plasma of animals in group 2 increased 2.5-fold (p < 0.001), whereas during melatonin application, LDH activity was suppressed (p < 0.001). Against the background of melatonin application in group 3, there was a statistically significant decrease in b-D-glucuronidase titres by 43.9% in comparison with group 2, (p < 0.05). It can be assumed that cardioprotective effects of melatonin in oxidative damage caused by ischaemia are probably associated with an increase in the amount of endogenous antioxidants.
1. Введение
Среди хронических заболеваний ишемическая болезнь сердца (ИБС) является наиболее частой причиной госпитализации в развитых странах. Наиболее оптимальной моделью воспроизведения ИБС у крыс является перевязка левой передней нисходящей артерии (ПЛПНА)
. Достоверно известно, что при ишемии, возникает дефицит подачи кислорода, блокируется митохондриальный синтез аденозинтрифосфата (АТФ), запускаются компенсаторные механизмы, ведущие к окислительному стрессу и апоптозу, и как итог ИБС . Мелатонин и его метаболиты – прямые поглотители свободных радикалов, в ходе данного исследования мы проверили гипотезу о том, что мелатонин, благодаря своим антиоксидантным эффектам, может оказывать терапевтическое действие при ИБС. Цель данной работы – изучить влияние экзогенного мелатонина на ряд биохимических показателей и гистопатологические изменения при перевязке левой передней нисходящей артерии у крыс в эксперименте.2. Методы и принципы исследования
Все манипуляции с животными проводились в соответствии с Руководством по содержанию и использованию лабораторных животных
. Эксперимент проводился на 45 животных (нелинейные белые крысы обоего пола массой 210-345 г.). Все животные находились в стандартных условиях вивария. Животным выполнен (наркоз), включающее интраперитонеальное введение (и/п) препаратов: «Ксилазин» (0,5 мл/кг массы тела) и «Золетил 100» (8мг/кг массы тела) . На аппаратном комплексе «BIOPAC» в соответствии со стандартными методиками производился мониторинг артериального давления (АД) и частоты сердечных сокращений (ЧСС), в соответствии со стандартными методиками . Животные были разделены на 3 группы: 1-ая группа (контроль 1) (n=15) ложнооперированные животные (n = 15): крысам, предварительно введено 0,9% раствор NaCl, 1 мл/кг, интраперитонеально (и/п) за 72 часа, 48 часов, 24 часа и 30 минут до операции. 2-ая - контроль 2 (n = 15): крысам предварительно введен 0,9% раствор NaCl, 1 мл/кг, за 72 часа, 48 часов, 24 часа и 30 минут до операции в течение 60 минут, затем под наркозом выполнена левосторонняя торакотомия, с обеспечением доступа к сердцу и последующей ПЛПНА по стандартной методике, на 30 минут с последующей реперфузией . 3-ья – операция+мелатонин (n = 15): крысам, предварительно вводился мелатонин (фармацевтическая субстанция, CAS Number: 73-31-4) и\п в дозе 10 мг/кг, за 72 часa, 48 часов, 24 часа и 30 минут до операции, затем под наркозом выполнена левосторонняя торакотомия, с обеспечением доступа к сердцу и последующей ПЛПНА, по стандартной методике на 30 минут с последующей реперфузией . Образцы крови были взяты из хвостовой вены по стандартной методике, через 60 минут после операции. Уровни лактатдегидрогеназы (ЛДГ), креатинкиназы (КФК), аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ), b-D-глюкуронидазы, b-галактозидазы, щелочной фосфатазы (ЩФ) в плазме измеряли с использованием стандартных диагностических наборов (анализатор BS-240). После вывода животных из эксперимента путем эвтаназии, проводилось гистопатологическое исследование сердечной ткани (предварительно ее фиксировали в 10% формальдегиде, обезвоживали в спиртовой серии, обрабатывали толуолом, готовили парафиновые срезы, которые окрашивали гематоксилином и эозином по стандартной методике), делали микрофотографии, отцифровывали их и оценивали изменения. Для статистической обработки был применен t-критерия Стьюдента и критерий Манна-Уитни. Результаты представлены следующим образом, М ± m (М – среднее, m – ошибка среднего). Данные принимались за статистически значимые при р<0,05.3. Результаты и их обсуждение
Статистически значимых различий между группами по уровню АД и ЧСС, зафиксированных в начале эксперимента, не отмечено. В группе №3, после операции уровень АД составил 104,69±1,18 мм.рт.ст., что статистически значимо ниже на 12,5% в сравнении с группой 1, (р <0,05); и на 16,95 % статистически значимо ниже в сравнении с группой 2, (р <0,05). При анализе ЧСС после операции, нами не отмечено, статистически значимых различий: так ЧСС составила в группе 1 – 388,5±9,34 уд/мин, в группе 2 - 403,5±8,59 уд/мин, в группе 3 – 399,5±5,31 уд/мин. Перевязка коронарных артерий не оказала никакого влияния на ЧСС, учитывая неизмененную частоту сердечных сокращений после перевязки коронарной артерии, можно предположить, что поддержание высокого сердечного ритма в раннем послеоперационном периоде, обусловленно компенсаторными механизмами, и адекватной сократительной функцией миокарда. На фоне ПЛПНА активность ЛДГ в плазме у животных в группе 2, увеличилась в 2,5 раза, что указывает на генерализованное повреждение тканей (р <0,001), тогда как при применении мелатонина, происходило подавление активности ЛДГ (р <0,001), (Таб. 1).
Таблица 1 - Биохимические показатели в исследуемых группах
| Группа 1. Ложнооперированные животные (n = 15). | Группа 2. Операция+ 0,9% раствор NaCl, 1 мл/кг (n = 15). | Группа 3. Операция+мелатонин и\п в дозе 10 мг/кг (n = 15). |
Показатель, ЕД/мл |
| ||
ЛДГ | 1366,43 ± 91,34 | 3344,65 ± 219,15* | 1965,85 ± 192,25 *# |
КФК | 1715,54 ± 146,4 | 2520,23 ± 169,31* | 1720,45 ± 193,23# |
АСТ | 62,16 ± 8,17 | 109,75 ± 9,1* | 76,15 ± 7,71*# |
АЛТ | 57,58 ± 5,47 | 117,7 ± 13,9 * | 70,13 ± 10,29*# |
b-D-глюкуронидаза | 0,35 ± 0,02 | 0,66 ± 0,05* | 0,37 ± 0,05# |
b-галактозидаза | 0,47 ± 0,02 | 0,79 ± 0,05* | 0,50 ± 0,05# |
ЩФ | 1,77 ± 0,08 | 2,57 ± 0,21* | 1,94 ± 0,12# |
Примечание: * – различия статистически значимы по отношению к группе 1 (контроль) (р < 0,05);
# – различия статистически значимы по отношению к группе 2 (р < 0,05)
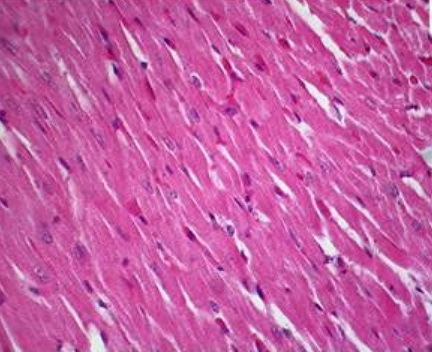
Рисунок 1 - Пример гистологических изменений в миокарде у крыс в экспериментальной группе 2
Примечание: Окраска гематоксилином и эозином. Ув. x400. Отек и миолиз кардиомиоцитов, потеря исчерченности, нечеткость границ мышечных волокон, ядра пикнотичные
4. Заключение
Результаты исследования показали, что введение мелатонина, оказывает кардиопротекцию при окислительном повреждении, вызванном ишемией, что может быть обусловлено увеличением количества эндогенных антиоксидантов и ингибированием ПОЛ за счет поддержания баланса оксидантно-антиоксидантного статуса. Можно предположить, что ПОЛ, как система, генерирующая свободные радикалы, тесно связана с ишемическииндуцированным повреждением тканей, и вполне целесообразным является изучение влияния экзогенного мелатонина на титры малонового диальдегида, супероксиддисмутазы, каталазa и пероксидазы, надеемся, что в следующих исследованиях мы сможем дать ответ на эти вопросы.
