BLOOD LEVELS IN RATS FOLLOWING CHRONIC INJECTION OF NEW PARTIALLY HYDROGENATED PYRIDINES DERIVED FROM α-CYANOTHIOCETAMIDE
BLOOD LEVELS IN RATS FOLLOWING CHRONIC INJECTION OF NEW PARTIALLY HYDROGENATED PYRIDINES DERIVED FROM α-CYANOTHIOCETAMIDE
Abstract
Blood is one of the most important markers of the general state of the body, which can be used to assess adaptive and pathological changes in the context of long-term exposure to various xenobiotics. An experimental study was conducted at the research laboratory of the St. Luke FSBEI HE LSMI of the Ministry of Health of Russia. The aim of the study was to perform a biochemical analysis of rat blood to determine the haematotoxicity of new experimental samples. The experiment was conducted on 120 mongrel laboratory animals — sexually mature male rats. The comparison drugs were metamizole sodium (7 mg/kg) and mefenamic acid (5 mg/kg). Biochemical analysis was performed using a Solar PM2111 analyser with the required reagents. The highest haemoglobin level was recorded in the group of rats receiving compound cv-099. The lowest result with suspected manifestations of leukopenia was recorded in the group receiving the comparison drug metamizole sodium — 4,99±0,41 x 109/L. This was followed by the result obtained in the group of animals receiving mefenamic acid — 6,71±0,41 x 109/L. The lowest platelet count was recorded in rats receiving metamizole sodium intragastrically — 568,13±4,12 x 109/L. In the other experimental groups, the results were stable and comparable to those in the control group. In terms of erythrocyte sedimentation rate (ESR), no relative deviations from the values of the intact and control groups were recorded during the laboratory study. During the experiment, the C-reactive protein indicator was also studied, and negative results were obtained in all experimental groups. During the experimental research on the hematotoxicity of new samples derived from α-CTA, it was established that compounds cv-091, cv-095, cv-099, and cv-142 do not affect the level of haemoglobin in the blood and do not cause pronounced manifestations of leukopenia or thrombocytopenia.
1. Введение
Потребление лекарственных препаратов пациентами имеет тенденцию к неуклонному росту. Согласно информации, изложенной в базе данных «Аудит розничных продаж лекарственных препаратов в России» аналитической компании RNC Pharma, каждый житель Российской Федерации в 2024 году приобрел 33,4 упаковки лекарств . Хроническое и бесконтрольное использование лекарственных препаратов — актуальная проблема современной фармакологии. Полипрагмазия, сочетанное применение препаратов, самолечение не проходят для организма человека бесследно. Каждый препарат обладает определенным спектром нежелательных фармакологических явлений (побочных эффектов) , , которые в той или иной степени проявляются, оказывая значительное действие на органы-мишени и могут варьироваться в зависимости от возраста пациента, пола, а также тяжести основных и сопутствующих заболеваний, острых состояний и хронических патологий .
В связи с этим актуальным является реализация научных исследований в области поиска новых эффективных и безопасных биологически активных компонентов. Особый интерес для исследователей представляет α-цианотиоацетамид и его производные, которые в схожих экспериментальных опытах показали себя как активные и относительно безопасные полифункциональные химические структуры , , , . В ходе данного исследования реализовано изучение влияния производных α-цианотиоацетамида на гемостаз и сердечно-сосудистую систему лабораторных крыс, основанном на биохимическом анализе крови. Кровь является одним из важнейших показателей общего состояния организма, по которому возможно оценить адаптационные и патологические изменения на фоне длительного воздействия различных ксенобиотиков, что имеет значимую роль в доклинических испытаниях новых лекарственных средств и позволяет определить ранние признаки токсического действия препаратов , , .
2. Методы и принципы исследования
Экспериментальные исследования проводились на базе научно-исследовательской лаборатории ФГБОУ ВО ЛГМУ им. Свт. Луки Минздрава России (Российская Федерация, Луганская народная республика, г. Луганск, кв. 50-летия Обороны Луганска, д. 1г). В качестве опытных животных использованы белые беспородные крысы-самцы, полученные из специализированного вивария учебного заведения. Животные на протяжении исследования содержались в соответствии с руководством ARRIVE, правилами работы с лабораторными животными на основе положений Хельсинской декларации и рекомендаций, содержащихся в Директиве ЕС 86/609ЕСС и Конвенции Совета Европы по защите позвоночных животных, используемых для экспериментальных и других научных целей, а также иных актов, соответствующих современным требованиям по реализации доклинических исследований на животных. Исследования одобрены комиссией по биоэтике ФГБОУ ВО ЛГМУ им. Свт. Луки Минздрава России (протокол заседания № 5 от 10.12.2022 г.).
Во время эксперимента опытные животные содержались на стандартном пищевом рационе с соблюдением питьевого режима и постоянным доступом к воде. На протяжении экспериментальной части работы все исследования реализовывались в соответствии с Федеральным законом «Об ответственном обращении с животными и о внесении изменений в отдельные законодательные акты Российской Федерации» от 27.12.2018 № 498-ФЗ; Федеральным законом «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ; ГОСТ 33216-2014 «Правила работы с лабораторными грызунами и кроликами» (принят Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 22 декабря 2014 г. № 73-П)), учитывающий положения Европейской конвенции о защите позвоночных животных, используемых в экспериментах и в других научных целях (European Convention for the protection of Vertebrate animals used for experimental and other scientific purposes (EST № 123)), а также в соответствии с иными соответствующими нормативно-правовыми актами.
До начала эксперимента все животные были тщательно осмотрены и отобраны согласно следующим критериям: масса тела, состояние кожного и шерстистого покрова, состояние слизистых, отсутствие видимой травматизации животного и нагноений кожных покровов, отсутствие повреждения зоны вибрисс, передних и задних конечностей, хвоста. Помимо вышеуказанного, оценивалась общая двигательная и поведенческая активность животного. Согласно данным критериям, для участия в экспериментальном исследовании отобрано 120 животных, которые распределены на 12 опытных групп рандомизированным методом «конвертов». Общий дизайн исследования сформирован в виде схемы (см. рис. 1).
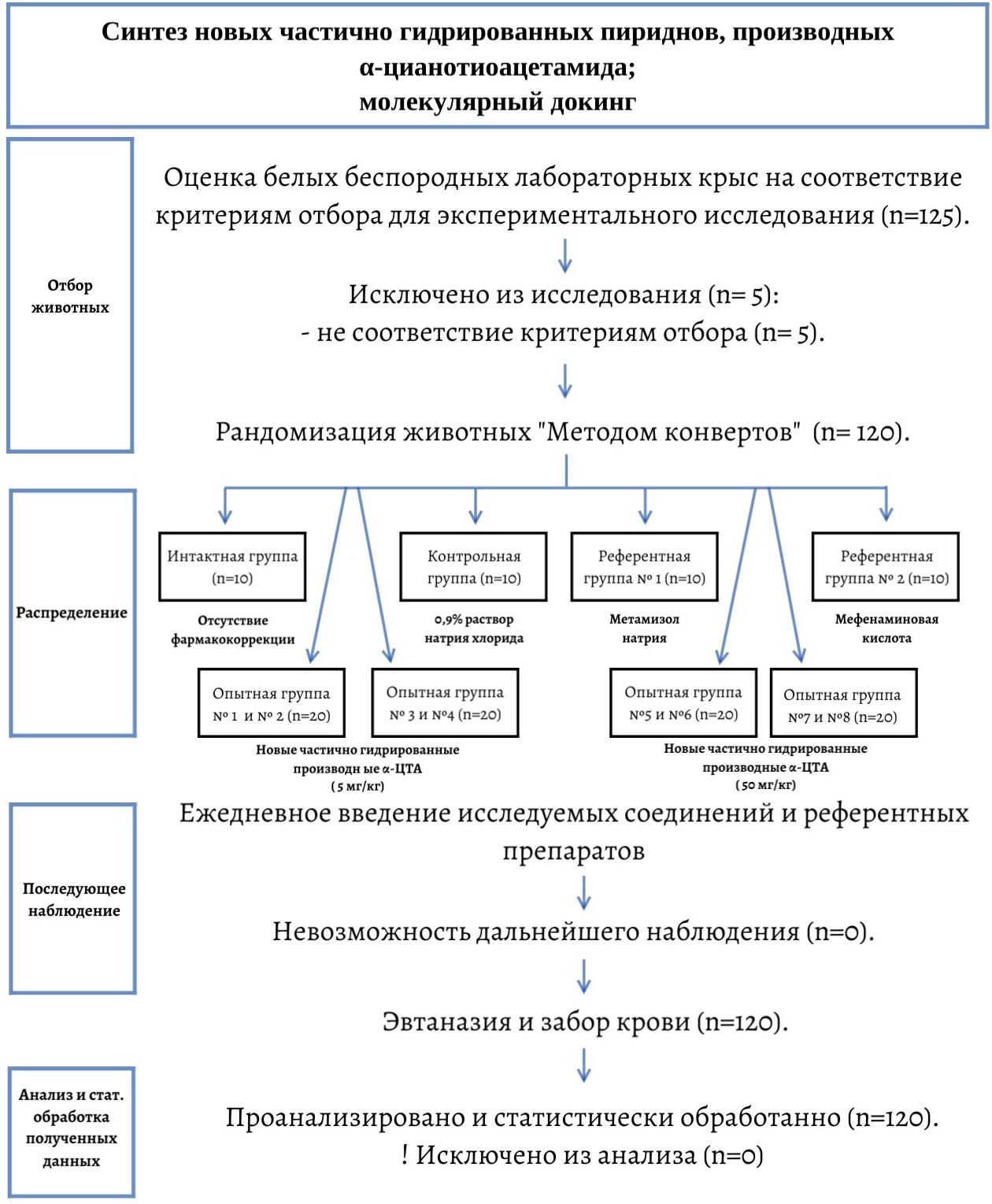
Рисунок 1 - Дизайн исследования хронической токсичности новых частично гидрированных пиридинов, производных α-ЦТА
Опытные образцы, частично гидрированные пиридины, производные α-цианотиоацетамида (см. рис. 2), синтезированы и предоставлены для исследований научно-исследовательской лабораторией «ХимЭкс» ФГБОУ ВО ЛГУ им. В. Даля, под руководством д.х.н., проф. С.Г. Кривоколыско.
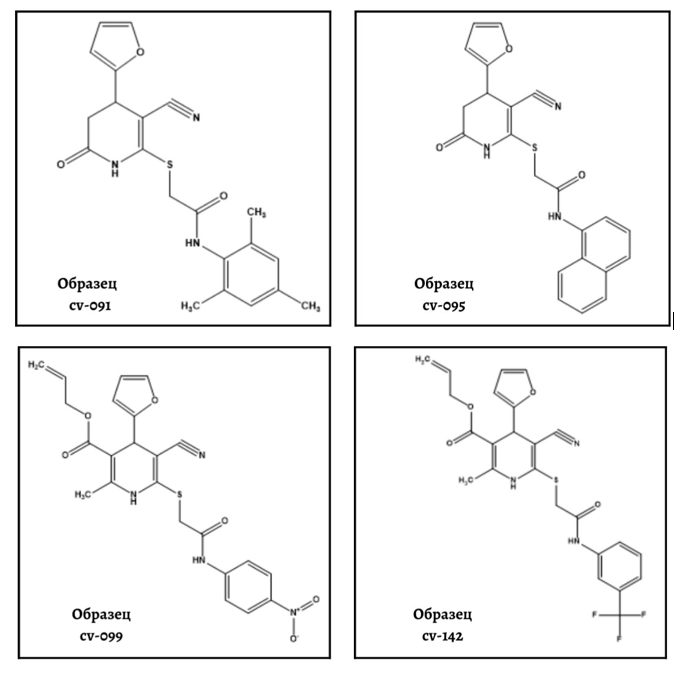
Химическая структура новых частично гидрированных пиридинов, производных α-ЦТА
В исследованиях по определению биологической активности производные α-цианотиоацетамида показали значимые результаты в опытах по исследованию анальгетической, противовоспалительной и жаропонижающей активности , , .
Фармакокоррекция осуществлялась в соответствующих условиях: группа сравнения № 1 получала метамизол натрия (производное пиразолона, неопиоидный анальгетик) в дозировке 7 мг/кг массы тела; группа сравнения № 2 получала мефенаминовую кислоту (фенамат, производное антраниловой кислоты) в дозировке 5 мг/кг; опытные группы № 1 (cv-091), № 2 (cv-095), № 3 (cv-099), № 4 (cv-142) получали образцы новых частично гидрированных пиридинов, производных α-ЦТА, в дозировке 5 мг/кг; опытные группы № 5 (cv-091), № 6 (cv-095), № 7 (cv-099), № 8 (cv-142) получали образцы новых частично гидрированных пиридинов, производных α-ЦТА, в дозировке 50 мг/кг.
Путь введения — внутригастральный, с помощью желудочного зонда. В интактной группе отсутствовала фармакокоррекция. В группе контроля животные на протяжении всего экспериментального исследования получали внутрижелудочно 0,9% раствор натрия хлорида. Растворителем во всех случаях являлась вода очищенная (aqua destillata).
Хроническое воздействие на организм животного смоделировано ежедневным введением препаратов на протяжении 14-ти календарных дней с принудительным голоданием в течение 16 часов до введения суспензии согласно методическим рекомендациям . На пятнадцатые сутки произведена эвтаназия животных с забором крови. Биохимический анализ реализован с помощью анализатора Solar PM2111 с использованием требуемых реактивов.
Статистическая обработка полученных результатов проведена с применением программ Microsoft Excel 2019, а также Statistica 10.0 для Windows. Ввиду ненормального характера распределения выборки беспородных лабораторных крыс, использован непараметрический метод обработки данных с помощью Т-критерия Уилкоксона и расчета коэффициентов вариации. Изменчивость ряда принято считать незначительной в случае, если коэффициент вариации менее 10% .
3. Основные результаты
Одним из ключевых показателей состояния кровеносной системы является гемоглобин (Hb) — железосодержащий белок, находящийся внутри эритроцитов. Согласно полученным результатам (см. табл. 1), можно сделать вывод о том, что наименьшие значения гемоглобина, согласно данным биохимического анализа, зафиксированы в референтной группе № 1, получавшей метамизол натрия.
Таблица 1 - Результаты биохимического анализа крови по показателю гемоглобин
Опытная группа | а, ед/л | Ме, ед/л | σ | σ2 | К, % | p |
Интактная | 134,88 ±0,95 | 135,0 | 2,70 | 7,27 | 2,0% | - |
Контрольная (0,9% NaCl) | 135,63 ±0,84 | 136,5 | 2,39 | 5,70 | 1,76% | *0,595 |
Референтная 1 (метамизол натрия) | 108,13 ±2,18 | 106,5 | 6,17 | 38,13 | 5,70% | **0,0009 |
Референтная 2 (мефенаминовая кислота) | 114,63 ±1,05 | 114,5 | 2,97 | 8,84 | 2,60% | **0,00089 |
cv-091 | 132,75 ±1,23 | 133,0 | 3,24 | 10,5 | 2,40% | **0,0788 |
cv-095 | 131,75 ±0,92 | 131,0 | 2,60 | 6,79 | 1,98% | **0,00733 |
cv-099 | 135,0 ±0,6 | 135,0 | 1,69 | 2,86 | 1,25% | **0,556 |
cv-142 | 132,88 ±1,30 | 132,0 | 3,68 | 13,55 | 2,77% | **0,062 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Стоит отметить, что относительно среднего показателя, полученного в интактной группе, который составил 134,88±0,95 г/л и в контрольной группе 135,63±0,84 г/л, в группе сравнения № 1 наблюдаются первичные признаки анемии. В группе сравнения № 2 результат также отличается от данных интактной и контрольной групп и составляет 114,63±1,05. Опытные группы показывают удовлетворяющий результат. Наивысший уровень гемоглобина зарегистрирован в группе, получавших соединение с шифром cv-099. Из всех опытных соединений наименьший результат по данному показателю у группы cv-142. В группах cv-095 и cv-091 данные стабильны, с минимальным разбросом относительно контрольной группы. В результате статистической обработки определено, что зафиксированные отклонения статистически значимы, различия достоверны.
Снижение уровня гемоглобина в крови крыс можно связать с потенциальным воздействием нестероидных противовоспалительных средств на желудочно-кишечный тракт, в частности, на слизистую оболочку кишечника, что влияет на всасываемость железа.
Хроническое потребление НПВС также зачастую сопряжено с воздействием на уровень лейкоцитов в крови. Снижение количества лейкоцитов приводит к ослаблению иммунной реакции организма и возрастанию риска развития инфекций в организме. В ходе исследования, в интактной группе был получен следующий показатель содержания лейкоцитов — 8,26±0,1 х 109/л, а в группе контроля — 8,26±0,098 х 109/л. Остальные группы в порядке возрастания имеют следующую тенденцию (см. табл. 2).
Таблица 2 - Концентрация лейкоцитов в периферической крови крыс, получавших новые производные α-ЦТА
Опытная группа | а, × 10⁹/л | Ме, × 10⁹/л | σ | σ2 | К, % | p |
Интактная | 8,26 ±0,100 | 8,25 | 0,28 | 0,08 | 3,42% | - |
Контрольная (0,9% NaCl) | 8,26 ±0,098 | 8,25 | 0,28 | 0,78 | 3,36% | *0,563 |
Референтная 1 (метамизол натрия) | 4,99 ±0,145 | 4,90 | 0,40 | 0,16 | 8,12% | **0,00046 |
Референтная 2 (мефенаминовая кислота) | 6,71 ±0,146 | 6,75 | 0,41 | 0,17 | 6,14% | **0,00047 |
cv-091 | 8,39 ±0,104 | 8,35 | 0,29 | 0,087 | 3,51% | **0,525 |
cv-095 | 8,50 ±0,146 | 8,50 | 0,34 | 0,17 | 4,87% | **0,246 |
cv-099 | 8,59 ±0,32 | 8,50 | 0,44 | 0,169 | 4,84% | **0,225 |
cv-142 | 7,96 ±0,131 | 7,95 | 0,37 | 0,137 | 4,65% | **0,161 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Наименьший результат с предполагаемыми проявлениями лейкопении зарегистрирован в группе, получавшей препарат сравнения метамизол натрия, и составляет 4,99±0,145 х 109/л. Затем следует результат, полученный в группе, получавшей мефенаминовую кислоту — 6,71±0,146 х 109/л. Среди новых образцов, производных α-ЦТА, умеренно стабильный результат относительно контрольной группы был получен в группах cv-091, cv-095, cv-099. В опытной группе cv-142 у животных зафиксирован результат, превышающий данные референтных групп, однако уступающий результатам группы контроля. В ходе исследования отсутствовала возможность исследования развернутой лейкоцитарной формулы, данные показатели требуют дальнейшего детального изучения.
Хроническое потребление ксенобиотиков может влиять на количество тромбоцитов в крови, воздействовать на функцию тромбоцитов, особенно в сочетании с иными факторами риска. В ходе исследования изучены показатели количества тромбоцитов в крови животных (см. табл. 3).
Таблица 3 - Концентрация тромбоцитов в периферической крови крыс, получавших новые производные α-ЦТА
Опытная группа | а, × 10⁹/л | Ме, × 10⁹/л | σ | σ2 | К, % | p |
Интактная | 620,63 ±2,51 | 621,5 | 7,09 | 50,27 | 1,14% | - |
Контрольная (0,9% NaCl) | 623,0 ±4,35 | 626,0 | 12,31 | 151,43 | 1,98% | *0,4420 |
Референтная 1 (метамизол натрия) | 568,13 ±1,46 | 569,5 | 4,12 | 16,9 | 0,73% | **0,00016 |
Референтная 2 (мефенаминовая кислота) | 581,75 ±1,36 | 580 | 3,85 | 14,79 | 0,66% | **0,00093 |
cv-091 | 613,75 ±1,78 | 612,5 | 5,04 | 25,36 | 0,82% | **0,0736 |
cv-095 | 620,0 ±3,78 | 618,5 | 3,78 | 14,29 | 0,61% | **0,2470 |
cv-099 | 614,75 ±1,50 | 614,0 | 4,23 | 17,90 | 0,69% | **0,0910 |
cv-142 | 612,63 ±5,18 | 619,0 | 14,65 | 214,55 | 2,39% | **0,0570 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Наименьшее количество тромбоцитов зафиксировано в группе животных, получавших внутрижелудочно метамизол натрия — 568,13±1,46 х 109/л. Однако стоит отметить, что в группе животных, получавших мефенаминовую кислоту, зафиксирован результат с относительно минимальным разбросом — 581,75±1,36 х 109/л, что может свидетельствовать о начальных проявлениях тромбоцитопении в данных группах. В остальных опытных группах результаты стабильны и сопоставимы с данными, полученными в контрольной группе.
По показателю скорости оседания эритроцитов (СОЭ), в ходе лабораторного исследования, не зафиксированы относительные отклонения от интактной и контрольной групп. Данные стабильны с минимальным разбросом (см. табл. 4).
Таблица 4 - Результаты биохимического анализа крови по показателю скорости оседания эритроцитов (СОЭ)
Опытная группа | а, мм/ч | Ме, мм/ч | σ | σ2 | К, % | p |
Интактная | 2,10 ±0,020 | 2,10 | 0,060 | 0,0030 | 2,73% | - |
Контрольная (0,9% NaCl) | 2,11 ±0,018 | 2,11 | 0,047 | 0,0022 | 2,24% | *0,816 |
Референтная 1 (метамизол натрия) | 1,97 ±0,027 | 1,97 | 0,078 | 0,0060 | 3,94% | **0,0062 |
Референтная 2 (мефенаминовая кислота) | 1,98 ±0,026 | 2,0 | 0,073 | 0,0053 | 3,66% | **0,0091 |
cv-091 | 2,11 ±0,040 | 2,11 | 0,038 | 0,0015 | 1,84% | **0,955 |
cv-095 | 2,13 ±0,030 | 2,14 | 0,038 | 0,0014 | 1,77% | **0,281 |
cv-099 | 2,08 ±0,030 | 2,08 | 0,033 | 0,0011 | 1,59% | **0,162 |
cv-142 | 2,11 ±0,020 | 2,11 | 0,023 | 0,0005 | 1,10% | **0,769 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Показатель СОЭ является относительным маркером воспалительных реакций, протекающих в организме животного, однако зависит от многих факторов и не имеет тенденции к неуклонному снижению.
В ходе эксперимента был также исследован показатель С-реактивного белка и во всех опытных группах получен отрицательный результат.
Биохимические показатели крови крыс, получавших внутрижелудочно новые соединения — частично гидрированные пиридины, производные α-цианотиоацетамида, в дозировке 50 мг/кг представлены в таблице 5.
Таблица 5 - Результаты биохимического анализа крови животных, получавших, производные α-ЦТА, в дозе 50 мг/кг
Опытная группа | Показатель гемоглобина, ед/л | Концентрация лейкоцитов, × 10⁹/л | Концентрация тромбоцитов, × 10⁹/л |
cv-091 | 133,63 ± 0,91 **p = 0,1970 | 8,43 ± 0,11 **р = 0,3620 | 613,75 ± 1,78 **p = 0,2340 |
cv-095 | 132,08 ± 0,74 **p = 0,1370 | 8,37 ± 0,20 **p = 0,4290 | 625,85 ± 2,64 **p = 0,1547 |
cv-099 | 133,20 ± 1,03 **p = 0,2350 | 8,46 ± 0,25 **p = 0,4680 | 617,88 ± 2,11 **p = 0,1880 |
cv-142 | 133,12 ± 0,72 **p = 0,2790 | 8,01 ± 0,17 **p = 0,1370 | 614,93 ± 4,07 **p = 0,1720 |
Примечание: **р – достоверно в отношении контрольной группы (при p≥0,05)
Показатель скорости оседания эритроцитов в группах, получавших опытные соединения в дозе 50 мг/кг стабилен и не имел значимых отклонений от данных, полученных в интактной и контрольной группе. Зафиксированные различия не имели статистической значимости.
Также стоит отметить, что введение десятикратной дозировки (50 мг/кг) синтезированных соединений не повлияло на поведенческую активность лабораторных животных, было зафиксировано нормальное состояние глаз и слизистых оболочек, их цвет оставался неизменным, рефлексы и реакции на болевые, световые, звуковые и тактильные раздражения в норме.
4. Заключение
В результате реализованного экспериментального исследования гематотоксичности новых частично гидрированных пиридинов, производных α-цианотиоацетамида, с лабораторными шифрами cv-091, cv-095, cv-099, cv-142 в дозировках 5 мг/кг и 50 мг/кг установлено, что опытные образцы не влияют на уровень гемоглобина в крови, не вызывают выраженных проявлений лейкопении и тромбоцитопении.
В ходе доклинических исследований фармакологической активности исследуемых образцов, установлена выраженная анальгетическая активность, противовоспалительные и жаропонижающие свойства, что делает данные образцы перспективными для дальнейших исследований их безопасности с увеличением числа экспериментальных животных.
