AN EVALUATION OF LIPOSOMAL PENTOXIFYLLINE APPLICATION IN CEREBRAL ISCHAEMIA IN RATS IN AN EXPERIMENT
AN EVALUATION OF LIPOSOMAL PENTOXIFYLLINE APPLICATION IN CEREBRAL ISCHAEMIA IN RATS IN AN EXPERIMENT
Abstract
The half-life of pentoxifylline after administration is 1.6 h, so prolonged release forms are of particular interest. The aim of this work is to evaluate whether liposomal pentoxifylline can exert neuroprotective effect in vivo in cerebral ischaemia. During middle cerebral artery occlusion, pathological EEG patterns appeared in animals in groups #2-4. An analysis of the results showed a smaller infarct area in animals in group 4 receiving i\n liposomal pentoxifylline compared with control 2. Although the exact mechanism by which pentoxifylline exerts its neuroprotective effects in vivo is unknown, effects from interaction with its adenosine receptor have been experimentally demonstrated in biological systems.
1. Введение
Пентоксифиллин – производное ксантина. Механизм его действия связан с ингибированием фосфодиэстеразы и накоплением циклического аденозинмонофоефата (цАМФ) в клетках, снижением концентрации внутриклеточного кальция. Пентоксифиллин обладает слабым положительным инотропным эффектом на сердце, улучшает микроциркуляцию в зонах нарушенного кровообращения. Период полувыведения пентоксифиллина после введения составляет 1,6 ч, поэтому особый интерес представляют пролонгированные формы с длительным высвобождением
, .Цель данной работы – оценить, может ли липосомальный пентоксифиллин оказывать нейропротекторное действие in vivo при церебральной ишемии.
2. Методы и принципы исследования
Все манипуляции с животными проводились в соответствии с Руководством по содержанию и использованию лабораторных животных
. Эксперимент проводился на 60 животных (нелинейные белые крысы обоего пола массой 220-335 г.). Все животные находились в стандартных условиях вивария. Животным выполнен (наркоз), включающее интраперитонеальное введение (и/п) препаратов: «Ксилазин» (0,5 мл/кг массы тела) и «Золетил 100» (8мг/кг массы тела) . На аппаратном комплексе «BIOPAC» в соответствии со стандартными методиками производился мониторинг ЭЭГ, ректальной температуры . Животные были разделены на 4 группы: 1-ая группа (контроль 1) (n=15) – ложнооперированные животные, оперативное пособие заключалось в обеспечении доступа к средней мозговой артерии (СМА), при этом окклюзия СМА не производилась. 2-ая группа (контроль 2) (n=15) – инсульт (окклюзия СМА); животным выполнялась 45-минутная окклюзия СМА по методике J. Koizumi , с последующей реперфузией. 3-ью группа (контроль 3) (n=15) – инсульт (окклюзия СМА); животным выполнялась 45-минутная окклюзия СМА по методике J. Koizumi, с последующей реперфузией+пентоксифиллин (ПТХ) и\п 10 (мг\кг) за 1 минуту до реперфузии; 4-ая группа (n=15) – инсульт (окклюзия СМА); животным выполнялась 45-минутная окклюзия СМА по методике J. Koizumi, с последующей реперфузией+ липосомальный пентоксифиллин и\п 10 мг\кг за 1 минуту до реперфузии. Липосомальные формы были получены из лецитина (500 мг) и холестерина (5 мг) методикой обращения фаз. Инкапсуляция пентоксифиллина выполнена пассивной загрузкой. Раствор пентоксифиллина 100 мг (5 мл) медленно вливали в мерную колбу объёмом 50 мл, добавляли трисаминометан 3,5 мл с последующим постепенным нагревом на ультразвуковой водяной бане до 40°С, затем вливали деионизированную воду до 50 мл, перемешивали в течение 45 минут. На следующем этапе лецитин (500 мг) и холестерин (5 мг) помещали в колбу, добавляли хлороформ. Хлороформ выпаривался, при центрифугировании и постепенном увеличении количества оборотов со 100 об/мин до 1700 об/мин. Проводилось высушивание, и образование липидной плёнки. После чего её гидратировали 5-ю мл раствора пентоксифиллина. Полученную дисперсию подвергали экструдированию, для фильтрации применяли диализный фильтр с диаметром пор 100 нм. Размер липосом был определен на наносайзере NANO-flex, с автоматическим подсчетом при помощи программного комплекса Microtrac Flex 11.0.0.2. Распределение, полученных липосом по диаметру (nm) получили следующее: 80,5 nm – 100%. На 3 сутки часть животных выводилась из эксперимента путем эвтаназии. Полученный биоматериал (головной мозг) фиксировали в 10% растворе формалина, осуществлялось иссечение биоматериала, заливка в парафин, приготовление срезов, с последующим окрашиванием гематоксилином и эозином по стандартной методике. На следующем этапе происходила оценка области инфаркта с подсчетом в % (оценка области инфаркта происходила после отцифровки микрофографий в программной среде Windows 10 c использованием стандартного графического редактора). Для статистической обработки был применен t-критерия Стьюдента и критерий Манна-Уитни. Результаты представлены следующим образом, М ± m (М – среднее, m – ошибка среднего). Данные принимались за статистически значимые при р<0,05.3. Результаты и их обсуждение
Во время окклюзии СМА у животных в группах №2-4 появлялись патологические ЭЭГ-паттерны (вспышка-подавление и паттерны распада). С момента окклюзии СМА у животных в группах № 2- 4 фиксировалось плавное угасание суммарной альфа и бетта –активности, с последующей дезорганизацией и исчезновением альфа-активности. Снижение суммарной амплитуды и полное угасание потенциалов регистрировалось в группах животных №2-4 на 17,4±4,65 секунде с момента окклюзии СМА, статистически значимые различия между данными группами не выявлены. В период реперфузии, отмечено возобновление биоэлектрической активности, начинающееся с восстановления альфа-активности и фокального восстановления тета-активности, и суммарным повышением амплитуды потенциалов. Наиболее обширный инфаркт головного мозга отмечен у животных в группе №2 – локализованный преимущественно в неокортексе, с коагуляционным некрозом, вовлекающим лобные и теменные области коры (рис.1).
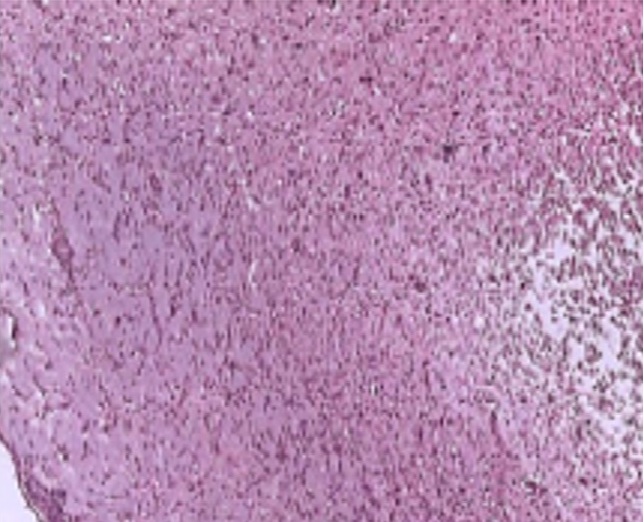
Рисунок 1 - Пример деструкции вещества мозга с диффузной лейкоцитарной инфильтрацией в области инфаркта головного мозга у крыс в контрольной группе
Примечание: группа №2; окр. гематоксилином и эозином, ув. х100
Хотя точный механизм, посредством которого пентоксифиллин оказывает нейропротекторное действие in vivo, неизвестен, в биологических системах экспериментально продемонстрированы эффекты, которые могут привести к защите от ишемического повреждения головного мозга, возможно, они связаны с механизмом его аденозинового рецептора, связанного с G-белком A2BAR (GPCR)
, . Прямое воздействие пентоксифиллина и его метаболитов на окислительно-восстановительные процессы, уменьшают NMDA-опосредованный приток кальция, in vivo это, вероятно, приводит к уменьшению размера инфаркта.Роль оксида азота в нейротоксичности, опосредованной рецептором NMDA, остается спорной
, . Если оксид азота действительно играет важную роль, пентоксифиллин и его метаболиты могут быть важны в его метаболизме , , учитывая эффективность, как нейтрализатора супероксида с образованием пероксинитрита. Токсичность пероксинитрита и эффективность ПТХ и его метаболитов в удалении супероксида, позволяет предположить, что ингибирование образования пероксинитрита может быть дополнительным механизмом нейропротекции. Экспериментально, острая ишемия, сопровождаемая реперфузией, связана с повышением и последующей депрессией восстановленного никотинамидадениндинуклеотида. Таким образом, окислительно-восстановительная активность ПТХ может приводить к удалению или образованию супероксида, и к взаимодействию в окислительно-восстановительных реакциях в зависимости от молекулярно-рецепторного окружения во время ишемии и реперфузии.4. Заключение
В данном исследовании мы оценили, может ли липосомальный пентоксифиллин оказывать нейропротекторное действие in vivo при церебральной ишемии. Во время окклюзии СМА у животных в группах №2-4 появлялись патологические ЭЭГ-паттерны (вспышка-подавление и паттерны распада). Поскольку краниальная и ректальная температура у животных, получавших липосомальный пентоксифиллин, не отличалась от групп № 1-3, маловероятно, что нейропротекторный эффект опосредован изменениями температуры во время ишемии. Таким образом, можно предположить, что и\п введение липосомального пентоксифиллина в дозе 10 мг\кг оказывает нейропротективное действие у выживших животных. Поскольку липосомальный пентоксифиллин оказался перспектиным соединением, весьма целесообразным является проведение дальнейших исследований, включающей оценку неврологического дефицита в отдаленной перспективе и выявление других вероятных эффектов данного соединения.
