QUANTITATIVE DETERMINATION OF THE TOTAL CONTENT OF HYDROXYCINNAMIC ACIDS IN BETONY GRASS
QUANTITATIVE DETERMINATION OF THE TOTAL CONTENT OF HYDROXYCINNAMIC ACIDS IN BETONY GRASS
Abstract
The object of the study was betony grass grown in the I.I. Sprygin Botanical Garden of Penza State University. The raw material was dried in the air without exposure to direct sunlight. Thin-layer chromatography (TLC) was used to identify hydroxycinnamic acids in betony grass. Direct spectrophotometry confirmed the presence of hydroxycinnamic acids in betony grass extracts and determined the analytical maxima of the studied compounds (330±2 nm). The optimal conditions for the extraction of phenylpropanoids from raw materials were established:
- extractant — 40% ethyl alcohol;
- raw material to extractant ratio — 1:200;
- extraction time — 30 minutes;
- degree of raw material grinding — 1.0 mm.
The aim of the research is to identify and quantitatively determine the sum of hydroxycinnamic acids in betony grass. A metrological evaluation of the method for determining the sum of hydroxycinnamic acids was carried out.
1. Введение
Высокий интерес к гидроксикоричным кислотам (ГКК) обусловлен их широким спектром фармакологической активности и низкой токсичностью , , что стимулирует поиск новых растительных источников этих ценных соединений. Буквица лекарственная (Betonica officinalis L.) представляет собой перспективный источник HCA, а также других биологически активных веществ.
Химический состав буквицы лекарственной достаточно разнообразен и включает эфирные масла (с преобладанием -мууролена, -кариофиллена, бензальдегида и фитола), флавоноиды (ориентин, лютеолин-7-глюкозид, апигенин-7-глюкозид, апигенин-3-глюкозид, апигенин, цинарозид), гидроксикоричные кислоты (хлорогеновая, феруловая, кофейная и розмариновая кислоты), жирные кислоты (линолевая и линоленовая), а также дубильные вещества и сапонины. Такое разнообразие состава обуславливает широкий спектр фармакологических свойств этого растения , .
Буквица лекарственная — это многолетнее травянистое растение, широко распространенное в Европе (за исключением северных и средиземноморских регионов), Западной Сибири, на Кавказе, в Северной Анатолии и северо-западной Африке, произрастающее на высоте до 450 метров над уровнем моря.
Для стандартизации лекарственного растительного сырья и успешного внедрения травы буквицы в медицинскую практику необходимо разработать воспроизводимые методики качественного и количественного анализа, выбрать оптимальные методы (например, cпектрофотометрию), оптимизировать условия экстракции и установить четкие показатели качества. Важным этапом является разработка соответствующей нормативной документации.
Одним из наиболее распространенных методов количественного определения ГКК является прямая спектрофотометрия, широко используемая как зарубежными, так и отечественными исследователями ,,, . В соответствии с требованиями Государственной фармакопеи XV издания, для идентификации ГКК рекомендована тонкослойная хроматография, а для количественного определения — спектрофотометрический метод .
В медицине буквица лекарственная используется благодаря ее вяжущим, противовоспалительным, противогеморрагическим, противоревматическим, цитотоксическим и противогрибковым свойствам. Показаниями к применению являются гастроинтестинальные расстройства, нервные заболевания, воспаления полости рта и горла, заболевания верхних дыхательных путей, кашель, мигрень и инфицированные раны , . Однако в настоящий момент не разработана нормативная документация и данное сырье не включено в государственную фармакопею.
2. Методы и принципы исследования
Для подтверждения присутствия гидроксикоричных кислот в траве буквицы использовали тонкослойную хроматографию (ТСХ)
, . Методика идентификации гидроксикоричных кислот методом ТСХ: подготовка пластинки (хроматографическая пластинка активируется в сушильном шкафу при температуре 100–105°С, наносится линия старта и происходит нанесение проб). На линию старта наносится 0,02 мкл водно-спиртового извлечения из травы буквицы и параллельно наносятся стандартные образцы: лютеолин-7-глюкозид, кофейная кислота, хлорогеновая кислота, рутин, гиперозид, кверцетин. Условия хроматографирования: система растворителей: хлороформ — этиловый спирт 70% — вода (26:16:3), тип хроматографирования: восходящий, пластинка: «Сорбфил-ПТСХ-АФ-Ф-УФ», камера предварительно насыщается парами растворителей в течение 24 часов, процесс продолжается до прохождения фронта растворителя на 8 см. Принципы детектирования: визуальный осмотр при дневном свете, просмотр в УФ-свете при λ=366 нм, просмотр в УФ-свете при λ=254 нм, обработка щелочным раствором ДСК, обработка фосфорно-молибденовой кислотой. Данная методика позволяет достоверно идентифицировать наличие гидроксикоричных кислот в исследуемом сырье благодаря использованию стандартных образцов и многоступенчатому процессу детектирования , , .Разработанный способ предназначен для эффективного извлечения и количественного определения содержания гидроксикоричных кислот (ГКК) в траве Betonica officinalis с целью оценки качества лекарственного растительного сырья. Метод базируется на разовой экстракции ГКК этанолом различной концентрации (95%, 70% и 40%) с последующей термообработкой на кипящей водяной бане в течение получаса. Количественный анализ осуществляют спектрофотометрическим методом на спектрофотометре СФ-102, фиксируя оптическую плотность спиртового извлечения при длине волны 330 нм. Точную массу (1,0 г) размельченного растительного материала помещают в колбу вместимостью 250 мл с притертой пробкой. К подготовленному сырью прибавляют 200 мл выбранного растворителя - этанола необходимой концентрации. После охлаждения полученный экстракт процеживают через бумажный фильтр, предварительно увлажненный тем же спиртом. Первые 10 мл отфильтрованного раствора не используют (полученный раствор именуют как раствор А). В мерную колбу объемом 50 мл вносят 1,0 мл раствора А и доводят объем до необходимой отметки тем же растворителем (полученный раствор определяется как раствор Б). В роли раствора сравнения выступает чистый этанол соответствующей концентрации. Количество суммарных гидроксикоричных кислот рассчитывали, используя формулу (1):
где, D — оптическая плотность испытуемого раствора;
m — масса сырья, г;
W — потеря в массе при высушивании сырья (влажность), %;
497 — удельный показатель поглощения хлорогеновой кислоты при 330 нм.
3. Основные результаты и обсуждение
Результаты хроматографического анализа показали следующие данные: оранжевое пятно с Rf = 0,53 (совпадает с СО хлорогеновой кислотой), желтое пятно с Rf = 0,62 (совпадает с СО лютеолин-7-глюкозидом). Рекомендации по проведению качественного анализа: использовать хлорогеновую кислоту в качестве вещества-стандарта и производить расчет значений Rf для подтверждения идентичности компонентов. Методологические особенности: сравнение Rf исследуемых веществ с Rf стандартных образцов позволяет достоверно идентифицировать компоненты. Наличие характерных цветов пятен (оранжевый и желтый) дополнительно подтверждает идентификацию. Такой подход к анализу позволяет: достоверно идентифицировать присутствующие компоненты, подтвердить качество исследуемого сырья, обеспечить воспроизводимость результатов анализа. Использование хлорогеновой кислоты как стандартного образца особенно рационально, так как она является одним из основных компонентов в исследуемом материале и имеет характерные показатели Rf и цвет пятна.
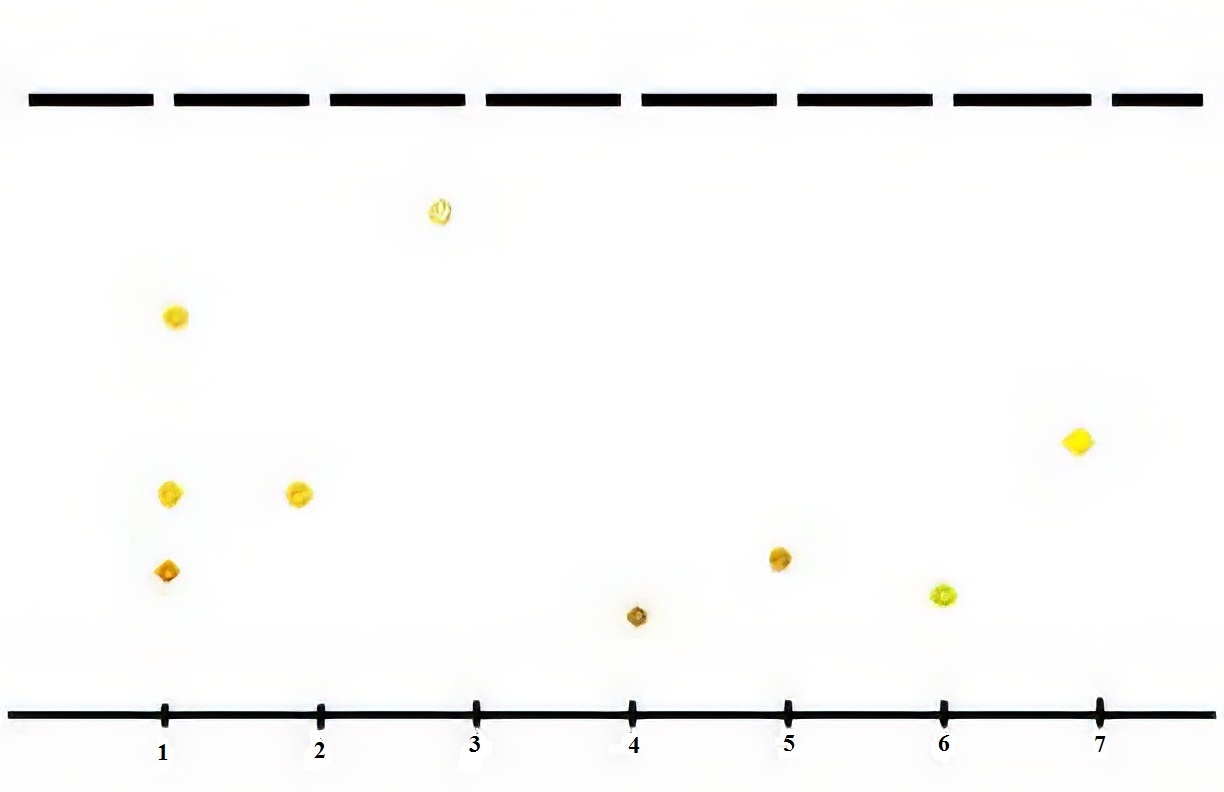
Рисунок 1 - Схема хроматограммы извлечения из травы буквицы

Рисунок 2 - Электронный спектр стандартного образца хлорогеновой кислоты (2) и извлечения из надземной части Betonica officinalis (1)
Таблица 1 - Зависимость выхода гидроксикоричных кислот травы буквицы от концентрации экстрагента
Концентрация экстрагента | Содержание суммы гидроксикоричных кислот в пересчете на абсолютно сухое сырье и хлорогеновую кислоту, % |
Этанол 20% | 1,62±0,11 |
Этанол 40% | 3,31±0,08 |
Этанол 70% | 3,08±0,09 |
Этанол 95% | 2,02±0,08 |
Таблица 2 - Зависимость выхода гидроксикоричных кислот от времени извлечения на кипящей водяной бане
Время настаивания на кипящей водяной бане, мин | Содержание суммы гидроксикоричных кислот в пересчете на абсолютно сухое сырье и хлорогеновую кислоту, % |
15 | 3,11±0,12 |
30 | 3,48±0,09 |
60 | 3,22±0,07 |
90 | 3,11±0,08 |
Таблица 3 - Зависимость выхода гидроксикоричных кислот от соотношения «сырье-экстрагент»
Соотношение «сырье-экстрагент» | Содержание суммы гидроксикоричных кислот в пересчете на абсолютно сухое сырье и хлорогеновую кислоту, % |
1:100 | 3,20±0,06 |
1:200 | 3,48±0,09 |
1:300 | 3,29±0,07 |
Размер частиц 1 мм обеспечивает оптимальную поверхность контакта сырья с экстрагентом, 40% этиловый спирт является оптимальным растворителем для извлечения гидроксикоричных кислот, соотношение 1:200 гарантирует достаточное количество экстрагента для максимального извлечения, 30-минутная экстракция обеспечивает полное извлечение компонентов при температуре 90°C, данная температура ускоряет процесс экстракции без разрушения термолабильных компонентов. Необходимо тщательно измельчать сырье до однородного состояния и соблюдать точное соотношение сырья и экстрагента, контролировать температуру водяной бани, обеспечивать равномерное перемешивание. Данная методика позволяет получить максимально полное извлечение гидроксикоричных кислотиз травы буквицы при сохранении их качественных характеристик. Она может быть рекомендована для анализа и контроля качества растительного сырья.
Выбор сделан в пользу одностадийного процесса экстракции, так как происходит минимизация ошибок при пробоподготовке, сокращение времени анализа, простота выполнения процедуры, уменьшение потерь аналитика, повышение воспроизводимости результатов.
Выявлено, что содержание гидроксикоричных кислот, при использовании в качестве экстрагента этанола 40% составляет 3,46%.
Проведена метрологическая оценка методики определения суммы гидроксикоричных кислот
. В результате пяти параллельных определений (Хср= 3,48) установлена дисперсия (S2 = 0,005), стандартное отклонение (S = 0,074), стандартное отклонение среднего результата (SXср = 0,033), относительное стандартное отклонение среднего результата (RSD = 2,13%), полуширина доверительного интервала (ΔХср = 0,092). Погрешность среднего результата (ε, %) суммы гидроксикоричных кислот с доверительной вероятностью (Р,%) 95% в сырье буквицы лекарственной составила ±2,74 %, в пересчете на хлорогеновую кислоту.4. Заключение
В результате исследования подтверждено наличие хлорогеновой кислоты методом тонкослойной хроматографии (ТСХ). В рамках исследования разработана и валидирована методика количественного определения суммы ГКК в растительном сырье, основанная на принципе прямой спектрофотометрии при длине волны 330 нм. Количественный анализ проводился с использованием хлорогеновой кислоты в качестве стандарта. Для достижения максимального выхода ГКК были оптимизированы параметры экстракции:
- размер частиц сырья: 1 мм;
- экстрагирующий агент: 40% водный раствор этанола;
- соотношение «сырье/экстрагент»: 1:200 (г/мл);
- продолжительность экстракции: 30 минут;
- температура экстракции: кипящая водяная баня.
Применение разработанной методики к исследованному образцу позволило установить содержание ГКК на уровне 3,46% в пересчете на хлорогеновую кислоту. Полученные результаты свидетельствуют о пригодности разработанной методики для рутинного количественного определения содержания ГКК в растительных материалах. Методика может быть рекомендована для использования при разработке фармакопейных статей и другой нормативной документации, направленной на стандартизацию новых видов лекарственного растительного сырья, содержащего гидроксикоричные кислоты, поскольку обеспечивает надежное и воспроизводимое определение.
