SYNTHESIS, INVESTIGATION OF THE STRUCTURE AND PROPERTIES OF COMPLEX COMPOUNDS OF HYDROXYL AMINO ACIDS WITH COPPER IONS
СИНТЕЗ, ИССЛЕДОВАНИЕ СТРОЕНИЯ И СВОЙСТВ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ ГИДРОКСИАМИНОКИСЛОТ С ИОНАМИ МЕДИ
Научная статья
ORCID: 0000-0003-0615-8928,
Забайкальский государственный университет, Чита, Россия
* Корреспондирующий автор (kns2702[at]yandex.ru)
АннотацияСинтезированы новые комплексные соединения на основе ионов меди и протеиногенных аминокислот L-серина и L-треонина. Реакции проводились при нагревании в растворах с последующим промыванием и высушиванием выпавших осадков солей. Состав и строение полученных соединений изучены методами ИК-спектроскопии, рН-потенциометрии, титриметрии, спектрофотометрии. Показано, что образуются комплексы в мольном соотношении металл-лиганд 1 : 2. Подтверждена бидентатная координация меди аминокислотами и N,O-хелатирование за счет донорно-акцепторных связей карбоксильной и аминогруппы. В ИК-спектрах регистрируются полосы поглощения, характерные для связей Cu-N, Cu-O и смещение максимумов функциональных групп аминокислот. Рассчитаны константы нестойкости треонината и серината меди.
Ключевые слова: треонин, серин, медь, комплексное соединение, инфракрасная спектроскопия, потенциометрия, спектрофотометрия.
SYNTHESIS, INVESTIGATION OF THE STRUCTURE AND PROPERTIES OF COMPLEX COMPOUNDS OF HYDROXYL AMINO ACIDS WITH COPPER IONS
Research article
Kuznetsova N.S.*
ORCID: 0000-0003-0615-8928,
Transbaikal State University, Chita, Russia
* Corresponding author (kns2702[at]yandex.ru)
AbstractThe research synthesizes new complex compounds based on copper ions and proteinogenic amino acids L-serine and L-threonine. The reactions were carried out by heating in solutions followed by washing and drying of the precipitated salts. The composition and structure of the obtained compounds were studied by IR spectroscopy, pH potentiometry, titrimetry, and spectrophotometry. The study shows that complexes are formed in a molar metal-ligand ratio of 1 : 2. The authors confirm bidentate coordination of copper by amino acids and N,O-chelation due to donor-acceptor bonds of the carboxyl and amino groups. The absorption bands characteristic of Cu-N, Cu-O bonds, and the displacement of the maxima of functional groups of amino acids are recorded in the IR spectra. The instability constants of threoninate and copper serinate are calculated.
Keywords: threonine, serine, copper, complex compound, infrared spectroscopy, potentiometry, spectrophotometry.
Введение
Интерес к координационным соединениям металлов связан с их высокой биологической активностью, в то время как неорганические металлосодержащие вещества токсичны для живых организмов [5], [6], [7]. В биохимии и фармакологии в целях снижения негативного действия и повышения биодоступности используется перевод ионов металлов в комплексные соединения. В координационной химии нативные аминокислоты являются актуальными лигандами, благодаря наличию карбоксильной и аминогрупп, дополнительных функциональных, электронодонорных заместителей в радикале, способных к комплексообразованию, хелатированию с металлами [2], [5], [8].
На простых моделях взаимодействия металл – аминокислота можно изучать белковые, ферментные, рецепторные, регуляторные механизмы в клетках, понимание которых далеко не ясно в настоящее время [4], [7], [8]. Не создана и единая теория взаимодействия минерального и органического компонентов биомолекул, что может быть достигнуто только путем систематических исследований и накопления экспериментальных данных. Полученные результаты помогут в понимании фундаментальных биохимических закономерностей, послужат теоретической базой при направленном синтезе новых фармакологических препаратов для таргетной терапии.
Целью данной работы было получение и исследование комплексных соединений меди с гидроксиаминокислотами.
Материалы и методы
В качестве исходных использовались реактивы марки «х.ч.»: L-аминокислоты (серин, треонин), производитель ООО «Панэко» (Россия) и оксид меди (II). Комплексы получали в водном растворе при температуре 70-80 °C путем смешивания взятых с точностью до 0,0001 г навесок прекурсоров лиганд : металл (L : М) в мольных соотношениях 2 : 1 в слабощелочной среде [5], [6]. Перемешивали содержимое 30 минут на магнитной мешалке и оставляли при комнатной температуре до кристаллизации. Выпавшие в виде синего осадка продукты реакции фильтровали, промывали дистиллированной водой, спиртом, высушивали при н.у.
Исследование строения хелатов, таблетированных с KBr, проведено методом инфракрасной спектроскопии на ИК-Фурье спектрометре FTIR-8400S «Shimadzu» (в области 400-4000 см-1). Интерпретацию спектров проводили по литературным данным [1], [3], [6], [9].
Процессы комплексообразования были изучены методом рН-потенциометрического титрования (pH-метр Mettler Toledo FEP20 - FiveEasy Plus), основанного на регистрации изменения равновесного потенциала электрода в процессе химической реакции между потенциалопределяющим ионом в растворе и специально введенным реактивом (0,1 М NaOH) в качестве титранта [1], [10].
Количественный состав комплексов аминокислот с ионами меди (II) был исследован классическим методом изомолярных смесей (метод разбавления Остромысленского-Жоба) на спектрофотометре СФ-2000 в кварцевых кюветах l=1 см при λ=740 нм. Определение содержания меди (II) в полученных соединениях проводили с помощью комплексонометрического титрования. Содержание аминокислот определяли формольным титрованием по методу Серенсена [1].
Результаты и их обсуждениеПрактический выход синтеза составил 83,3% треонината меди и 85,6% серината меди, что несколько ниже, чем в данных литературы, где эти значения для других протеиногенных аминокислот составляют до 97 % [5].
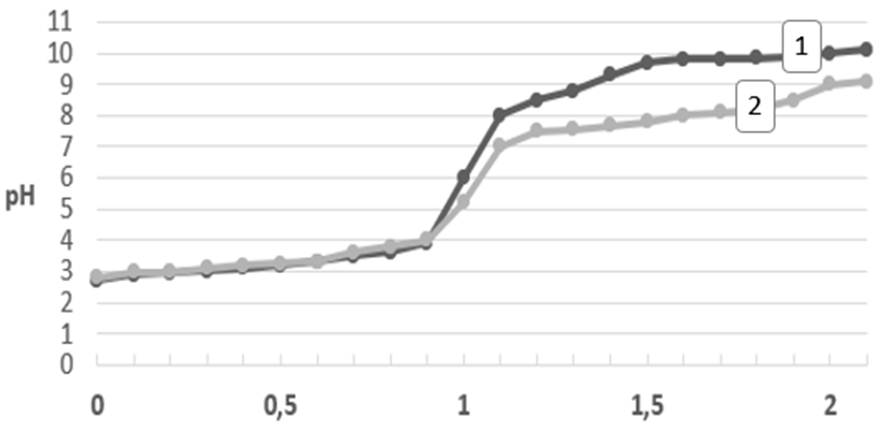
Исследование комплексообразования Cu (II) c аминокислотами методом потенциометрического титрования показало, в водных растворах возможно образование соединений состава 1 : 2. На рисунке 1 приведены кривые титрования серина и системы «серин-медь» в координатах рН = f(a), где а – степень оттитрованности раствора. Диаграмма треонина и треонината меди была сходной. В работе [10], где применялся этот же метод для исследования соединений цинка, зафиксированы аналогичные кривые, характеризующие образование комплексов с глицином, валином, аланином, серином, аспарагиновой кислотой мольного состава 1:1 и 1:2.
Рис. 1 – Интегральная pH-кривая потенциометрического титрования серина и его смеси с ионами меди:
1 – серин; 2 – серин : Cu2+ = 2 : 1
Рассчитанные по классическим формулам константы нестойкости (К) солей составили: K=1,85×10-4 для Cu(Tre)2) и K=1,83×10-5 у Cu(Ser)2. Их значения свидетельствуют о достаточной устойчивости соединений, что может быть связано с проявлением хелатного эффекта [2], [4], [10].
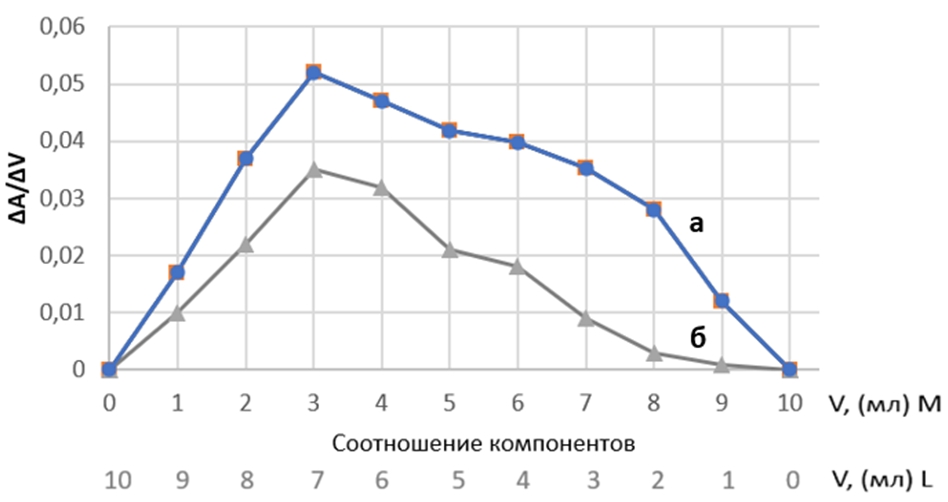
Результаты спектрофотометрического определения состава синтезированных соединений представлены в виде дифференциальной изомолярной кривой зависимости «ΔA/ΔV – состав комплекса» (рисунок 2).
Рис. 2 – Зависимость оптической плотности (А) от соотношения компонентов водных растворов Cu2+ (М) с аминокислотами (L): а) серин; б) треонин
На рисунке 2 видно, что максимум кривой лежит в области мольных отношений 3 : 7, что соответствует составу комплекса «металл : аминокислота» примерно 1 : 2,3. Наличие на графике одного резко выраженного максимума свидетельствует об образовании в системе устойчивого комплекса.
Результаты титриметрического определения содержания меди и аминокислот позволили рассчитать молярные соотношения серина и треонина относительно концентрации металла в образовавшихся комплексах. Так, пропорция Cu2+ (M) : аминокислота (L) для серината меди составила 0,1752 : 0,3640 = 1 : 2,1; для треонината меди соответственно: 0,1811 : 0,3919 = 1 : 2,2. Это подтверждает состав продуктов синтеза Cu(Ser)2 и Cu(Tre)2. В работе [3] подобное взаимодействие показано на примере хлорида индия с аминокислотами аланином и фенилаланином.
Способ координации определяли по данным ИК-спектрального анализа синтезированных соединений. ИК-спектры серината и треонината меди достаточно характерны для интерпретации их как спектров координационных соединений меди (II) с аминокислотами (таблица 1). В ИК-спектре аминокислот наблюдаются характерные полосы поглощения карбоксильной и аминогрупп [2], [3], [7], [9]. В полученных комплексах зафиксированы изменения интенсивности и смещение максимумов характеристических полос функциональных групп.
При сопоставлении спектров исходных аминокислот и их комплексов с медью (II) значимыми отличиями являются появление интенсивных полос в области 3000 – 3200 см-1 (колебания протонированной аминогруппы), что можно объяснить возникновением новой связи Cu-N по донорно-акцепторному механизму. В спектрах солей виден сдвиг полос, соответствующих валентным колебаниям карбоксилат-иона относительно спектров серина и треонина [2], [6], [9], что позволяет интерпретировать факты образованием связи Cu-O. N,O-координацию подтверждает появление полос в диапазоне 538-572, 605-616 см-1 ν(Ме-N), 434-455 см-1 ν(Me-O) [2], [3], [7], [9].
Таблица 1 – Волновые числа максимумов характеристических полос поглощения (см-1) в ИК-спектрах исходных аминокислот (серина и треонина) и их комплексах с Cu2+
| Соединение | ν(COO-) | ν(NH3+) | Ме-N | Ме-О | ||||
| as | s | δ | as | s | δ | |||
| Серин | 1594 | 1407 | 612 | 3070 | 3170 | 2040 1622 1480 | ||
| Треонин | 1628 | 1418 | 635 | 3052 | 3206 | 1595 | ||
| Серинат меди | 1615 | 1391 | 3291 | 3022 | 1579 1624 | 572 605 1116 | 434 | |
| Треонинат меди | 1621 | 1385 | 3200 | 3101 | 1565 | 538 616 1080 | 455 | |
Кроме того, в спектрах присутствовали характерные полосы поглощения углеводородных групп, которые заметно не меняли своей интенсивности при хелатировании: С-Н валентные колебания (as, s) 2982, 2979, 2911, 2843 см-1, деформационные при 1444, 1382, 1355 см-1; С-С валентные при 933, 830 см-1 [2], [3], [7], [9].
На основе анализа данных спектров комплексов Cu (II), учитывая литературные данные, можно предположить, что L-аминокислоты в Cu(Ser)2, Cu(Tre)2, являются бидентатными лигандами, которые взаимодействуют с Cu2+ за счет СООН- и NH2-групп [2], [5], [7], [9].
ЗаключениеБыли синтезированы два координационных соединения протеиногенных аминокислот L-серина и L-треонина с ионами меди (II) в растворе. Состав полученных солей изучен химическими и инструментальными методами (потенциометрия, спектрофотометрия, ИК-спектроскопия, титриметрия). Проведенный анализ позволяет предположить образование комплексов состава 1 : 2 (металл : аминокислота) и рассчитать их константы нестойкости: K=1,85×10-4 для Cu(Tre)2) и K=1,83×10-5 у Cu(Ser)2. Координация иона металла происходит бидентатно, за счет карбоксильной и аминогруппы лигандов. Исследование взаимодействия гидроксиаминокислот и Cu2+ представляет научный и практический интерес, так как позволяет расширить представления о лигандных взаимодействиях биомолекул, механизмах их биологической активности.
| Финансирование Работа выполнена в рамках гранта ЗабГУ №327. | Funding The work was carried out within the framework of a grant from the Trans-Baikal State University №327. |
| Конфликт интересов Не указан | Conflict of Interest None declared |
Список литературы / References
- Бек М. Исследование комплексообразования новейшими методами. Пер. с англ. / М. Бек, И. Надьпал. Москва: Мир, 1989. 413 с.
- Берестова Т.В. ИК-характеристики стереоизомеров транс-, бис- и разнолигандных комплексов Сu (II) с D,L-треонином / Т.В. Берестова и др. // Вестник ТвГУ. Серия Химия. – 2015. - № 2. – С. 118-124.
- Вергейчик Е.Н. Получение и изучение соединений индия хлорида с α-аланином и фенилаланином / Е.Н. Вергейчик, М.А. Мокрушина // Курский научно-практический вестник "Человек и его здоровье". – 2007. - № 4. – С. 92-96.
- Голованова О.А. Кинетика и термодинамика образования соединений ионов кальция с аминокислотами, их строение и устойчивость / О.А. Голованова, И.А. Томашевский // Журнал физической химии. – 2019. – Т. 93, №1. – С. 11-22.
- Кадырова Р.Г. Синтез и свойства комплексных солей биогенных кислот макро- и микроэлементов. Монография / Р.Г. Кадырова, Г.Ф Кабиров, Р.Р. Муллахметов. – Казань: Казан. гос. энерг. ун-т, 2016. – 115 с.
- Крылова Л.Ф. Стереоизомерные комплексы Pd (II) с серином, треонином и аллотреонином / Л.Ф. Крылова // Журнал неорганической химии. 2011. - Т. 56, № 1. - С. 56-64.
- Новикова Г.В. Синтез и физико-химические характеристики комплексов 6s2 и ndm-ионов металлов с аминокислотами: автореф. дисс… канд. хим. наук : 02.00.01 / Новикова Галина Владимировна. - Красноярск: СибГТУ, 2006. – 22 с.
- Огородникова Н.П. Химическое взаимодействие металлов – меди, железа и марганца с α- и β-аминокислотами в водных и органических средах: автореф. дисс…. канд. хим. наук : 02.00.04 / Огородникова Надежда Петровна. - Ростов-на-Дону: ЮжФУ – 2010. – 24 с.
- Тачаев М.В. Комплексные соединения никеля (II), палладия (II) с аминокислотами, аденином и цитозином: автореф. дисс… канд. хим. наук : 02.00.01 / Тачаев Максим Владимирович. - Москва: РУДН, 2008. – 22с.
- Чернова С.П. Потенциометрическое изучение поведения ионов Zn (II) в водных растворах аминокислот и комплексонов / С.П. Чернова, Л.В. Трубачева // Аналитика и контроль. – 2006. – Т.10, № 3-4. – С. 336 – 341.
Список литературы на английском языке / References in English
- Bek M. Issledovanie kompleksoobrazovanija novejshimi metodami [Investigation of complexation by the latest methods]. Per. s angl. / M. Bek, I. Nad'pal. Moskva: Mir, 1989. 413 p. [in Russian]
- Berestova T.V. IK-harakteristiki stereoizomerov trans-, bis- i raznoligandnyh kompleksov Su (II) s D,L-treoninom [IR characteristics of stereoisomers of trans-, bis-, and mixed-ligand complexes of Cu (II) with D, L-threonine] / T.V. Berestova et al. // Vestnik TvGU. Serija Himija. – 2015. - № 2. – P. 118-124. [in Russian]
- Vergejchik E.N. Poluchenie i izuchenie soedinenij indija hlorida s α-alaninom i fenilalaninom [Preparation and study of compounds of indium chloride with α-alanine and phenylalanine] / E.N. Vergejchik, M.A. Mokrushina // Kurskij nauchno-prakticheskij vestnik "Chelovek i ego zdorov'e". – 2007. - № 4. – P. 92-96. [in Russian]
- Golovanova O.A. Kinetika i termodinamika obrazovanija soedinenij ionov kal'cija s aminokislotami, ih stroenie i ustojchivost' [Kinetics and thermodynamics of the formation of compounds of calcium ions with amino acids, their structure and stability] / O.A. Golovanova, I.A. Tomashevskij // Zhurnal fizicheskoj himii. – 2019. – Vol. 93, №1. – P. 11-22. [in Russian]
- Kadyrova R.G. Sintez i svojstva kompleksnyh solej biogennyh kislot makro- i mikrojelementov [Synthesis and properties of complex salts of biogenic acids of macro- and microelements]: Monografija / R.G. Kadyrova, G.F Kabirov, R.R. Mullahmetov. – Kazan': Kazan. gos. jenerg. un-t, 2016. – 115 p. [in Russian]
- Krylova L.F. Stereoizomernye kompleksy Pd (II) s serinom, treoninom i allotreoninom [Stereoisomeric complexes of Pd (II) with serine, threonine, and allotreonine] / L.F. Krylova // Zhurnal neorganicheskoj himii. - 2011. - vol. 56, № 1. - P. 56-64. [in Russian]
- Novikova G.V. Sintez i fiziko-himicheskie harakteristiki kompleksov 6s2 i ndm-ionov metallov s aminokislotami [Synthesis and physicochemical characteristics of complexes of 6s2 and ndm metal ions with amino acids]: avtoref. dis… of PhD in Chemistry : 02.00.01 / Novikova Galina Vladimirovna. - Krasnojarsk: SibGTU, 2006. – 22 p. [in Russian]8. Ogorodnikova N.P. Himicheskoe vzaimodejstvie metallov – medi, zheleza i marganca s α- i β-aminokislotami v vodnyh i organicheskih sredah [Chemical interaction of metals - copper, iron and manganese with α- and β-amino acids in aqueous and organic media]: avtoref. dis… of PhD in Chemistry : 02.00.04 / Ogorodnikova Nadezhda Petrovna. - Rostov-na-Donu: JuzhFU – 2010. – 24 p. [in Russian]
- Tachaev M.V. Kompleksnye soedinenija nikelja (II), palladija (II) s aminokislotami, adeninom i citozinom [Complex compounds of nickel (II), palladium (II) with amino acids, adenine and cytosine]: avtoref. dis… of PhD in Chemistry : 02.00.01 / Tachaev Maksim Vladimirovich. - Moskva: RUDN, 2008. – 22 p. [in Russian]
- Chernova S.P. Potenciometricheskoe izuchenie povedenija ionov Zn (II) v vodnyh rastvorah aminokislot i kompleksonov [Potentiometric study of the behavior of Zn (II) ions in aqueous solutions of amino acids and complexones] / S.P. Chernova, L.V. Trubacheva // Analitika i kontrol'. – 2006. – Vol.10, № 3-4. – P. 336 – 341. [in Russian]