EXTERNAL RISK FACTORS FOR THE FORMATION OF ATOPIC MARCH IN CHILDREN UNDER 6 YEARS OLD
EXTERNAL RISK FACTORS FOR THE FORMATION OF ATOPIC MARCH IN CHILDREN UNDER 6 YEARS OLD
Abstract
According to statistical data, there has been a significant increase in the prevalence of allergic diseases worldwide. Modern research has shown that allergic diseases develop over time: from atopic dermatitis and food allergies in infancy to the gradual development of allergic asthma and allergic rhinitis in childhood.
The aim of our study was to identify significant risk factors for the development of allergic rhinitis and/or bronchial asthma in children under 6 years old with food allergy in order to identify a risk group for the implementation of atopic march for the development of recommendations to prevent its development.
Within the framework of this study, external risk factors in children under 6 years of age with food allergy were analysed, which allowed to identify the following risk factors: correctable and uncorrectable, which have a significant effect on the programming of children's future health. Such children, especially those with a complicated genetic anamnesis, should be singled out as a special risk group.
1. Введение
Атопический марш (АМ) – вариант течения атопии, характеризующийся, как правило, началом атопического дерматита (АтД) в раннем детском возрасте с последующим развитием других аллергических заболеваний (бронхиальной астмы (БА), аллергического ринита (АР) в более старшем возрасте , . Распространенность АтД в развитых странах у детей составляет 1-3%, а у взрослых достигает 20% .
В типичных случаях АтД у детей раннего возраста ассоциирован с пищевой аллергией (ПА), тогда как БА и АР связаны с сенсибилизацией к ингаляционным аллергенам, формирующейся в более позднем возрасте . Также существует группа пациентов с АтД, у которых бронхиальная обструкция развивается также рано, как и поражение кожи, или даже предшествует ему, в связи с чем в данном случае нельзя говорить о развитии БА как итога «АМ» , .
Существуют внешние и внутренние факторы развития АтД. К внутренним факторам развития относят наличие мутации гена филаггрина в нарушении функции эпидермального барьера при атопическом дерматите, а также семейный анамнез аллергических заболеваний . С дефектами иммунной системы связано развитие воспалительной реакции в коже с участием T-лимфоцитов. В острую фазу заболевания преобладает Th2-ответ, когда происходит стимуляция Th2-клеток с последующей гиперпродукцией IgE; в хроническую –происходит переключение с Th2- на Th1-иммунный ответ. Ключевыми цитокинами, вовлеченными в патофизиологические механизмы атопического дерматита, являются ИЛ-4, ИЛ-5, ИЛ-13, ИЛ-31 и ИФН-γ, которым для передачи сигнала требуется участие сигнальной системы JAK/STAT, в том числе Янус-киназы 1 (JAK-1) . Во многих исследованиях описана патогенетическая роль ИЛ-4 в развитии аллерген-специфических IgE-опосредованных реакций при атопическом дерматите, которая заключается в переключении синтеза антител на IgE. ИЛ-4 связывается не только с рецептором ИЛ-4, но и с рецептором ИЛ-13, данные цитокины имеют схожие биологические функции. ИЛ-13 также играет важную роль в развитии Th2-типа иммунного ответа при атопическом дерматите . Доказана роль аллергии к клещам домашней пыли, энтеротоксинам золотистого стафилококка, плесневым грибам, а также IgE-аутореактивности в механизмах развития заболевания . Исследования последних лет продемонстрировали большое значение факторов внешней среды, обладающих эпигенетическим эффектом и усиливающих действие триггеров.
Цель исследования. Определить значимые факторы риска развития АР и /или БА у детей до 6 лет с ПА для прогнозирования АМ.
Задачи исследования:
1. Изучить особенности анамнеза у детей до 6 лет с аллергическим анамнезом и/или АБ.
2. Выявить значимые факторы риска формирования АР и БА у детей с ПА.
3. Обосновать необходимость выделения детей с ПА и наличием факторов риска по развитию АР и/или БА в группу риска по реализации АМ.
2. Методы и принципы исследования
Работа выполнена на базе института педиатрии ФГОУ ВО ТГМУ Минздрава России (ректор, д.м.н., проф. В.Б. Шуматов, директор института Т.А. Шуматова).
Были проанализированы анамнестические факторы риска у 31 ребенка с пищевой аллергией, у которых развились явления АР и/или БА до 6 лет.
Исследование внешних факторов риска формирования АМ осуществлялось с помощью анкетирования 31 родителя. Данный опрос был специально разработан для этого исследования и состоял из 24 вопросов (рис.1, 2, 3)

Рисунок 1 - Анкета для исследования факторов риска, часть 1

Рисунок 2 - Анкета для исследования факторов риска, часть 2

Рисунок 3 - Анкета для исследования факторов риска, часть 3
3. Результаты и обсуждения
Возрастная структура пациентов основной группы представлена на рисунке 4. Среди опрошенных преобладают дети возраста 5 лет – 58% (n=18), возраста 4 лет – 10% (n=3), возраста 3 лет – 16% (n=5), возраста 2 лет – 6% (n=2), возраста 1 года – 6% (n=20), до 1 года 3% (n=1).
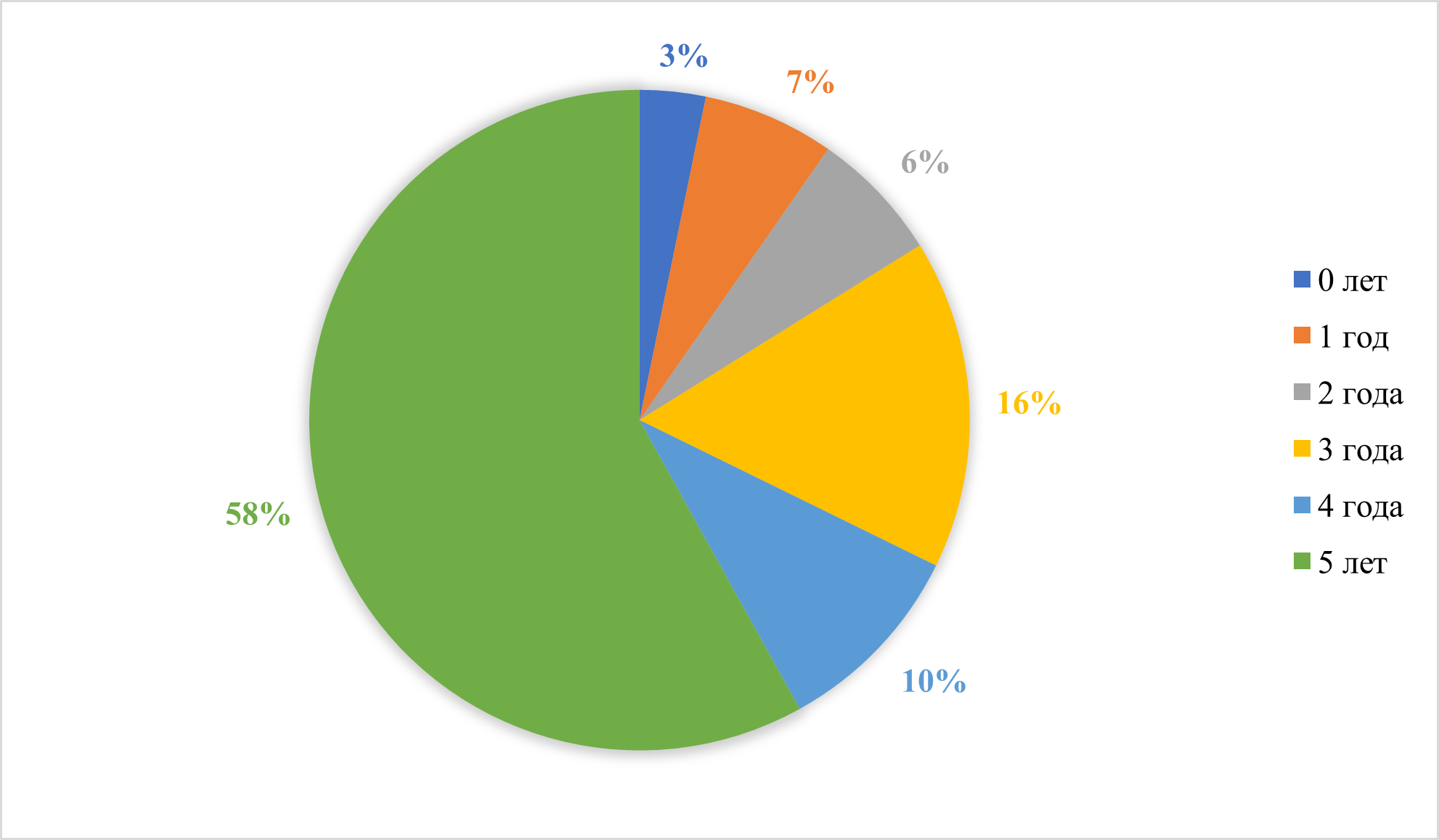
Рисунок 4 - Возрастная структура пациентов
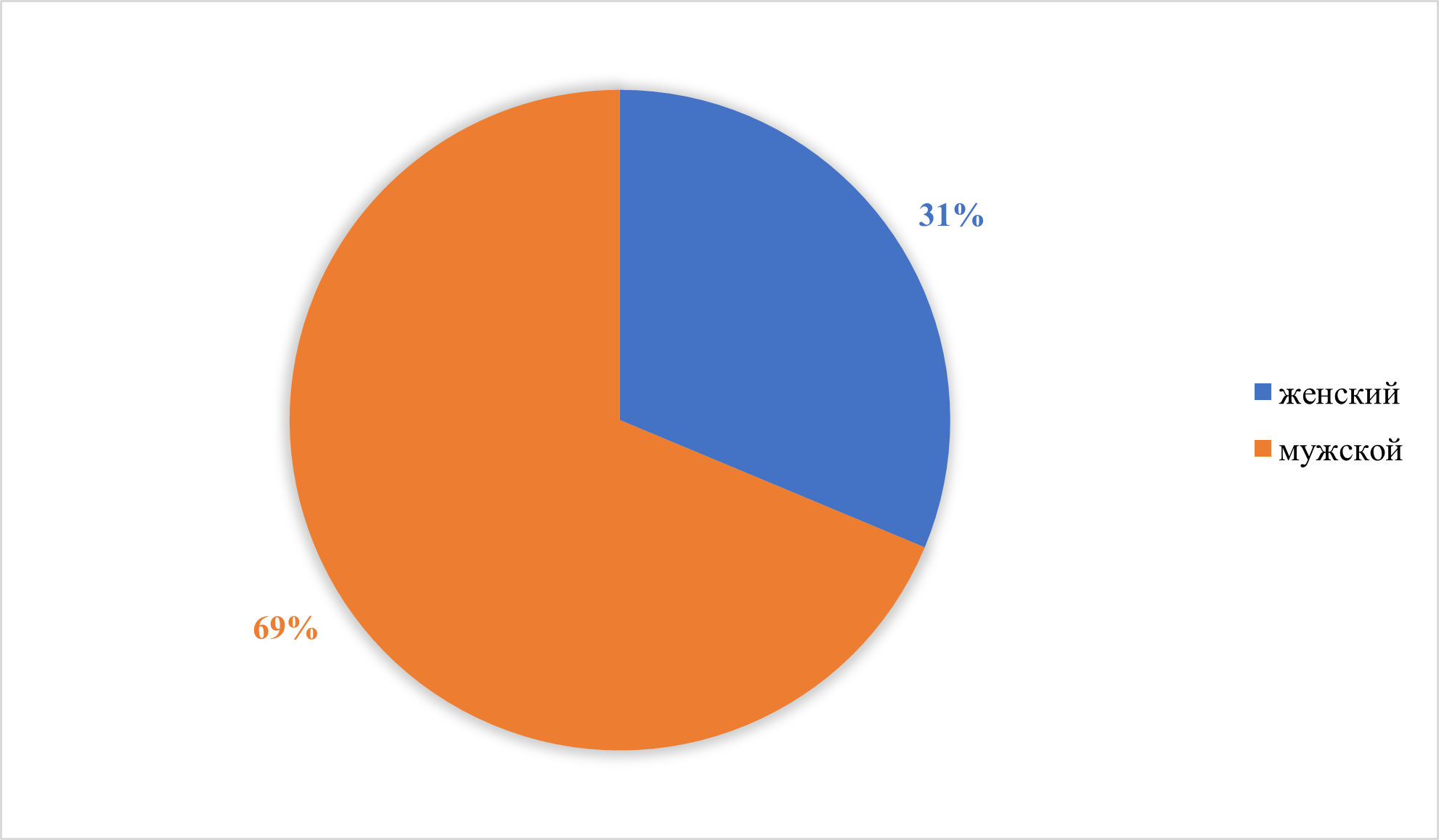
Рисунок 5 - Гендерная структура пациентов
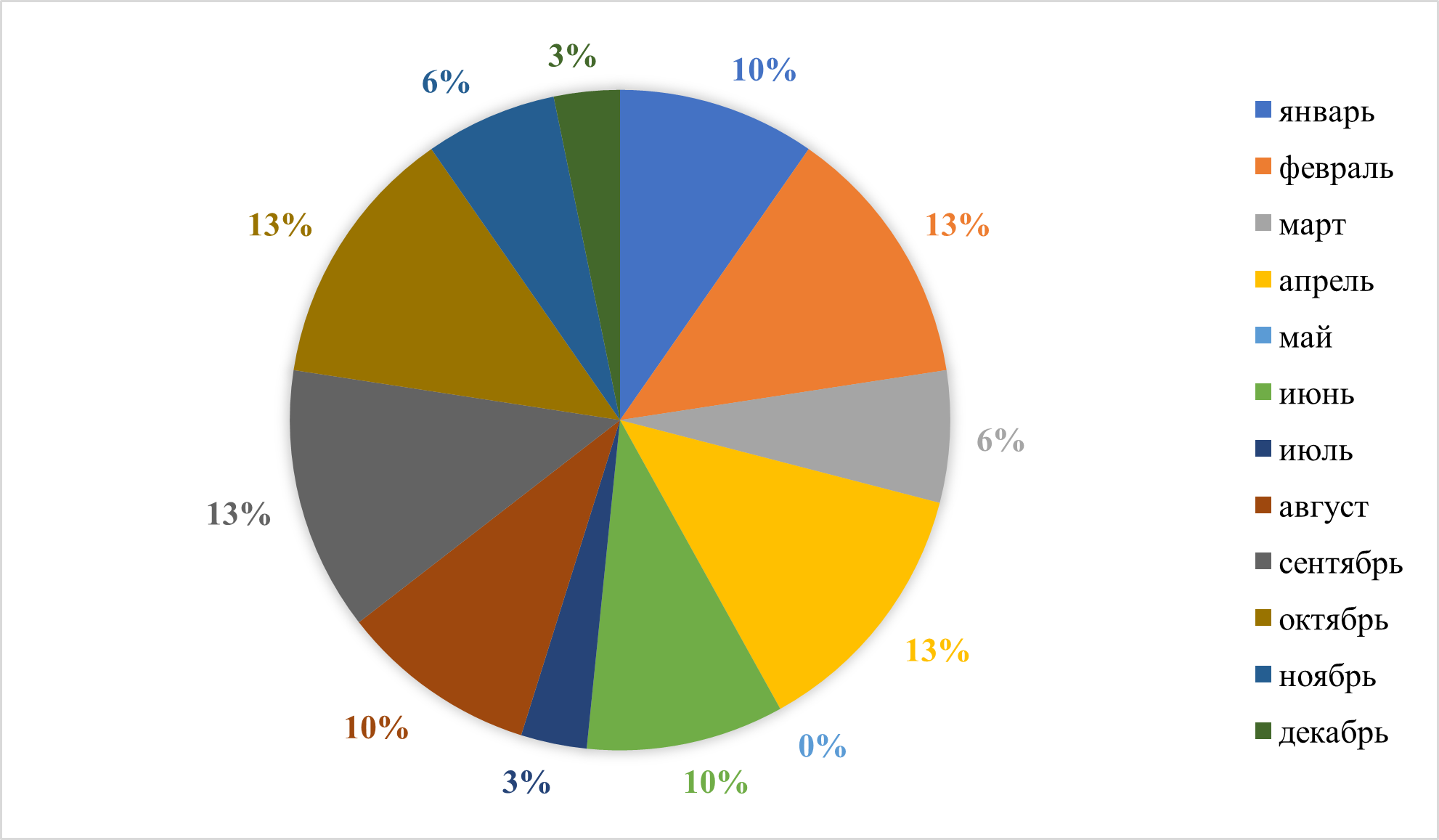
Рисунок 6 - Месяц рождения ребенка
Наличие других детей в доме ОШ = 1,232, 95% ДИ= 1,013-1,498.
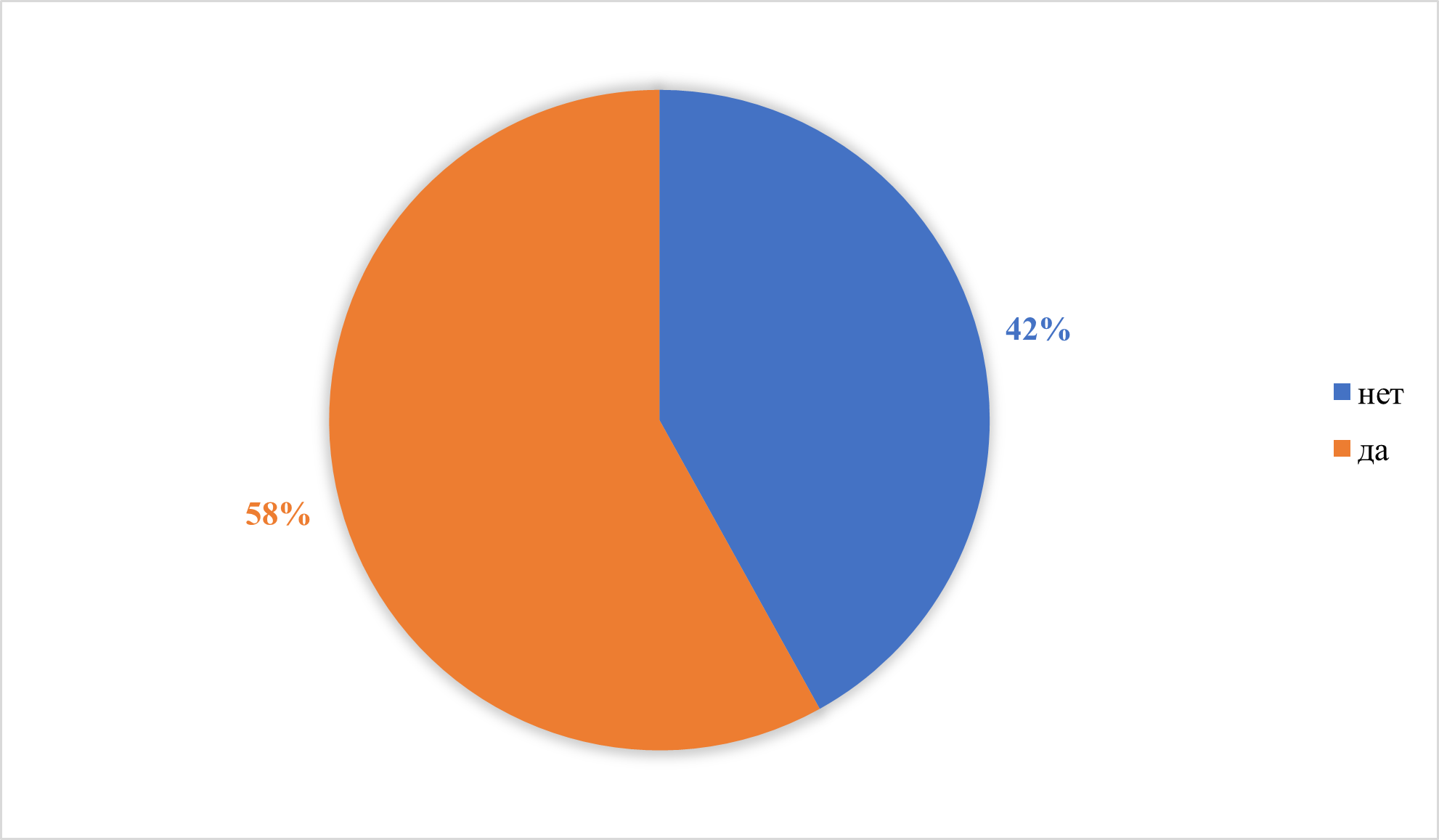
Рисунок 7 - Наличие других детей в доме
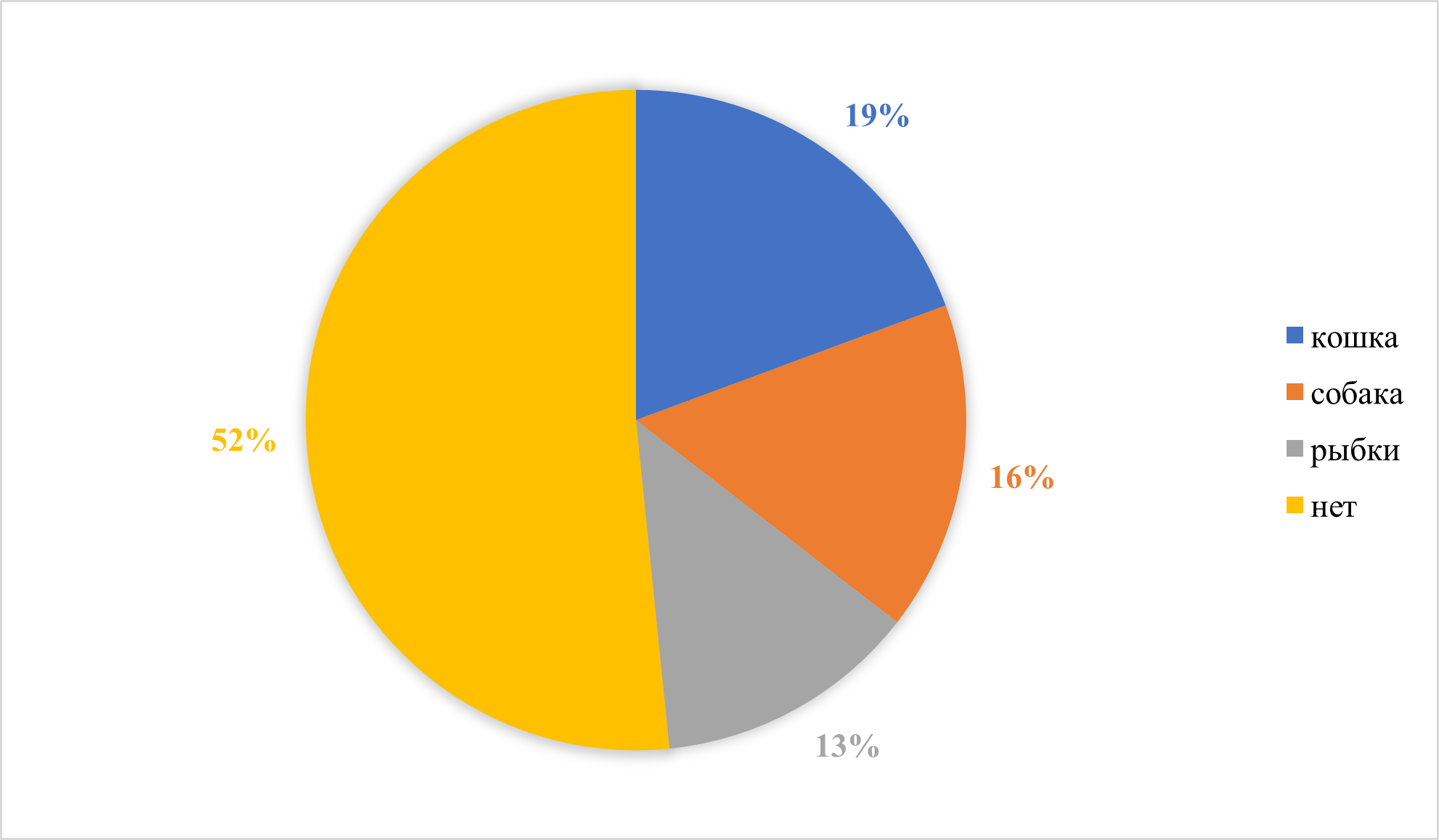
Рисунок 8 - Наличие домашних животных
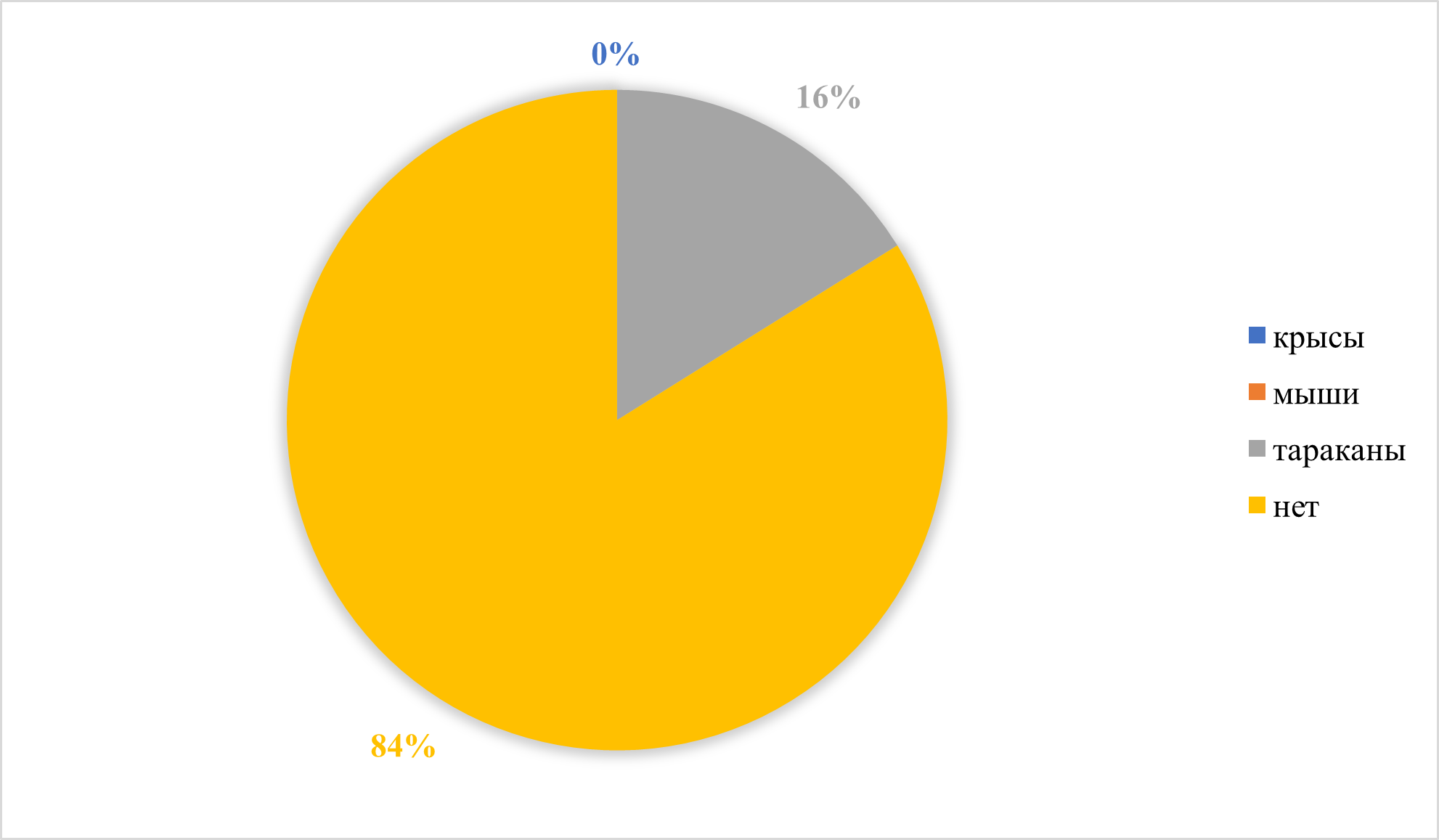
Рисунок 9 - Наличие мышей, крыс и/или тараканов дома
Наличие в доме ковров у пациентов основной группы представлено на рисунке 10. У 48% (n=15) есть в доме ковры, а у 52% (n=16) нет. Сенсибилизация к клещам домашней пыли ОШ = 1,89, 95% ДИ= 1,10–3,25. Без воздействия клещей домашней пыли ОШ = 3,58, 95% ДИ = 1,81-7,08.
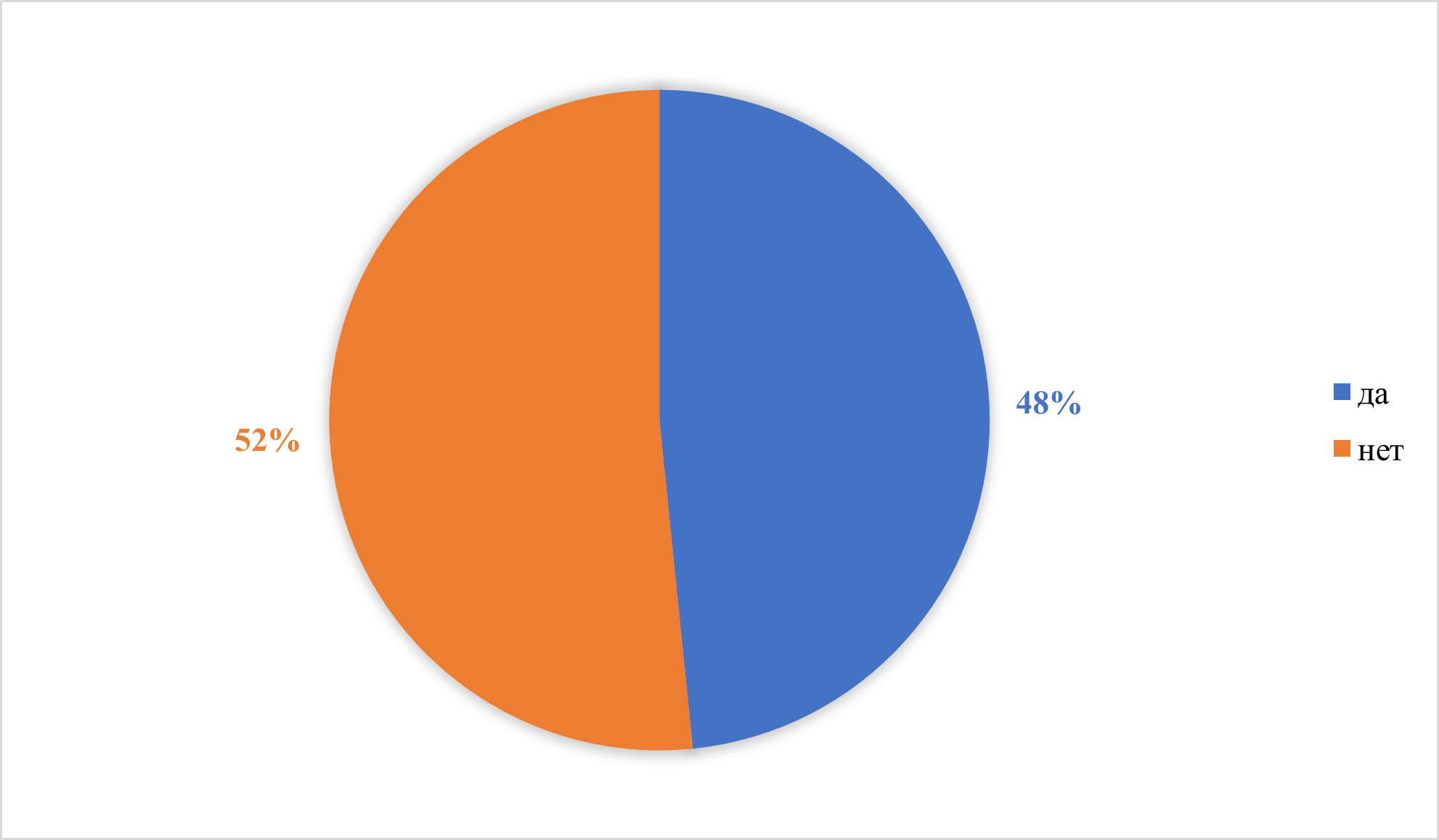
Рисунок 10 - Наличие ковров в доме
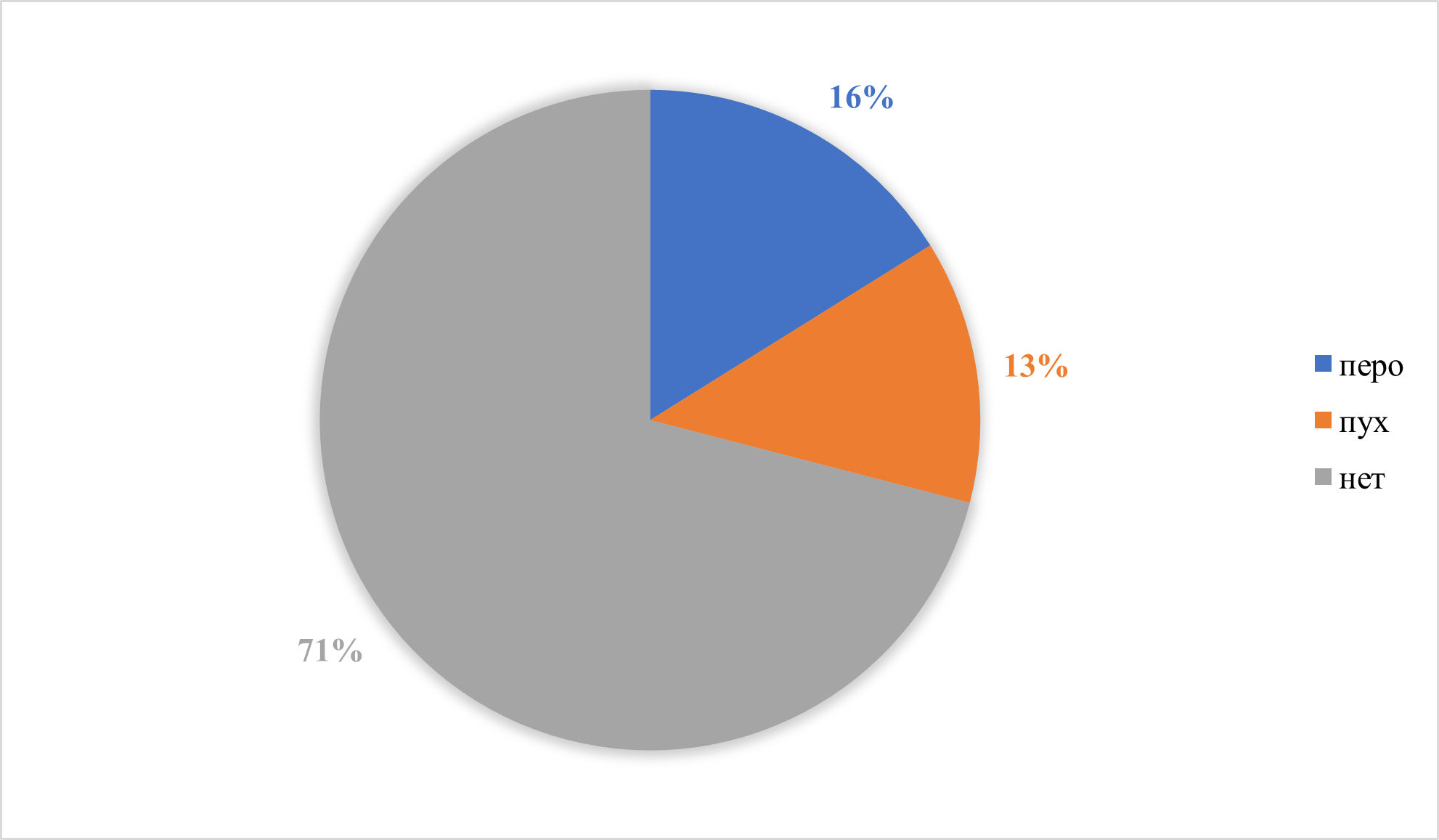
Рисунок 11 - Наличие в доме перьевых или пуховых подушек, одеял и др. предметов
Рисунок 12 - Наличие плесени в доме
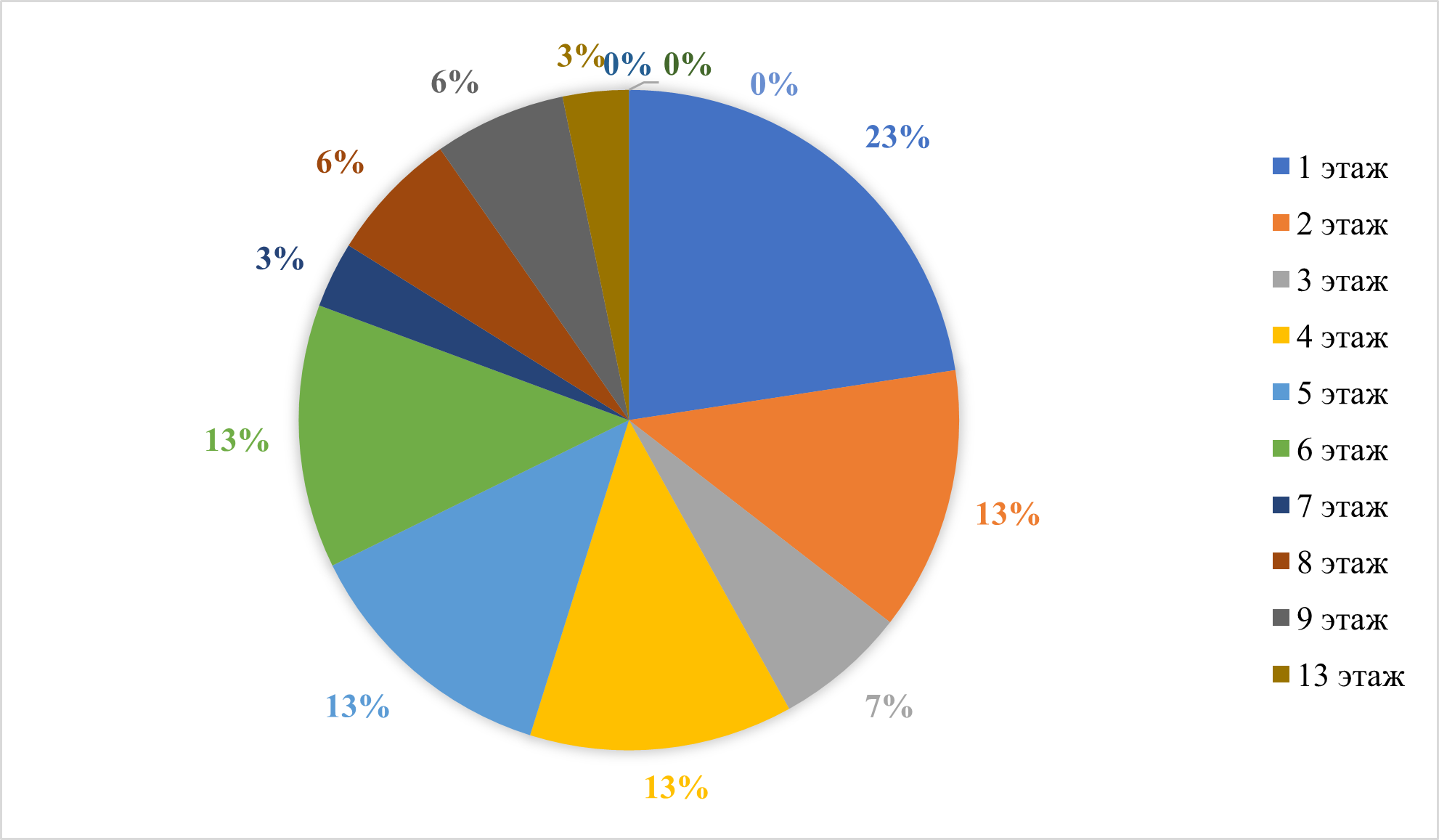
Рисунок 13 - Этаж проживания
Рисунок 14 - Раннее (до 3 месяцев) искусственное или смешанное вскармливание смесями на основе цельных белков коровьего молока
1) на первом году жизни, редко – n=14, часто – n=6;
2) на втором году жизни, редко – n=10, часто – n=7;
3) на третьем году жизни, редко – n=10, часто – n=7;
4) на четвертом году жизни, редко – n=6, часто – n=9;
5) на пятом году жизни, редко – n=4, часто – n=5.
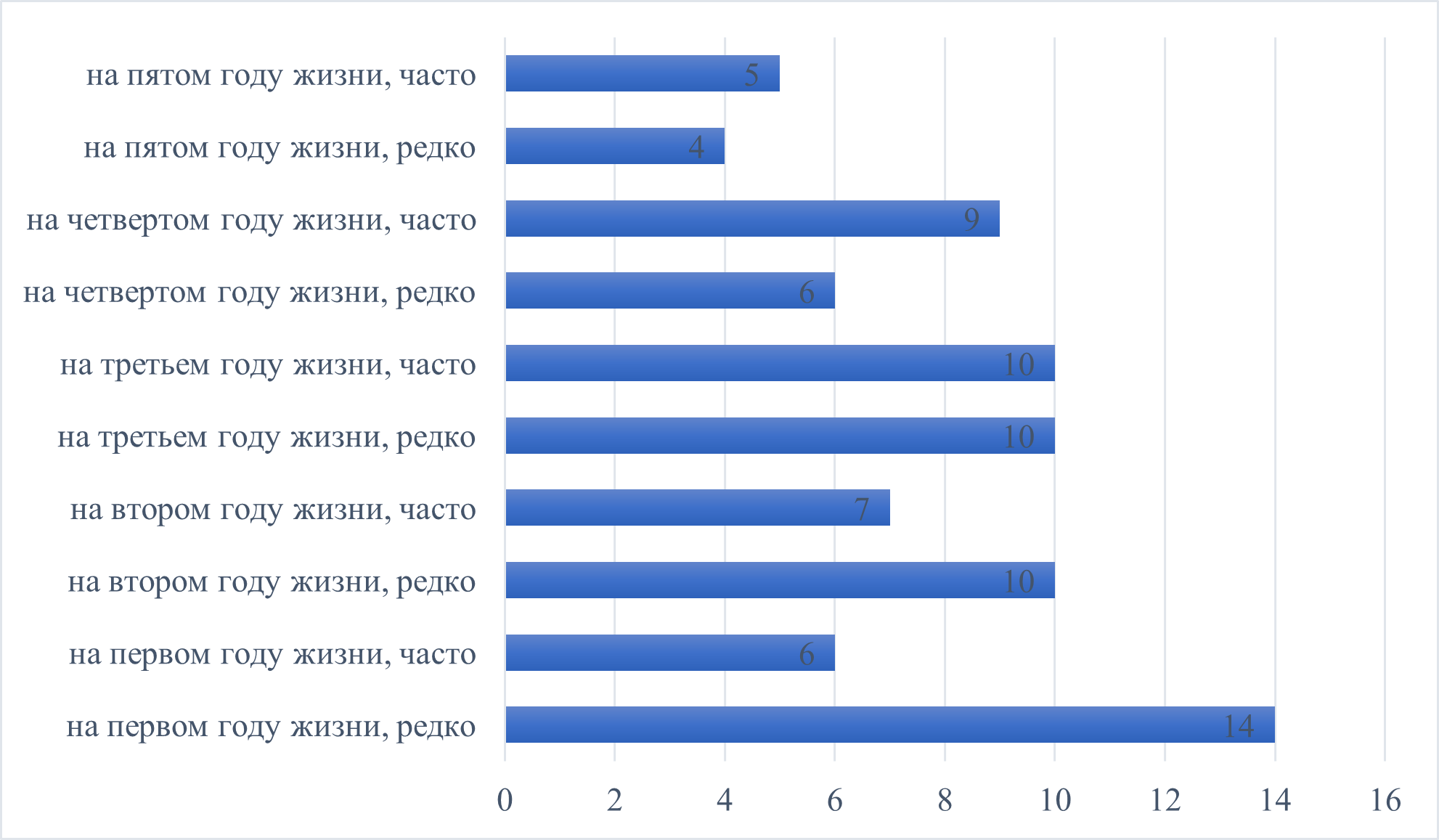
Рисунок 15 - Перенесенные ребенком острые респираторные заболевания
1) на первом году жизни, редко – n=16, часто – n=7;
2) на втором году жизни, редко – n=11, часто – n=5;
3) на третьем году жизни, редко – n=12, часто – n=5;
4) на четвертом году жизни, редко – n=9, часто – n=9;
5) на пятом году жизни, редко – n=7, часто – n=3.
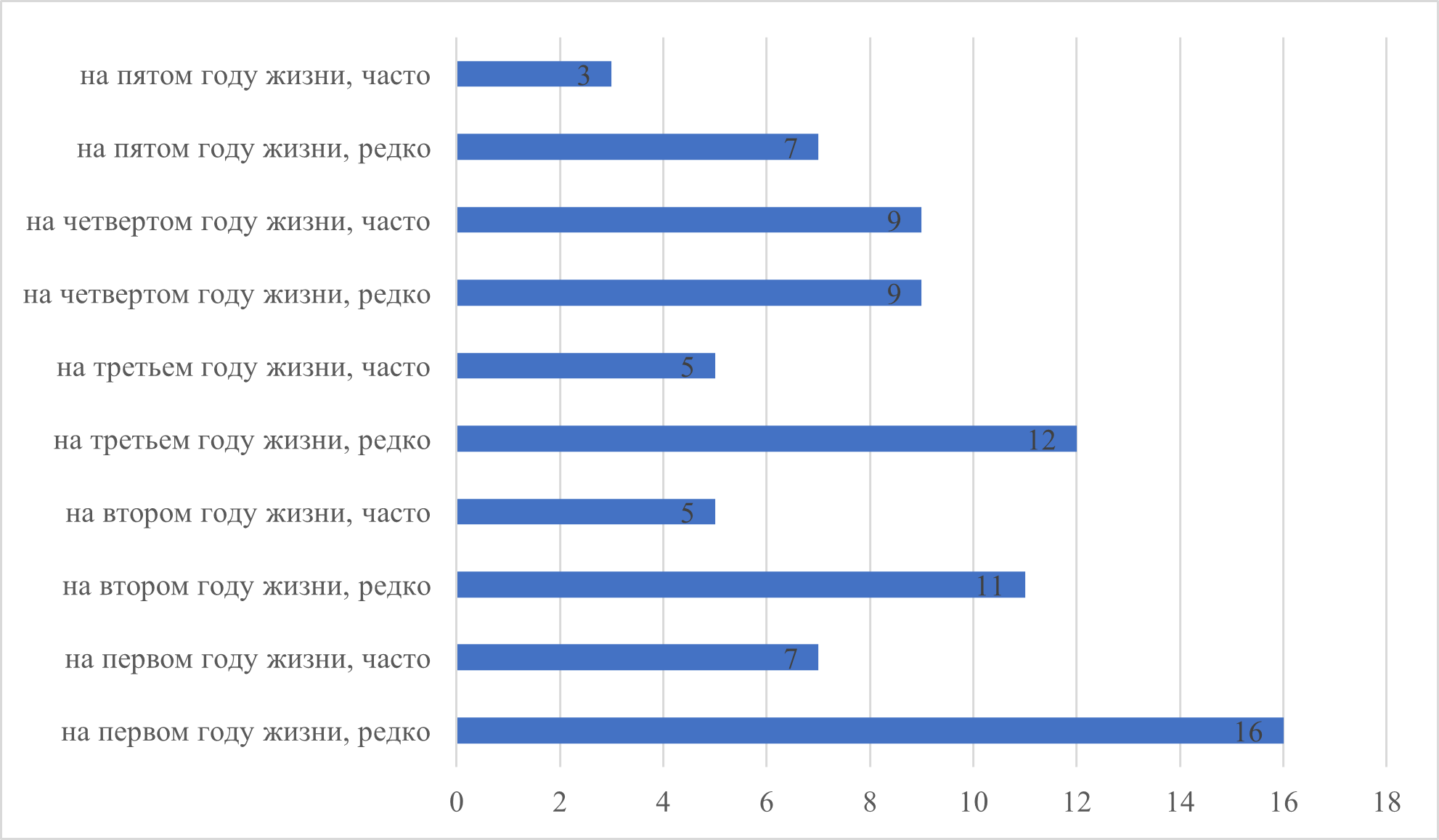
Рисунок 16 - Применение лекарств ребенком
Примечание: парацетамол и/или НПВС
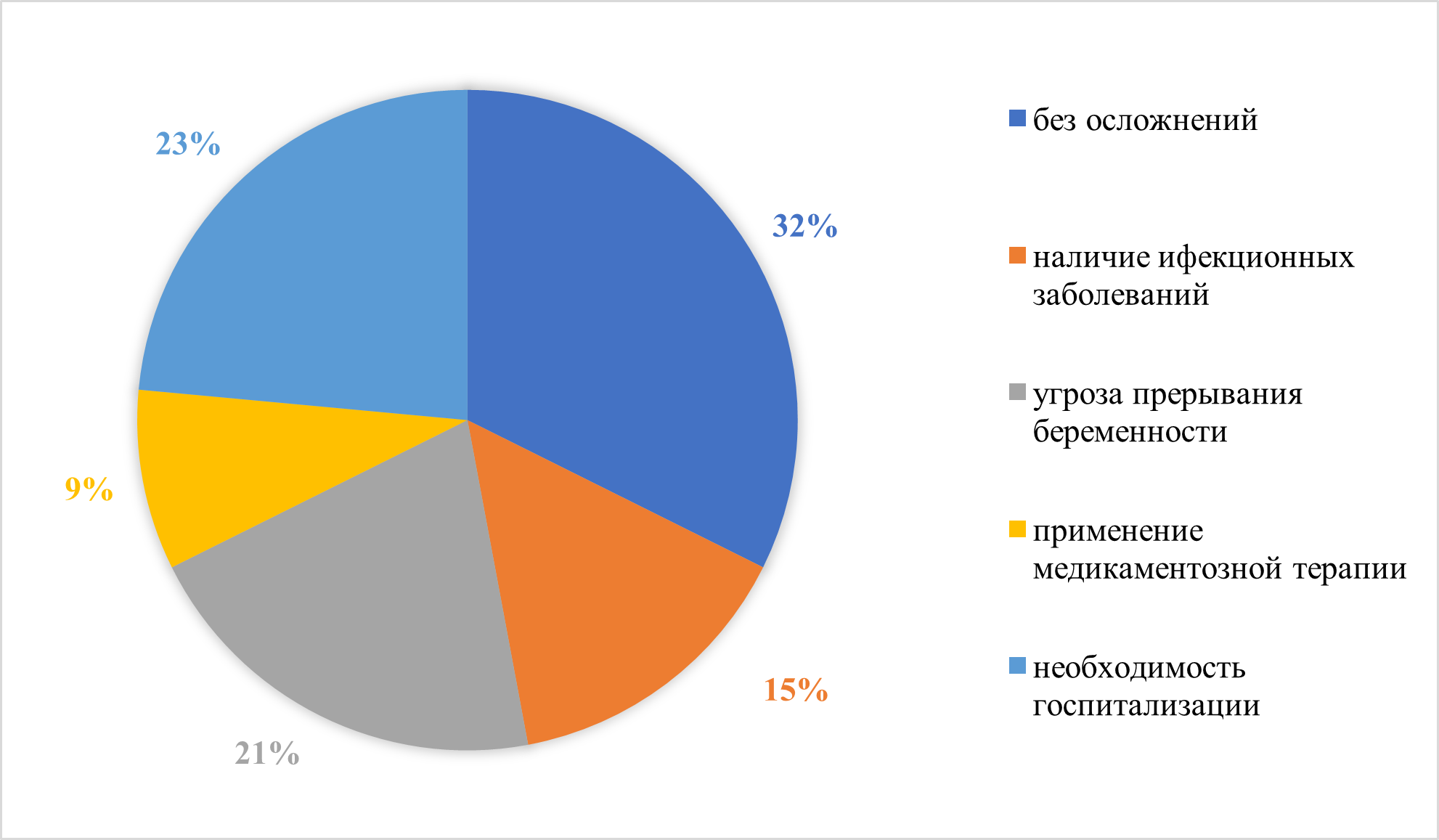
Рисунок 17 - Течение беременности
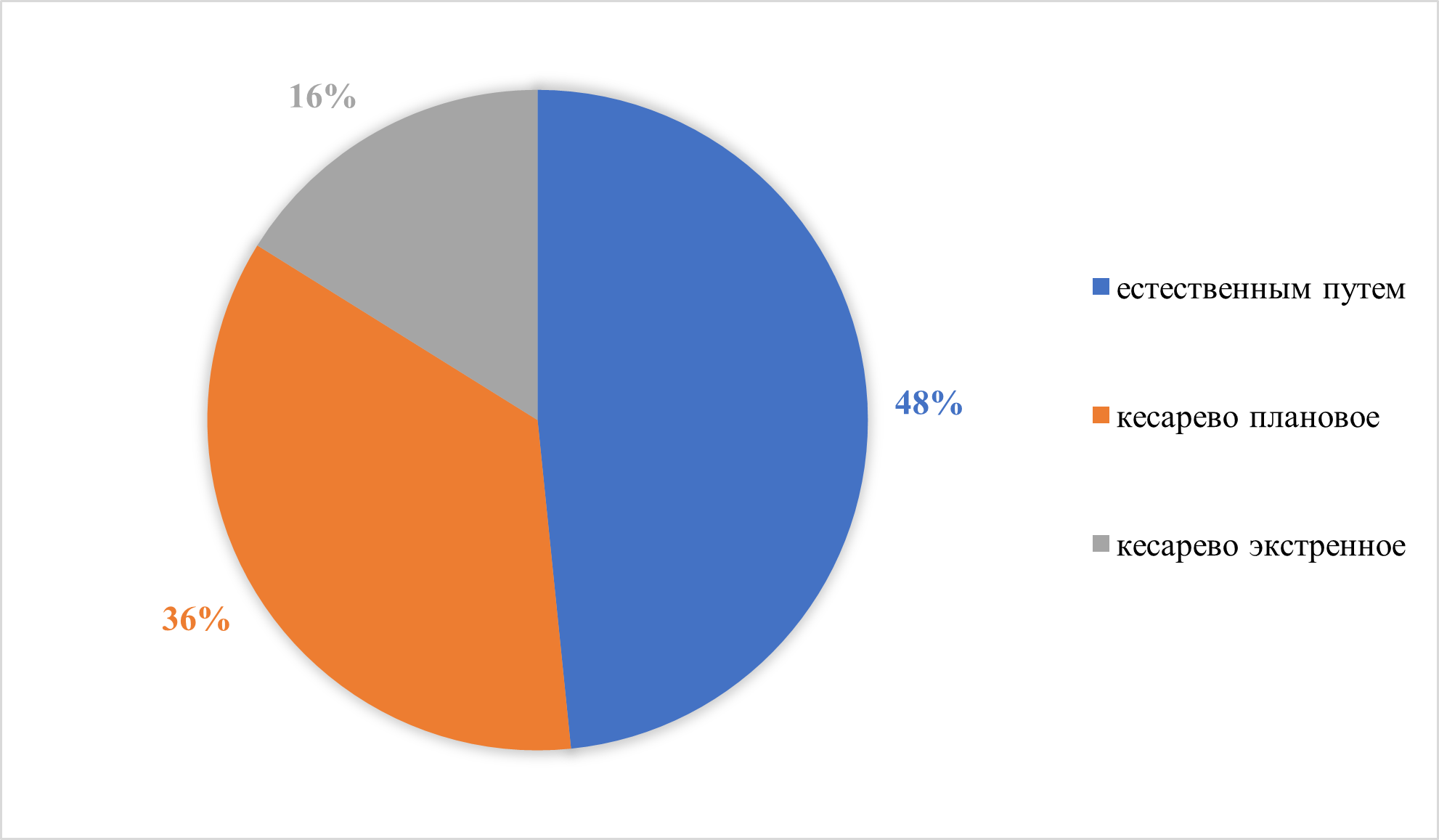
Рисунок 18 - Течение периода родов
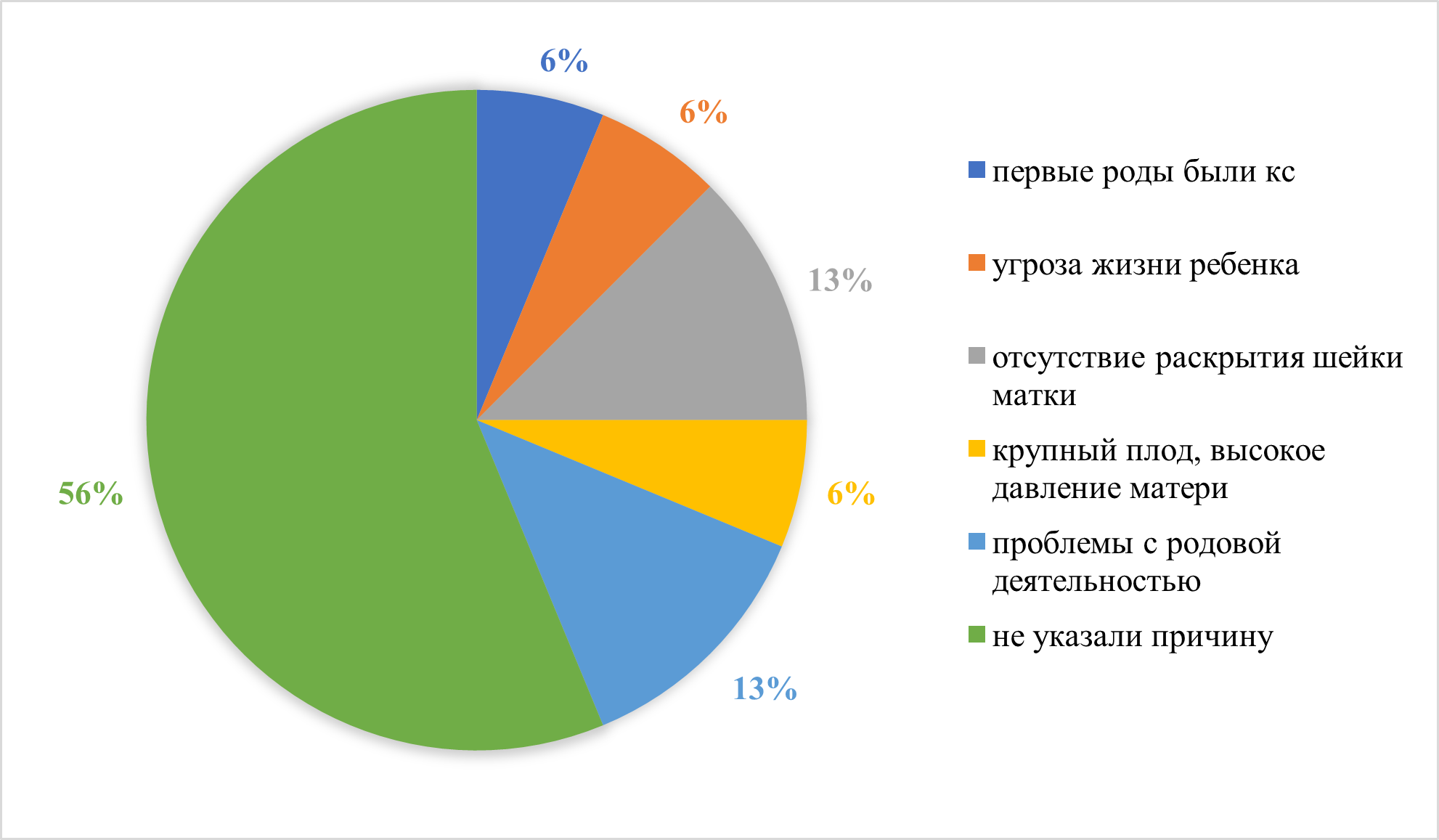
Рисунок 19 - Причины кесарева сечения
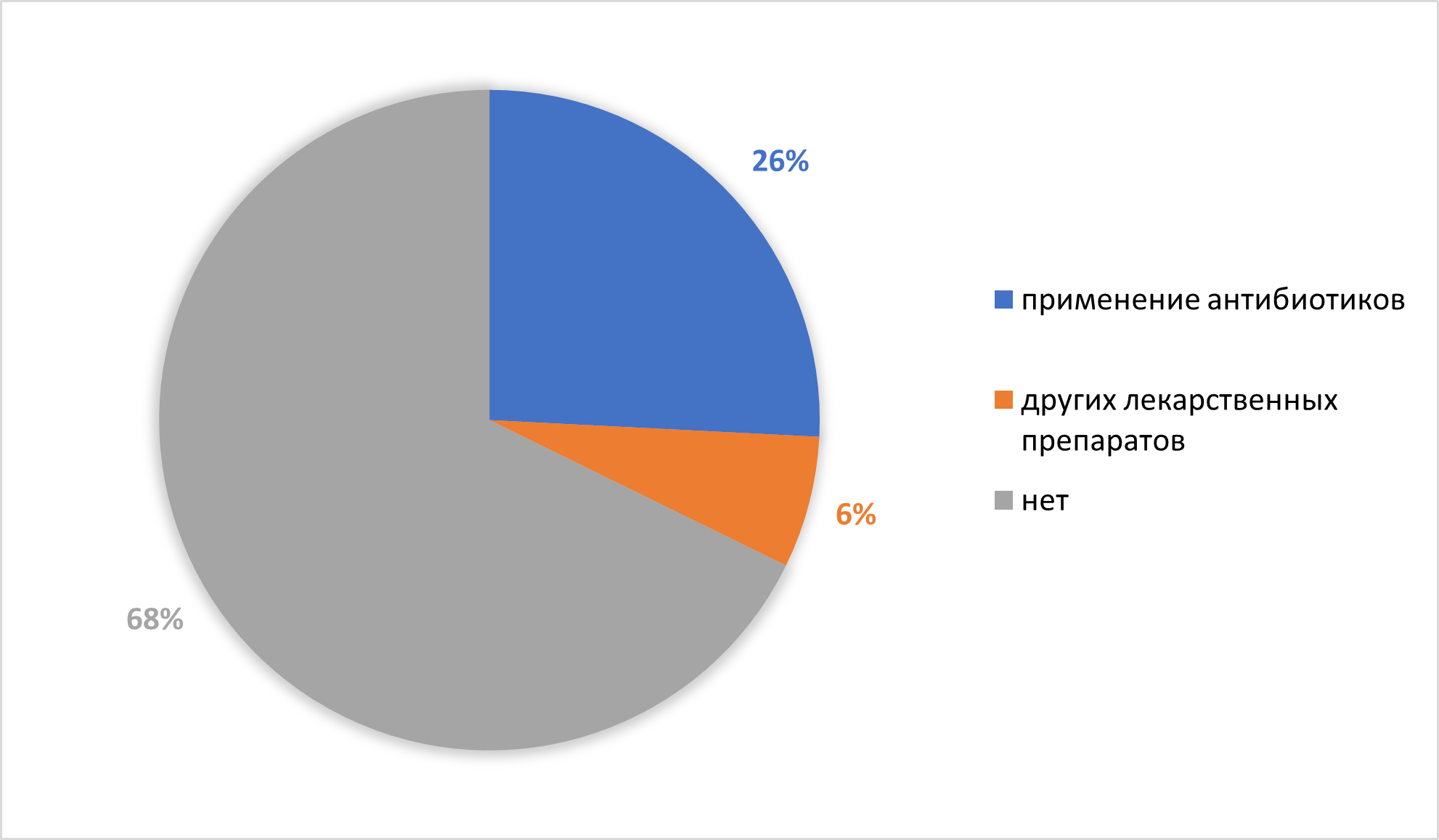
Рисунок 20 - Применение лекарственных препаратов в неонатальном периоде
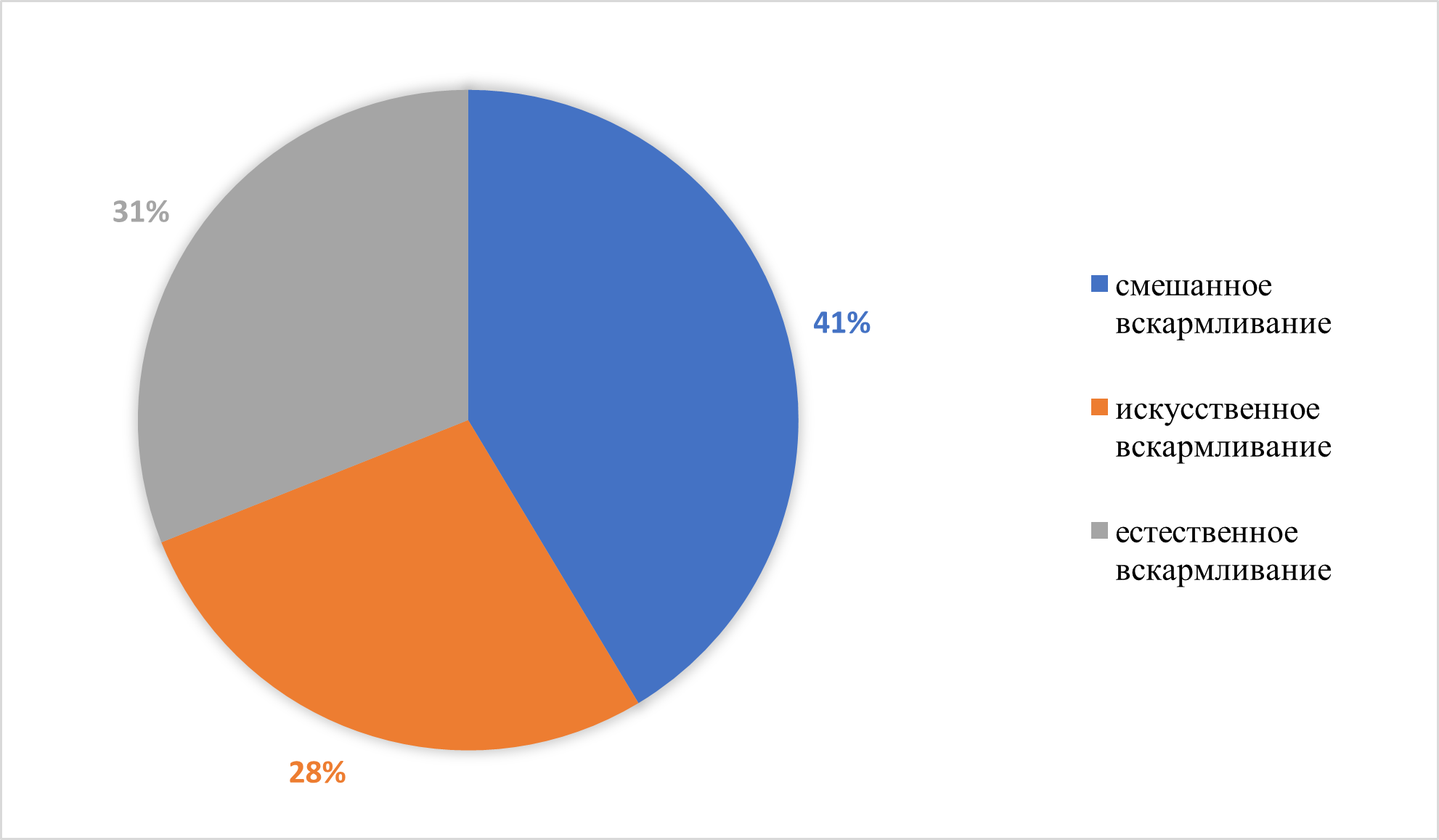
Рисунок 21 - Вскармливание в неонатальном периоде
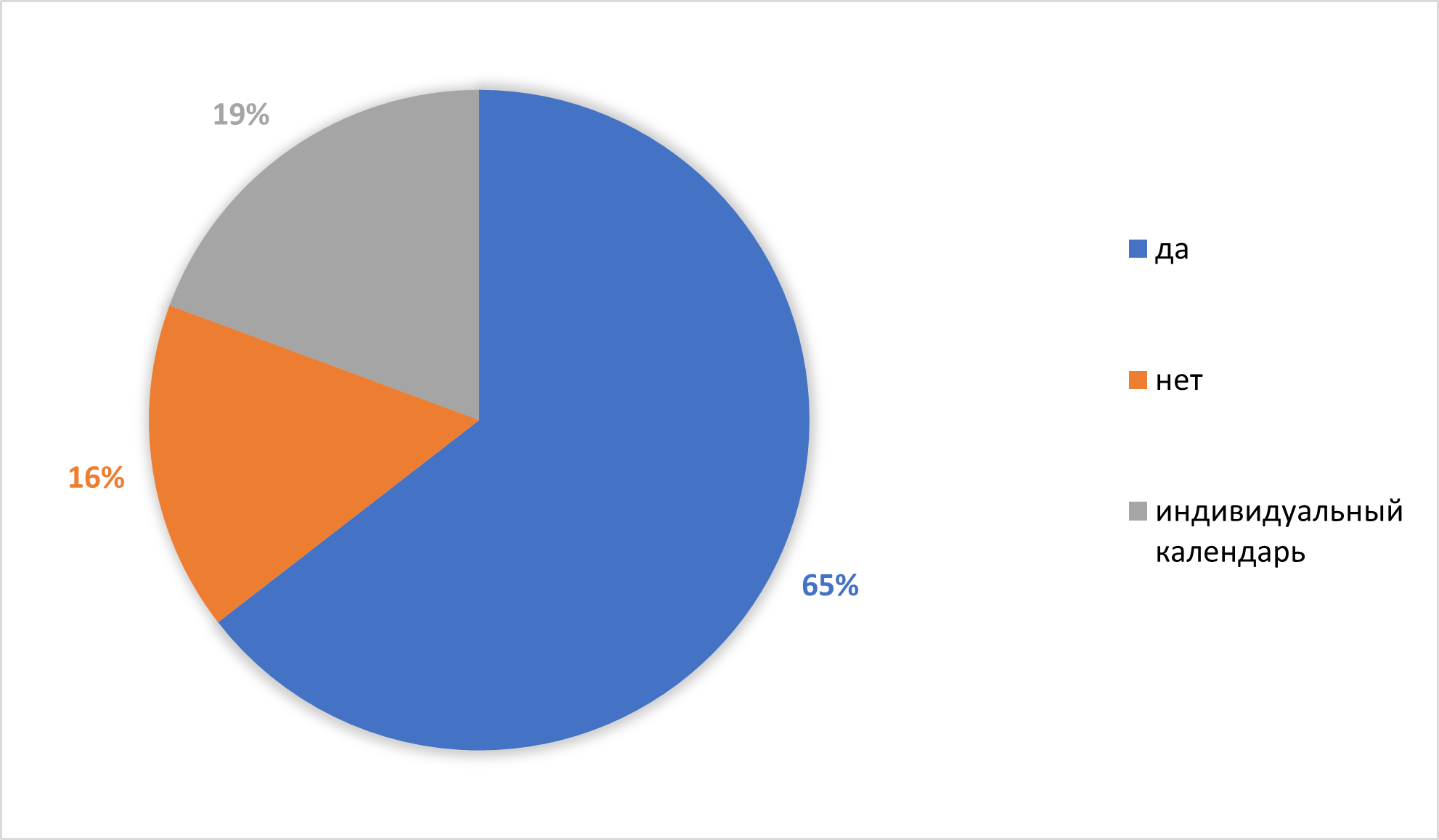
Рисунок 22 - Вакцинация ребенка согласно календарю прививок
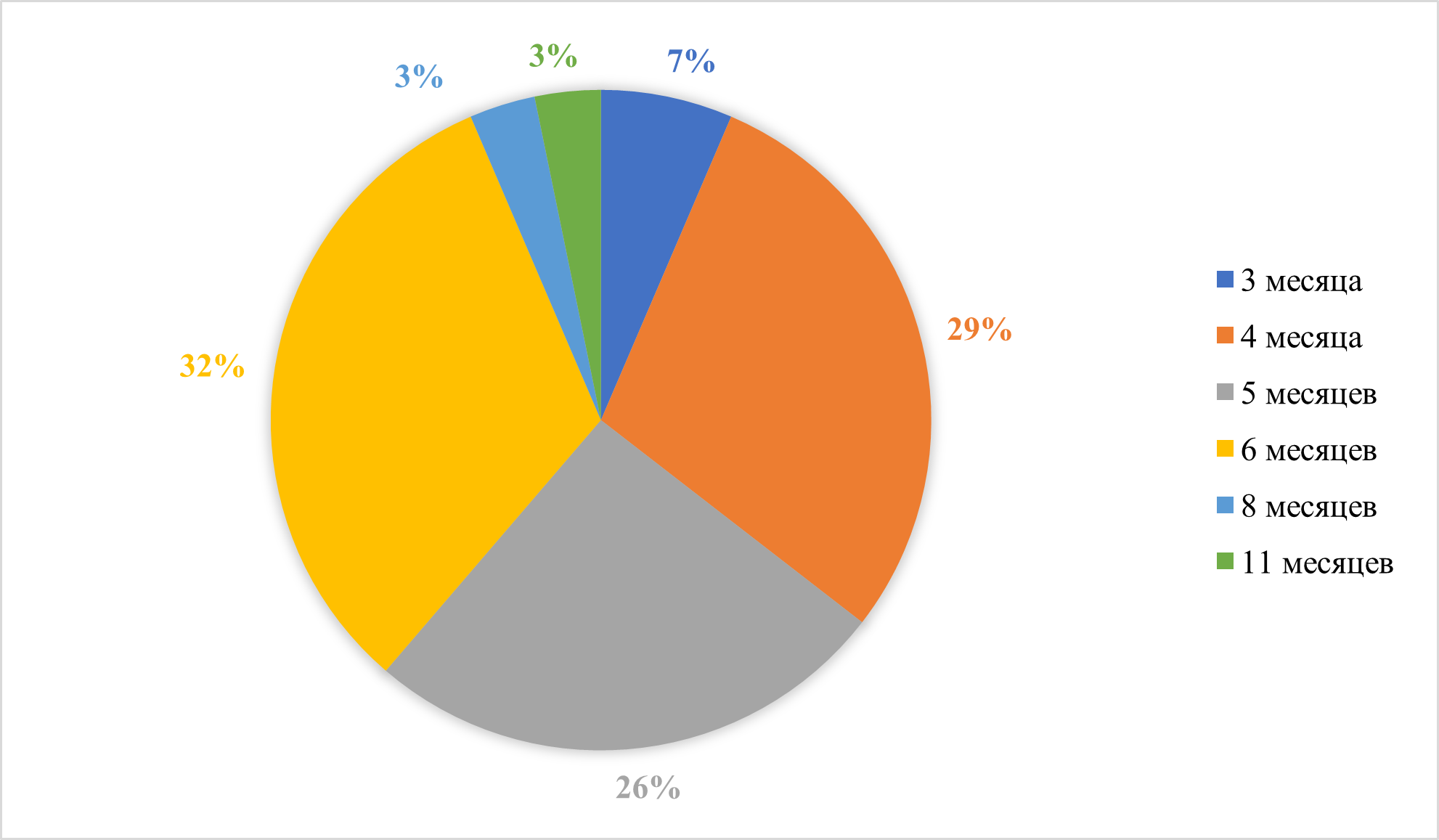
Рисунок 23 - Начало введения прикорма
Количество введенных продуктов пациентам основной группы в 6 месяцев представлено на рисунке 24. У 40% (n=13) в прикорм было введено 4 продукта, у 15% (n=5) – 5 продуктов, у 12% (n=4) – 2 продукта, у 6 % (n=2) – 1 продукт, у 6 % (n=2) – 3 продукта, у 3% (n=1) – 6 продуктов. У 18 % (n=6) прикорма не было.
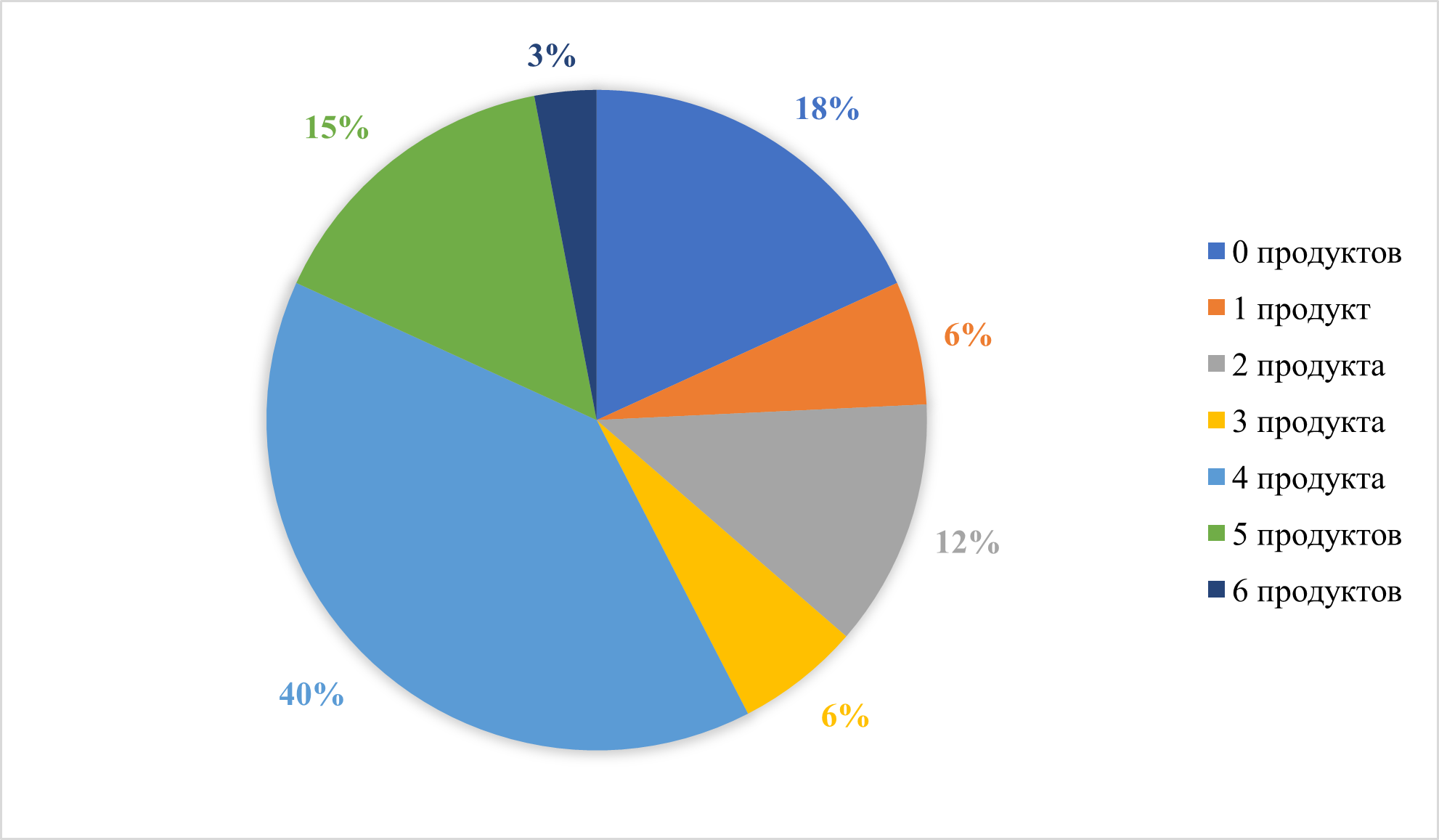
Рисунок 24 - Количество продуктов, введенных в прикорм ребенку в 6 месяцев
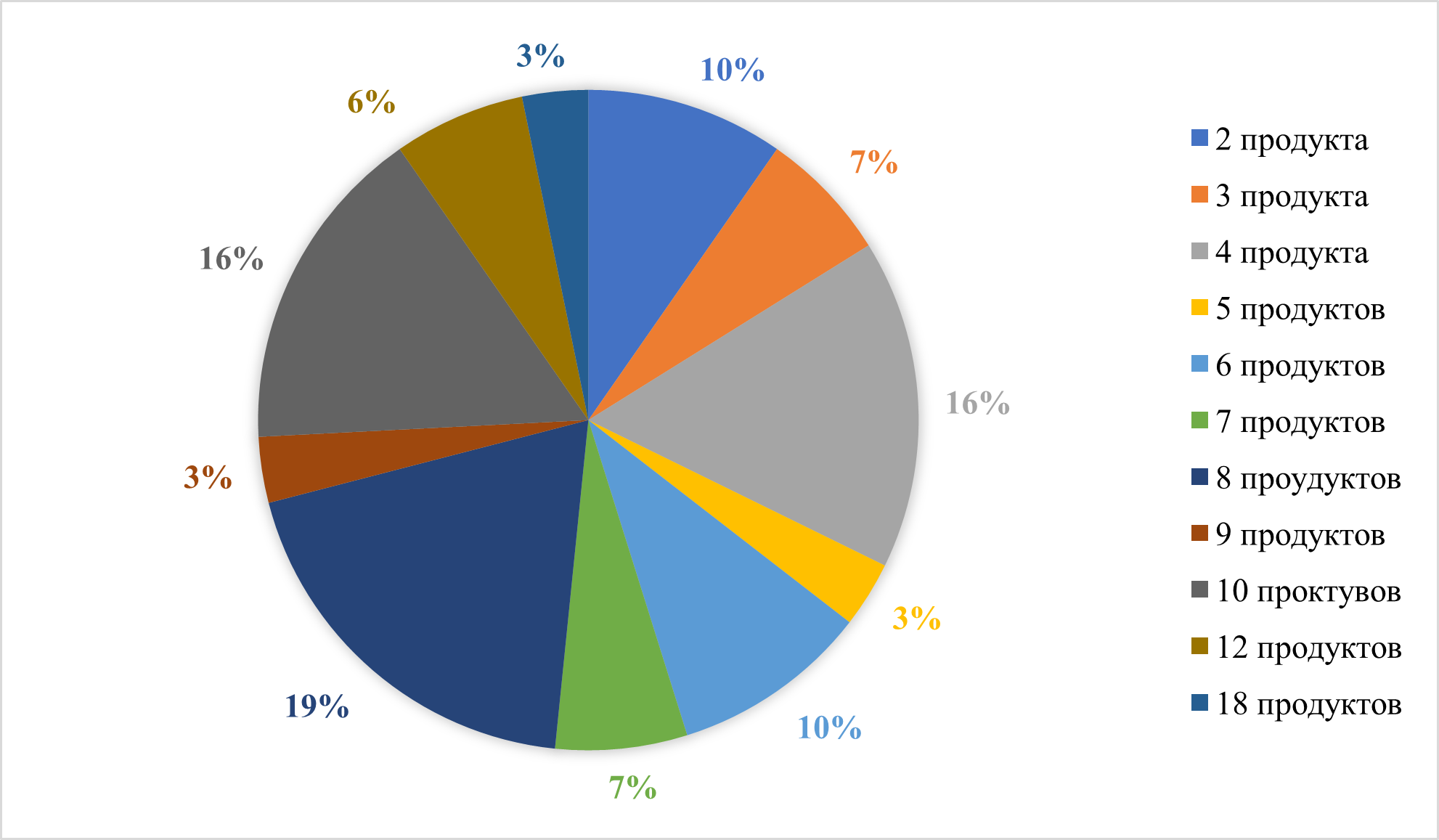
Рисунок 25 - Количество продуктов, введенных в прикорм ребенку в 9 месяцев
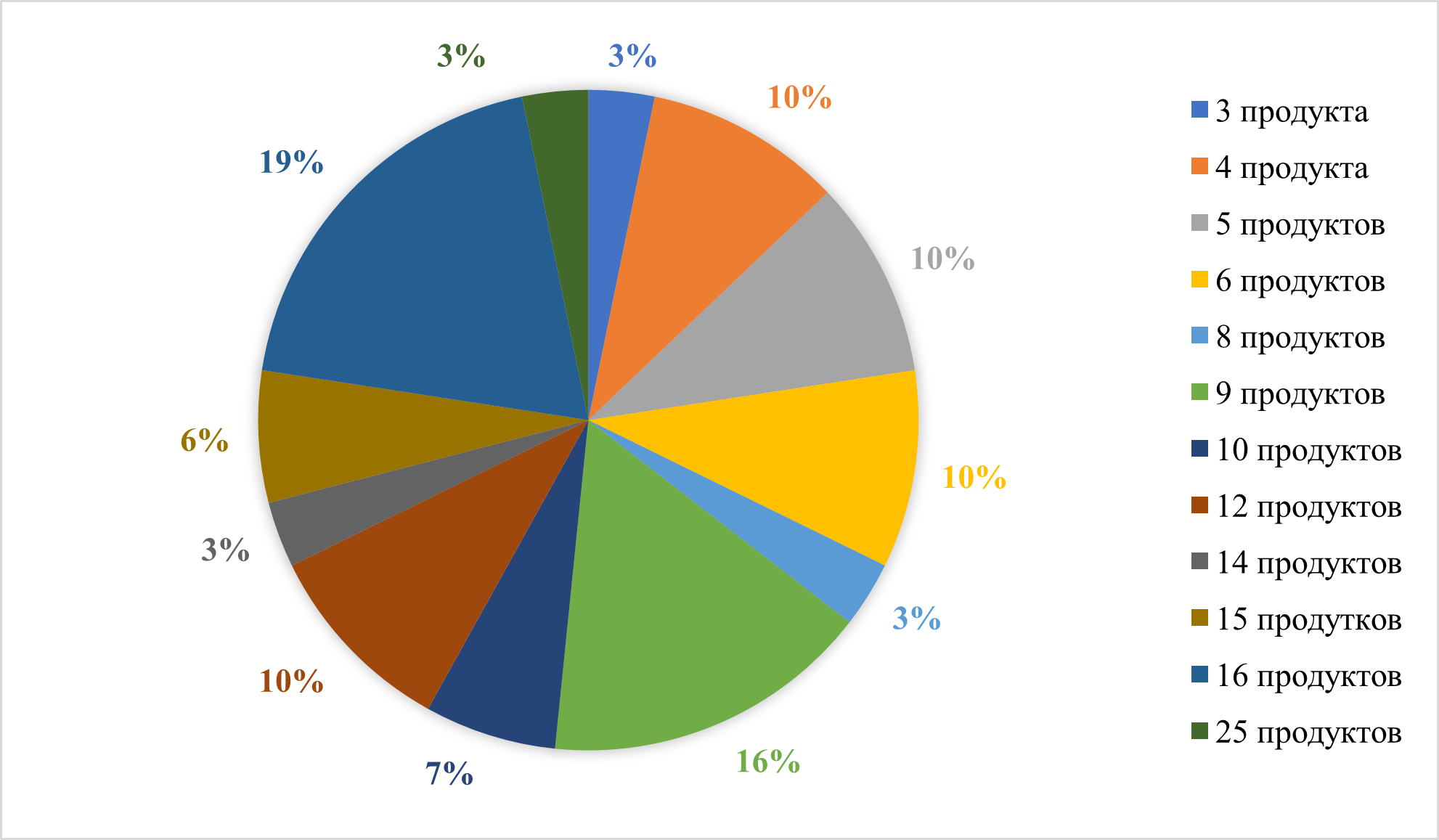
Рисунок 26 - Количество продуктов, введенных в прикорм ребенку в 12 месяцев
4. Заключение
В настоящее время известно, что основным фактором развития аллергических заболеваний является генетическая предрасположенность к АР и БА, но ее реализация у детей с пищевой аллергией может осуществляться при действии целого ряда неблагоприятных факторов внешней среды. И элиминация которых является одним из условий успешного лечения пациентов с этим серьезным заболеванием.
В рамках проведенного нами исследования были проанализированы современные научные данные, посвященные формированию АМ, проведен анализ внешних факторов риска у детей в возрасте до 6 лет с ПА.
Наиболее значимыми факторами риска с наибольшим отношением шансов являются генетическая предрасположенность, позднее введение прикормов.
Отягощенная наследственность по аллергическим болезням выявляется у 60-80% больных АМ. АтД возникает по данным различных исследований у 81% детей, если оба родителя больны атопическим дерматитом, у 59% – в случаях заболевания одного из родителей АтД и респираторной аллергией у другого и у 56% – если один из родителей болен АтД. Вероятность развития АтД у ребенка выше, если атопическим заболеванием страдает мать .
Развитие атопии обычно начинается с ранней сенсибилизации к пищевым аллергенам. Поэтому эта сенсибилизация часто рассматривалась в качестве фактора риска и предиктора других проявлений атопии, в особенности астмы.
Грудное вскармливание для младенцев является защитным фактором, так как материнское молоко обеспечивает оптимальное питание для новорожденных, и защиту от инфекционных агентов и аллергенов. Риск развития АМ если прикорм введен до 6 месяцев ОШ =6,13, 95% ДИ= 1,45–25,86; если прикорм введен старше 6 месяцев ОШ= 9,70, 95% ДИ= 2,47–38,15.
Проведенный анализ литературы и данные собственных исследований позволили нам выделить дополнительные факторы риска, обладающие значимым эффектом программирования будущего здоровья детей. Их можно разделить на две группы: корригируемы и некорригируемые.
К корригируемым факторам риска относятся такие факторы, как вакцинация ребенка, избыточный вес и ожирение детей, применение лекарственных препаратов в неонатальном периоде, аэроаллергены, нарушение барьерной функции кожи, изменение микробиома, наличия в доме плесени, перьевых или пуховые подушек, одеял и др. предметов.
К некоррегируемым факторам риска относятся такие факторы, как течение беременности и родов, месяц рождения ребенка. Таких детей, особенно с осложненным генетическим анамнезом, следует выделять в особую группу риска.
Соответственно, именно этим детям необходимо проводить вакцинацию с дополнительными вакцинами, что предотвратит развитие аллергических заболеваний. Также необходимо правильное питание, соответствующее режиму с правильным соотношением белков, жиров и углеводов, чтобы предотвратить появление избыточного веса и ожирения у детей. При нарушении барьерной функции кожи следует использовать эмоленты на первом году жизни. При изменении микрообиома следует, во-первых, применение курса мепробиотиков, а, во-вторых, следить за разнообразным питанием, которое обогащает микробиом. Контролировать и не допускать в доме наличия плесени, перьевых или пуховые подушек, одеял и других предметов.
