СТАНДАРТИЗАЦИЯ ПОЛУПРОДУКТА (ФИЛАМЕНТОВ) ПРИ ПОЛУЧЕНИИ ТАБЛЕТОК МЕТОДОМ ТРЕХМЕРНОЙ ПЕЧАТИ
СТАНДАРТИЗАЦИЯ ПОЛУПРОДУКТА (ФИЛАМЕНТОВ) ПРИ ПОЛУЧЕНИИ ТАБЛЕТОК МЕТОДОМ ТРЕХМЕРНОЙ ПЕЧАТИ
Аннотация
Цель. Разработка методик оценки качества полупродукта печатных таблеток индапамида – филаментов, полученных экструзией расплава, и количественного определения индапамида в них.
Материалы и методы. Филаменты индапамида получали экструзией расплава на двухшнековом лабораторном экструдере Haake™ miniCTW (Thermo Fisher Scientific, Германия). Высвобождение индапамида из филаментов и таблеток Арифон® изучали с использованием тестера растворения Erweka DT 626/1000 HH (ERWEKA GmbH, Германия). Содержание индапамида в филаментах, однородность дозирования, а также количество перешедшего в среду растворения вещества определяли спектрофотометрически (спектрофотометр СФ-2000, ООО «ОКБ Спектр», Россия).
Результаты. Изучена совместимость индапамида с полимерами Kollidon® VA 64 и Soluplus®. Разработана методика и обоснованы условия проведения теста «Растворение» для филаментов как полупродукта печатных таблеток индапамида, растворимых в желудке: аппарат «Лопастная мешалка», скорость вращения – 100 об/мин, среда растворения – раствор 0,1 М кислоты хлористоводородной, объем среды растворения – 500 мл. За 15 мин должно высвободиться не менее 85% индапамида от заявленного содержания.
Заключение. Разработаны методики для оценки качества филаментов, содержащих индапамид: методика количественного определения индапамида в филаментах, испытания «Однородность дозирования» и теста «Растворение». Альтернативным аппаратом для изучения высвобождения индапамида из филаментов, в связи с его низким процентным содержанием, может быть аппарат «Проточная ячейка». Аналогичным образом можно адаптировать методики количественного определения в филаментах других субстанций.
1. Введение
Последние десятилетия в системе здравоохранения наметились изменения, характеризующиеся появившейся и активно развивающейся тенденцией перехода от массовой к персонализированной медицине , . Персонализация заключается в подборе оптимальной лекарственной формы (ЛФ) конкретного фармакологически активного вещества в дозировке, определенной на основании фармакокинетических и фармакогеномных данных пациента , , . Это особенно важно для таких групп населения как новорожденные, пациенты детского и пожилого возраста и др. , . Применение индивидуально подобранных лекарственных средств (ЛС) поможет повысить не только эффективность терапии, но и приверженность пациента предписанному врачом лечению , .
Точная доза активной фармацевтической субстанции (АФС) для достижения оптимального терапевтического эффекта необходима при лечении многих заболеваний, среди которых можно выделить сердечно-сосудистые патологии, и особенно артериальную гипертензию (АГ). Для лечения АГ широко используются диуретические ЛС, оказывающие выраженный антигипертензивный эффект , . Одним из представителей данной группы препаратов является индапамид, широко используемый в монотерапии АГ, а также совместно с другими антигипертензивными ЛС .
Таблетки как лекарственная форма широко представлены на фармацевтическом рынке. Однако появление новых технологий, в частности, трёхмерной печати, позволило из ранее известных ЛС, используя аддитивные технологии, получать лекарственные препараты (ЛП) принципиально новым способом , , . Таблетки могут быть напечатаны в соответствии с нуждами и требованиями пациента на любых этапах лечения, включая профилактику и диагностику , , .
Одним из видов аддитивного производства является печать послойным наплавлением (Fused Deposition Modeling, или FDM-печать) , . Данный вид печати заключается в расплавлении материала, содержащего действующее вещество, и осаждении его слоями с целью получения твердого объекта определенной геометрической формы .
Для производства твердых дозированных ЛФ по технологии FDM-печати необходим полупродукт в виде нити – филамента. К филаментам предъявляется ряд требований :
- постоянный диаметр по всей длине филамента;
- пластичность;
- температура плавления филамента не должна превышать допустимых температур нагрева печатающей головки.
Материал филамента также должен обеспечивать адгезию первого слоя с рабочей поверхностью принтера, а АФС должна быть распределена равномерно по всему объему филамента.
В связи с интеграцией технологии трехмерной печати в фармацевтическую разработку персонализированных ЛС становится актуальной разработка показателей качества и методик их определения для филаментов, как полупродукта, от которого зависит качество готового ЛП.
2. Методы и принципы исследования
2.1. Субстанция
Субстанция: индапамид (АО «Активный компонент», Россия, серия 10220); вспомогательные вещества: сополимер поливинилпирролидона и винилацетата Kollidon® VA64 (BASF, Германия), ПЭГ 6000-винилкапролактам-винилацетат Soluplus® (BASF, Германия), стеарат магния («Peter Greven Nederland C.V.», Нидерланды); Арифон® таблетки, покрытые пленочной оболочкой, 2,5 мг (производства «Лаборатории Сервье Индастри», Франция, серия 6006406); реактивы: вода очищенная, кислота хлористоводородная, ос.ч. (АО «ВЕКТОН», Россия), этанол 96%.
2.2. Оборудование
Двухшнековый лабораторный экструдер Haake™ miniCTW, Thermo FisherScientific (Германия); штангенциркуль электронный Matrix; тестер растворения Erweka DT626/1000 HH (Германия), спектрофотометр СФ-2000 (ООО «ОКБ Спектр», Россия); весы лабораторные СЕ 224-С (Сартогосм, Россия).
2.3. Приготовление филамента, содержащего индапамид
Индапамид и Kollidon® VA 64 смешивали вручную, используя ступку и пестик. Содержание индапамида в филаментах составляло 2; 4 и 6%. Полученную смесь загружали в питатель экструдера и экструдировали при постоянной температуре 135 °С через сопло диаметром 0,5 мм при скорости вращения шнеков 20 об/мин.
Филаменты, содержащие 2% индапамида и Soluplus®, получали аналогичным образом при температуре 125 °С через сопло диаметром 0,5 мм при скорости вращения шнеков 20 об/мин.
2.4. Оценка совместимости полимеров с индапамидом
Готовили растворы индапамида и физических смесей полимеров Kollidon® VA 64 и Soluplus® с индапамидом в 0,1 М растворе хлористоводородной кислоты. Снимали их ультрафиолетовые (УФ) спектры поглощения.
2.5. Количественное определение индапамида в филаментах
Навеску филаментов, содержащих индапамид, отбирали путем отламывания частей одинаковой длины от исходного филамента. Отрезки имели длину (10 ± 2) мм и массу около 50, 25 и 20 мг для филаментов с содержанием индапамида 2; 4 и 6%, соответственно (рисунок 1).

Рисунок 1 - Внешний вид навесок филамента для проведения испытаний
Приготовление раствора рабочего стандартного образца (РСО) индапамида: около 25 мг (точная навеска) РСО индапамида помещали в мерную колбу вместимостью 25 мл, растворяли в этаноле 96 %, и доводили объем раствора тем же растворителем до метки (раствор А). В мерную колбу вместимостью 200 мл помещали 1,0 мл раствора А и доводили объем 0,1 М раствором кислоты хлористоводородной до метки.
Количественное содержание индапамида определяли спектрофотометрически в кювете из кварцевого стекла с толщиной поглощающего слоя 10 мм в интервале длин волн от 220 нм до 350 нм.
2.6. Определение однородности дозирования
Условия для испытания подбирались в соответствии с требованиями ОФС.1.4.2.0008 «Однородность дозирования» Государственной Фармакопеи (ГФ) Российской Федерации (РФ) XV издания.
Для определения однородности дозирования индапамида в филаментах на основе полимера Kollidon® VA 64 использовался метод спектрофотомерии в УФ-области спектра. Навеску филаментов, содержащих индапамид, отбирали путем отламывания частей одинаковой длины из разных точек исходного филамента. Приготовление испытуемого раствора и раствора РСО проводилось аналогично методике количественного определения.
2.7. Изучение высвобождения индапамида из филаментов
За основу была взята методика количественного определения индапамида в таблетках и адаптирована для филаментов, содержащих индапамид . Испытание «Растворение» для филаментов проводили также по адаптированной методике, предлагаемой для таблеток Арифон® («Лаборатории Сервье Индастри», Франция). В качестве среды растворения использовали 0,1 М раствор кислоты хлористоводородной объемом 500 мл. Температура среды находилась в диапазоне (37 ± 0,5) °C. Испытание проводили в аппарате «Лопастная мешалка» со скоростью вращения 100 об/мин. Для построения профиля высвобождения отбирали пробы через 10, 15, 20, 30, 45 и 60 мин.
Навески для испытания «Растворение» представляли собой отрезки филамента длиной (10 ± 2) мм, аналогично определению количественного содержания индапамида.
3. Основные результаты
Исследование включало несколько этапов: оценку совместимости полимеров с индапамидом; разработку методик количественного определения индапамида в филаментах; разработку методики для проведения испытания «Однородность дозирования» и разработку методики теста «Растворение» для филаментов с индапамидом.
3.1. Оценка совместимости полимеров с индапамидом
Филаменты получали путем смешивания и дальнейшей экструзии смеси индапамида и полимера-носителя, поэтому первоначально необходимо было установить совместимость исходных компонентов. Для этого были сняты ультрафиолетовые спектры поглощения субстанции индапамида и 0,05 % растворов физических смесей полимеров Kollidon® VA 64 и Soluplus® с индапамидом в 0,1 М растворе хлористоводородной кислоты (рисунки 2 и 3, соответственно). В качестве среды растворения была выбрана кислота хлористоводородная как имитация кислой среды желудка, в которой заявлено растворение будущей ЛФ.
Установлено, что УФ спектр физической смеси полимера Kollidon® VA 64 с индапамидом имеет максимум при 242 нм и плечи при 279 и 287 нм, характерные для субстанции индапамида (рисунок 2). Стоит отметить, что полимер способен поглощать излучение в том же диапазоне длин волн, что и индапамид; впоследствии этот факт учитывался при расчетах количественного содержания индапамида в образцах.
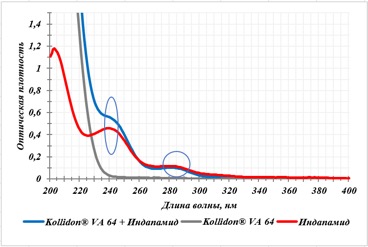
Рисунок 2 - Спектры поглощения субстанции индапамида, полимера Kollidon® VA 64 и их физической смеси
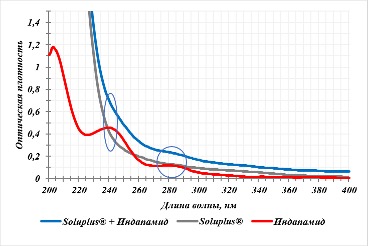
Рисунок 3 - Спектры поглощения субстанции индапамида, полимера Soluplus® и их физической смеси
3.2. Количественное определение индапамида в филаментах
Далее необходимо было разработать методику количественного определения индапамида в филаментах. За основу была взята методика определения индапамида в таблетках, валидированная со следующими характеристиками: RSD = 0,13%, R2=0,975.
Содержание индапамида в филаментах составило (1,90 ± 0,04)%; (3,77 ± 0,08)% и (5,70 ± 0,13)%, что соответствовало 95,1%; 94,2% и 95,0% от заявленного количества для филаментов с индапамидом 2; 4 и 6%. Данный показатель необходимо учитывать при разработке спецификации качества на препарат.
3.3. Однородность дозирования
Поскольку филамент – это полупродукт для производства дозированной ЛФ – таблетки, на следующем этапе исследования проводилась разработка методики для проведения испытания «Однородность дозирования». Условия для испытания подбирались в соответствии с требованиями ОФС.1.4.2.0008.18 «Однородность дозирования» ГФ РФ XIV издания.
Для определения однородности дозирования индапамида в филаментах на основе полимера Kollidon® VA 64 использовался метод спектрофотомерии в УФ-области спектра. Взятие навески филамента, приготовление испытуемого раствора и раствора РСО проводилось аналогично методике количественного определения, описанной выше.
Результаты испытания, полученные на 10 навесках филаментов каждой концентрации, приведены в таблице 1. Из представленных данных следует, что образцы филаментов, изготовленные на основе полимера Kollidon® VA 64 и содержащие 2; 4 и 6% индапамида, однородны.
Таблица 1 - Результаты проведения испытания «Однородность дозирования» для филаментов, изготовленных на основе полимера Kollidon® VA 64
Наименование показателя | Содержание индапамида в филаменте, % | ||
2 | 4 | 6 | |
Содержание АФС в 1 навеске (в % от номинального значения), | x1 = 94,50 x2 = 98,00 x3 = 94,00 x4 = 94,00 x5 = 92,50 x6 = 93,00 x7 = 96,50 x8 = 94,50 x9 = 97,50 x10 = 96,50 | x1 = 93,50 x2 = 97,25 x3 = 92,75 x4 = 93,25 x5 = 96,00 x6 = 96,25 x7 = 95,25 x8 = 90,50 x9 = 92,25 x10 = 95,25 | x1 = 92,50 x2 = 97,17 x3 = 94,00 x4 = 97,50 x5 = 92,50 x6 = 97,50 x7 = 94,33 x8 = 92,67 x9 = 94,83 x10 = 97,17 |
Среднее арифметическое значений (%), = | 95,10 | 94,23 | 95,02 |
Константа приемлемости, k | 2,4 | ||
Стандартное отклонение, s s = | 1,90 | 2,11 | 2,14 |
Эталонное значение дозы (% от номинального значения), M | 98,5 | ||
Первый показатель приемлемости (%), AV AV = | 7,95 | 9,33 | 8,62 |
Максимально допустимое значение АV(%), L1 | 15,0 | ||
Интерпретация результата | AV ≤ L1 Филамент однороден | ||
Примечание: АФС – активная фармацевтическая субстанция
3.4. Разработка методики теста «Растворение» для филаментов с индапамидом
В настоящее время индапамид представлен на фармацевтическом рынке РФ в виде таблеток, для которых имеется тест «Растворение». Методику данного испытания было решено использовать и для филаментов.
Было проанализировано по 12 образцов навесок филаментов, изготовленных на основе полимера Kollidon® VA 64, и содержащих 2; 4 и 6% индапамида. Профили высвобождения индапамида из филаментов на основе полимера Kollidon® VA 64 представлены на рисунке 4.
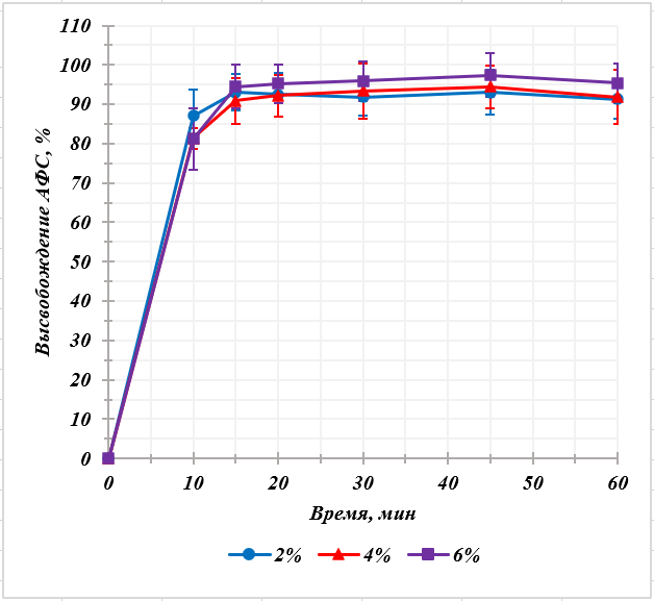
Рисунок 4 - Профили высвобождения индапамида из филаментов с различным содержанием АФС
4. Заключение
Разработаны методики оценки качества филаментов, содержащих индапамид. Определение количественного содержания индапамида в филаментах, а также испытание «Однородность дозирования» рекомендовано проводить методом спектрофотометрии при длинах волн от 220 до 350 нм в среде 0,1 М кислоты хлористоводородной. Сделан вывод, что отбор пробы филаментов для анализа необходимо осуществлять путем получения отрезка филамента определённой длины.
Разработана методика и обоснованы условия проведения теста «Растворение» для филаментов как полупродукта печатных таблеток индапамида, растворимых в желудке: аппарат «Лопастная мешалка», скорость вращения – 100 об/мин, среда растворения – раствор 0,1 М кислоты хлористоводородной, объем среды растворения – 500 мл. За 15 мин должно высвободиться не менее 85 % индапамида от заявленного содержания.
Подходы к разработке методик определения количественного содержания индапамида в филаментах можно перенести на разработку методик определения других АФС, схожих по свойствам.
Так как на данный момент нет нормативных документов, регламентирующих требования к контролю качества филаментов и напечатанных ЛФ, необходимо продолжить исследования на напечатанных ЛФ и филаментах, содержащих другие АФС.
