ПРОБЛЕМА ПРИМЕНЕНИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ «OFF-LABEL» В РОССИИ
ПРОБЛЕМА ПРИМЕНЕНИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ «OFF-LABEL» В РОССИИ
Научная статья
Кузнецова Е.Ю.1, Овчинникова П.П.2, *, Семёнчева А.С.3
1 ORCID: 0000-0002-6491-0287;
2 ORCID: 0000-0001-6657-8356;
3 ORCID: 0000-0002-2072-9355;
1, 2, 3 СГМУ им. В.И. Разумовского, Саратов, Россия
* Корреспондирующий автор (ovchinnikova.11b[at]gmail.com)
АннотацияВ статье всестороннее исследовано понятие «off-label» терапии, которое отсутствует в российском законодательстве. Рассмотрены процедура и критерии ее применения в России и зарубежных странах. Проанализирована судебная практика по вопросу использования лекарственных препаратов вне инструкции, изучено мнение российских врачей по данному вопросу. Авторы приходят к выводу о необходимости закрепить в российском законодательстве понятие «off-label» терапии, а также расширить критерии использования лекарств «off-label».
Ключевые слова: терапия вне инструкции, терапия, off-label, лекарственные препараты, международные стандарты.
THE PROBLEM OF APPLYING "OFF-LABEL" MEDICATION IN RUSSIA
Research article
Kuznetsova E.Yu.1, Ovchinnikova P.P.2, *, Semencheva A.S.3
1 ORCID: 0000-0002-6491-0287;
2 ORCID: 0000-0001-6657-8356;
3 ORCID: 0000-0002-2072-9355;
1, 2, 3 Saratov State Medical University named after V. I. Razumovsky; Saratov, Russia
* Corresponding author (ovchinnikova.11b[at]gmail.com)
AbstractThe article comprehensively examines the concept of "off-label" therapy, which is missing from the Russian legislation. The authors consider the procedure and criteria for its application in Russia and other countries. The article analyses the court practice on the usage of non-instructed medication and examines the opinion of Russian doctors on this issue. The authors conclude that it is necessary to fix the concept of "off-label" therapy in Russian legislation and to expand the criteria for using "off-label" medication.
Keywords: non-instructed therapy, therapy, off-label, medication, international standards.
ВведениеТерапия «вне инструкции» («off-label») – использование медицинских средств и препаратов согласно рекомендациям, лекарственной форме, дозировке для популяции, с учетом других критериев применения, которые не были прописаны в лекарственном препарате (ЛП) [1]. Таким образом, данная схема лечения не утверждена государственными органами, регулирующими обращение лекарственных средств. К «off-label» терапии принято относить обращение незарегистрированных в стране ЛП, а именно тех, на которых нет лицензии (unlicensed). Кроме того, к ней принято относить потребление зарегистрированных ЛП, которые по показаниям, дозировке, лекарственным формам и путям введения в организм не соответствуют утвержденной инструкции.
Врачи всех стран неизбежно сталкиваются с потребностью выписывать ЛП «off-label», поэтому в некоторых государствах указанную терапию утвердили законом, с контролем ее применения. В США, Евросоюзе контроль в медицине за использование препаратов «вне инструкции» осуществляют те же органы государственной власти, которые ответственны за осуществление клинических исследований, регистрирование, реализацию на территории государства медицинских средств и лекарств.
В США – FDA [2] (Food and Drug Administration – Управление по санитарному надзору за качеством пищевых продуктов и медикаментов), на официальном Интернет-ресурсе которого в понятной форме для врачей и пациентов указаны сведения об использовании препаратов «вне инструкции»: условия и принципы их применения для лечения больных. Управление, с одной стороны, строго регламентирует назначение ЛП, но, с другой стороны, предоставляет врачам относительную свободу. При необходимости доктор может выслать запрос производителю лекарства о возможности его применения в другой дозировке. Если производитель подтвердит, что для осуществления терапии можно назначать другую дозировку, то данной информации достаточно для применения препарата в иной дозировке.
В странах Европы было сформировано Европейское агентство лекарственных средств EMA [3] (European Medicines Agency – агентство по оценке ЛП на их соответствие параметрам, описанным в Европейской Фармакопее). Оно занимается проверкой потребления лекарств, включая «вне инструкции», взаимодействует с медицинскими организациями, врачами, занимающимися частной практикой, с целью определения побочных эффектов, способных стать поводом для изъятия из обращения данного препарата на территории Европы [4]. Кроме национальных исследований европейские государства могут апеллировать к результатам общеевропейских научных изысканий, что позволяет существенно расширить доказательную базу при назначении препаратов «вне инструкции».
Бесконтрольное использование ЛП «off-label» может являться причиной возникновения весьма отрицательных последствий как для врачей, так и для обратившихся к ним пациентов. Произошедший во Франции в 2011 году случай указывает на необходимость обязательного законодательного регулирования применения и контроля медицинских средств «off-label». Препарат «Медиатор» (Mediator) выпускался с 1976 года и сначала прописывался только диабетикам, страдавшим от лишнего веса. Чуть позже он был рекомендован людям, желающим избавиться от избыточной массы тела, при этом являющимся абсолютно здоровыми. Позже выяснилось, что данный препарат оказывал негативное влияние на сердечно-сосудистую систему, что приводило к летальным исходам. Погибло более 500 человек, а многие исследователи озвучивают более страшные цифры: 2 тысячи смертей и до 3,5 тысячи тяжело заболевших. Описанный случай стал поводом для ужесточения мер контроля обращения лекарств во Франции [5].
В 2007 году больничные кассы Федеративной Республики Германии, выступающие в качестве страховых фондов, которые оплачивают лечение застрахованных жителей, врачебные палаты, защищающие интересы врачей, союзы фармакологических организаций пришли к единому мнению по поводу использования препаратов «off-label». Данные организации согласовали назначение лекарственных препаратов без инструкции при выполнении трех кумулятивных параметров [6]:
1) наличие тяжелого заболевания, угрожающего жизни человека, значительно ухудшающее его здоровье;
2) недоступность специфических или иных лечебных средств;
3) наличие данных о необходимости оказания больному паллиативной помощи.
Результатом многочисленных работ над принципами регулирования, правилами использования ЛП «вне инструкции» на общем европейском уровне стал проект Декларации о надлежащей практике использования лекарств не по назначению (Declaration on Good Off-Label Use Practice, в 2015 году) [7]. В июне 2016 г. этот документ был одобрен 30 профессиональными союзами медицинских работников Европы, общественными объединениями пациентов, среди которых наиболее известны European Federation of Neurological Associations, European Medical Association, European Confederation of Pharmaceutical Entrepreneurs. В Декларации были значительно расширены и детализированы критерии использования лекарств «off-label»:
1) наличие медицинской необходимости, основанной на полученных данных при осмотре и обследовании пациента;
2) отсутствие лицензированных альтернатив терапии, приемлемых для пациента;
3) обзор и критическая оценка имеющихся научных данных по определенному лекарственному препарату, что необходимо для принятия решения о непрямом использовании препарата в конкретном случае;
4) пациентам (или их законным представителям) должна быть предоставлена полная информация о назначенной терапии;
5) фиксация результатов применения в определенных документах, что важно для прогноза неблагоприятных событий, которые возникают при применении лекарств не по назначению.
Согласно статистическим данным «off-label» терапия чаще всего используется в педиатрической и онкологической практике. К данному виду терапии в педиатрии относится назначение антигипертензивных препаратов детям, имеющим сердечно-сосудистые заболевания, а также анальгетиков при болевом синдроме, психотропных препаратов – при болезнях центральной нервной системы. Это связано с тем, что производители ЛП не могут проводить клинические исследования на детях, в результате чего обязаны указывать в инструкции возрастные ограничения. Поэтому для детей в педиатрии во многих случаях отсутствуют аналоги лекарств, применяемых для лечения взрослых людей. Согласно зарубежным исследованиям частота назначений «вне инструкции» находится в широком диапазоне. А в определенных государствах она может составлять 80% [8],[9].
На официальном сайте Министерства здравоохранения Российской Федерации 30 января 2020 года были размещены временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекции (2019-nCoV)» [10], в которых в главе 4 было отмечено отсутствие этиотропный терапии с позиции доказательной медицины для лечения 2019-nCoV инфекции. Кроме того, в настоящее время отсутствуют ЛП, применение которых включают коронавирусную инфекцию, вызванную штаммом 2019-nCoV. Таким образом, упомянутые в методических рекомендациях лекарственные препараты применяются для лечения коронавирусной инфекции на основании анализа опыта их применения «офф-лейбл».
Порядок применения препаратов«off-label» в российском здравоохранении регламентируется п. 15 ст. 37 ФЗ 323 «Об охране здоровья граждан в Российской Федерации» [11], в соответствии с которым применение лекарственных средств, не входящих в список клинических рекомендаций, возможно по решению врачебной комиссиив случаях индивидуальной непереносимости или по жизненным показаниям. Согласно ПриказуМинздраваРоссииот 2 декабря 2013 года № 886н «О внесении изменений в порядок создания и деятельности врачебной комиссии медицинской организации, утвержденный приказом Министерства здравоохранения и социального развития Российской Федерации от 5.05.2012г. N 502н, и в порядок назначения и выписывания лекарственных препаратов, утвержденный приказом Министерства здравоохранения Российской Федерации от 20.12.2012г. N 1175н»[12], врачебная комиссия назначается по приказу руководителя медицинской организации. Положение о врачебной комиссии, порядок ее работы, состав комиссии утверждаются руководителем медицинской организации. Врачебная комиссия включает в себя председателя, одного или двух заместителей председателя, секретаря и членов комиссии. Руководитель медицинской организации или заместитель руководителя медицинской организации, как правило, является председателем врачебной комиссии. В состав врачебной комиссии входят заведующие структурными подразделениями медицинской организации, врачи-специалисты из числа работников медицинской организации. Заседания врачебной комиссии проводятся не реже одного раза в неделю на основании планов-графиков, утверждаемых руководителем медицинской организации, а также, при необходимости, могут проводиться внеплановые заседания врачебной комиссии по решению руководителя медицинской организации. Решение врачебной комиссии оформляется протоколом, который вносится в медицинскую карту больного. Выписка из протокола предоставляется пациенту или его законному представителю по его заявлению. При вынесении решения врачебная комиссия руководствуется действующим законодательством в сфере здравоохранения.
Вместе с тем, в документах отсутствуют чёткие критерии применения препаратов «off-label» врачами, что является правовой неопределенностью их назначения и применения, которая приводит к отрицательным последствиям профессиональной деятельности российских врачей и может весьма негативно сказаться на здоровье пациентов.
Например, основным показанием для назначения препарата «Сайтотек» является язвенная болезнь желудка и двенадцатиперстной кишки. В 2016 г. в республике Дагестан он применялся «вне инструкции», а именно, для прерывания беременности, что привело к летальному исходу молодой женщины. Родители погибшей обратились в суд с иском для возмещения вреда. Во время разбирательства было установлено, что причиной смерти стало применение «off-label» препарата «Сайтотек». В итоге, суд требования истцов удовлетворил, а медицинское учреждение было привлечено к гражданско-правовой ответственности [13].
В 2014 году в г. Улан-Удэ была осуждена фельдшер, которая выполнила пациенту инъекцию антибиотика «Цефтриаксон», предварительно разбавив препарат раствором для инъекций «Лидокаин-буфус». В результате проведенной медицинской манипуляции пациент скончался. В ходе судебного разбирательства было выяснено, что, согласно инструкции к Цефтриаксону, его разведение лидокаином не предусмотрено. Фельдшер скорой помощи была приговорена к лишению свободы согласно части 2 ст. 109 УК РФ («Причинение смерти по неосторожности вследствие ненадлежащего исполнения лицом своих профессиональных обязанностей») [14].
Методы и принципы исследованияС целью изучения реальной практики назначения лекарственных препаратов «off-label» в России нами было проведено анкетирование среди 168 врачей различных специальностей и категорий, работающих в государственных и муниципальных медицинских организациях г. Саратова. Каждому респонденту следовало ответить на вопросы анкеты анонимно, указав лишь данные о соответствующей профессиональной категории, специальности (см. рисунок 1), стаже и месте работы на специально предусмотренном индивидуальном бланке. Каждый вопрос предусматривал от одного до нескольких правильных ответов.
Полученные данные были обработаны и занесены в статистические таблицы программы Microsoft Excel для дальнейшего изучения. В ходе исследования нами были получены результаты, составлены диаграммы.
Основные результаты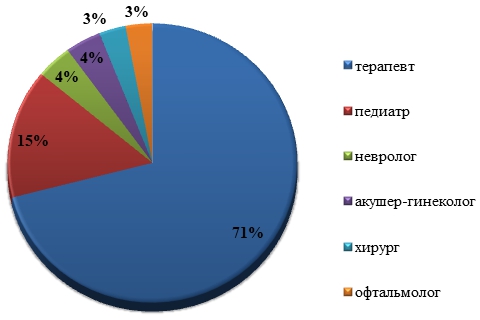
Рис. 1 – Структура специальностей респондентов в %
Средний возраст и стаж врачей женщин составил 39 и 12 лет соответственно, у врачей мужчин – 44 и 16 лет. Большая часть опрошенных, а именно – 72%, имеет высшую категорию, вторую – 17%, третью – 11%.
Все без исключения участники анкетирования считают, что врачу следует руководствоваться при назначении лекарственного препарата инструкцией к нему, при этом 96% из них добавляют, что необходимо в индивидуальном порядке учитывать его переносимость конкретным пациентом. 47% опрошенных врачей руководствуются клиническими рекомендациями по нозологии пациента, а 26% используют свой клинический опыт.
Знакомы с проблемой назначения лекарственных препаратов «off-label» 68% опрошенных.
62,5% респондентов согласились с необходимостью назначения препаратов «вне инструкции», при этом 65% из них сталкиваются с необходимостью назначения ЛП «off-label» довольно часто (примерно 2-3 раза в месяц), а 35% встречались с подобными назначениями единожды.
Исходя из практики врачей основными причинами назначения ЛП «off-label» являются «отсутствие альтернативных методов лечения», необходимость оказания паллиативной помощи тяжело больным пациентам (см. рисунок 2).
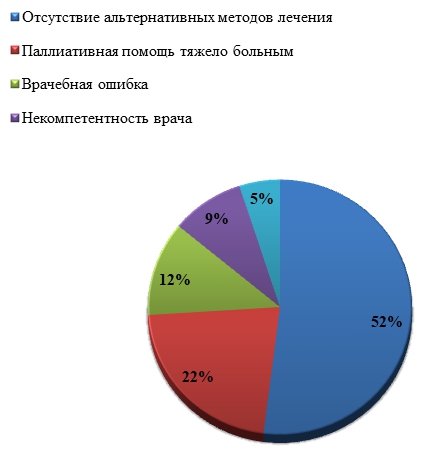
Рис. 2 – Распределение причин назначения терапии вне инструкции в %
Чаще всего назначают ЛП вне инструкции терапевты и педиатры. Из всех опрошенных терапевтов 82% используют данную практику, а педиатры её применяют все без исключения.
ЗаключениеТаким образом, проблема назначения лекарственных препаратов вне инструкции, или «off-label» существует и в российской системе здравоохранения. Врачи всех специальностей без исключения сталкиваются с необходимостью назначения ЛП «off-label». Отсутствие в российском законодательстве регламентации применения «off-label» терапии лишает пациентов возможности лечения тяжелых случаев заболеваний, при которых нет альтернативных методов лечения. Сложившаяся судебная практика по «off-label» терапии заставляет врачей не применять её на практике, что не является правильным и не соответствует интересам пациентов. Для решения этих проблем считаем необходимым закрепить в российском законодательстве понятие «off-label» терапии, а также критерии использования лекарств «off-label».
| Благодарности Авторы выражают благодарность Басовой Алле Викторовне, к.ю.н., доценту кафедры общественного здоровья и здравоохранения (с курсами правоведения и истории медицины) СГМУ им. В.И. Разумовского за ценные советы при планировании исследования и рекомендации по оформлению статьи. | Acknowledgement Authors express their gratitude to Basova Alla Viktorovna, PhD in Jurisprudence, associate professor of the Department of public health with courses in law and history of medicine Saratov State Medical University named after V. I. Razumovsky for valuable advice in planning research and recommendations for the design of the article. |
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Вольская Е. Off-label: зона риска. Назначения вне инструкции – пределы и возможности / Е. Вольская // Ремедиум. Журнал о российском рынке лекарств и медицинской технике – 2008 – №4. – С. 6-10.
- U.S. Food and Drug Administration [Electronic resource] - URL: https://www.fda.gov (accessed: 02.12.2019).
- European Medicines Agency. Official website of the European medicines Agency [Electronic resource] - URL: https://www.ema.europa.eu/en. (accessed: 02.12.2019).
- Официальный сайт 1 канала. Новости [Электронный ресурс] / Во Франции предстанет перед судом глава одной из крупнейших фармацевтических компаний – URL: https://www.1tv.ru/news/2011-09-22/113385vo_frantsii_predstanet_pered_sudom_ glava_odnoy_iz_krupneyshih_farmatsevticheskih_kompaniy (дата обращения: 02.12.2019).
- Марцевич С.Ю. Назначение лекарственных средств не в соответствии с официальной инструкцией по медицинскому применению (off-label). Возможные причины, виды и последствия. Правовое регулирование в Российской Федерации / Марцевич С. Ю., Навасардян А. Р., Комкова Н. А. // Рациональная фармакотерапия в кардиологии. – 2017. – №5. – С. 667-675.
- Резников Д. Организация медицинской помощи больным в Германии. Принципы и основы страховой медицины / Д. Резников // Вестник современной клинической медицины. – 2010. – №2. – С. 66-73.
- Declaration on Good Off-Label Use Practice. [Electronic resource] – URL: http://www.braincouncil.eu/golup/wp-content/uploads/2015/05/GOLUP-declaration.pdf (accessed:12.2019).
- Lifshitz M. Off label and unlicensed use of antidotes in paediatric patients / Lifshitz M., Gavrilov V., Gorodischer R. // Eur J Clin Pharmacol. – 2001. –P. 839-841.
- Incidence of unli-censed and off-label prescription in children / Langerova P., Vrtal J., Urbanek K.// ItalJPediatric. – 2014 –P. 12-14.
- Официальный сайт Министерства здравоохранения Российской Федерации [Электронный ресурс] – URL: https://static-2.rosminzdrav.ru/system/attachments/attaches/000/049/302/original/Временные_МР_2019-nCov_%2829.01.2020_-_9%291-3.pdf?1580370334 (дата обращения 20.09.2020).
- Российская Федерация. Законы. Об основах охраны здоровья граждан в Российской Федерации: федеральный закон:принят Государственной Думой от 21.11.2011 № 323-ФЗ (ред. от 29.05.2019) // Собрание законодательства РФ. – – № 48. – С. 6724.
- Приказ Минздрава России от 2 декабря 2013 года № 886н «О внесении изменений в порядок создания и деятельности врачебной комиссии медицинской организации, утвержденный приказом Министерства здравоохранения и социального развития Российской Федерации от 5.05.2012г. N 502н, и в порядок назначения и выписывания лекарственных препаратов, утвержденный приказом Министерства здравоохранения Российской Федерации от 20.12.2012г. N 1175н» [Электронный ресурс] – URL:https://www.garant.ru/products/ipo/prime/doc/70451698/ (дата обращения 20.09.2020).
- Решение по делу о компенсации морального вреда в связи с причинением вреда жизни и здоровью [Электронный ресурс] – URL: https://sudact.ru/regular/doc/6vIcquF4dy1e/ (дата обращения: 04.12.2019).
- Решение по делу о причинении смерти по неосторожности вследствие ненадлежащего исполнения лицом своих профессиональных обязанностей [Электронный ресурс] – URL: http://oktiabrsky.bur.sudrf.ru/modules.php?name=press_dep&op=1&did=135 (дата обращения 04.12.2019).
Список литературы на английском языке / References in English
- Vol'skaja E. Off-label: zona riska. Naznachenija vne instrukcii – predely i vozmozhnosti [OFF-LABEL: RISK ZONE. Assignments outside the instructions-limits and possibilities] / Remedium. Zhurnal o rossijskom rynke lekarstv i medicinskoj tehnike [Remedy. Journal of the Russian market of medicines and medical equipment] – 2008 – №4. – p. 6-10. [in Russian]
- FDA.U.S. Food and Drug Administration [Electronic resource] - URL: https://www.fda.gov (accessed: 02.12.2019).
- European Medicines Agency. Official website of the European medicines Agency [Electronic resource] - URL: https://www.ema.europa.eu/en. (accessed: 02.12.2019).
- Oficial'nyj sajt 1 kanala. Novosti [Electronic resource] / Vo Francii predstanet pered sudom glava odnoj iz krupnejshih farmacevticheskih kompanij [The head of one of the largest pharmaceutical companies will appear in court in France]– URL: https://clck.ru/QqVFg (accessed: 02.12.2019). [in Russian]
- Marcevich Sergej Jur'evich. Naznachenie lekarstvennyh sredstv ne v sootvetstvii s oficial'noj instrukciej po medicinskomu primeneniju (off-label). Vozmozhnye prichiny, vidy i posledstvija. Pravovoe regulirovanie v Rossijskoj Federacii [Prescribing medicines is not in accordance with the official instructions for medical use (off-label). Possible causes, types, and consequences. Legal regulation in the Russian Federation] / Marcevich Sergej Jur'evich, Navasardjan Artur Rubenovich, Komkova Nadezhda Alekseevna // Racional'naja farmakoterapija v kardiologii [Rational pharmacotherapy in cardiology] – 2017. – №5. – p. 667-675. [in Russian]
- Reznikov David-Anatol'. Organizacija medicinskoj pomoshhi bol'nym v Germanii. Principy i osnovy strahovoj mediciny [Organization of medical care for patients in Germany. Principles and bases of insurance medicine] // Vestnik sovremennoj klinicheskoj mediciny [Bulletin of modern clinical medicine]. – 2010. – №2. – p. 66-73. [in Russian]
- Declaration on Good Off-Label Use Practice. [Electronic resource] - URL: http://www.braincouncil.eu/golup/wp-content/uploads/2015/05/GOLUP-declaration.pdf (accessed: 04.12.19).
- Lifshitz M. Off label and unlicensed use of antidotes in paediatric patients / Lifshitz M., Gavrilov V., Gorodischer R. // Eur J Clin Pharmacol. – 2001. – P. 839-841.
- Langerova. Incidence of unli-censed and off-label prescription in children / Langerova P., Vrtal J., Urbanek K. // ItalJPediatric. – 2014 – P. 12-14.
- Official website of the Ministry of health of the Russian Federation [Electronic resource]– URL: https://static-2.rosminzdrav.ru/system/attachments/attaches/000/049/302/original/Временные_МР_2019-nCov_%2829.01.2020_-_9%291-3.pdf?1580370334 (accessed: 04.12.19)
- Rossijskaja Federacija. Zakony. Ob osnovah ohrany zdorov'ja grazhdan v Rossijskoj Federacii: federal'nyj zakon: prinjat Gosudarstvennoj Dumoj ot 21.11.2011 № 323-FZ (red. ot 29.05.2019)[Russian Federation. Laws.About the basics of health protection of citizens in the Russian Federation: federallawNo. 323-FZ:[acceptedbyStateDumaon21.11.2011 (ed. from 29.05.2019)] // Sobranie zakonodatel'stva RF. – 2011. – № – P. 6724. [in Russian]
- Order of the Ministry of health of the Russian Federation of December 2, 2013 No. 886n "On amendments to the procedure for creating and operating a medical Commission of a medical organization, approved by the order of the Ministry of health and social development of the Russian Federation of 5.05.2012 N 502n, and the procedure for prescribing and prescribing medicines, approved by the order of the Ministry of health of the Russian Federation of 20.12.2012 N 1175n"[O vnesenii izmenenij v porjadok sozdanija i dejatel'nosti vrachebnoj komissii medicinskoj organizacii, utverzhdennyj prikazom Ministerstva zdravoohranenija i social'nogo razvitija Rossijskoj Federacii ot 5.05.2012g. N 502n, i v porjadok naznachenija i vypisyvanija lekarstvennyh preparatov, utverzhdennyj prikazom Ministerstva zdravoohranenija Rossijskoj Federacii ot 20.12.2012g. N 1175n].[Electronic resource]– URL:https://www.garant.ru/products/ipo/prime/doc/70451698/(accessed: 20.09.2020).[in Russian]
- Reshenie po delu o kompensacii moral'nogo vreda v svjazi s prichineniem vreda zhizni i zdorov'ju [The Decision on the case of compensation for non-pecuniary damage in connection with the infliction of harm to life and health] [Electronic resource] – URL: https://sudact.ru/regular/doc/6vIcquF4dy1e/ (accessed: 04.12.2019).
- Reshenie po delu o prichinenii smerti po neostorozhnosti vsledstvie nenadlezhashhego ispolnenija licom svoih professional'nyh objazannostej [The Decision on the case of causing death by negligence due to improper performance by a person of their professional duties] [Electronic resource] – URL: https://clck.ru/QqVHx (accessed: 04.12.2019).
