MATRIX ELECTROLYTES BASED ON POROUS LAYERS OF AMORPHOUS SILICA WITH GRAFTED AMINOACETATE PVC DERIVATIVES ON CELLULOSE TISSUE AND SODIUM SULFATE ACAVA COMPLEXES
MATRIX ELECTROLYTES BASED ON POROUS LAYERS OF AMORPHOUS SILICA WITH GRAFTED AMINOACETATE PVC DERIVATIVES ON CELLULOSE TISSUE AND SODIUM SULFATE ACAVA COMPLEXES
Abstract
Solid electrolytes consisting of a donor solvent in the form of a porous layer consisting of glycinate PVC derivatives grafted to aerosil microparticles and dissolved sodium sulfate aquacomplexes were synthesized. Samples with mass fractions of aerosil 24.3, 45.9, and 67.1% were synthesized. The solvent sorption volume and solubility of sodium sulfate rise with increasing mass fraction of aerosil. The dependence of the current on the voltage in the circuit Pt (+) - Na2SO4 solution - solid electrolyte bridge - Na2SO4 Pt (-) solution was studied. The length of the bridge is 20 cm, its width is 10 cm. It is shown that electrolyte is a nonlinear ionic conductor, the conductivity and polarizability of which increase in proportion to the concentration of aqua complexes.
1. Введение
Электропроводные пористые слои аминоацетатных производных ПВХ на волокнах ткани с сорбированными аквакомплексами кислот и соединений щелочных металлов, описанные в [1], [2], перспективны как доступные полимерные твердые электролиты, которые на текущий момент не описаны в литературе и не имеют аналогов. Данные материалы в перспективе могут быть использованы как сенсоры, селективные растворители для катионов, в качестве ионных проводников. Стенки пор формируют макромолекулярные сетки из сочлененных циклических аминов с этанольными или ацетатными группами. В них атомы азота – электронодонорные атомы, которые участвуют в формировании сольватных оболочек катионов сорбируемых аквакомплексов. В этом плане слои можно классифицировать как твердые донорные растворители. В электрической цепи с мостиком из твердого электролита, катионы будут двигаться по стенам пор, а анионы в порах. Растворители синтезируют путем обработки тканей суспензией ПВХ в смеси бензилового спирта (БС) и тетрагидрофурана (ТГФ) с последующей одновременной пришивкой ПВХ к поверхности волокон и сшивания линейного полимера в макромолекулярные циклические глицинатные производные с пористой структурой, а электролит – путем сорбции кислот, солей и оснований из растворов. Содержание аквакомплексов около 10-4 ммоль/г, Электропроводность электролитов зависит от природы аквакомплексов, но не превышает 10-8 См. В [3] в эмульсию ПВХ были включены микрочастицы аморфного диоксида кремния типа «аэросил», который проявляет хорошие сорбирующие свойства [4], и на волокнах целлюлозной ткани синтезирован растворитель, в которой полимер через ->Si-O-(CH-CH2-)-(NCH<)-CH2COOK - группы привит к поверхности микрочастиц. Растворимость аквакомплесов сульфата натрия увеличилась на 2 порядка, а электропроводность электролита увеличилась на 5 порядков. Это указывает на то, что в растворимости аквакомплексов участвуют не только донорные атомы в стенках пор полимера, но и донорные атомы кислорода их стенок пор, сформированных группами, через которые полимер привит к аэросилу, а также стенок пор в микрочастицах аэросила. В этом аспекте можно ожидать, что с увеличением содержания аэросила будет возрастать растворяющая способность растворителя и соответственно электропроводность электролита с акавакомплексами сульфата натрия.
Цель работы: синтезировать электролиты из аквакомплексов сульфата натрия, растворенных в пришитом к целлюлозной ткани глицинатными производными ПВХ, привитыми к микрочастицам аэросила, слое с разным содержанием аэросила и методом вольтамперометрии исследовать их электропроводность.
2. Основные результаты
Материалы и реактивы:
Тетрагидрофуран, бензиловый спирт «ч», глицин «ч», гидроокись калия «хч», натрий сернокислой безводный «чда», смола ПВХ, марка SG-7, содержание ПВХ 88% пластификатор – эфиры терефталевой кислоты – около 10%, хлопковая марля, медицинская, отмытая в ТГФ, содержание целлюлозы 97,0-97,5%, плотность 1,45 г/см3. Были приготовлены: 3,33 моль/л раствор глицинат калия, и 1,5 моль/л сернокислого натрия.
Суспензии ПВХ и аэросила: отношение аэросил : ПВХ 1:1 (I) , 2:1 (II), и 3:1 (III). Приготовлены по методике [3]. В смеси из 400 см3 ТГФ и 75 см3 БС с помощью блендера диспергировали 15 г смолы ПВХ (марка SG-7, содержание ПВХ 88%), после чего дозировали 15 (I), 30 (II) или 45 (III) г аэросила, измельчая его до состояния однородной суспензии. Микрофотографирование проводили с помощью оптического микроскопа Motic DMBA 300, увеличение 40х, микрофотографии приведены на рис. 1.

Рисунок 1 - Микрофотографии суспензий
В суспензиях видны шарообразные или элипсообразные микрочастицы аэросила размером от 0,5 до 5 мкм, объединенные в агрегаты. В I – это нити разной формы и длины, в II – агломераты, а III - звезды из коротких нитей. Плотность: 0.941(I), 0.807 (II) 0,762(III) г/см3.
Растворители были синтезированы по методике [3]. Образец марли массы m0 пропитывали эмульсией, выдерживали на воздухе, прогревали при 110о С до удаления ТГФ, измеряли m1 массу образца марли с покрытием геля ПВХ с аэросилом в БС и рассчитывали массу покрытия по формуле mп = m1- m0. Затем образец кипятили в растворе аминоацетата калия, отгоняли БС путем кипячения образца в воде, сушили при 105о, измеряли m2 массу образца марли со слоем и рассчитывали массу слоя mс = m2- m0 и ее массовую долю wсл = mс/m0. Матрица, полученная с суспензией I обозначена как МI, с суспензией II – МII, а с суспензией III – МIII. wсл = 59% (МI), 52% (МII) и 53% (МIII).
Состав слоя был рассчитан используя, значения m0, mп и mс, исходя из следующего. Покрытие состоит из аэросила ПВХ и БС. В покрытии I массовая доля аэросила wАС(п) = 86%, в II = 64%, а в III = 43%. В растворе глицината калия, как соли сильного основания и слабой кислоты, одновременно происходят три реакции с участием ПВХ:
1. >Si-O-H + Cl-CH< + KOH = ->Si-O-CH< + KCl, с помощью которой происходит прививка ПВХ к поверхности аэросила,
2. >С-O-H + Cl-CH< + KOH = ->С-O-CH< + KCl, с помощью которой происходит пришивка ПВХ к поверхности волокон целлюлозы,
3. 2(>CH-Cl) + NH2CH2COOK +2KOH = (>CH-Cl)2NCH2COOK, с помощью которой происходит превращение участков ПВХ в макромолекулярные циклические аминоацетаты. Масса целлюлозы и аэросила в процессе реакций практически не меняется, то есть масса аэросила слое равна его массе в покрытии: mAC = mпwАС(п). Тогда массовая доля аэросила в слое wАС = mAC/ mс равна 24.3 (МI), 45.9 (МII) и 67.1( МIII) %.
Микрофотографии растворителей приведены на рис. 2. Для сравнения приведена микрофотография марли перед пропиткой.
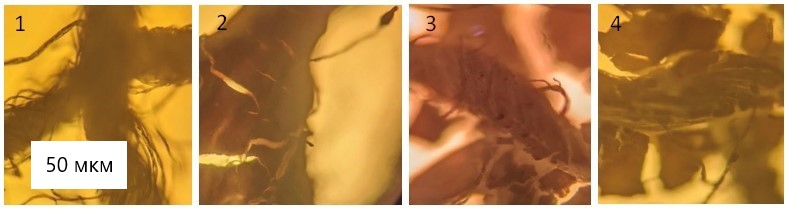
Рисунок 2 - Микрофотографии марли (1), MI (2), MII (3), MIII (4)
Марля состоят из переплетенных волокон, от которых отходят короткие волоконца. В растворителях волокна и волоконцы находятся в оболочках из полимера. В МI слой сформирован на преимущественно волокнах, а в МII и МIII на волокнах и на волокоцах. Микрочастицы аэросила относительно равномерно распределенв в объеме полимера. Плотность упаковки частиц коррелирует с содержанием аэросила.
ИК-спектры отражения растворителей были записаны на ИК -Фурье спектрометр Perkin-Elmer 2000. Они приведены на рис. 3.
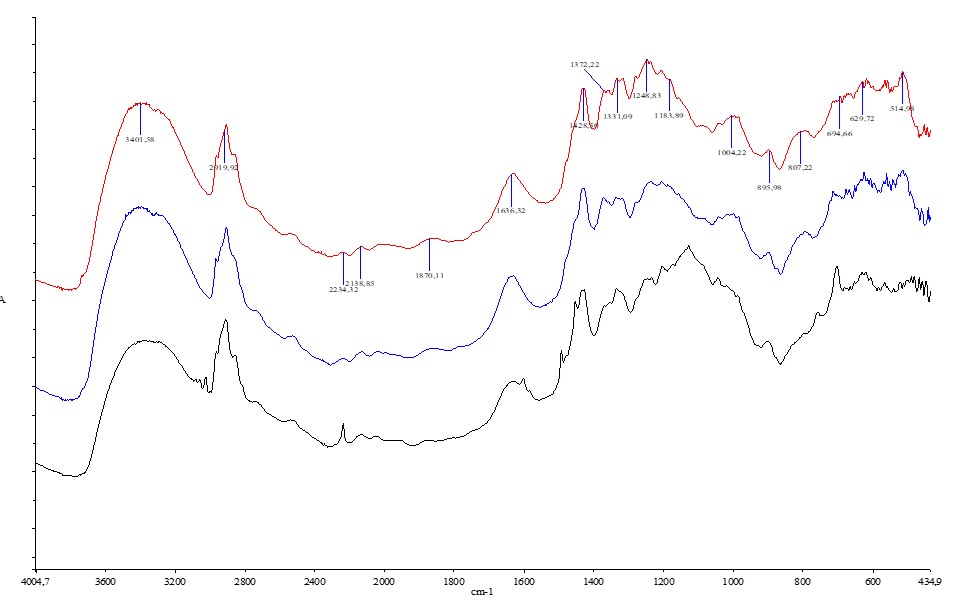
Рисунок 3 - ИК-спектр:
1 - МI, 2 - МII, 3 - МIII
Отнесение полос проводили согласно [5], [6], [7], [8], Во всех случаях имеются полосы 3400 и 3280 см-1 колебаний водородных связей в целлюлозе, в 2920 см-1 – С-Н колебаний в целлюлозе и полимере, 1870 и 1248 см-1 - С=О и С-О колебаний в эфирных группах пластификатора в ПВХ, 1636 и 1438 см-1 - СОО- антисимметричным и симметричным колебаний в глицинатных группах полимера, в 1185 см-1 колебаниям в С-О-С групп, через которые полимер пришит к волокнам целлюлозы, 807 см-1 к колебаниям Si-O-C- групп, через которые полимер привит к поверхности аэросила. Ее интенсивность возрастает с увеличением содержания аэросила. Положение полос - Si-O-Si колебаний в аморфном диоксиде кремния зависят от состава матрицы: в спектре MI имеются полосы 1100, 1065, 1000, 895 и 800 и 796 см-1, в спектре MII – 1090, 1035, 1004, 805 и 800 см-1, а в MIII – 1096, 1038 1020, 895 и 807 см1 и плечо 1128 см-1.
Объем сорбирующих пор был определен весовым методом по количеству воды, поглощаемой из паров. Расчеты проводили по формуле G = (m-m0)/m0, где m0 и m- масса до и после сорбции. G = 0.059, 0.081 и 0.114 см3/г для MI, MII и MIII соответственно.
Электролиты синтезированы следующим образом. Образцы растворителей массы m0 были пропитаны раствором сульфата натрия, отжаты между листами фильтровальной бумаги и высушены до постоянной массы mс при 120о и выдержаны при воздухе (влажность 80 - 100%) до постоянной массы mэ. Электролиты на основе MI, MII и MIII были обозначены как ЭI, ЭII и ЭIII. Содержание сорбированного сульфата натрия и воды рассчитывали по формулам: С(Na2SO4) = (mс- m0)/142*m0 и С(H2O) = (mэ- mс)/18*m0. С(Na2SO4) = 1.65, 2.80 и 3.87 ммоль/г, а С(H2O) = 1.57, 3.6 и 6.96 для ЭI, ЭII и ЭIII соответственно. На рис. 4 приведены ИК-спектры обезвоженных ЭI, ЭII и ЭIII.
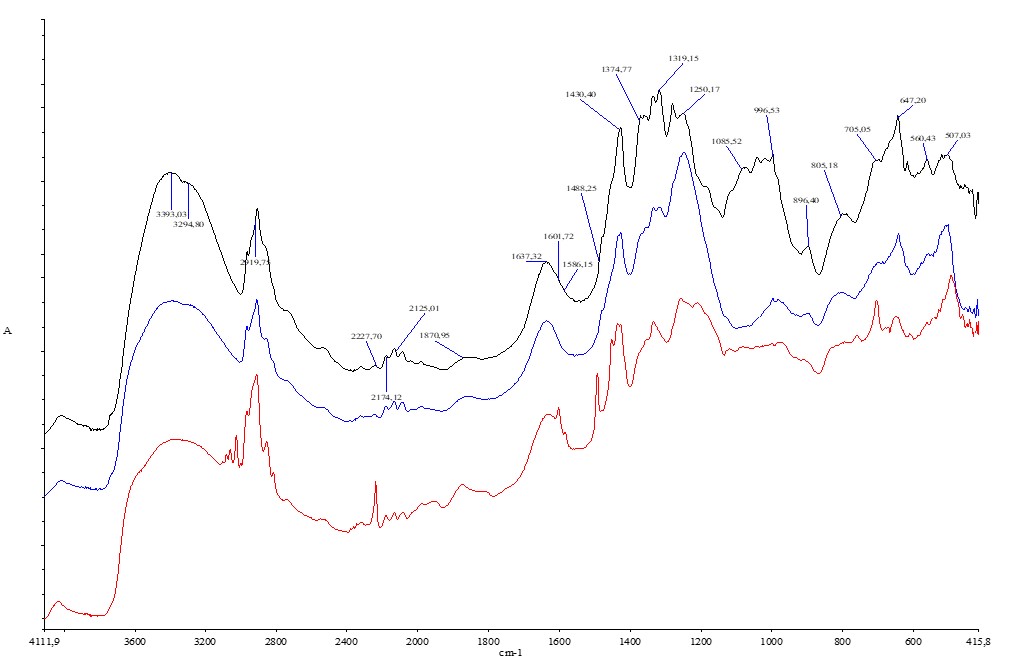
Рисунок 4 - ИК спектры обезвоженных ЭI(1) , ЭII (2) и ЭIII(3)
По сравнению со спектрами MI, MII и MIII в спектрах ЭI, ЭII и ЭIII появилась полоса около 647 см-1, относящаяся к деформационным колебаниям в SO42-. Так же и изменилась спектральная картина в областях 1430 – 1300 см-1 колебаний в полимере и 1100 -760 см-1 - Si-O- Si колебаний. Это указывает на то, что в сольватации аквакомплексов участвуют донорные атомы полимера и аэросила.
Измерение электропроводности электролитов проводили в электрохимической ячейке из двух стаканов с 1,5 М раствором сульфата натрия в каждом с помещенными в них платиновыми электродами. Полученные нами материалы-донорные растворители ЭI, ЭII и ЭIII попеременно использовались в данной ячейке в качестве электрохимических мостиков. Длина мостика 20 см, ширина 10 см. Концы мостика были опущены в каждый стакан с раствором сульфата натрия на глубину 0.3 см. Платиновые электроды были соединены с источником постоянного тока. Задавали напряжение U и измеряли J ток в цепи. Данные зависимости приведены на рис. 5.
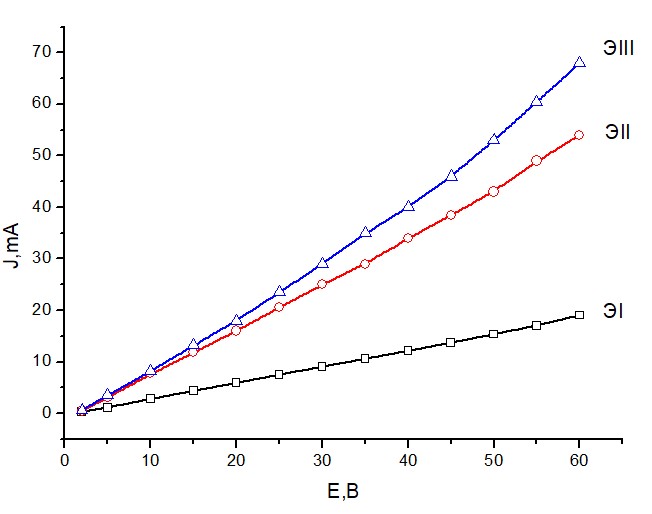
Рисунок 5 - Зависимость тока в цепи от напряжения
Видно, что при каждом заданном напряжении ток в цепи возрастает в ряду ЭI<ЭII<ЭIII. Установлено, что ЭI, ЭII или ЭIII – это не линейные проводники. Зависимость тока в цепи от напряжения описывается уравнением: J = σ(U-U0) + χ(U-U0)2, где U0 – напряжение начала движения ионов в проводнике, σ – проводимость проводника, а χ - поляризуемость проводника (в уравнении отвечает за нелинейность). Для ЭI Е0=0.00029 В, σ = 0.3*10-3 См и χ =0.32*10-6 См/В, для ЭII U0 =0.0039 В, σ =0.82 *10-3 См, χ = 1.6*10-6 См/В и для ЭIII U0 =0.013 В, σ = 0.84*10-3 См, χ = 5.09*10-6 См/В. Значения σ возрастают с увеличением С(Na2SO4), а χ – увеличением С(Na2SO4)2. При этом σ/С(Na2SO4) ≈ 0,23 См*г/моль, а χ/С(Na2SO4)2≈0,22*10-3 См*г2/В*моль2. Особенность структуры растворителя заключается в том, что водный раствор сульфата натрия контактирует с полимером, окружающим частицы аэросила. Согласно составу аквакомплексов числа молекул воды недостаточно для формирования первой сольватной оболочки Na+. В стенках пор полимера эту оболочку достраивают атомы азота и кислорода. Сродство иона Na+ к донорным атомам кислорода больше, чем к донорным атомам азота [9], [10]. Поэтому Na+ перемещаются в зону прививки и через них в стенки пор аэросила, состыкованных с порами полимера. С увеличением доли аэросила в слое уменьшается число донорных атомов полимера и увеличивается количество групп, формирующих переходную зону. При этом одновременно увеличивается объем сорбирующих пор. Вероятно, что в электропроводном мостике движение ионов происходит преимущественно в зоне прививки.
3. Заключение
Исследования показали перспективность синтеза твердых донорных растворителей с задаваемой растворяющей способностью и электролитов с требуемой электропроводностью. Для синтеза растворителей возможно варьирование составом суспензии микрочастиц аэросила и ПВХ в смеси ТГФ и БС), которые можно химически пришить к подложке из целлюлозной ткани использованием аминокислот, моноэтаноамина, первичных ди- и полиаминов как реагентов для превращения цепей ПВХ в макромолекулярные циклические амины. В дальнейших исследованиях будет определена зависимость варьирования природой акавакомплексов с задаваемым отношением катионов к анионам и природой подложек на растворяющую способность и электропроводность материалов.
