Organ-preserving urethral surgery: a new concept of anastomotic urethroplasty for bulbous urethral strictures
Organ-preserving urethral surgery: a new concept of anastomotic urethroplasty for bulbous urethral strictures
Abstract
Dorsal techniques of anastomotic urethroplasty without transection of the spongiosa body have certain disadvantages. Therefore, we proposed a new technique of urethroplasty without crossing the urethra using ventral access.
The prospective study included 59 men with bulbous urethral stricture who underwent anastomotic urethroplasty without urethral crossing using the technique developed by us from 2016 to 2023. Postoperative examinations were performed after 3, 6, 12, 18, 24 months, and annually thereafter.
The age of the patients ranged from 20 to 82 years (median: 51 years). The mean stricture length was 17 mm (range: 3-31 mm). Iatrogenic cause of urethral stricture occurred in 27 (45.8%) patients, inflammatory – in 26 (44.1%), traumatic (blunt perineal trauma) – in 6 (10.1%). The stricture was primary in 22 (37.3%) observations and recurrent in 37 (62.7%). Independent urination was preserved in 45 (76,3%) patients, cystostomy existed in 14 (23,7%) patients. Postoperative complications occurred in 7 (11.9%) patients and had a mild degree (Clavien-Dindo I). The time of postoperative follow-up of patients ranged from 3 to 93 months (median – 48 months). Recurrence of urethral stricture was noted in 5 (8.5%) observations. Deterioration of sexual function after surgery was not observed in the sample as a whole.
The technique of urethroplasty with anastomosis formation on the ventral surface of the urethra without complete mobilization and crossing of the dorsal semicircle of the urethral spongiosal body allows to ensure high efficiency and safety in the treatment of relatively short strictures of the bulbous urethra (up to 3 cm).
1. Введение
Для непротяженных стриктур бульбозной уретры (менее 2 см) традиционно лучшим вариантом уретропластики считается анастомоз конец в конец, что подразумевает пересечение уретры с целью удаления измененных тканей и последующего соединения здоровых частей уретры , . Пересечение уретры позволяет полностью удалить рубцовую ткань, но может привести к повреждению кровеносных и лимфатических сосудов, а также нервных волокон, расположенных вдоль стенки уретры. Кроме того, операционная травма наносится циркулярно по всей поверхности уретры и затрагивает все слои стенки уретры. Указанные обстоятельства способствуют нарушению кровоснабжения, лимфодренажа и иннервации в области оперативного вмешательства и дистальнее находящихся частей уретры. Возникающие вследствие этого трофические расстройства повышают риск фиброзирования стенки уретры, а нарушение иннервации может привести к различным сексуальным или другим функциональным нарушениям после операции. По данным различных исследований, после анастомотической уретропластики рецидив стриктуры уретры встречается до 20-25% случаев , , , сексуальные дисфункции – 18,0-22,5% , . В связи с этими обстоятельствами все чаще стали поднимать вопросы о негативных аспектах пересечения уретры в ходе уретропластики и актуальности поиска путей снижения травматизации данного органа при уретропластике. Одной из таких методик является разработанная G.H. Jordan et al. сосудосберегающая техника уретропластики без пересечения спонгиозного тела, согласно которой фиброзные ткани уретры иссекают циркулярно на дорзальной стороне и на этой же стороне формируют анастомоз между здоровыми концами, сохраняя вентральную часть спонгиозного тела интактной
. Следует отметить, что данная техника не может обеспечить радикальность иссечения спонгиофиброза, так как спонгиозная ткань в бульбозной уретре в основном развита на вентральной стороне. Из-за тонкого слоя спонгиозной ткани на дорзальной стороне бульбозной уретры сложно отделить спонгиозную ткань от стенки уретры, поэтому технические действия по повышению радикальности удаления спонгиофиброза с дорзальной стороны могут привести к возникновению широкой и овальной формы операционной раны, что может быть сопряжено с риском избыточного резецирования стенки уретры и создания грубого анастомоза в этой области.Более усовершенствованной в этом плане методикой служит разработанная D.E. Andrich и A.R. Mundy техника без пересечения уретры . Данная методика предполагает продольное рассечение уретры с дорзальной стороны с последующим иссечением рубцово-измененной слизистой внутри просвета уретры с сохранением подлежащего спонгиозного тела, после которого на вентральной стороне внутри просвета уретры формируют анастомоз между здоровыми концами слизистой уретры, а продольный разрез на дорзальной стороне ушивают поперечно по принципу Heineke-Mikulicz . Описанная методика также не лишена существенных недостатков. В частности, осуществление полной мобилизации и разворота уретры для получения доступа к вскрытию уретры с дорзальной стороны и проведение вышеуказанных манипуляций на вентральной стенке уретры со стороны слизистой связаны с повышенной кровоточивостью в области оперативного вмешательства. Из-за невозможности полного разворота уретры в данном отделе в силу анатомо-топографических особенностей образуется узкая и глубокая операционная рана. Все указанные обстоятельства ухудшают интраоперационную визуализацию и ограничивают технические действия хирурга, что потенциально снижает радикальность удаления фиброзных тканей уретры. К тому же, вскрытие стенки уретры с обеих сторон (как с дорзальной, так и с вентральной стороны) дополнительно увеличивает вероятность рубцевания стенки уретры и, следовательно, риска возникновения рецидива стриктуры уретры.
Таким образом, предложенные дорзальные методики уретропластики без пересечения уретры не обеспечивают радикальность иссечения пораженной части уретры и сопряжены с высоким риском рецидирования стриктуры. С учетом этого нами разработан новый подход к выполнению уретропластики без пересечения уретры с использованием вентрального доступа, направленный на обеспечение более лучших условий для обзора зоны операции, максимального иссечения пораженных тканей и полноценного соединения здоровых концов уретры.
2. Материалы и методы
В проспективное исследование включено 59 мужчин, которым на базе урологического отделения Городской клинической больницы им. С.П. Боткина г. Москвы с 2016 по 2023 гг. по поводу стриктуры бульбозного отдела уретры была выполнена анастомотическая пластика уретры без пересечения уретры по разработанной нами технике, на которую нами были получены 2 патента на изобретение , .
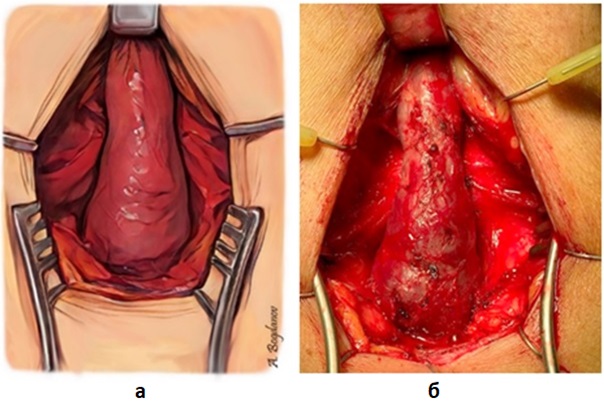
Рисунок 1 - Область доступа к вентральной полуокружности бульбозной уретры:
а – схема; б – интраоперационный вид
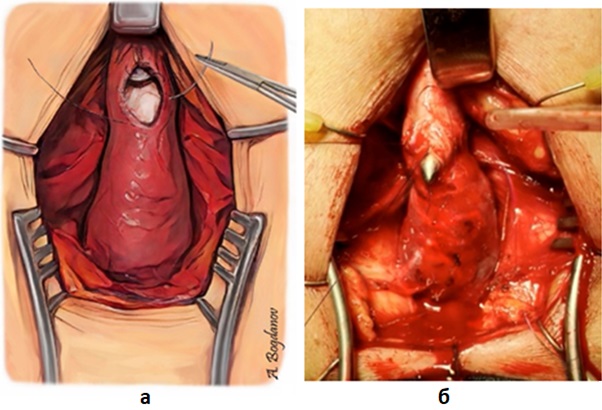
Рисунок 2 - Наложение первых гемостатических швов и вскрытие просвета уретры дистальнее стриктуры:
а – схема; б – интраоперационный вид
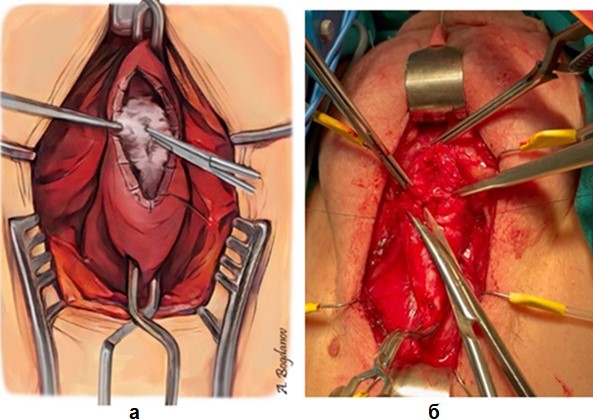
Рисунок 3 - Вскрытие просвета уретры в зоне стриктуры после наложения обшивающих гемостатических швов и начало иссечения стриктуры:
а – схема; б – интраоперационный вид
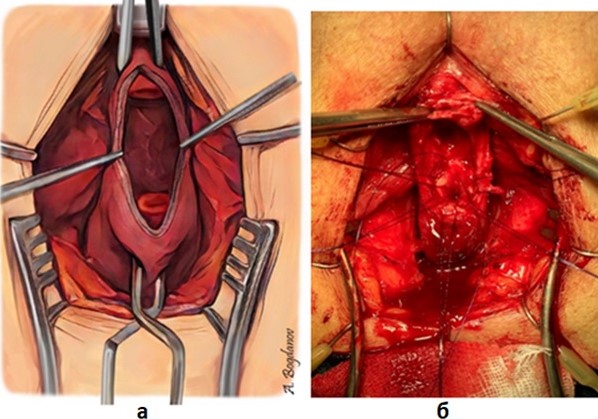
Рисунок 4 - Завершение иссечения рубцовых тканей и начало формирования проксимального и дистального концов уретры, включающих слизистую и подслизистую оболочки:
а – схема; б – интраоперационный вид
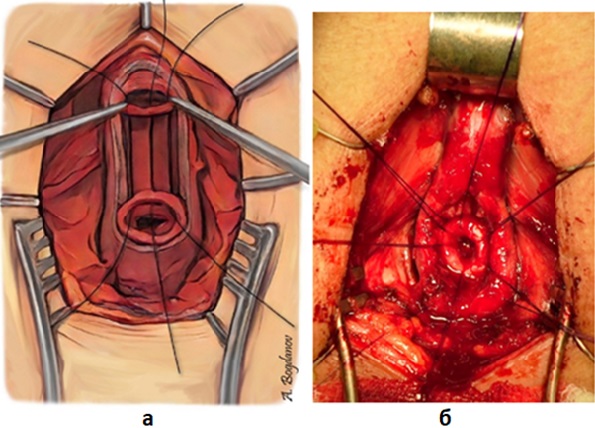
Рисунок 5 - Завершение формирования уретральных концов для наложения анастомоза:
а – схема; б – интраоперационный вид
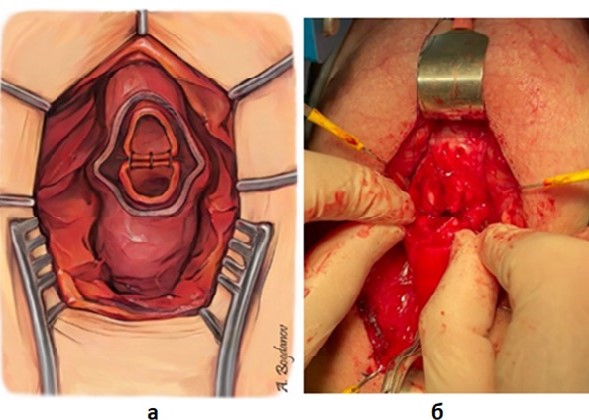
Рисунок 6 - Формирование задней полуокружности анастомоза, включающего слизистую и подслизистую оболочки:
а – схема; б – интраоперационный вид
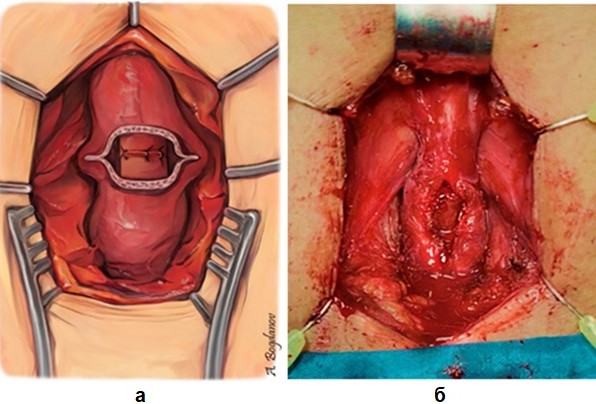
Рисунок 7 - Формирование передней полуокружности анастомоза, включающего слизистую и подслизистую оболочки:
а – схема; б – интраоперационный вид
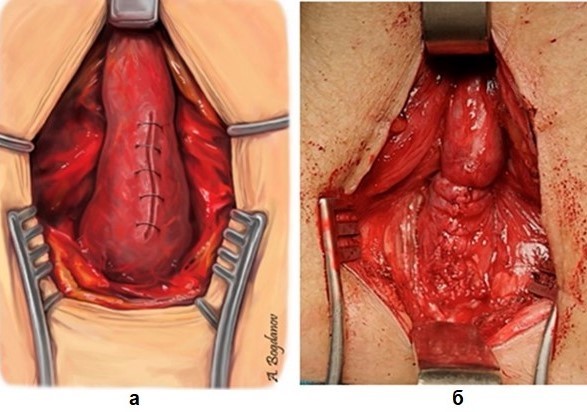
Рисунок 8 - Продольное ушивание спонгиозного тела:
а – схема; б – интраоперационный вид
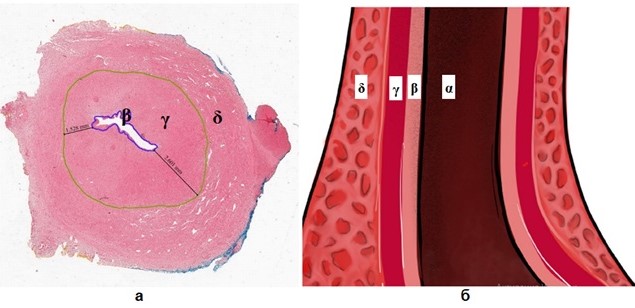
Рисунок 9 - Срез слоев уретры:
а – микроскопический вид поперечного среза средней части бульбозного отдела уретры: синей линией обведен слизистый слой (β), зеленой – подслизистый слой (γ), за зеленой линией находится спонгиозное тело (δ) (окрашивание гематоксилином и эозином, ×20); б – схематический вид продольного среза бульбозного отдела уретры: просвет уретры (α), слизистый слой (β), подслизистый слой (γ), спонгиозное тело (δ)
3. Результаты исследования
Результаты предоперационного обследования пациентов приведены в Таблице 1.
Таблица 1 - Клиническая характеристика пациентов
Параметры | Медиана | Диапазон |
Возраст, лет | 51 | 20–82 |
Длина стриктуры, мм | 17 | 3–31 |
Максимальная скорость мочеиспускания (при сохранении самостоятельного мочеиспускания), мл/с | 5,2 | 1,8–9,3 |
Объем остаточной мочи (при сохранении самостоятельного мочеиспускания), мл | 217 | 35–400 |
IIEF-5, баллы | 17 | 12–25 |
Этиология стриктуры | n | % |
Ятрогенная | 27 | 45,8 |
Травма (тупая травма промежности) | 6 | 10,1 |
Воспаление | 26 | 44,1 |
Клиническая форма стриктуры | n | % |
первичная | 22 | 37,3 |
рецидивная | 37 | 62,7 |
Наличие цистостомы | n | % |
Да | 14 | 21,3 |
Нет | 45 | 78,7 |
Продолжительность выполнения оперативного вмешательства варьировала от 110 до 165 минут (медиана – 137 минут). Объем интраоперационной кровопотери составлял от 50 до 500 мл (медиана – 267 мл). Сроки послеоперационного пребывания пациентов в стационаре составляли от 3 до 7 суток (медиана – 5 суток). Уретральный катетер удаляли на 10-й день после оперативного вмешательства.
Интра- и ранние послеоперационные осложнения были отмечены у 7 (11,9%) пациентов. Все они были легкой степени и соответствовали категории I по классификации Clavien-Dindo: лихорадка менее 24 часов – у 6 (10,2%) пациентов, небольшая гематома промежности – у 1 (1,7%) пациента.
Сроки послеоперационного наблюдения пациентов колебались от 3 до 93 месяцев (медиана – 48 месяцев). Динамика показателей мочеиспускания и сексуальной функции после операции относительно предоперационных значений продемонстрирована в Таблице 2. Так как пациенты имели разные сроки послеоперационного наблюдения, медиана послеоперационных значений данных параметров указана по наиболее позднему контрольному обследованию. Данные таблицы подтверждают, что в результате оперативного вмешательства наступило достоверное улучшение ключевых показателей мочеиспускания, а сексуальная функция пациентов не ухудшилась.
Таблица 2 - Динамика показателей мочеиспускания и сексуальной функции
Параметры | Медиана | p | |
До операции | После операции | ||
Максимальная скорость мочеиспускания, мл/с | 5,2 | 22,9 | <0,05 |
Объем остаточной мочи, мл | 217 | 0 | <0,05 |
IIEF-5, баллы | 17 | 16 | >0,05 |
Примечание: p – по критерию Вилкоксона
Рецидив стриктуры уретры отмечен в 5 (8,5%) наблюдениях. Все случаи рецидива возникли среди пациентов, имевших рецидивную форму стриктуры перед нашей операцией. При этом три случая рецидивы возникло в первые 2 года после операции (через 13, 18 и 21 месяц соответственно), а два других случаях – в более поздние сроки (на 7-ом году наблюдения).
Таким образом, успех лечения при использовании нашей техники составил 91,5% при длительных сроках наблюдения до 5 лет.
4. Обсуждение
Наши результаты несколько превосходят или сопоставимы с показателями лечения, полученными в других исследованиях при использовании дорзальной техники уретропластики без пересечения спонгиозного тела. Например, в исследовании K.M. Anderson et al. после анастомотической уретропластики без пересечения спонгиозного тела из 50 пациентов успех лечения был получен в 41 (82%) наблюдении при среднем сроке послеоперационного наблюдения 48 месяцев. В работе N. Lumen et al. среди 75 пациентов после аналогичной операции рецидив стриктуры уретры возник в 8% случаев при медиане наблюдения 30 месяцев, послеоперационные осложнения – в 18,7% и эректильную дисфункцию de novo – в 21,9%. В другой недавней работе, проведенной D.W. Chapman et al. , среди 94 пациентов после уретропластики без пересечения спонгиозного тела при среднем сроке наблюдения 64,2 мес. был достигнут достаточно высокий успех лечения (97,9%), однако имело место более частое возникновение послеоперационных осложнений (4,3%) и сексуальной дисфункции (4,3%), чем в нашем исследовании. Более того, в одном из последних мета-анализов, включившего 19 исследований, было установлено, что методики анастомотической уретропластики с пересечением и без пересечения спонгиозного тела не имеют значимых различий по частоте рецидива стриктуры уретры, тогда как для техник без пересечения спонгиозного тела характерны более лучшие результаты с точки зрения сохранения сексуальной функции .
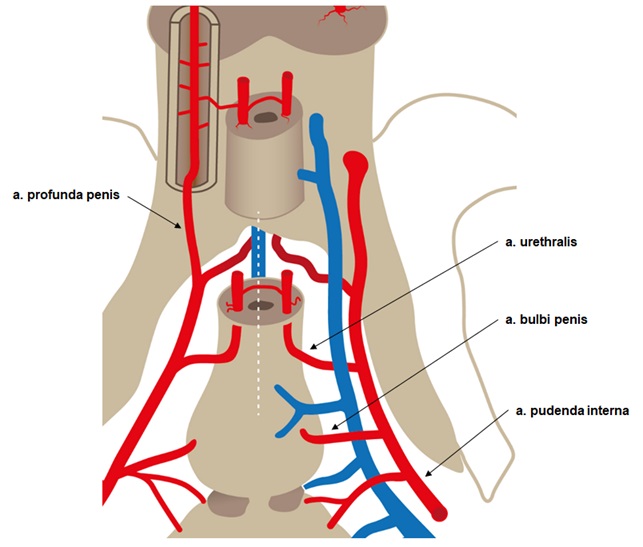
Рисунок 10 - Схема кровоснабжения бульбозной уретры
Примечание: по ист. [16]; пунктирной линией показана линия разреза на вентральной поверхности уретры
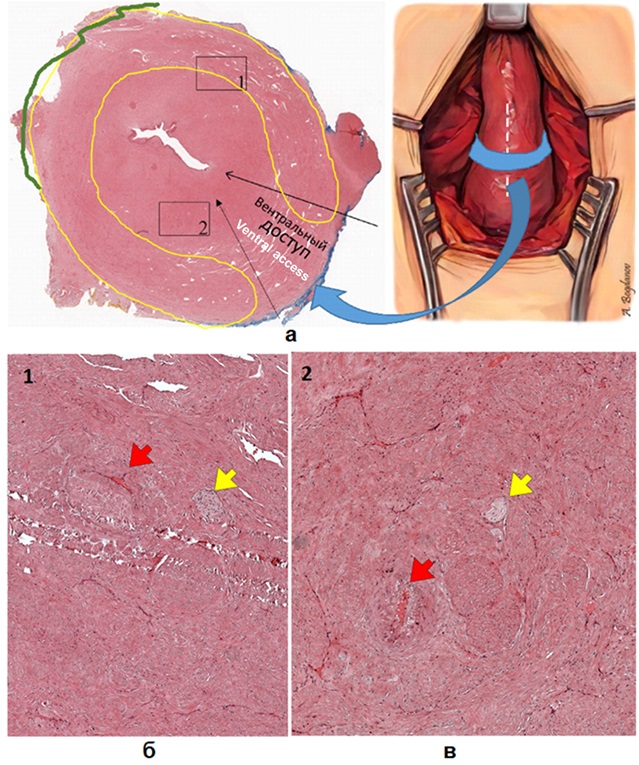
Рисунок 11 - Сосудистые и нервные структуры, идущие в толще спонгиозной ткани:
а – гистологический препарат бульбозной уретры, демонстрирующий доступ через вентральную поверхность спонгиозного тела: обведена желтым цветом часть спонгиозного тела, которая будет сохранена после иссечения рубцовых тканей; зеленой линией отмечена зона дорзальной полуокружности, сохраняющей фиксацию к кавернозным телам (окрашивание гематоксилином и эозином, ×40); б, в – сосуды и нервы в зонах 1 и 2: красная стрелочка – артерия, желтая – нервное волокно (окрашивание гематоксилином и эозином, ×100)
5. Заключение
Разработанная нами техника уретропластики с формированием анастомоза на вентральной поверхности уретры без полной мобилизации и пересечения дорзальной полуокружности спонгиозного тела уретры продемонстрировала высокую эффективность. Такой результат был достигнут за счет различных приемов, которые позволили обеспечить более лучший обзор зоны операции, максимальное сохранение кровоснабжения и иннервации уретры, полноценное иссечение рубцовых тканей и адекватное сопоставление здоровых тканей уретры. К таковым приемам можно использование гемостатических обвивных непрерывных швов при вскрытии просвета уретры, что помогает детально оценить протяженность стриктуры уретры и степень спонгиофиброза, тем самым давая возможность более корректного принятия решения об объеме операции. А отказ от полного выделения и пересечения спонгиозного тела (как при традиционной анастомотической технике), а также от полной мобилизации бульбозного отдела и разворачивания уретры (как при дорзальной технике уретропластики без пересечения спонгиозного тела) позволяют снизить риск повреждения кровеносных сосудов и нервных волокон в этой области, а также позволяет сохранить природную геометрию просвета уретральной трубки. Безусловно, несмотря на обнадеживающие первоначальные результаты, необходимо продолжение дальнейших исследований по изучению эффективности предложенной методики, и окончательные выводы можно будет сделать только по результатам подобных работ. Тем не менее следует признать, что благодаря появляющимися новым публикациям и существенному приросту внедряющихся технологий без полного пересечения спонгиозного тела с хорошим функциональным результатом формируется новое понятие в хирургии уретры – это уретросохраняющие операции. Возможно, мы находимся в самом начале эры орган-сохраняющей хирургии уретры.
