Structural and thermodynamic characteristics of alloys of Al-Zn system
Structural and thermodynamic characteristics of alloys of Al-Zn system
Abstract
Metal alloys in non-equilibrium states often have important technological properties. Practical use of such materials requires a comprehensive study of their physical properties and structure. On the example of alloys of Al-Zn system by the choice of hardening modes the non-equilibrium hardened state was obtained. Wide application of aluminium-zinc alloys in industry stipulates interest to their further study. Thermodynamic properties of alloys are one of their most important characteristics. However, the study of these properties in multiphase systems is a difficult experimental task. The research of structure and thermodynamic characteristics of Al-Zn alloys has shown their correspondence and interrelation. The possibility of non-equilibrium x-phase formation in quenched samples, which leads to a noticeable change in the thermodynamic properties of alloys, has been identified.
1. Введение
Многие используемые в настоящее время в технике материалы являются неравновесными в условиях эксплуатации. Они могут находиться либо в метастабильном, либо в неравновесном закаленном состоянии. Часто сильное отклонение от равновесия необходимо для реализации желаемых эксплуатационных свойств, например, высокой механической прочности, коррозионной стойкости, необычных магнитных и электрических свойств, сверхпластичности, аномальной упругости и других. Примерами материалов, получаемых в состоянии далеком от равновесия и обладающих такими свойствами, являются закаленные аустенитные и мартенситные сплавы черных и цветных металлов, быстрозакаленные аморфные и нанокристаллические материалы, неравновесные фазы, получаемые путем механоактивационного синтеза. Для практики важнейшим является вопрос о сохранении комплекса физических и механических свойств подобных материалов на протяжении предполагаемого срока эксплуатации и при возможной термообработке. Одним из направлений решения этой проблемы является термодинамическое исследование металлических сплавов для последующего анализа устойчивости различных типов структур и их склонности к релаксации. Особые, иногда экстремальные условия эксплуатации могут привести к сокращению времени релаксации неравновесных состояний. Так, например, относительно медленный процесс диффузионной релаксации может резко ускориться в процессе пластической деформации
. Следовательно, изучение проблемы термодинамической устойчивости неравновесных и метастабильных состояний, возникающих в реальных материалах, приобретает важное значение для решения вопросов их практического использования.Сплавы на основе системы алюминий-цинк широко используются в авиационной и автомобилестроительной отрасли промышленности. При изучении этой системы А.А. Бочваром было открыто явление сверхпластичности. Усовершенствование методов синтеза и расширение эксплуатационных возможностей уже известных и пока что незаменимых металлических материалов, в том числе и сплавов системы Al-Zn, невозможно без знания фундаментальных термодинамических характеристик и их взаимосвязи со структурой и строением вещества. Имеющиеся в литературе данные по термодинамическим свойствам бинарных сплавов системы Al-Zn в равновесном твердом состоянии получены при температуре 380°С. Однако во многих случаях сплавы используются в неравновесном состоянии и температуре значительно ниже 380°С. Обзор литературных данных показал, что сплавы системы Al-Zn в закалённом состоянии не изучались. Поэтому была поставлена задача: применяя различные режимы и способы закалки получить сплавы Al-Zn в закалённом (неравновесном) состоянии
, .2. Основные результаты
2.1. Диаграмма состояния сплава алюминий – цинк
Из диаграммы состояния системы Al-Zn (рис. 1) , следует, что алюминий и цинк обладают взаимной растворимостью в твердом состоянии, значительной для сплавов, богатых алюминием, и крайне ограниченной для сплавов, богатых цинком.
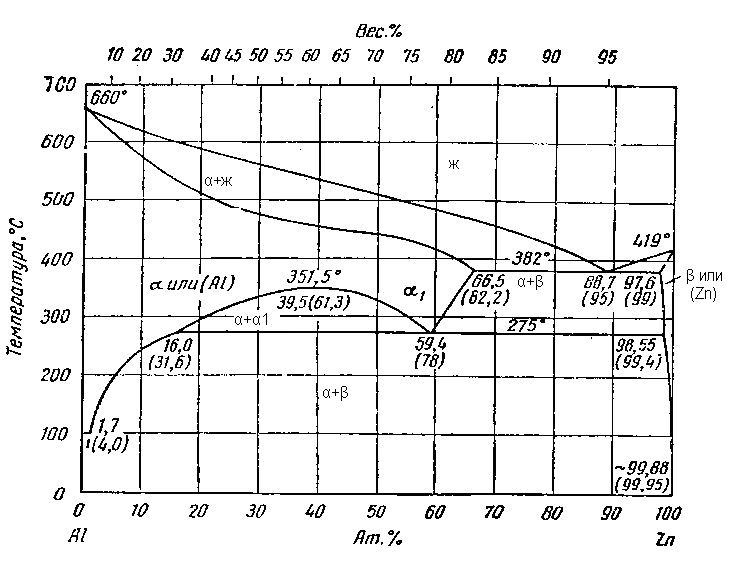
Рисунок 1 - Диаграмма состояния сплава алюминий – цинк
Примечание: по данным работы [5]
α – твердый раствор имеет гранецентрированную кубическую структуру, а β – твердый раствор — гексагональную плотноупакованную структуру. Постоянная кристаллической решетки α – твердого раствора при содержании в нем 4,25% Zn определена при 18° С равной 4,0402 Å, а постоянные решетки β-фазы при той же температуре и содержании цинка 99,95 % составили: а = 2,6584 Å и с = 4,9387 Å .
Определения постоянных кристаллических решеток производились при предельном содержании цинка (α-фаза) и алюминия (β-фаза) в твердом растворе.
α и α1-фазы имеют гранецентрированную кубическую структуру и различаются между собой по составу и величине постоянной кристаллической решетки.
β-фаза после эвтектоидного превращения трансформируется в β'-фазу с гексагональной решеткой .
2.3. Приготовление образцов
Для получения сплавов системы Al-Zn, помещали навески металлов в алундовый тигель. Для предотвращения окисления кислородом, сверху шихта покрывалась слоем углерода (древесный уголь) толщиной 5 мм. Нагрев тигля с шихтой проводился в шахтной электрической печи до температуры 730° С (1003 К), при которой сплавы выдерживался 15 минут. До и после 15 минутной выдержки он тщательно перемешивался. Закалку проводили путем выдерживания образцов сплавов при 300 °С в течение 20 минут, и дальнейшего резкого охлаждения в воде с помощью специально изготовленного приспособления.
Имеющийся опыт в применении термодинамического анализа для исследования неравновесного состояния различных металлических материалов
, , , привел к попытке получения равновесной при 400оС α-фазы сплава Al-Zn в «замороженном» состоянии и изучения её при комнатной температуре. Закалку проводили с применением специально изготовленного устройства таким образом, чтобы понижение температуры образцов между окончанием процесса нагрева и воздействием воды на его поверхность было минимальным.2.4. Рентгенофазовый анализ
Дифрактограммы для фазового рентгеновского анализа снимались на дифрактометр ДРОН-3.0 в медном монохроматизированном излучении в диапазоне углов со скоростью 2 град/мин. Для оценки параметра решетки, сравнении интенсивности и уширений некоторые линии снимались со скоростью 0,25 град/мин.
Межплоскостные расстояния, определенные из рентгенограмм сравнивались с межплоскостными расстояниями известных для этой системы фаз (цинк, – фаза с ГЦК-решеткой на основе алюминия,
– фазой с ГЦК решеткой с параметром, большим чем у алюминия). Последняя фаза была обнаружена ранее
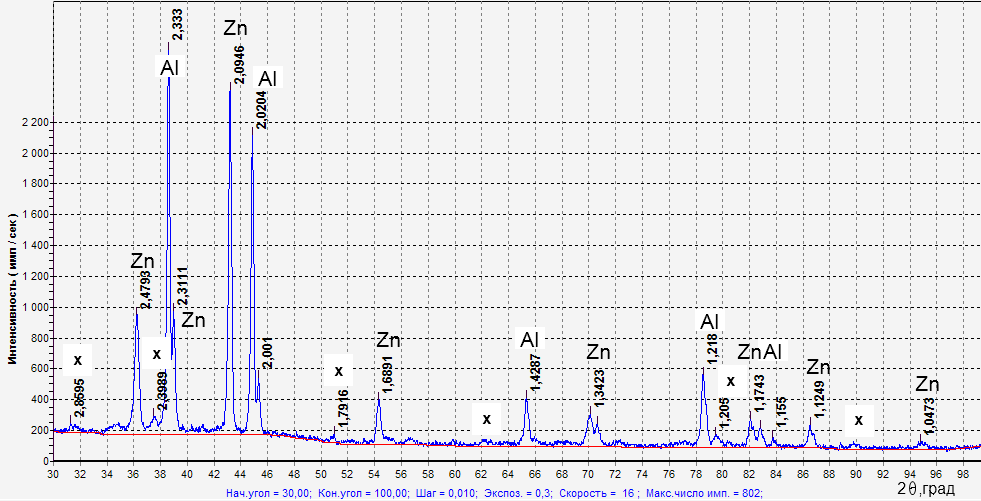
Рисунок 2 - Дифрактограмма закаленного образца, содержащего 62% цинка
Примечание: символом х обозначена-фаза
Остальные образцы имеют очень похожую структуру. В них присутствуют чистый цинк, -фаза, в некоторых образцах – чистый алюминий и
-фаза (объект).
-фаза была обнаружена в серии опытов, проводимых ранее. Она имеет ГЦК-решетку, но ее параметр больше, чем у решетки алюминия. Содержание этой фазы достигало максимума в образцах 60-80% цинка. Поэтому для дальнейших исследований выбраны эти образцы.
Позднее, при проведении экспериментов на другой серии чистых сплавов Al-Zn, в которых не содержался свинец, а примеси других металлов не превышали 0,2-0,3 мас. %. При этом – фаза в закаленных образцах или не обнаруживалась совсем, или обнаруживалась а следовых количествах. Например, в закаленном образце Al – 62 ат. % Zn содержится чистый цинк, чистый алюминий,
– раствор на основе алюминия (с ГЦК-решеткой) и в очень малом количестве х-фаза (
– раствор также с ГЦК решеткой, но с отличным от
– раствора параметром решетки). Однако столь аномального изменения параметра решетки уже не наблюдалось. Поиск причин появления х-фазы привел к необходимости изменения условий закалки. Кроме закалки в воду с помощью специального приспособления, была проведена закалка непосредственно в жидкий азот.
2.5. Термодинамическое исследование методом мгновенного фиксирования ЭДС (МФЭ)
2.5.1. Метод мгновенного фиксирования ЭДС
Одним из немногих методов, пригодных для термодинамических исследований закаленных сплавов, является вариант метода ЭДС – метод мгновенного фиксирования ЭДС (МФЭ). Впервые метод МФЭ был предложен японскими учеными К. Окаджима и Х. Сакао
, при определении химических потенциалов компонентов жидких сплавов Pb-Sn и др. в электрохимических элементах с солевыми расплавами в качестве электролита. В работах этих авторов метод МФЭ носил название TIE – Touch Instant Electromotive Force Method или «метод касания». Основная идея метода сводится к гипотезе о том, что при замыкании электрохимической цепи, производимом в момент касания электролита поверхности электродов (до измерения электроды и электролит содержатся раздельно), устанавливающаяся в первый момент времени величина ЭДС соответствует равновесному значению, то есть является разностью равновесных скачков электродных потенциалов. Такая величина может установиться только в результате обратимого протекания электрохимических процессов на электродах. Это предположение является обоснованным в случае быстрого установления электродных потенциалов, то есть высоких значений токов обмена. В каждом опыте, при исследованиях методом МФЭ, заранее подготовленные электроды и электролит тем или иным способом приводят в соприкосновение и фиксируют ЭДС, возникающую в гальваническом элементе (как правило, применяется осциллографическая запись сигнала). Следующим этапом является анализ полученных осциллограмм.Низкотемпературные термодинамические исследования могут быть проведены с использованием водных растворов электролитов
. Применение таких электролитов для обычного варианта метода ЭДС ранее справедливо считалось невозможным, так как большинство металлов и сплавов активно взаимодействуют с водой. Кроме того, при низких температурах диффузионные процессы замедлены и нельзя надеяться на восстановление активности потенциалобразующего компонента на поверхности сплава, измененной в результате взаимодействия электрода с электролитом. Такое взаимодействие в случае водных растворов в большинстве случаев, если не всегда, будет необратимым. Тогда только применение метода МФЭ может дать возможность зафиксировать равновесную величину ЭДС, «опередив» процесс взаимодействия, и рассчитать на ее основе термодинамические свойства сплава.При измерении равновесных величин ЭДС в первый момент времени можно надеяться на «опережение» такого вида взаимодействия электродов с электролитом, как коррозия металлических сплавов и применять в качестве растворителя коррозионно активную среду – воду. Использование водных растворов обладает практическими преимуществами. В первую очередь, они доступны и просты в приготовлении. Кроме того, использование водных растворов позволяет проводить измерения при низких температурах, что очень важно для изучения термодинамических свойств закаленных (неравновесных) материалов.
Главную трудность во время работы представляет выбор условий эксперимента в каждом конкретном случае. Анализ и «расшифровка» большого количества получаемых осциллограмм состоят в выделении горизонтального плато – участка, отвечающего термодинамически обусловленной равновесной величине ЭДС. С этой целью в работе В.В. Егоркина
предложено варьировать в ходе эксперимента кинетические и термодинамические параметры системы. Значение ЭДС, не зависящее от концентрации и вида электролита (при сохранении потенциалобразующего иона, например, ZnCl2 и ZnSO4), размеров и взаимного расположения электродов, геометрии ячейки, способа подготовки электродов к измерению, принимается за «истинное». Зависимость полученных величин от термодинамических параметров (состава и температуры), как правило, имеет закономерный характер.К достоинствам метода МФЭ можно отнести следующие:
Метод дает возможность определить непосредственно из эксперимента активность более благородного компонента сплава, а также обоих компонентов, близких по электроотрицательности, что принципиально невозможно сделать традиционным методом ЭДС из-за протекания реакции обменного типа
:В методе МФЭ появляется возможность зафиксировать термодинамически равновесную величину ЭДС до того момента, как процесс (1) существенно ее изменит.
В случае экспериментального определения изменения химических потенциалов обоих компонентов бинарного сплава значительно упрощается расчет интегральной энергии Гиббса его образования. Для этого не требуется знать зависимость изменения химического потенциала одного из компонентов от состава в широком его интервале, что необходимо для расчета DG по уравнению Гиббса-Дюгема.
Метод МФЭ позволяет проводить измерения при низких температурах, в ряде случаев с использованием водных растворов электролитов.
Все перечисленные достоинства метода МФЭ имеют непосредственное значение для термодинамического изучения закаленных (неравновесных) сплавов.
Экспериментальное исследование термодинамических характеристик (изменений химических потенциалов цинка ΔμZn = μZn - μZnO) в бинарных сплавах системы Al-Zn в зависимости от состава (мольная доля цинка изменялась в пределах XZn : 0.05–0.85) было проведено с помощью варианта метода ЭДС – метода мгновенного фиксирования ЭДС (МФЭ) при комнатной температуре (Т=295 К). В качестве регистрации временной развертки ЭДС применяли цифровой осциллограф с памятью GDS-806C. Метод МФЭ дает возможность проводить исследования термодинамических характеристик металлических сплавов при низких (близких к комнатной) температурах, что, с одной стороны, сокращает время измерения, с другой, что более важно, позволяет сохранить неизменным термодинамическое состояние образцов, которое может сильно отличаться от равновесного (например, для закаленных сплавов)
, .Измерения ЭДС проводили в концентрационных элементах следующих типов:
Изменения химических потенциалов цинка в образцах рассчитывали по известной формуле: ΔμZn = -zFE, где z – заряд иона потенциалобразующего компонента (в нашем случае он равен 2), F – число Фарадея, E – ЭДС электрохимического элемента.
Термодинамическое исследование выявило закономерное изменение парциальной энергии Гиббса (т.е. изменения химического потенциала) цинка в зависимости от состава (см. таблицу 1).
Таблица 1 - Экспериментальные значения ЭДС и расчетные значения изменения химического потенциала элементов
Номер элемента | Мольная доля цинка в сплаве | ЭДС элемента, мВ | Изменение химического потенциала, Дж/г-атом |
1 | 0,04 | 15,6±0,3 | -3010±60 |
2 | 0,05 | 45,2±1,7 | -8720±300 |
3 | 0,07 | 6,9±0,2 | -1330±40 |
4 | 0,40 | 3,6±0,3 | -690±60 |
5 | 0,50 (з) | 1,5±0,2 | -290±40 |
6 | 0,50 (н) | 2,5±0,2 | -480±40 |
7 | 0,50 | 1,5±0,2 | -290±40 |
8 | 0,70 | 1,8±0,2 | -350±40 |
9 | 0,80 (з) | 0,8±0,2 | -150±40 |
10 | 0,80 (н) | 2,3±0,2 | -440±40 |
11 | 0,80 | 1,5±0,2 | -280±40 |
12 | 0,85 | 0±0,2 | 0±40 |
Примечание: обозначение (з) означает сплав, закаленный в жидкий азот;
обозначение (н) означает сплав, не закаленный в жидкий азот
На основе экспериментальных данных были произведены расчеты изменения химического потенциала для двенадцати образцов сплавов Al-Zn разного состава (по формуле ). Полученные результаты сравнивали с литературными данными , для образцов сплавов системы Al-Zn в равновесном состоянии при температуре 380oC
Используя рассчитанное изменение химического потенциала, был построен график зависимости , где х – мольная доля цинка в сплаве.
Такой вид зависимости качественно совпадает с приведенными в литературе данными.
Таблица 2 - Значения изменений химических потенциалов цинка (ΔμZn) в зависимости от состава при Т = 653 К
хZn | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,662 | 0,978 | 1,00 |
ΔμZn | -3330 | -1990 | -1640 | -1590 | -1400 | -810 | -120 | -120 | 0 |
Примечание: составлено по данным [17]
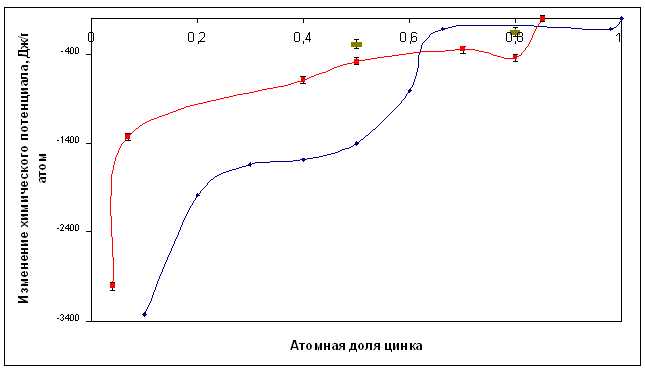
Рисунок 3 - Зависимость изменения химического потенциала от состава сплава
Кроме того было обнаружено, что значения химического потенциала цинка закаленных в жидкий азот сплавов выше на 200-300 Дж/г-атом, чем в равновесных образцах того же состава. Повышение энергии Гиббса неравновесных образцов связано с более высокой концентрацией дефектов, появлением остаточных напряжений, вызванных закалкой, наличием микротрещин и других несовершенств. Результаты рентгенофазового анализа, исследование микроструктуры и определение термодинамических характеристик, для закаленных образцов сплавов системы Al-Zn позволило выявить взаимосвязь структурных и термодинамических характеристик.
3. Заключение
В итоге проведённых исследований в сплавах Al-Zn в пределах воспроизводимости результатов эксперимента установлено:
1. Увеличение скорости закалки позволяло зафиксировать структуру α2-фазы (или х-фазы), в том числе и для образцов, не содержащих примесей. Этот вывод следует из анализа кривых распределения интенсивностей диффузного рассеяния рентгеновских лучей – вместо наблюдаемого в предыдущих экспериментах ближнего расслоения зафиксирован ближний порядок.
2. Х-фаза образуется в тонком поверхностном слое толщиной измеряемой десятыми долями миллиметра и в заметных количествах в образцах, содержащих определенные примеси, например, свинец.
3. Если поверхностный слой образца насыщен дефектами после механической обработки, то образование х-фазы существенно подавляется.
4. Образование х-фазы подтверждается независимыми термодинамическими экспериментами, выполненными методом мгновенного фиксирования ЭДС.
5. В ходе работы впервые было проведено определение термодинамических характеристик (изменений химических потенциалов) сплавов системы Al-Zn нескольких составов при комнатной температуре (Т = 295 К).
6. Полученные значения изменения химического потенциала удовлетворительно согласуются с равновесными величинами, полученными при Т = 653 К, приведенными в справочной литературе, с учетом разных температур исследования и отличия структур равновесных и неравновесных состояний образцов.
7. Апробированная методика была использована для исследования термодинамических характеристик неравновесных (закаленных) образцов системы Al-Zn. Изменение химического потенциала цинка для закаленных образцов оказалось выше (менее отрицательным), чем для незакаленных. Это может быть связано с положительным вкладом во внутреннюю энергию образцов дефектов и напряжений, вызванных закалкой.
8. Сравнение результатов рентгенофазового анализа и определение термодинамических свойств, выполненное методом МФЭ, для закаленных и равновесных образцов сплавов системы Al-Zn позволило выявить взаимосвязь структурных и термодинамических характеристик. Это может служить основой для установления дополнительных внутренних параметров, необходимых для характеристики и термодинамического описания неравновесных систем металлических сплавов
.9. Применение данного подхода и методик возможно для описания свойств неравновесных состояний в других системах, а получаемые данные могут послужить основой для оптимизации синтеза и эксплуатации
.