SORPTION CONCENTRATION DOXYLAMINE AND AMIKACIN ON ACTIVATED CARBON
Кузнецова Д.К.1, Шамина О.А.2, Шачнева Е.Ю. 3
1 Студентка 4 курса Химического факультета, Астраханский государственный университет; 2 студентка 4 курса Химического факультета, Астраханский государственный университет
3 кандидат химических наук, доцент кафедры аналитической и физической химии Астраханский государственный университет
СОРБЦИОННОЕ КОНЦЕНТРИРОВАНИЕ ДОКСИЛАМИНА И АМИКАЦИНА НА АКТИВНОМ УГЛЕ
Аннотация
Проведено изучение адсорбции доксиламина и амикацина на активном угле. Изучены изотермы сорбции, рассчитаны изменение энтальпии (∆Н), изобарно-изотермического потенциала (∆G) и энтропии (∆S) сорбции, рассмотрена кинетика сорбции.
Ключевые слова: доксиламин, амикацин, активный уголь, сорбция, фотометрия.
Кuznetsova D. K.1, Shamina О. А.2, Shachneva E. Yu.3
1Student of the 4rd course of the faculty of Chemistry, Astrakhan State University, 2 student of the 4rd course of the faculty of Chemistry, Astrakhan State University
3 candidate of chemical Sciences, senior lecturer of the Department of analytical and physical chemistry, Astrakhan State University
SORPTION CONCENTRATION DOXYLAMINE AND AMIKACIN ON ACTIVATED CARBON
Abstract
The study of the adsorption of doxylamine and amikacin on activated carbon. Studied isotherms calculated enthalpy change (∆H), isobaric-isothermal potential (∆G) and entropy (∆S) sorption kinetics of sorption considered.
Keywords: doxylamine, amikacin, active carbon, sorption, photometry.
В данной работе приведены результаты изучения адсорбции снотворных препаратов (на примере доксиламина) и аминогликозидных препаратов (на примере амикацина) активным углем с использованием фотометрического (СФ) метода исследования. Доксиламин (Донормил) – препарат по химической структуре и действию близок к димедролу и некоторым противогистаминным препаратам, блокаторам H1-рецепторов, обладающим наряду с антиаллергическим действием седативно-снотворной активностью. Амикацина сульфат - один из наиболее активных антибиотиков-аминогликозидов, обладающий широким спектром антибактериального действия [1, 2].
Построение градуировочного графика для определения доксиламина. В серию из 10 пробирок объемом 10 см3 вносили 0; 0,05; 0,1; 0,2; 0,4; 0,6; 0,8; 1,0; 1,5; 2,0 см3 раствора доксиламина с концентрацией 1·10-2 М, к раствору прибавляли по 2 см3 раствора метилового оранжевого и доводили объемы раствором хлороформом до 10 см3. Полученные растворы перемешивали и измеряли оптические плотности растворов при 430 нм в кювете толщиной 0,3 см относительно воды. По результатам измерений строили градуировочный график.
Построение градуировочного графика для определения амикацина. В серию из 10 пробирок объемом 10 см3 вносили 0; 0,05; 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8 см3 раствора амикацина с концентрацией 1·10-3 М, к раствору прибавляли по 2 см3 раствора эриохрома черного и доводили объемы растворов до 10 см3 pH 3, перемешивали и давали отстояться 1час. Далее растворы центрифугировали 10 мин при 1500 об./мин, после сливали раствор ценрифугата, оставляя образовавшиеся осадки на дне пробирок. Затем осадок растворяли 10-2 М раствором NaOH, перемешивали и измеряли оптические плотности растворов при длине волны 560 нм в кювете на 0,1 см относительно воды. По результатам измерений строили градуировочный график.
Изучение адсорбции доксиламина на активном угле. В серию из 10 пробирок объемом 10 см3 вносили 0; 0,05; 0,1; 0,2; 0,4; 0,6; 0,8; 1,0; 1,5; 2,0 см3 раствора доксиламина с концентрацией 1·10-2 М, доводили объем растворов до 6 см3 буферным раствором pH 3. В полученный раствор вносили по 0,2 г сорбента, встряхивали 3 мин, отстаивали, центрифугировали при 1500 об./мин. Сливали 5 см3 полученного раствора в пробирки, добавляли 2 см3 органического реагента метилового оранжевого и 5 см3 раствора хлороформа. Растворы стабилизировали добавлением кристаллов сульфата натрия. Полученные растворы перемешивали и измеряли оптические плотности растворов при 430 нм в кювете толщиной 0,3 см относительно воды. Опыты проводили при трех температурах.
Адсорбция амикацина на активном угле. В серию из 10 пробирок объемом 10 см3 вносили 0; 0,05; 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8 см3 раствора амикацина с концентрацией 10-3 М, доводили объем растворов до 8 см3 буферным раствором pH 3. В полученный раствор вносили по 0,2 г сорбента, встряхивали 3 мин, отстаивали, центрифугировали при 1500 об./мин. Сливали 2 см3 полученного раствора в пробирки, добавляли 2 см3 органического реагента эриохрома черного и 6 см3 раствора 10-2 М гидроксида натрия. Полученные растворы перемешивали и измеряли оптические плотности растворов при 560 нм в кювете толщиной 0,1 см относительно воды. Опыты проводили при трех температурах. Строили графические зависимости оптической плотности от концентрации амикацина.
По градуировочному графику, с использованием результатов опытов, определяли равновесные концентрации исследуемого вещества. Строили изотермы сорбции в координатах «сорбция (Г) - равновесная концентрация [c]». Сорбцию (Г) рассчитывали по уравнению (1):
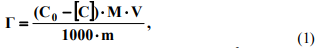
где С0 – исходная концентрация сорбата, моль/дм3; V – объем исследуемого раствора, см3; [С] – остаточная (равновесная) концентрация сорбата, моль/дм3; M – молярная (или атомная) масса сорбата, г/моль; m – масса угля, г.
Изотермы сорбции были перерассчитаны в изотермы уравнения Ленгмюра в прямолинейной форме, а с их использованием были рассчитаны константы сорбции (К) и величины предельной сорбции (Г∞) при данных температурах. По величинам констант сорбции были рассчитаны изменение энтальпии (DН) и изобарно-изотермического потенциала (DG), а с их использованием были рассчитаны значения изменения энтропии (DS) (2-4):
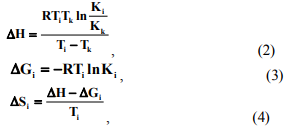
Результаты опытов и расчетов приведены в табл. 1.
Таблица 1 Основные характеристики сорбции доксиламина и амикацина на активном угле (n=6, Р=0,95, tp=2,57)
|
Определяемая характеристика |
Температура, К |
Активный уголь |
Определяемая характеристика |
Температура, К |
Активный уголь |
|
Доксиламин |
Амикацин |
||||
|
Константы сорбции · 10-2 |
277 |
0,28 |
Константы сорбции · 10-3 |
277 |
8,71 |
|
298 |
0,34 |
298 |
12,34 |
||
|
313 |
0,35 |
310 |
19,90 |
||
|
-ΔG, кДж/моль |
277 |
17,65 |
-ΔG, кДж/моль |
277 |
20,89 |
|
298 |
18,68 |
298 |
23,34 |
||
|
313 |
21,27 |
310 |
25,46 |
||
|
-ΔH, кДж/моль |
1,33 |
-ΔH, кДж/моль |
1,45 |
||
|
ΔS, Дж·моль/К |
277 |
58,10 |
ΔS, Дж·моль/К |
277 |
70,20 |
|
298 |
58,22 |
298 |
73,46 |
||
|
313 |
63,70 |
310 |
77,45 |
||
|
Емкость сорбента (Г∞), мг/г |
277 |
23,26 |
Емкость сорбента (Г∞), мг/г |
277 |
6,66 |
|
298 |
30,3 |
298 |
10,00 |
||
|
313 |
35,71 |
310 |
17,28 |
||
Полученные результаты позволяют считать, что происходит образование прочных адсорбционных комплексов, при этом емкость угля по отношению к препаратам достаточно высока.
Методика определения доксиламина. В серию из 10 пробирок объемом 10 см3 вносили 0; 0,05; 0,1; 0,2; 0,4; 0,6; 0,8; 1,0; 1,5; 2,0 см3 раствора доксиламина с концентрацией 1·10-2 М, к раствору прибавляли по 2 см3 раствора метилового оранжевого, доводили до 6 см3 буферным раствором рН 3 и до 10 см3 раствором хлороформа. Растворы перемешивали и давали отстояться 40 мин. Далее растворы центрифугировали 10 мин при 1500 об./мин, после избирали шприцом нижнею светлую часть раствора в чистые пробирки добавляли туда кристаллики сульфата натрия, перемешивали и измеряли оптические плотности при 430 нм в кювете толщиной 0,3 см. Окраска растворов получилось от прозрачного до насыщенного желтого. Окраска устойчива длительное время (рис. 1).
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
|
0 |
0,05 |
0,1 |
0,2 |
0,4 |
0.6 |
0,8 |
1,0 |
1,5 |
2,0 |
|
моль/дм3 доксиламина в пробе |
|||||||||
|
Рис. 1. Колористическая тест-шкала для определения содержания доксиламина в водных растворах |
|||||||||
Результаты определения доксиламина в водных растворах методом «введено-найдено» по предлагаемой методике представлены в табл. 2.
Методика определения амикацина. В серию из 10 пробирок объемом 10 см3 вносили 0; 0,05; 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8 см3 раствора амикацина с концентрацией 1·10-3 М, к раствору прибавляли по 2 см3 раствора эриохрома черного и доводили объемы растворов до 10 см3 pH 3, перемешивали и давали отстояться 1час. Далее растворы центрифугировали 10 мин при 1500 об./мин, после сливали раствор центрифугата, оставляя образовавшиеся осадки на дне пробирок. Затем осадок растворяли 10-2 М раствором NaOH, всё тщательно перемешивают и через 20 минут оценивают окраску раствора, которая меняется от бледно-розового до насыщенно-фиолетового. Окраска устойчива длительное время (рис. 2).
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
|
0 |
0,01 |
0,015 |
0,022 |
0,025 |
0,03 |
0,03 |
0,032 |
0,035 |
0,04 |
|
Моль/см3 амикацина в пробе |
|||||||||
|
Рис. 2. Колористическая тест-шкала для определения содержания амикацина в водных растворах |
|||||||||
Результаты определения амикацина в водных растворах методом «введено-найдено» по предлагаемой методике представлены в табл. 2.
Таблица 2 Результаты определения доксиламина и амикацина в водных растворах (n = 6, р = 0,95, tp = 2,57)
|
Введено, моль/см3 |
Содержание в пробе, моль/см3 |
Найдено, |
Содержание в пробе, моль/см3 |
Найдено, |
|
Доксиламин |
Амикацин |
|||
|
0,00 |
0,00 |
0,00 |
0,00 |
0,00 |
|
0,05 |
0,01 |
0,01±0,001 |
0,010 |
0,01±0,001 |
|
0,1 |
0,02 |
0,02±0,002 |
0,015 |
0,015±0,001 |
|
0,2 |
0,05 |
0,05±0,005 |
0,022 |
0,022±0,002 |
|
0,3 |
0,14 |
0,14±0,010 |
0,025 |
0,025±0,002 |
|
0,4 |
0,21 |
0,21±0,020 |
0,030 |
0,03±0,003 |
|
0,5 |
0,26 |
0,26±0,030 |
0,030 |
0,03±0,003 |
|
0,6 |
0,49 |
0,49±0,050 |
0,032 |
0,032±0,003 |
|
0,7 |
0,55 |
0,55±0,060 |
0,035 |
0,035±0,004 |
|
0,8 |
0,69 |
0,69±0,070 |
0,040 |
0,04±0,004 |
Таким образом, разработаны чувствительные методики определения компонентов, позволяющие определять их содержание в водных растворах, что результаты исследования могут быть внедрены в практику.
References
Машковский М.Д. Лекарственные средства. М.: ООО «Издат. Новая Волна», 2002. В 2 т. Т. 1. 540 с. 8 с. ил.
Шачнева Е.Ю., Алыков Н.М., Арчибасова Д.Е. Адсорбция кадмия из водных растворов на модифицированных сорбентах // Техника и технология пищевых продуктов. – 2012. – № 4. – С.171-176.
References
Машковский М.Д. Лекарственные средства. М.: ООО «Издат. Новая Волна», 2002. В 2 т. Т. 1. 540 с. 8 с. ил.
Шачнева Е.Ю., Алыков Н.М., Арчибасова Д.Е. Адсорбция кадмия из водных растворов на модифицированных сорбентах // Техника и технология пищевых продуктов. – 2012. – № 4. – С.171-176.
