AN EVALUATION OF THE EFFECTIVENESS OF NEOADJUVANT CHEMOHORMONAL AND HORMONAL THERAPY FOR HIGH-AND VERY HIGH-RISK PROSTATE CANCER
ОЦЕНКА ЭФФЕКТИВНОСТИ НЕОАДЪЮВАНТНОЙ ХИМИОГОРМОНАЛЬНОЙ И ГОРМОНАЛЬНОЙ ТЕРАПИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ВЫСОКОГО И ОЧЕНЬ ВЫСОКОГО РИСКА
Научная статья
Буевич Н.Н.1, *, Проценко С.А.2, Носов А.К.3, Рева С.А.4, Толмачев С.С.5, Артемьева А.С.6
1, 2, 3, 4, 5, 6 Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова Минздрава России, Санкт-Петербург, Россия;
4 Первый Санкт-Петербургский государственный медицинский университет имени И. П. Павлова Минздрава России, Санкт-Петербург, Россия
* Корреспондирующий автор (buevich_nn[at]mail.ru)
АннотацияРак предстательной железы (РПЖ) является актуальной, социально-значимой проблемой мужского населения. Около 20% пациентов имеют высокий и очень высокий риск заболевания, что говорит о более неблагоприятном прогнозе у данной группы. Тактика ведения таких больных остается спорной. В настоящее время все чаще возникает интерес к неоадъювантному лечению в попытке искоренить микрометастазы и улучшить хирургические результаты лечения. Проведение неоадъювантной терапии не является стандартным методом лечения РПЖ, однако может быть, потенциально эффективным. В данной статье мы осветим результаты собственного исследования – неоадъювантной стратегии лечения РПЖ высокого и очень высокого риска.
Ключевые слова: рак предстательной железы, неоадъювантная терапия, высокий риск, химиотерапия, гормонотерапия.
AN EVALUATION OF THE EFFECTIVENESS OF NEOADJUVANT CHEMOHORMONAL AND HORMONAL THERAPY FOR HIGH-AND VERY HIGH-RISK PROSTATE CANCER
Research article
Buevich N.N.1, *, Protsenko S.A.2, Nosov A.K.3, Reva S.A.4, Tolmachev S.S.5, Artemyeva A.S.6
1, 2, 3, 4, 5, 6 N.N. Petrov Research Institute of Oncology, St. Petersburg, Russia;
4 First Pavlov State Medical University of St. Petersburg, St. Petersburg, Russia
* Corresponding author (buevich_nn[at]mail.ru)
AbstractProstate cancer is an relevant, socially significant problem among the male population. About 20% of patients have a high and very high risk of this disease, which indicates a more unfavorable prognosis in this group, while the tactics of managing such patients remains controversial. Currently, there is an increasing interest in neoadjuvant treatment in an attempt to eradicate micrometastases and improve the results of surgical treatment. Neoadjuvant therapy is not a standard method of treating prostate cancer, but it has the potential to be effective. The article highlights the results of an originak study – a neoadjuvant strategy for the treatment of high-and very high-risk prostate cancer.
Keywords: prostate cancer, neoadjuvant therapy, high risk, chemotherapy, hormone therapy.
Введение
Рак предстательной железы (РПЖ) является одной из наиболее важных, социально значимых медицинских проблем, так как данная опухоль лидирует в структуре онкологической заболеваемости и смертности [1, С.244].
Важнейшую роль в выборе тактики лечения имеет определение группы риска [2, С. 476]. Около 20% пациентов, на момент постановки диагноза, относятся к группе высокого риска развития рецидива заболевания [3, С. 211], [4, С. 2164]. Данная группа пациентов имеет более неблагоприятный прогноз в отношении прогрессирования, метастазирования и выживаемости [5, С. 343]. РПЖ высокого и очень высокого риска является потенциально летальным заболеванием, требующим активного мультимодального подхода, опции и режимы которого в настоящее время широко обсуждаются [6, С. 1082].
Однако, тактика ведения больных таких больных остается спорной. Ввиду того, что около 15% пациентов не отвечают на проводимые локальные методы лечения, что требует дополнительных поисков методов терапии [7, С. 343].
В настоящее время все чаще возникает интерес к неоадъювантному лечению в попытке искоренить микрометастазы и улучшить хирургические результаты лечения [8, С. 20]. Проведение неоадъювантной терапии не является стандартным методом лечения РПЖ, однако может быть, потенциально эффективным [9, С.339].
Учитывая все вышесказанное, целесообразно проведение исследования эффективности применения доцетаксела и дегареликса в качестве неоадъювантной химиогормонотерапии и неоадъювантной гормональной терапии в монорежиме перед радикальной простатэктомией при раке предстательной железы высокого риска с целью улучшения результатов лечения пациентов с данной патологией.
Методы и принципы исследования
В исследование включено 138 больных РПЖ высокого и очень высокого риска развития прогрессирования, получавших лечение в НМИЦ онкологии им. Н.Н. Петрова в период с марта 2014 г. по август 2019 г.
Критериями высокого и очень высокого риска являются: ПСА>20 нг/мл и/или сумма баллов по шкале Глисона >8 и/или клиническая стадия > T2c.
Пациенты разделены на 3 группы. Первой группе пациентов выполнялось оперативное лечение, в объеме РПЭ (n=46). Второй группе пациентов проводилась неоадъювантная химиогормональная (ХГТ) терапия (химиотерапия доцетакселом (75 мг/м2, в/в, кап, 1 раз в 21 день) в сочетании с гормонотерапией антагонистом гонадотропин релизинг-гормона (ГнРГ) дегареликсом (в инициальной дозе 240 мг, разделенной на 2 введения по 120 мг, далее в поддерживающем режиме по 80 мг, 1 раз в 28 дней, п/к) с последующим хирургическим лечением (ХГТ+РПЭ, n=46). Третья группа была набрана ретроспективно, в ней применялись различные варианты гормональной поддержки (антагонисты гонадотропин релизинг-гормона, терапия агонистами лютеинизирующего гормона релизинг гормона, терапия антиандрогенами, а также МАБ (комбинации антиандрогенов и аналогов ЛГРГ). Учитывая сопоставимость эффективности препаратов гормональной терапии (ГТ), пациенты были объединены в одну группу.
Пациенты во всех трех группах были сопоставимы по возрасту, объему предстательной железы (р=0,435), уровню общего ПСА (р=0,684). Средний возраст пациентов в группе РПЭ составил 62,08±6,67, в группе ХГТ+РПЭ - 62,89±7,25, в группе ГТ+РПЭ - 63,07±5,60 (р=0,472). Медиана объема предстательной железы в группе РПЭ составила 46,86±17,76, в группе ХГТ+РПЭ - 51,61±37,47, в группе ГТ+РПЭ - 37,90±11,09 (р=0,435). Медиана уровня ПСА в группе РПЭ составила 29,47±31,13, в группе ХГТ+РПЭ - 34,62±34,85, в группе ГТ+РПЭ - 27,15±29,70 (р=0,684).
Основными объективными критериями оценки эффективности лекарственного лечения РПЖ остаются динамика ПСА и изменение объема предстательной железы. Нами проведена сравнительная оценка данных параметров.
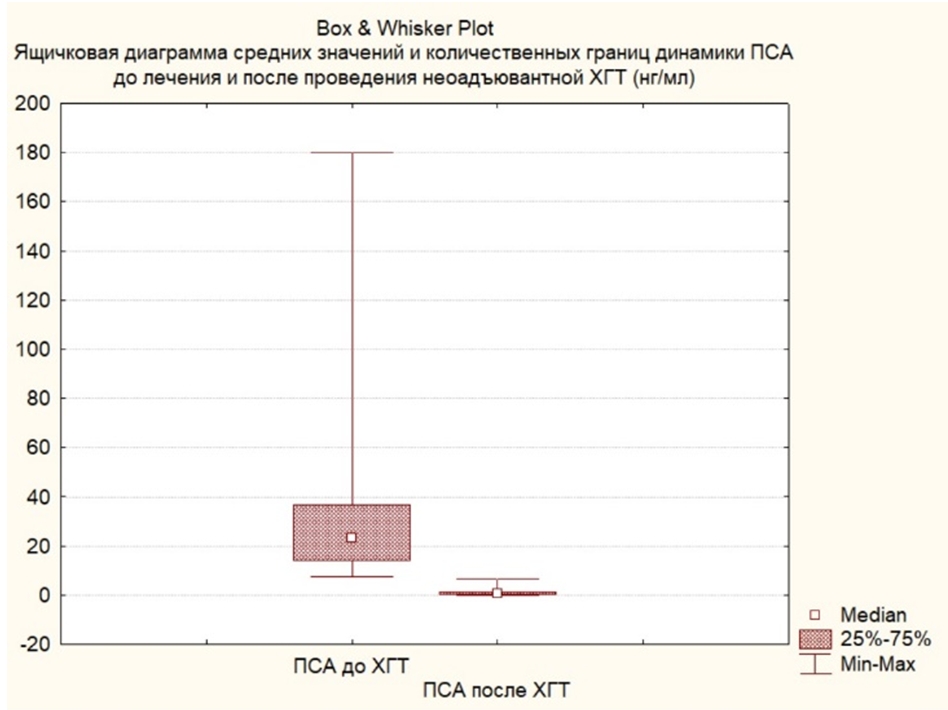
Уровень ПСА до начала лечения в группе пациентов, получавших неоадъювантную ХГТ, в среднем составил 34,6 нг/мл (7,4-180 нг/мл). После проведенного лечения уровень антигена в среднем составлял 1,3 нг/мл (0,001– 6,5 нг/мл), отмечено статистически значимое снижение показателя в 27 раз, р= 0,001 (см. рисунок 1).
Рис. 1 – Динамика уровня ПСА на фоне неоадъювантной ХГТ
Примечание: р= 0,001
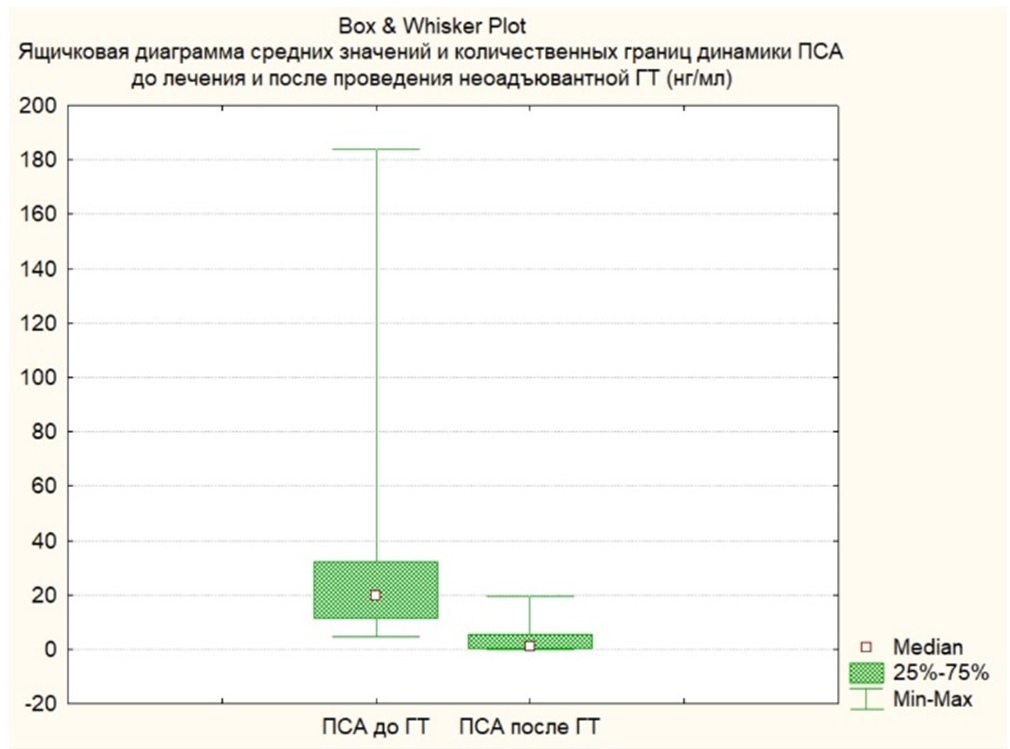
Уровень ПСА до начала лечения в группе пациентов, получавших неоадъювантную ГТ, в среднем составил 27 нг/мл (4,6-184 нг/мл). После проведенного лечения уровень антигена в среднем составлял 3,4 нг/мл (0,04 -19,50 нг/мл), отмечено статистически значимое снижение показателя в 7,7 раз, р= 0,001 (см. рисунок 2).
Рис. 2 – Динамика уровня ПСА на фоне неоадъювантной ХГТ
Примечание: р= 0,001
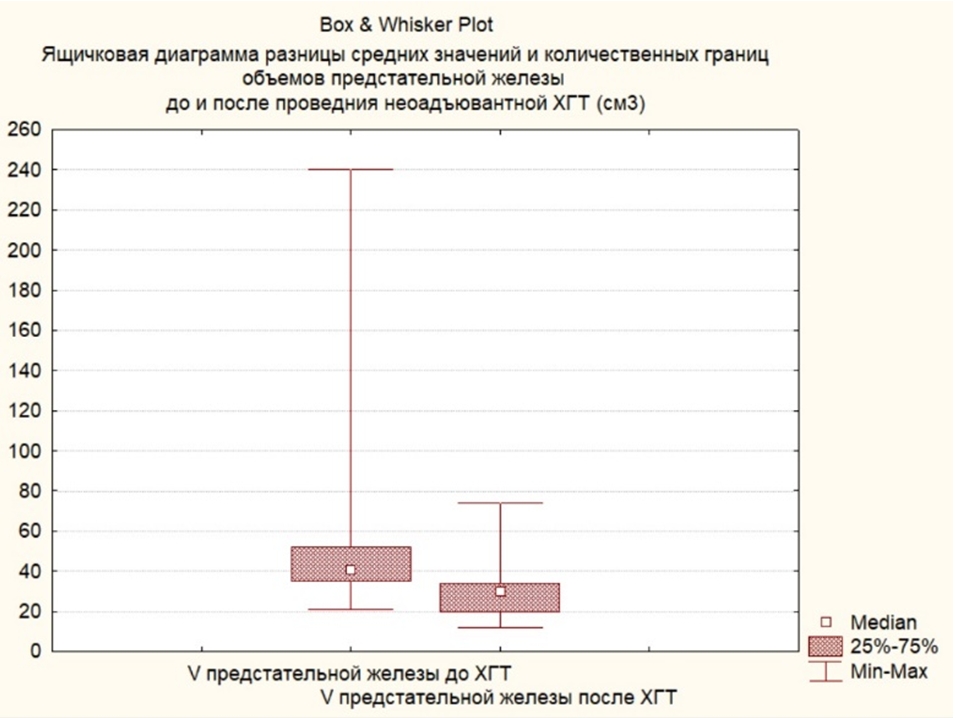
Объем предстательной железы до начала лечения в группе пациентов, получавших неоадъювантную ХГТ, в среднем составил 51,6 см3 (21-240 см3). После проведенного лечения объем железы в среднем составлял 30,9 см3 (12-74 см3), отмечено статистически значимое снижение показателя в 1,6 раз, р=0,001 (см. рисунок 3).
Рис. 3 – Динамика объема предстательной железы на фоне неоадъювантной ХГТ
Примечание: р= 0,001
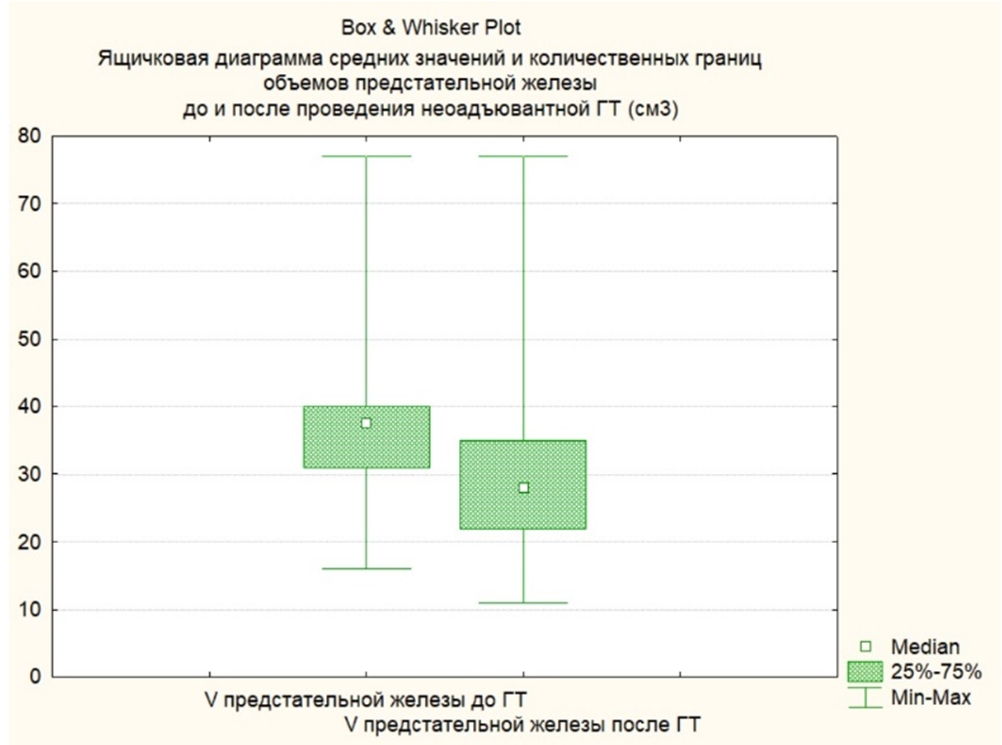
Объем предстательной железы до начала лечения в группе пациентов, получавших неоадъювантную ГТ в среднем составил 38 см3 (16-77 см3). После проведенного лечения объем простаты в среднем составлял 30 см3 (11-77 см3), отмечено статистически незначимое снижение показателя в 1,2 раза (р=0,001) (см. рисунок 4).
Рис. 4 – Динамика объема предстательной железы на фоне неоадъювантной ГТ
Примечание: р= 0,001
В нашей работе оценены нежелательные (НЯ) на фоне неоадъювантного лекарственного лечения доцетакселом в сочетании с дегареликсом, а также самостоятельной ГТ, в соответствии с Международной терминологией критериев НЯ (CTCAE) v5.0. от 2017 года. За время проведения исследования в группе пациентов неоадъювантной ХГТ всего выполнено 266 введений доцетаксела и дегареликса.
НЯ в группе ХГТ наблюдались у 89% пациентов. Основную часть осложнений составили НЯ 1-2 ст., корректировались симптоматической терапией, что не повлияло на проводимую лечебную тактику. НЯ 3-4 степени наблюдались у 21,7% пациентов. Редукция дозы доцетаксела произведена в следствии серьезных НЯ, таких как, фебрильной нейтропении, периферической нейропатии, стоматита, герпетической инфекции, астении.
Опосредованно, гормональное лечение, как компонент неоадъювантной схемы или в монорежиме, не привело к развитию серьезных нежелательных явлений. Суммарно проведено 270 циклов гормональной неоадъювантной терапии. Основную часть НЯ ГТ составили осложнения 1-2 степени и были отмечены у 89% мужчин. Спектр НЯ был достаточно разнообразен: наибольший дискомфорт доставляли пациентам болезненность и инфильтрат передней брюшной стенки в месте введения препарата, а также потливость и чувство приливов.
Обсуждение результатовНами проведен анализ литературных данных с целью оценки сопоставимости результатов нашего исследования. Основными критериями эффективности проводимого комбинированного лечения рака простаты в неоадъювантном режиме считаются динамика ПСА, изменение объема железы. В большинстве работ отмечено снижение уровня антигена на фоне лекарственной терапии перед оперативным этапом лечения, а также уменьшение объема самой железы. Более доступным методом определения объема простаты остается проведение МРТ до и после неоадъювантного лечения [10, С. 4778].
В ходе проведения нашего исследования получена высокая частота ответа пациентов по данным показателям. В 95% случаев уровень ПСА снижался более, чем на 50% у пациентов в группе ХГТ+РПЭ и в 78% в группе неоадъювантной ГТ+РПЭ. Полученные нами результаты сопоставимы с литературными данными. У двух пациентов в обеих группах отмечено повышение ПСА на фоне проведенного лечения и расценено как прогрессирование заболевания.
При изучении безопасности предложенного нами неоадъювантного лекарственного лечения у больных РПЖ высокого риска был выявлен приемлемый профиль токсичности проводимой противоопухолевой терапии. Высокой степени токсичности с летальным исходом не наблюдалось.
Подводя итог, можно отметить, что основная масса НЯ в обеих группах неоадъювантной терапии не превышала 1-2 степени тяжести, что говорит о приемлемом профиле токсичности и переносимости терапии у больных РПЖ высокого риска. НЯ 3-4 степени, отмечены только в группе неоадъювантной ХГТ+РПЭ, что обусловлено многокомпонентностью схемы лекарственной лечения. Увеличение интервала до проведения РПЭ после неоадъювантной терапии потребовалось 4 пациентам (8,6%), что было связано с НЯ. Наиболее частыми побочными эффектами в группе дегареликса были реакции в месте инъекции. Стоит сказать, что у 5 пациентов (10,8%) получающих неоадъювантную ХГТ и у 5 пациентов (10,8%), получавших неоадъювантную ГТ, не было отмечено НЯ за период лечения.
Заключение
Анализ результатов проведенного исследования неоадъювантной лекарственной терапии показал высокую клиническую эффективность предложенного вида лечения на основании динамики уровня ПСА и объема предстательной железы (р=0,001).
Предложенный вариант неоадъювантного лечения показал приемлемый профиль токсичности и переносимости у пациентов группы высокого и очень высокого риска.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Epstein, J.I. The 2014 International Society of Urological Pathology (ISUP) Consensus Conference on Gleason Grading of Prostatic Carcinoma: Definition of Grading Patterns and Proposal for a New Grading System / J.I.Epstein [et al.] // Am. J. Surg. Pathol. – 2016. – №40. – pp.244.
- Ferris M.J. The Addition of Chemotherapy in the Definitive Management of High Risk Prostate Cancer / Matthew J Ferris, Yuan Liu, Jingning A.O. [et al.] // Urol. Oncol. – 2018. – Vol.36(11). – pp. 475-487.
- Cooperberg M.R. High-risk prostate cancer in the United States, 1990–2007 / Cooperberg M.R., Cowan J., Broering J.M. et al. // World J Urol 2008;26(3):211–8. DOI: 10.1007/s00345-008-0250-7.
- D’Amico A.V. Cancer-specific mortality after surgery or radiation for patients with clinically localized prostate cancer managed during the prostate-specific antigen era / D’Amico A.V., Moul J., Carroll P.R. et al. // J Clin Oncol 2003; 21:2163–72. DOI: 10.1200/JCO.2003.01.075.
- Mano R. The very high risk prostate cancer – a contemporary update / R. Mano, J. Eastham, O. Yossepowitch // Prostate Cancer Prostatic Dis. – 2016. – Vol.19, №4. – pp. 340–8.
- Mohler J.L. Prostate cancer, Version 3.2012: featured updates to the NCCN guidelines / Mohler J.L., Armstrong A.J., Bahnson R.R. et al. // J. Natl. Compr. Canc. Netw. — 2012. — Vol. 10. — P. 1081–1087.
- Joniau S. Results of surgery for high-risk prostate cancer / Joniau S, Tosco L, Briganti A. et al. // Curr Opin Urol 2013;23(4):342-348
- Thalgott M. Long-term results of a phase II study with neoadjuvant docetaxel chemotherapy and complete androgen blockade in locally advanced and high-risk prostate cancer / M.Thalgott, T.Horn, M.M. Heck [et al.] // J. Hematol Oncol. – 2014. – №7. –pp.20.
- Goldberg H. Defining high-grade prostate cancer / Goldberg H., Baniel J., Yossepowitch O. // Curr. Opin. Urol. — 2013. — Vol. 23. — P. 337-341. — DOI: 10.1097/MOU.0b013e328361dba6.
- Ross R.W. Phase II study of neoadjuvant chemotherapy with docataxel and bevacizumab in patients with high-risk localized prostate cancer: a prostate cancer clinical trials consortium trial / R.W. Ross, M.D. Galsky, P. Febbo [et al.] // Cancer. – 2012. – Vol.118(19). – pp. 4777-4784