The role of thrombodynamics in the course of acute pancreatitis: from predicting complications to personalized therapy
The role of thrombodynamics in the course of acute pancreatitis: from predicting complications to personalized therapy
Abstract
The article presents the results of a retrospective analysis of data from a controlled clinical and laboratory study of patients with acute pancreatitis. The parameters of the thrombin generation test were examined, and their potential contribution to optimizing treatment approaches for this condition was assessed.
The aim of this research was to establish a correlation between the severity of patients’ condition and serum fibrin levels, as well as to determine the impact of these indicators on the development of treatment strategies for various forms of pancreatitis. Based on the obtained data, the development and subsequent clinical evaluation of the effectiveness of an optimized diagnostic and treatment algorithm for patients with acute pancreatitis is planned.
1. Введение
Острый панкреатит представляет собой асептическое воспаление, протекающее по демаркационному типу. Ключевым звеном его патогенеза выступает некротическое поражение ацинарных клеток паренхимы поджелудочной железы в сочетании с феноменом ферментной агрессии. Данные процессы инициируют нарастающие дистрофические и деструктивные изменения в органе, которые часто распространяются на парапанкреатическую клетчатку и создают предпосылки для развития вторичной гнойной инфекции .
Возникающее воспаление запускает каскад реакций в системе гемостаза, что проявляется снижением активности естественных антикоагулянтных механизмов и расстройствами в работе фибринолиза. Такие нарушения существенно повышают вероятность возникновения тромботических событий у пациентов , .
Диагностика деструктивных форм панкреатита сегодня строится на комплексном подходе, направленном на определение степени тяжести состояния и степени полиорганной недостаточности. Этот подход подразумевает использование лабораторных анализов, инструментальных исследований и различных прогностических шкал , . Тем не менее, в ряде случаев, особенно при тяжёлых органных дисфункциях в первую неделю болезни, стандартные методы визуализации (УЗИ и МСКТ) могут оказаться недостаточно информативными для точного выявления зон панкреонекроза, что представляет значительную проблему для клиницистов , .
Невозможность чётко верифицировать патологический процесс и дать ему однозначную клиническую оценку при остром панкреатите сужает возможности для выбора оптимальной тактики лечения. Это нередко ведёт к запаздыванию с принятием ключевых врачебных решений у таких больных . В этих условиях эффективность рутинных диагностических алгоритмов ограничена, что актуализирует поиск и внедрение более совершенных методик. Их цель — обеспечить высокоточную диагностику и, как результат, повысить эффективность ведения пациентов в критических состояниях .
2. Материалы и методы
Клинический материал исследования составили данные 50 пациентов в возрастном интервале от 20 до 50 лет, с диагностированным острым панкреатитом средней степени тяжести и тяжёлого течения. Пациенты проходили лечение в экстренных хирургических стационарах города Чита в период с 2022 по 2024 год.
Всем участникам исследования в течение первых 24 часов после поступления, а также при наличии клинических показаний в последующие дни, осуществлялся забор образцов венозной крови. Для этой цели использовались вакуумные системы забора крови VACUTAINER, содержащие 3,2% цитрат натрия в качестве антикоагулянта. Отобранные пробы объёмом 2,5 мл подвергались двухэтапному центрифугированию для получения бестромбоцитарной плазмы. Полученная плазма незамедлительно помещалась в измерительные ячейки оригинальной кюветы, входящей в комплект «Анализатора тромбодинамики Т2-Т (СЛ АТ Т2-Т)».
В ячейку устанавливалась активирующая вставка, поверхность которой была покрыта иммобилизованным тканевым фактором и фосфолипидным матриксом, имитирующим субэндотелиальный слой повреждённой сосудистой стенки. При контакте плазмы с иммобилизованным тканевым фактором происходила активация каскада реакций свёртывания, что инициировало локальное образование фибринового сгустка и его последующее пространственное распространение в объёме плазмы.
Процесс роста фибринового сгустка регистрировался в реальном времени с использованием метода тёмного поля микроскопии. Для этого применялась цифровая камера, осуществляющая покадровую съёмку. Анализ полученных изображений выполнялся автоматизированным программным обеспечением анализатора. Программа на основе видеопотока в динамике определяла геометрические параметры растущего сгустка, строила графическую зависимость его линейного размера от времени и вычисляла ключевые показатели тромбодинамики: линейную скорость роста фибрина и стабильный размер фибринового сгустка.
Прогрессивное увеличение параметров динамики фибрина Cs (размер роста сгустка) через 30 минут ≥ 1900 мин и Vi (начальная скорость сгустка) ≥ 71 мкм/мин, отражающие фазу распространения свертывания, в течение не менее первых суток от начала заболевания, позволяет прогнозировать отрицательное течение заболевания на фоне проводимой терапии с развитием панкреонекроза, с последующим вторичным инфицированием, формированием абсцессов и кист ткани поджелудочной железы.
Статистическая обработка проводилась с использованием пакета программ Statistica 21.
3. Случай из практики
3.1. Пример 1
Анамнез и первичное обследование. Пациент А., 50 лет, доставлен в стационар экстренно через 24 часа от дебюта заболевания с клинической картиной, включающей интенсивный диффузный абдоминальный болевой синдром и тошноту. При поступлении диагностировано тяжёлое общее состояние. Объективно: кожные покровы физиологической окраски. Отмечалась тахикардия до 100 уд./мин. на фоне выраженной артериальной гипотензии (АД 90/50 мм рт. ст.). Пальпаторно определялся вздутый, резко болезненный во всех отделах живот с положительными перитонеальными симптомами.
Результаты первичного лабораторно-инструментального обследования. Ультразвуковое исследование выявило диффузные структурные изменения поджелудочной железы. В общеклиническом анализе крови зафиксирован лейкоцитоз до 24,51×10⁹/л. Биохимические и коагулологические показатели: амилаза крови — 210 U/L, МНО — 1,12, уровень фибриногена — 3,2 г/л, АЧТВ — 27,8 сек. Методом тромбодинамики исследованы параметры пространственного роста фибрина: стационарный размер сгустка (Cs через 30 мин.) составил 1982 мкм, начальная скорость роста (Vi) — 79,2 мкм/мин.
Хирургическое вмешательство и послеоперационный период. На фоне отрицательной клинической динамики пациенту после кратковременной предоперационной подготовки выполнена диагностическая лапаротомия. Интраоперационно обнаружен значительный объём серозно-фибринозного экссудата в верхних отделах брюшной полости и некроз пряди большого сальника в парапанкреатической зоне. Произведено дренирование брюшной полости с формированием управляемой лапаростомы. Послеоперационный диагноз: «Острый деструктивный панкреатит тяжёлой степени. Распространённый серозно-фибринозный перитонит». Пациент переведён в отделение реанимации для проведения инфузионной и комплексной медикаментозной терапии.
Динамика состояния на 3-и сутки. Сохранялось тяжёлое состояние, прогрессировали гипотензия и анурия. По лапаростоме отмечалось серозно-гнойное отделяемое. Компьютерная томография подтвердила увеличение объёма поджелудочной железы, снижение её плотности, наличие отёка и инфильтрации парапанкреатической клетчатки. Лабораторные показатели: лейкоцитоз 19,3×10⁹/л, амилаза 211 U/L, фибриноген 3,8 г/л, АЧТВ 37,1 сек. Контрольное исследование тромбодинамики: Cs — 2001 мкм, Vi — 81,2 мкм/мин.
Исход и патологоанатомическое заключение. Несмотря на проводимую интенсивную терапию, на 4-е сутки стационарного лечения наступил летальный исход вследствие прогрессирующей полиорганной недостаточности. При патологоанатомическом исследовании выявлен субтотальный некроз паренхимы поджелудочной железы (головка, тело, частично хвост) с участками гнойного расплавления в области тела органа. В парапанкреатической клетчатке обнаружены очаги гнойного воспаления по типу флегмоны размером 2–3 см. Гистологически верифицирован субтотальный некроз головки железы с массивной нейтрофильной инфильтрацией (гнойный панкреатит) и явлениями гнойного перипанкреатита (см. рис. 1)
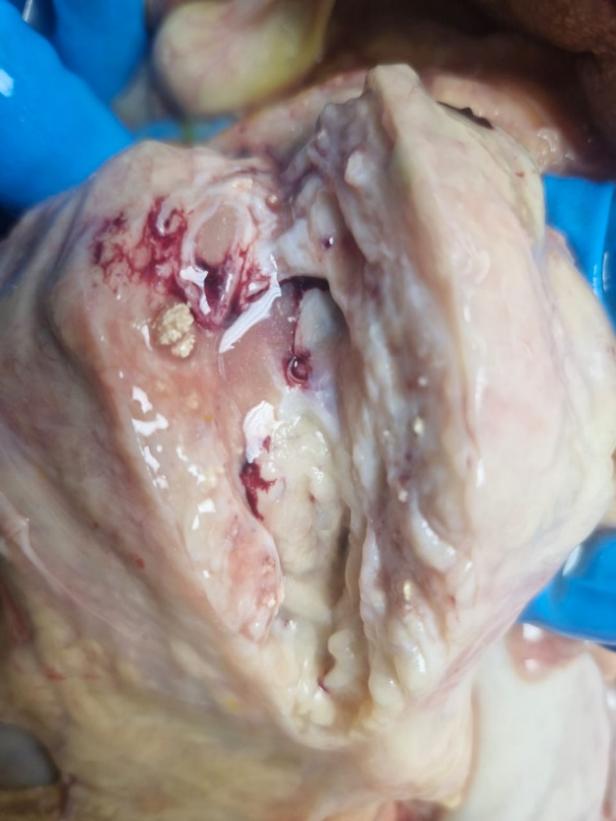
Рисунок 1 - Пример аутопсийного материала, деструктивные изменения поджелудочной железы
3.2. Пример 2
Анамнез и первичное обследование. Пациентка Д., 38 лет, доставлена в хирургический стационар в экстренном порядке спустя 48 часов от момента дебюта заболевания. При поступлении предъявляла жалобы на абдоминальную боль, тошноту и рвоту. Объективно состояние было расценено как средней степени тяжести. Кожные покровы были обычной окраски, видимые слизистые чистые. Гемодинамические показатели: ЧСС 82 уд./мин., артериальное давление 124/80 мм рт. ст. При осмотре живота: конфигурация симметричная, участвует в дыхании, при пальпации определяется резкая локальная болезненность в эпигастральной области. Симптомы раздражения брюшины отрицательные.
Результаты первичного лабораторно-инструментального обследования. Ультразвуковое исследование органов брюшной полости выявило диффузные структурные изменения поджелудочной железы. В общеклиническом анализе крови отмечен лейкоцитоз — 14,27×10⁹/л. Биохимический и коагулологический анализ крови показал: уровень амилазы 225 U/L, МНО 1,37, концентрация фибриногена 2,2 г/л, АЧТВ 23,9 сек. В рамках углублённого гемостазиологического обследования методом тромбодинамики получены следующие параметры: стационарный размер фибринового сгустка (Cs через 30 мин.) составил 1912 мкм, начальная скорость его роста (Vi) — 68,5 мкм/мин.
Динамика состояния и коррекция терапии. Пациентка была госпитализирована в хирургическое отделение, где была начата комплексная консервативная терапия, включавшая инфузионную, спазмолитическую, антибактериальную терапию, а также аналоги соматостатина. Через два часа после поступления отмечено ухудшение состояния в виде нарастания абдоминального болевого синдрома. В связи с этим выполнена блокада круглой связки печени и к лечению добавлены препараты антикоагулянтного действия. К третьим суткам стационарного лечения устойчивой положительной динамики достичь не удалось: сохранялся болевой синдром, тошнота, при осмотре положительные симптомы разражения брюшины.
Контрольное обследование на третьи сутки. Повторный лабораторный контроль выявил следующие показатели: лейкоциты 14,1×10⁹/л, амилаза 187 U/L, фибриноген 2,8 г/л, АЧТВ 32,4 сек. Повторное исследование тромбодинамики показало изменение параметров: Cs — 14 мкм, Vi — 59,3 мкм/мин. Данные компьютерной томографии поджелудочной железы свидетельствовали о сохраняющемся увеличении её объёма, снижении плотности паренхимы, а также о наличии отёка и инфильтративных изменений в парапанкреатической клетчатке.
Хирургическое вмешательство и исход лечения. Принято решение о выполнении диагностической лапароскопии. Интраоперационно обнаружен серозный выпот в брюшной полости, множественные очаги стеатонекроза и участки геморрагического пропитывания забрюшинной клетчатки. В качестве лечебно-диагностического мероприятия выполнено дренирование сальниковой сумки. В послеоперационном периоде пациентка продолжила стационарное лечение в течение 14 дней. При контрольном ультразвуковом исследовании поджелудочной железы накануне выписки были отмечены неровность её контуров, наличие единичных кистозных образований, а также повышение эхогенности паренхимы, что расценено как признак формирования очагов фиброза.
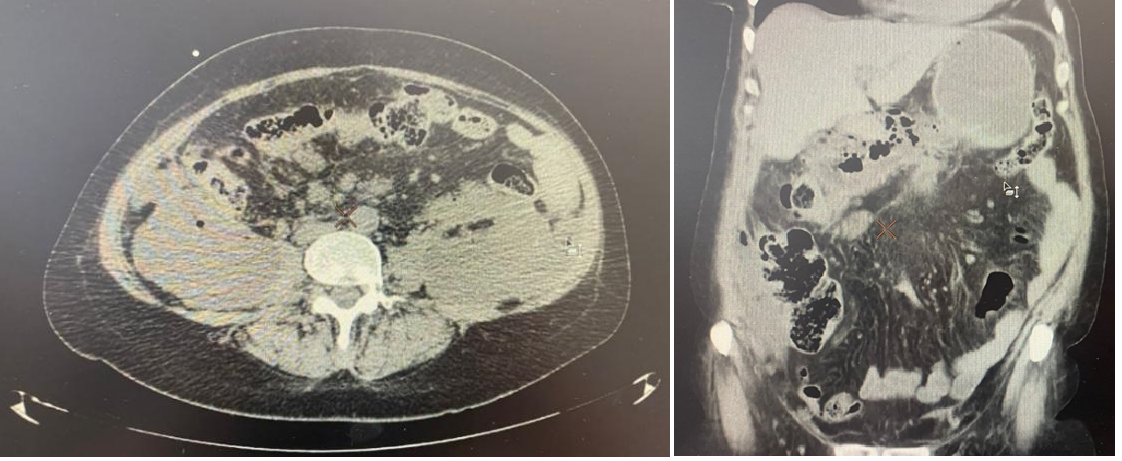
Рисунок 2 - Пример компьютерной томографии течения острого панкреатита
3.3. Пример 3
Анамнез и первичное обследование. Пациент Т., 27 лет, доставлен в стационар по экстренным показаниям через 24 часа от момента появления первых симптомов. Основными жалобами при госпитализации были болевые ощущения в верхних отделах живота и общая слабость. При объективном осмотре состояние было классифицировано как средней степени тяжести. Кожные покровыбез патологических изменений. Показатели гемодинамики были стабильными: ЧСС 72 уд./мин., артериальное давление 125/74 мм рт. ст. При пальпации живота выявлена резкая локальная болезненность в эпигастральной области; живот мягкий, симметричным, участвует в дыхательных движениях. Перитонеальные симптомы отрицательные.
Результаты первичного лабораторно-инструментального обследования. Ультразвуковое исследование визуализировало диффузные изменения структуры поджелудочной железы. Общеклинический анализ крови показал умеренный лейкоцитоз (10,6×10⁹/л). Результаты биохимического и коагулологического исследования сыворотки крови: активность амилазы — 321 U/L, МНО — 1,29, концентрация фибриногена — 3,7 г/л, АЧТВ — 24,9 сек. В рамках дополнительного обследования проведена оценка тромбодинамики. Исходные параметры пространственного роста фибрина составили: стационарный размер сгустка (Cs через 30 мин.) — 1430 мкм, начальная скорость его формирования (Vi) — 50,2 мкм/мин.
Лечебная тактика и динамика состояния. Пациент госпитализирован, ему назначена комплексная консервативная терапия, включавшая инфузионные растворы, спазмолитики, антибактериальные препараты, аналоги соматостатина к лечению добавлены антикоагулянты. На фоне проводимого лечения отмечена положительная клиническая динамика. К третьим суткам госпитализации наблюдалась значительная регрессия симптоматики.
Контрольное обследование на третьи сутки. Данные повторного лабораторного мониторинга демонстрировали нормализацию показателей: уровень лейкоцитов снизился до 6,2×10⁹/л, активность амилазы уменьшилась до 182 U/L. Коагулограмма показала следующие значения: фибриноген 2,1 г/л, АЧТВ 25,3 сек. Повторное исследование тромбодинамики выявило тенденцию к нормализации показателей гемостаза: Cs составил 1012 мкм, Vi — 46,2 мкм/мин.
Исход и отдалённое наблюдение. Пациент был выписан из стационара на 10-е сутки от начала заболевания в удовлетворительном состоянии. При контрольном ультразвуковом исследовании органов брюшной полости, проведённом через один месяц, признаков формирования очагов некроза паренхимы, псевдокист или других остаточных структурных изменений выявлено не было.
3.4. Пример 4
Анамнез и первичное обследование. Пациент Г., 47 лет, был госпитализирован в экстренном порядке в отделение общей хирургии через 5 часов от момента манифестации заболевания. При поступлении предъявлял жалобы на интенсивный разлитой болевой синдром в животе, сопровождающийся тошнотой и рвотой. Объективный статус соответствовал состоянию средней степени тяжести. Гемодинамические показатели оставались в пределах нормы: частота сердечных сокращений 72 уд./мин., артериальное давление 128/74 мм рт. ст. При обследовании органов брюшной полости живот был симметричным, мягким, активно участвовал в дыхательных движениях; пальпаторно определялась болезненность в проекции эпигастрия. Симптомы раздражения брюшины отрицательные.
Результаты первичной диагностики. Ультрасонография органов брюшной полости визуализировала диффузные изменения паренхимы поджелудочной железы. Общий клинический анализ крови выявил лейкоцитоз (12,76×10⁹/л). Биохимический и коагулологический анализ сыворотки крови показал: амилаза (310 U/L) при следующих параметрах гемостаза: МНО — 1,26, уровень фибриногена — 3,3 г/л, АЧТВ — 31,7 сек. Проведённое исследование тромбодинамики зафиксировало исходные параметры: стационарный размер фибринового сгустка (Cs) через 30 минут составил 1438 мкм, а начальная скорость его роста (Vi) — 56,2 мкм/мин.
Лечебная тактика и динамическое наблюдение. После госпитализации была инициирована комплексная консервативная терапия, включающая инфузионную поддержку, спазмолитики, антибактериальные препараты и аналоги соматостатина. С учётом данных тромбодинамики в схему лечения были включены антикоагулянты. На фоне проводимого лечения отмечалась положительная клинико-лабораторная динамика. Контрольное исследование тромбодинамики на третьи сутки продемонстрировало тенденцию к нормализации показателей: значение Cs снизилось до 987 мкм, а Vi — до 42,1 мкм/мин.
Исход и отдалённые результаты. Пациент был выписан из стационара на 8-е сутки стационарного лечения в удовлетворительном состоянии. При контрольном ультразвуковом исследовании, проведённом через один месяц после выписки, сохранялись признаки диффузных изменений структуры поджелудочной железы. Однако признаков формирования кистозных полостей или локальных участков фиброза выявлено не было, что свидетельствует об отсутствии тяжёлых деструктивных осложнений в исходе заболевания.
4. Заключение
Проведённое исследование демонстрирует, что анализ параметров системы фибриногена у пациентов с острым панкреатитом обладает прогностической значимостью в отношении риска развития деструктивных форм заболевания. Изменения данных показателей регистрируются на этапе, предшествующем появлению развёрнутых клинических и инструментальных признаков осложнений, что позволяет своевременно корректировать лечение.
