A case of acute drug-induced liver injury in the treatment of osteoarthritis
A case of acute drug-induced liver injury in the treatment of osteoarthritis
Abstract
The problem of drug-induced liver injury (DILI) is becoming more and more urgent every year. The widespread use of numerous antibiotics and other drugs during the COVID-19 pandemic, the use of over-the-counter biologically active herbal and other drugs, taking medications without a doctor's prescription – all this has led to an increase in the incidence of DILI.
Acute hepatitis is now a widely known manifestation, and accounts for more than 90% of drug-induced liver damage. Most often, liver damage develops when prescribing drugs from the group of non-steroidal anti-inflammatory drugs used in the treatment of pathology of the bone and joint system. The necessity of early diagnosis, difficult differential-diagnostic search, lack of specific laboratory tests make this pathology quite difficult for the practitioner.
1. Введение
Впервые о повреждающем действии лекарств на организм заговорили в начале 20 века. С тех пор частота лекарственной патологии только растет
.Лекарственные поражения печени (ЛПП) – это разнородная группа клинико-морфологических вариантов повреждения печени, причиной развития которых явилось применение лекарственных средств по медицинским показаниям в терапевтических дозах и введенных в организм предусмотренными для каждого медикамента путями.
Наиболее часто ЛПП развиваются при применении противотуберкулезных и антибактериальных средств, НПВП, гормональных препаратов, цитостатиков, гипотензивных и антиаритмических препаратов
, , , . В последние годы обращает на себя внимание рост случаев ЛПП в результате употребления биологически активных добавок (БАД) . Лекарства, поражающие печень, подразделяют на 2 группы .Первая группа – истинные гепатотоксины, оказывающие прямое поражающее действие на печень. Повреждение регистрируется у большого числа пациентов, принимающих эти препараты. При этом период от приема лекарств до появления клинических признаков повреждения печени короткий, эффект дозозависимый, в целом, поражение печени ожидаемо, может быть отслежено. К этой группе принадлежат нестероидные противовоспалительные средства (парацетамол), салицилаты (аспирин), антиметаболиты, цитостатики., иммунодеперссанты (метатрексат, циклофосфамид, циклоспорин), антибиотики (тетрациклин), некоторые антиаритмики (амиодарон).
Вторая группа – гепатотоксины, активность которых определяется действием их метаболитов. Их действие непредсказуемо и не зависит от дозы. Поражение развивается лишь у небольшого числа пациентов, имеющих предрасположенность к иммуноаллергическим реакциям. Сроки появления симптомов неизвестны, изменения могут появиться спустя несколько месяцев после приема препаратов или их отмены, и их не всегда связывают с лекарственным воздействием. Такой тип поражения может вызвать любой препарат, но с наибольшей частотой он регистрируется при применении изониазида, сульфаниламидов флуконазола, кетоканазола, фторотана, вальпроата натрия, зидовудина и ряда других.
К факторам риска развития ЛПП относятся старший возраст, женский пол, наличие предшествующей патологии печени, ожирение или снижение массы тела, диабет, полипрагмазия, межлекарственные взаимодействия, курение, употребление алкоголя
, , , . Следует быть особенно осторожными при назначении препаратов в пожилом возрасте, поскольку обычно пациенты вынуждены принимать большое количество лекарств, а количество функционирующих гепатоцитов уменьшается, и активность метаболизирующих ферментов снижается . При употреблении алкоголя и наличии фоновых заболеваний печени, поражение гепатоцитов может развиться при более низких дозировках препаратов , , . Необходимо четко следовать рекомендациям по дозировке и длительности назначения лекарственных средств и их комбинаций. Спектр поражения печени при воздействии лекарств может быть очень широк, от субклинического гепатита до тяжелого фульминантного поражения и опухолей печени .Классификация лекарственных поражений печени:
- острые:
- вирусоподобный (цитолитичсский) острый гепатит;
- простой (каналикулярный) холестаз;
- холангиолитический (гепатоканаликулярный) гепатит;
- гранулематозный гепатит;
- хронические:
- хронический активный гепатит;
- хронический персистирующий гепатит;
- стеатогепатит;
- хронический холестаз;
- фиброз печени;
- фосфолипидоз;
- цирроз печени;
- гепатоваскулярные поражения (Вено-окклюзионная болезнь (синдром Бадда–Киари); Пелиоз; Тромбоз печеночной вены);
- опухоли (Фокальная нодулярная гиперплазия; Аденома; Гепатоцеллюлярный рак; Ангиосаркома).
Одной из самых частых соматических патологий, при лечении которых развивается поражение печени, являются ревматические заболевания
, , , . Это связано с большой длительностью терапии, часто использованием высоких доз препаратов, а также высокой частотой развития ревмопатологии у женщин. Так, по данным Reuben A и др., В США более 60% случаев фульминантной печеночной недостаточности связано с приемом ЛС, из них большинство – с приемом парацетамола . При использовании НПВП поражение печени варьирует от бессимптомного повышения уровней трансаминаз до тяжелых форм лекарственного гепатита. ЛПП вследствие приема НПВП может развиваться во время приема препаратов, либо спустя недели или даже месяцы после его отмены. Наиболее часто ЛПП развиваются при назначении нимесулида, диклофенака, напроксена, индометацина, кеторолака, мелоксикама , , , . Клиника ЛПП имеет «маску» всех известных заболеваний печени, в связи с чем клиническая картина чрезвычайно разнообразна, а диагностика трудна , , . Лекарственное поражение печени можно предполагать если увеличение показателей аланинаминотрансферазы (АЛТ), щелочной фосфатазы (ЩФ) в 2 раза и более, а также появление желтухи возникают у пациента в течение 3 месяцев от начала применения нового препарата. Этиологическая связь считается: предположительной, если продолжительность интервала между приемом препарата и развитием гепатотоксической реакции составляет 5-90 дней и определенной — 90 дней и более , , , . Для установления взаимосвязи между приемом препарата, как предписанного врачом, так и принимаемого самостоятельно, в т.ч. растительных препаратов и БАДов и развитием поражения печени используются оценочные шкалы :- RUCAM (Roussel Uclaf Causality Assessment Method);
- DILIN (Drug-Induced Liver Injury Network) Maria & Victorino (M & V) и др;
- Benichou С. Criteria of drug-induced liver disorders: report of an international consensus meeting.
2. Методы и принципы исследования
Диагноз ЛПП – это диагноз исключения, поэтому диагностика зачастую занимает продолжительное время. Необходимо исключить вирусные, гепатиты, алкогольное поражение печени, аутоиммунные гепатиты, наследственные заболевания, сосудистые болезни печени. Необходимо тщательно собрать анамнез заболевания, сведения о клинической картине и течении заболевания, а также результаты лабораторных исследований. Диагностический минимум для постановки диагноза ЛПП включает: АЛТ, АСТ, ЩФ, билирубин, гамма-ГТП, МНО, ОАК, УЗИ
, , . В зависимости от результатов обследования, выделяют гепато-целлюлярный, холестатический и смешанный вариант ЛПП (табл. 1).Таблица 1 - Характеристики типов поражения
Тип поражения | АЛТ | ЩФ | Соотношение АЛТ\ЩФ (R) |
Гепатоцеллюлярный | >2 N | N | Высокое >5 |
Холестатический | N | >2 N | Низкое <2 |
Смешанный | >2 N | >2 N | 2-5 |
Выраженность цитолитического процесса обычно характеризуется степенью активности АЛТ:
- повышение в 1,5–5 раз по сравнению с верхней границей нормы рассматривается как незначительная гиперферментемия;
- в 6–10 раз – как гиперферментемия средней степени;
- более чем в 10 раз – как высокая
.Важными диагностическими симптомами являются скорость нормализации нарушенных функций после отмены препарата. Этиологическая связь считается очень предположительной, если повышенный уровень печеночных ферментов снижается на 50% в течение 8 дней; предположительной – в течение 30 дней для гепатоцеллюлярного и 180 дней – для холестатического поражения печени
, . Более длительные биохимические сдвиги свидетельствуют о наличии сопутствующего заболевания печени .Развитие желтухи при лекарственно индуцированном гепатоцеллюлярном повреждении является чрезвычайно опасным признаком. Для оценки тяжести в этом случае используют закон Хая («Hy’s Rule» – индикатор тяжелого лекарственного поражения печени) – если в случае лекарственно-индуцированного поражения печени появляется желтуха в отсутствии обструкции желчных протоков, летальный исход следует ждать по крайне мере у 1 из 10…»
.В настоящее время не существует универсального препарата для лечения ЛПП, лишь для некоторых препаратов применяются антидоты. Например, припоражении парацетамолом назначается N–ацетилцистеин
.В большинстве случаев острых лекарственных поражений печени достаточна отмена «причинного» препарата. В качестве базисной терапии также назначается лечебное питание, дезинтоксикация, сорбенты, прокинетики, пробиотики, электролиты. При выраженном синдроме цитолиза возможно применение глюкокортикостероидов. Ускорению регресса патологических изменений в печени и улучшению биохимических показателей способствует прием гепатопротекторных препаратов (адеметионин, урсодезоксихолевая кислота, препараты расторопши пятнистой, бициклол, ремаксол) При благоприятном течении и отмене ЛС обратное развитие клинической симптоматики наступает достаточно быстро
, , , .Профилактика развития ЛПП состоит в индивидуализации назначаемой терапии, тщательном сборе лекарственного и аллергологического анамнеза, исключении полипрагмазии.
Перед назначением потенциально гепатотоксических препаратов необходимо перед началом терапии и во время ее проверять функциональное состояние печени (АСАТ, АЛАТ, ЩФ, ГГТП).
3. Основные результаты
В качестве примера лекарственного поражения печени приведем клинический случай.
Пациентка П, 46 лет, воспитательница детского сада. В течение 2 месяцев 10-11/2023 получала терапию по поводу остеоартрита плечевого сустава. Были назначены эторикоксиб по 60 мг в течение 6 недель и ацеклофенак по 100 мг в день – 20 дней. 27 декабря 2023 г появился кожный зуд, через 3 дня потемнела моча, появилась желтуха – иктеричность склер. В связи с ухудшением самочувствия – нарастающей слабостью, тошнотой, вызвала скорую помощь и была доставлена в хирургический стационар.
При обследовании по результатам УЗИ брюшной полости обнаружены признаки неалкогольной жировой болезни печени, желчнокаменная болезнь – отключенный желчный пузырь. Консультирована хирургом, острая хирургическая патология исключена. Направлена в инфекционный стационар для исключения вирусных гепатитов. После чего госпитализирована в гастроотделение с подозрением на аутоимунный гепатит. Употребление алкоголя отрицает на протяжении 15 лет. На момент госпитализации состояние средней тяжести.
Жалобы на слабость, снижение аппетита, тошноту.
Объективно: рост 152 см, вес 76 кг, ИМТ 32,9. Кожные покровы чистые, желтушные, геморрагического синдрома нет. Во времени и пространстве ориентирована. Печночного запаха, тремора нет. Положительные внепеченочные знаки – яркая пальмарная эритема, единичные сосудистые звездочки. Тоны сердца ритмичные, пульс и давление в норме. В легких везикулярное дыхание. Пальпация живота безболезненна, печень увеличена на 2-3 см, плотно-эластической консистенции, безболезненная при пальпации. Селезенка не увеличена. Физиологические отправления в норме.
Данные лабораторных анализов – общий анализ крови- Ле 6,2*10 9, Не 48%, Лим 34%, Мон 10,5%, Эр 4,9*10 12, Тр 236 10 9. ОАМ – без патологии, амилаза мочи 150Ед/л. Биохимические анализы Билирубин общий 175мкмоль/л, прямой 95 мкмоль/л, АсАт 145 Ед/л, АлАт 350 Ед/л, ГГТП 105 Ед/л, ЩФ 175 Ед./л, мочевина 3,6 ммоль/л, креатинин 66 мкмоль/л, глюкоза 6,2 ммоль/л. Маркеры аутоиммунных реакций (панель Ливер-лайн-9) отрицательные. Маркеры вирусных гепатитов А, В, С, Д – отрицательны.
Установлен диагноз: Острый лекарственный гепатит по смешанному типу высокой степени активности на фоне неалкогольной жировой болезни печени. Сопутствующий диагноз: Желчно-каменная болезнь, хронический калькулезный холецистит. Ожирение 1 степени.
Назначена дезинтоксикационная терапия, адеметионин по 800мг 2 раза в день 10 дней, урсодезоксихолевая кислота (УДХК) 1000 мг в день, ремаксол по 400 мл в/в через день N5, преднизолон 60 мг в/в капельно – 5 дней, с последующим переходом на пероральный прием 30 мг в день. На фоне лечения отмечена положительная динамика – уменьшение кожного зуда, желтухи, астении и диспептических явлений. В динамике показатели общего анализа крови остались стабильными, уровень билирубина снизился до 58,6 мкмоль/л, прямой 30мкмоль/л, АсАт 154 Ед/л, АлАт 370,7 Ед/л, ГГТП 62,3 Ед/л, ЩФ 123,9 Ед./л.
Пациентка была выписана на дневной стационар и последующее амбулаторное наблюдение. Продолжена терапия УДХК 1000мг в сутки и преднизолоном под контролем биохимических анализов. Через 2 недели показатели печеночных проб улучшились, динамика приведена на рисунке 1. В связи с положительной динамикой начато медленное снижение дозы стероидов – по 2,5 мг в неделю, при достижении суточной дозы 10 мг – 1,25 мг в неделю до полной отмены. После отмены стероидов терапия УДХК была продолжена для коррекции НАЖБП.
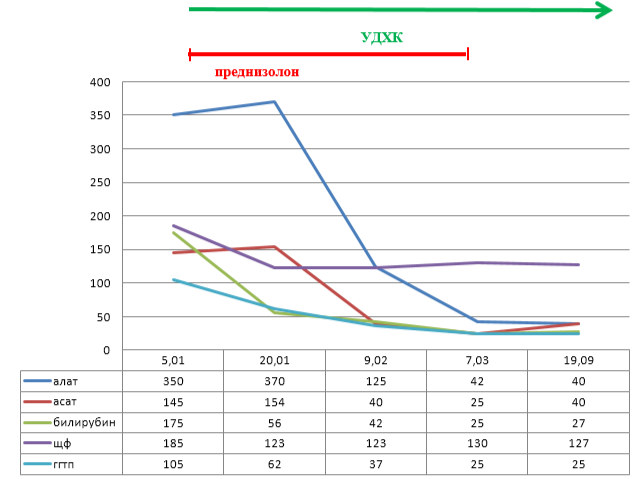
Рисунок 1 - Динамика биохимических показателей больной П. на фоне лечения
4. Заключение
Данный клинический случай иллюстрирует развитие тяжелого лекарственного гепатита в результате комбинированной терапии ревмопатологии. Известны различные группы ЛС, вызывающих ЛПП. Учитывая возможность поражения печени при назначении медикаментозной терапии, особенно длительной, комбинированной, для обеспечения безопасности пациентов следует периодически оценивать состояние функции печени, контролируя биохимические критерии ЛПП.
