Identification and quantitative determination of hydroxycinnamic acids in European verbena (Verbena officinalis) herb
Identification and quantitative determination of hydroxycinnamic acids in European verbena (Verbena officinalis) herb
Abstract
The object of the study was European verbena herb grown in the I.I. Sprygin Botanical Garden of Penza State University. The raw materials were dried in the air without exposure to direct sunlight. Thin-layer chromatography (TLC) was used to identify hydroxycinnamic acids in verbena herb. Direct spectrophotometry confirmed the presence of hydroxycinnamic acids in verbena herb extracts and determined the analytical maxima of the studied compounds (330±2 nm). The optimal conditions for the extraction of hydroxycinnamic acids from raw materials were established: extractant — 70% ethyl alcohol; raw material to extractant ratio — 1:100; extraction time — 60 minutes; degree of raw material grinding — 1.0 mm. The aim of the research is to identify and quantitatively determine the sum of hydroxycinnamic acids in European verbena herb. A metrological evaluation of the method for determining the sum of hydroxycinnamic acids was carried out.
1. Введение
Перспективы исследований лекарственных растений, содержащих гидроксикоричные кислоты (ГКК), выглядят весьма многообещающими в связи с их широким спектром биологической активности и потенциальной пользой для здоровья человека. Углубленное изучение ГКК, содержащихся в различных растительных источниках, открывает возможности для разработки новых лекарственных средств и функциональных продуктов питания. Другим важным направлением является разработка эффективных методов экстракции и очистки ГКК из растительного сырья. Оптимизация этих процессов позволит получать высококачественные экстракты и индивидуальные соединения для дальнейших исследований и применения в фармацевтической и пищевой промышленности. Также актуальным является изучение биодоступности и метаболизма ГКК в организме, что позволит определить оптимальные способы их применения и дозировки , .
Польза гидроксикоричных кислот заключается в их способности оказывать положительное влияние на здоровье человека благодаря своим антиоксидантным, противовоспалительным и другим биологически активным свойствам. Они могут способствовать защите клеток от повреждений, вызванных свободными радикалами, снижать риск развития хронических заболеваний, таких как сердечно-сосудистые заболевания, рак и нейродегенеративные расстройства. Кроме того, ГКК могут оказывать благотворное влияние на пищеварительную систему, иммунную систему и общее состояние организма , .
Одним из ключевых преимуществ хлорогеновой кислоты является ее антиоксидантное действие. Она эффективно нейтрализует свободные радикалы, которые повреждают клетки и способствуют развитию различных заболеваний, включая сердечно-сосудистые и онкологические. Помимо антиоксидантной активности, хлорогеновая кислота оказывает положительное влияние на метаболизм глюкозы и липидов. Исследования показывают, что она способна улучшать чувствительность к инсулину, что особенно важно для людей с диабетом 2 типа или предрасположенностью к нему. Также хлорогеновая кислота способствует снижению уровня холестерина в крови, что благоприятно сказывается на здоровье сердца и сосудов. Кроме того, хлорогеновая кислота обладает противовоспалительными свойствами , , . Существует потребность в новых источниках растительного сырья с высоким содержанием данных соединений. Перспективным в этом отношении объектом изучения является вербена лекарственная (Verbena officinalis L.) семейства вербеновые (Verbenaceae) , .
2. Методы и принципы исследования
Для подтверждения присутствия гидроксикоричных кислот в траве вербены использовали тонкослойную хроматографию (ТСХ)
, . На линию старта хроматографической пластинки наносили 0,02 мкл водно-спиртового извлечения. В качестве стандартных образцов на пластинку наносили СО цинарозида, СО хлорогеновой кислоты, СО розмариновой кислоты, СО гиперозида, СО кверцетина. Хроматографический анализ: пластинки с образцами помещают в хроматографическую камеру; хроматографирование проводили восходящим методом в системе с растворителем: хлороформ — этиловый спирт 70% — вода в соотношении 26:16:3; использовали пластинки типа «Сорбфил-ПТСХ-АФ-Ф-УФ». Хроматограммы просматривали при дневном свете, а также под ультрафиолетовым светом при длинах волны 366 нм и 254 нм. Обрабатывали щелочным раствором ДСК и фосфорно-молибденовой кислотой для выявления или повышения контрастности анализируемых веществ. Методика извлечения гидроксикоричных кислот: используется однократная экстракция этиловым спиртом с различной концентрацией: 95%, 70%, 40%; экстракцию проводят на водяной бане при кипячении в течение 60 минут; после охлаждения извлечения фильтруют через бумажный фильтр, смоченный тем же спиртом, сбрасывая первые 10 мл фильтрата (раствор А). В мерную колбу 25 мл добавляют 1 мл фильтратa и доводят объем до метки спиртом (раствор Б). Определение содержания гидроксикоричных кислот: используется спектрофотометр СФ-102; оптическую плотность измеряют при длине волны 330 нм в этанольном растворе. Расчет содержания осуществляется по формуле (1):где D — оптическая плотность испытуемого раствора;
m — масса сырья, г;
W — потеря в массе при высушивании сырья (влажность), %;
497 — удельный показатель поглощения хлорогеновой кислоты при 330 нм.
3. Основные результаты
Результаты хроматографического анализа показали следующие данные (рис.2): оранжевое пятно с Rf = 0,44 (совпадает с СО хлорогеновой кислотой), желтое пятно с Rf = 0,64 (совпадает с СО цинарозида), с Rf = 0,69 (совпадает с СО кверцетина). Рекомендации по проведению качественного анализа: использовать хлорогеновую кислоту в качестве вещества-стандарта и производить расчет значений Rf для подтверждения идентичности компонентов. Методологические особенности: сравнение Rf исследуемых веществ с Rf стандартных образцов позволяет достоверно идентифицировать компоненты. Наличие характерных цветов пятен (оранжевый и желтый) дополнительно подтверждает идентификацию. Такой подход к анализу позволяет: достоверно идентифицировать присутствующие компоненты, подтвердить качество исследуемого сырья, обеспечить воспроизводимость результатов анализа.
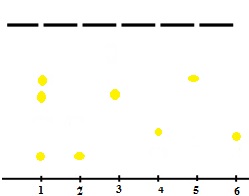
Рисунок 1 - Схема хроматограммы извлечения из травы вербены:
1 - извлечение из травы вербены; 2 - СО хлорогеновой кислоты; 3 - СО цинарозида; 4 - СО розмариновой кислоты; 5 - СО кверцетина; 6 - СО гиперозида

Рисунок 2 - Электронный спектр стандартного образца хлорогеновой кислоты (2) и извлечения из надземной части вербены лекарственной (1)
Таблица 1 - Влияние степени измельченности
Экстрагент | Соотношение сырье – экстрагент | Измельченность, мм | Время извлечения, мин | Суммарное содержание гидроксикоричных кислот, % |
Этанол 70 % | 1:100 | 0,5 | 60 | 3,36±0,06 |
Этанол 70 % | 1:100 | 1,0 | 60 | 3,42±0,09 |
Этанол 70 % | 1:100 | 2,0 | 60 | 3,38±0,06 |
Этанол 70 % | 1:100 | 3,0 | 60 | 3,34±0,08 |
Таблица 2 - Влияние экстрагента
Экстрагент | Соотношение сырье – экстрагента | Измельченность, мм | Время извлечения, мин | Суммарное содержание гидроксикоричных кислот, % |
Этанол 40 % | 1-100 | 1,0 | 60 | 1,29±0,05 |
Этанол 70 % | 1-100 | 1,0 | 60 | 3,42±0,09 |
Этанол 95 % | 1-100 | 1,0 | 60 | 0,75±0,03 |
Таблица 3 - Влияние соотношения «сырье – экстрагент»
Экстрагент | Соотношение сырье – экстрагента | Измельченность, мм | Время извлечения, мин | Суммарное содержание гидроксикоричных кислот, % |
Этанол 70 % | 1-50 | 1,0 | 60 | 2,90±0,09 |
Этанол 70 % | 1-100 | 1,0 | 60 | 3,42±0,09 |
Этанол 70 % | 1-200 | 1,0 | 60 | 2,75±0,10 |
Таблица 4 - Влияние времени экстрагирования
Экстрагент | Соотношение сырье – экстрагента | Измельченность, мм | Время извлечения, мин | Суммарное содержание гидроксикоричных кислот, % |
Этанол 70 % | 1-100 | 1,0 | 30 | 2,55±0,07 |
Этанол 70 % | 1-100 | 1,0 | 60 | 3,42±0,09 |
Этанол 70 % | 1-100 | 1,0 | 90 | 2,39±0,09 |
Суммарное содержание гидроксикоричных кислот извлекаемых из травы вербены в оптимальных условиях составило 3,42%.
Проведена метрологическая оценка предложенной методики. В результате пяти параллельных определений (Хср= 3,42) установлена дисперсия (S2 = 0,005), стандартное отклонение (S = 0,071), стандартное отклонение среднего результата (SХср = 0,031), относительное стандартное отклонение среднего результата (RSD = 2,08%), полуширина доверительного интервала (ΔХср = 0,088). Погрешность среднего результата (ε, %) суммы гидроксикоричных кислот с доверительной вероятностью (Р,%) 95% в сырье вербены лекарственной составила ±2,58 %, в пересчете на хлорогеновую кислоту.
4. Заключение
Для количественного определения суммарного содержания гидроксикоричных кислот в траве вербены разработана методика, основанная на спектрофотометрическом анализе при длине волны 330 нм. Этот метод позволяет с высокой точностью оценивать содержание данных биологически активных веществ, что критически важно для контроля качества лекарственного растительного сырья. Оптимизация условий экстракции является ключевым этапом в разработке методики. Экспериментально установлено, что оптимальными параметрами являются: степень измельчения сырья до 1 мм, что обеспечивает максимальную площадь поверхности для контакта с экстрагентом; использование 70% этанола в качестве экстрагента, поскольку он эффективно извлекает гидроксикоричные кислоты; соотношение сырья к экстрагенту 1:100, обеспечивающее полное извлечение целевых соединений; время экстракции 60 минут на кипящей водяной бане, что достаточно для достижения равновесия между сырьем и растворителем.
Содержание гидроксикоричных кислот в траве вербены, определённое с использованием разработанной методики, составило 3,42% в пересчёте на хлорогеновую кислоту. Этот показатель может служить критерием для оценки качества сырья и его пригодности для дальнейшего использования в фармацевтической промышленности. Разработанная методика и полученные результаты имеют практическое значение для стандартизации травы вербены как нового вида лекарственного сырья. Они могут быть использованы при разработке нормативной документации, включая фармакопейные статьи и технические условия, что позволит обеспечить стабильное качество и эффективность лекарственных препаратов на основе этого растения.
