GRANULAR PROTONATED POTASSIUM POLYTITANATE BASED ION EXCHANGE MATERIAL FOR LITHIUM EXTRACTION
GRANULAR PROTONATED POTASSIUM POLYTITANATE BASED ION EXCHANGE MATERIAL FOR LITHIUM EXTRACTION
Abstract
In the present work, a granular ion-exchange material based on protonated potassium polytitanate and polyvinyl butyral (PVB-K0.8H1.2Ti4.3O9) was obtained. The structure of the obtained material was studied by scanning electron microscopy. The sorption capacity of the obtained composite during lithium extraction from aqueous LiOH solution is 0.8, 3.6 and 6.1 mmol/g at C0(Li+)= 0.01, 0.03 and 0.06 mol/l. The mechanism of sorption interaction is well described by pseudo-first-order and pseudo-second-order kinetic models. The granular ion-exchange material has the ability to regenerate with maintaining high efficiency during three adsorption/desorption cycles. The selectivity of the ion exchange material towards lithium ions in the presence of other alkali metal ions is demonstrated.
1. Введение
С развитием технологий возобновляемой энергетики в области накопителей электроэнергии и новых электрических транспортных средств возрастает спрос на соли лития , . Основными источниками лития являются литиевые руды и литийсодержащие водные объекты. Однако из-за интенсивной добычи качество руд заметно ухудшается, поэтому одним из перспективных направлений получения солей лития становится извлечение щелочного металла из природных растворов таких, как морская вода и рассолы соленых озер , . Известно , что концентрация ионов лития в морской воде и рассоле составляет около 300 мг/л, при этом ионы Li+ сосуществуют с другими катионами, преимущественно Na+, K+, Mg2+, Ca2+, что осложняет эффективное извлечение лития. Среди разработанных технологий селективного извлечения лития из водных растворов наибольшее внимание приобретает ионообменная адсорбция благодаря экономическим и экологическим преимуществам , , .
На данный момент для извлечения лития наиболее исследованы три типа адсорбентов: на основе солей алюминия , , перовскитные структуры марганцевого типа , , а также слоистые и туннельные соединения титанового типа , . По сравнению с адсорбентами на основе солей алюминия, ионообменные материалы марганцевого типа и титанового типа имеют более высокую адсорбционную способность по отношению к ионам лития. Так, средняя адсорбционная способность сложных оксидов марганца составляет ~ 40 мг/г , а сложных оксидов титана достигает ~ 30 мг/г , . В отличие от марганцевых структур ионообменные материалы на основе титанатов с более прочной Ti-O связью обладают преимуществами с точки зрения стабильной структуры и хорошей кислотостойкости, отсюда относительно стабильными адсорбционными характеристиками и возможностью многократного использования.
Более привлекательной альтернативой известным соединениям титанового типа (H4Ti5O12 со структурой шпинели и H2TiO3 со слоистой структурой) является протонированный полититанат калия, который в зависимости от условий протонирования характеризуется варьируемым химическим составом K2-xHxTi4.3O9 (x = 0,5-1,2) . H4Ti5O12/H2TiO3 получают путем протонирования прекурсоров Li4Ti5O12/Li2TiO3, синтезированных твердофазным методом при высоких температурах, гидротермальным методом с использованием специального оборудования или золь-гель методом, требующим дорогостоящих и не всегда безопасных реактивов. В отличие от аналогов, прекурсор протонированного ионообменника – полититанат калия – синтезируется в расплаве, содержащем TiO2, KOH и KNO3 при температуре 500°С, что делает процесс получения функционального материала технологически простым, доступным и экономически выгодным. В предыдущих работах продемонстрирована эффективность и селективность подобных материалов , .
Промышленное использование ионообменных материалов при извлечении лития требует разработки композитов в виде гранул или мембран, обеспечивающих стабильность структуры функционального материала для непрерывности процесса, а также быстроту, полноту и простоту разделения ионообменника и раствора. В качестве связующих материалов могут быть использованы поливинилхлорид (ПВХ), поливиниловый спирт (ПВС), поливинилиденфторид (ПВДФ) и т.д. При этом важно учитывать, что неправильно подобранное соотношение ионообменного материала и связующего приводит к снижению адсорбционной способности композита.
В связи с вышесказанным цель работы заключается в получении эффективного гранулированного ионообменного материала на основе протонированного полититаната калия и исследование его адсорбционной способности по отношению к ионам лития.
2. Методы и принципы исследования
Синтез и протонирование полититаната калия с получением материала состава K0.8H1.2Ti4.3O9 проведены по методике, подробно описанной в предыдущих работах , .
Сферические композиционные материалы состава ПВБ-K0.8H1.2Ti4.3O9 подготовлены по следующей методике: 3,0 г поливинилбутираля (ПВБ) растворяли в 27,0 мл N-N-диметилформамида (ДМФ). В раствор ПВБ добавляли 10,0 г порошка K0.8H1.2Ti4.3O9 и перемешивали на магнитной мешалке до равномерного распределения. С использованием микродозатора суспензию капали в дистиллированную воду для быстрого формирования небольших гранул диаметром 1,0-2,0 мм, которые промывали дистиллированной водой для удаления растворителя и формирования микропористого скелета ПВБ. Затем сферы дополнительно обрабатывали 0,5 М раствором HCl для удаления остатков низкомолекулярных полимеров и растворителя. Содержание ПВБ в ионообменном композите составляло на уровне 23 масс.%. Указанное содержание полимерного связующего позволяет сохранить форму сфер и обеспечивает максимально доступную рабочую поверхность композита при экстракции лития из водного раствора.
Морфология гранулированного ионообменного материала исследована с использованием сканирующего электронного микроскопа ASPEX Explorer (США).
Ионообменные свойства полученного гранулированного композиционного материала исследованы на примере растворов LiOH с концентрациями С(Li+) = 0,01; 0,03 и 0,06 моль/л при объеме раствора 100 мл и массе гранул 0,5 г. Концентрацию Li+ в растворе фиксировали через 10, 20, 30 мин и далее каждые полчаса в течение 5 ч потенциометрическим методом с использованием иономера И-160МП (Гомельский завод измерительных приборов, Беларусь) с литий-селективным электродом ЭЛИС-142Li (Измерительная техника, Россия).
Сорбционная емкость (q, ммоль/г) гранулированного композиционного материала на основе протонированного полититаната калия и поливинилбутираля рассчитана по формуле (1):
где C0 and Ct – начальная и в момент времени t концентрация Li+ в растворе, ммоль/л, соответственно; V – объем раствора, л; m – масса ионообменного композита, г.
Исследование кинетики ионообменного процесса с расчетом константы скорости и равновесной сорбционной емкости проведено с использованием кинетических моделей псевдо-первого (уравнение 2) и псевдо-второго порядка (уравнение 3).
где qe и qt – сорбционная емкость при равновесии и в момент времени t, ммоль/г, соответственно; k1, мин-1 and k2, г/ммоль·мин – константы скорости моделей псевдо-первого и псевдо-второго порядка, соответственно.
Способность к регенерации гранулированного композиционного материала на основе протонированного полититаната калия и поливинилбутираля исследована путем проведения трех циклов адсорбции-десорбции. После ионообменного процесса в растворе LiCl композит состава ПВБ-K0.8H1.2Ti4.3O9 обрабатывали в 0,2 М растворе HCl в течение 3 часов, промывали дистиллированной водой, высушивали и подвергали последующему циклу адсорбции-десорбции. После каждого цикла рассчитывали сорбционную емкость.
Селективность гранулированного композиционного материала на основе протонированного полититаната калия и поливинилбутираля исследована на примере модельного солевого раствора, содержащего Li+ (202 мг/л), Na+ (681 мг/л), К+ (1182 мг/л), Mg2+ (718 мг/л) и Са2+ (1226 мг/л), рН которого поддерживался в щелочной области с помощью аммиачного буферного раствора. Навеску гранул в 0,5 г помещали в 100 мл модельного раствора, выдерживали при перемешивании в течение 3 часов и фиксировали концентрацию ионов щелочных металлов Li+, Na+, K+ с использованием иономера И-160МП и ионоселективных электродов ЭЛИС-142Li, ЭЛИС-112Na, ЭЛИС-121K. По результатам исследования по формулам (4) и (5) рассчитаны коэффициент распределения (Kр) и коэффициент разделения (α):
где Ме = Na и К.
3. Основные результаты и обсуждение

Рисунок 1 - Гранулированный ионообменный материал на основе протонированного полититаната калия
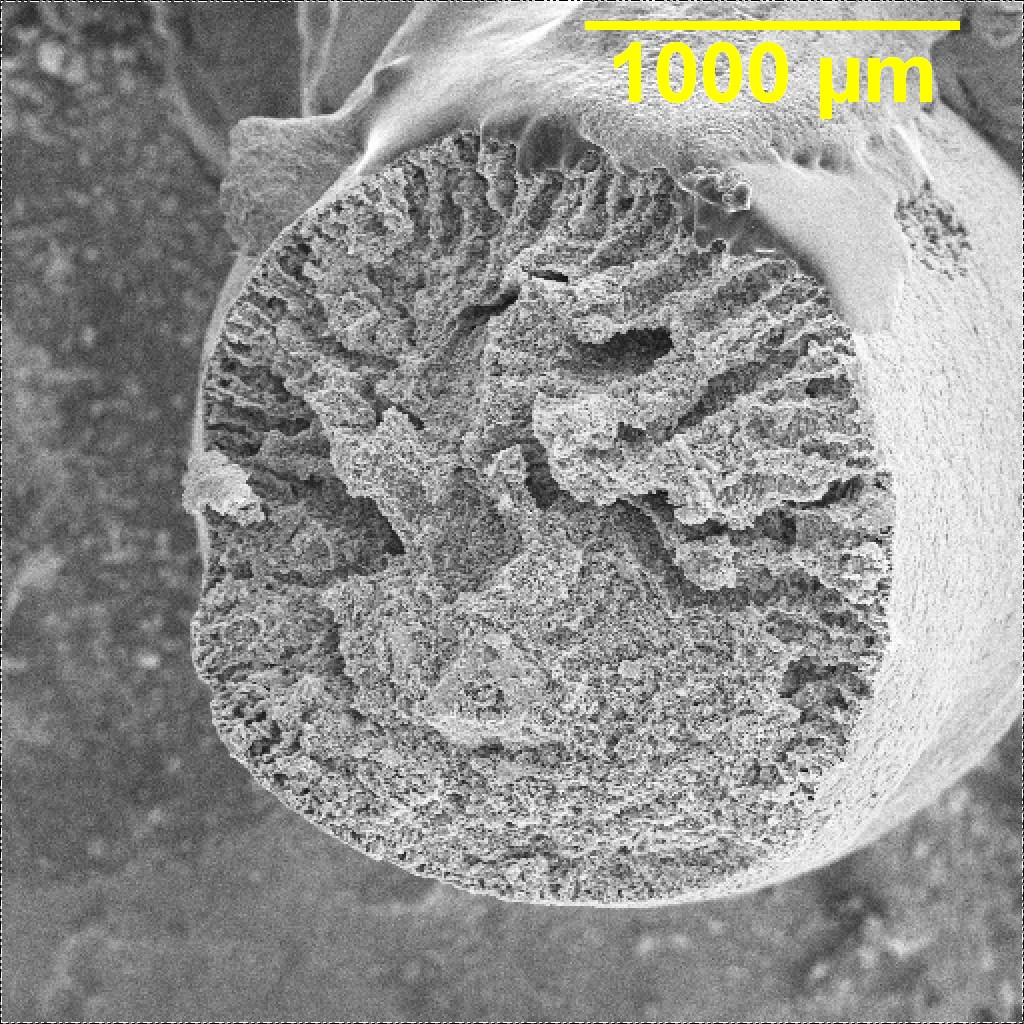
Рисунок 2 - СЭМ-изображение гранулированного ионообменного материала на основе протонированного полититаната калия

Рисунок 3 - СЭМ-изображение гранулированного ионообменного материала на основе протонированного полититаната калия

Рисунок 4 - СЭМ-изображение гранулированного ионообменного материала на основе протонированного полититаната калия
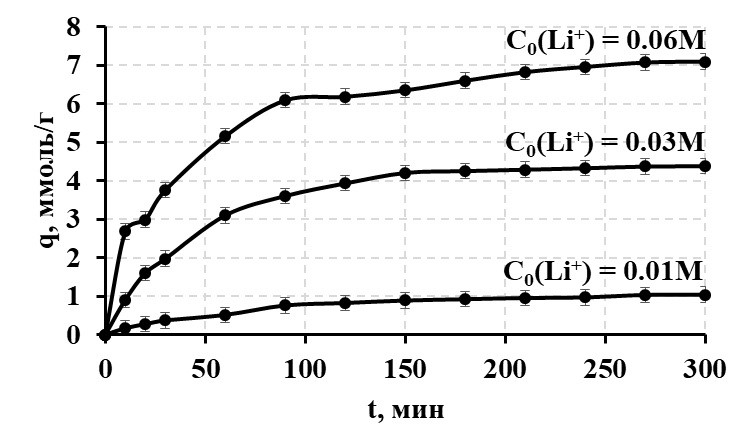
Рисунок 5 - Кинетика извлечения лития гранулированным ионообменным материалом на основе протонированного полититаната калия из раствора LiOH с различной концентрацией
Выявление лимитирующей стадии и предположение о механизме сорбционного взаимодействия возможно по результатам моделирования экспериментальных данных с использованием уравнений псевдо-первого и псевдо-второго порядка, которое проведено на примере результатов, полученных для ионообменных процессов в растворе с концентрацией ионов лития 0,01 моль/л (рисунок 6).
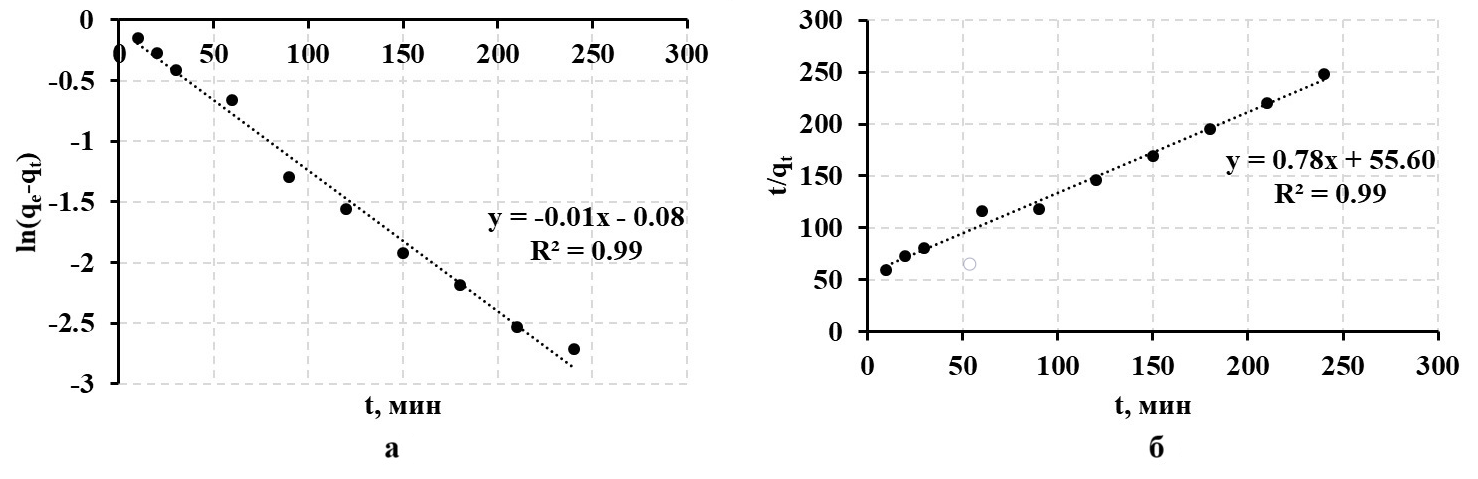
Рисунок 6 - Кинетика извлечения лития гранулированным ионообменным материалом на основе протонированного полититаната калия в координатах модели псевдо-первого (а) и псевдо-второго (б) порядков
Таблица 1 - Кинетические параметры извлечения лития гранулированным ионообменным материалом на основе протонированного полититаната калия
Модель | Параметры модели | ||
Псевдо-первого порядка | qe, ммоль/г | k1, мин-1 | R2 |
1,08 | 0,01 | 0,99 | |
Псевдо-второго порядка | qe, ммоль/г | k2, г/(ммоль·мин) | R2 |
1,28 | 0,01 | 0,99 | |
Видно, что как равновесная сорбционная емкость, так константы скорости, оцененные по обеим моделям близки и коррелируют с экспериментальным значением q, что дополнительно подтверждает механизм ионообменного взаимодействия гранулированного ионообменного материала на основе протонированного полититаната калия и лития в растворе.
Способность к регенерации и сохранение высокой эффективности на протяжение нескольких циклов адсорбции/десорбции является важной характеристикой для потенциального практического применения ионообменного материала. Композит состава ПВБ-K0.8H1.2Ti4.3O9 подвергался процессу регенерации путем обработки в 0,2 М растворе соляной кислоты в течение 3 часов. Эффективность композиционного ионообменного материала оценена на протяжение 3 циклов извлечения лития с промежуточной регенерацией (рисунок 7).
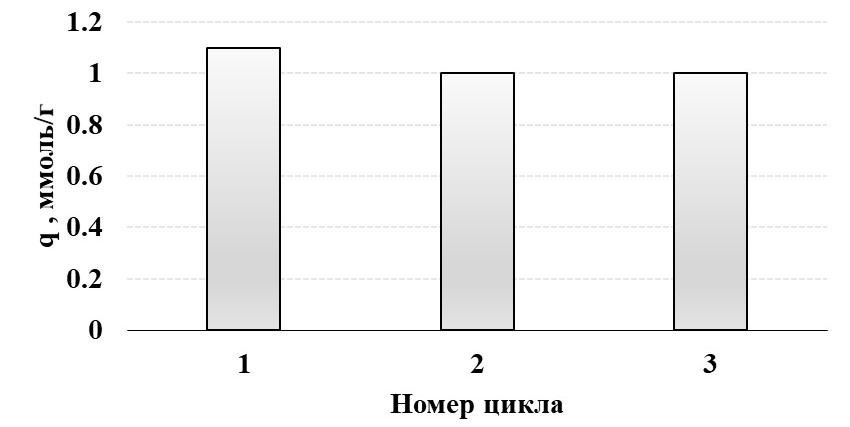
Рисунок 7 - Сорбционная емкость гранулированного ионообменного материала на основе протонированного полититаната калия в трех циклах литирования/делитирования
Из-за наличия в растворе совместно с ионами Li+ других катионов (таких как Na+, K+, Mg2+ и Ca2+) происходит конкурентная ионообменная адсорбция сосуществующих сорбтивов на гранулированном ионообменном материале. Исследование селективности композита ПВБ-K0.8H1.2Ti4.3O9 по отношению к ионам Li+ относительно ионов Na+ и K+ проведено на примере модельного солевого раствора, содержащего хлориды перечисленных щелочных и щелочно-земельных металлов. Установлено, что гранулированный ионообменный материал на основе протонированного полититаната калия и поливинилбутираля сорбирует ионы лития в количестве 27,7 ± 0,5 мг/л (4,0 ± 0,2 ммоль/г) при начальной концентрации С0(Li+) = 202 мг/л, при этом концентрация ионов Na+ в ходе ионообменного процесса не изменяется, а ионы K+ извлекаются в количестве 48,1 мг/г композита при С0(K+) = 1182 мг/л. Однако коэффициенты распределения для лития и калия составляют 0,44 и 0,05 л/г, т.е. Кр(Li) ˃ Кр(K), при этом коэффициент разделения α = 8,5 ˃ 1, что свидетельствует о высокой селективности ПВБ-K0.8H1.2Ti4.3O9 по отношению к ионам лития в присутствии ионов других щелочных металлов (Na+ и K+).
4. Заключение
Методом фазовой инверсии получен сферический композиционный материал состава ПВБ-K0.8H1.2Ti4.3O9 с массовым соотношением компонентов 23:77. Исследование сорбционной способности гранулированного материала по отношению к ионам лития на примере растворов LiOH с различной начальной концентрацией Li+ показало, что через 5 часов взаимодействия q = 1,0, 4,4 и 7,1 ммоль Li / г ПВБ-K0.8H1.2Ti4.3O9. Механизм исследованного сорбционного взаимодействия хорошо описывается кинетическими моделями псевдо-первого и псевдо-второго порядка, что говорит о влияние явления пленочной диффузии в приповерхностном слое гранул перед проникновением в поры ионообменного материала и лимитируется химической реакцией между сорбентом и сорбатом. Установлено, что композит способен к регенерации и сохраняет эффективность на протяжении трех циклов адсорбции/десорбции (снижение величины q в третьем цикле на ~9%). По рассчитанным коэффициентам распределения (Кр(Li) = 0.44 ˃ Кр(K) = 0,05) и разделения (α = 8,5 ˃ 1) для лития и калия можно сделать вывод о высокой селективности ПВБ-K0.8H1.2Ti4.3O9 по отношению к ионам лития в присутствии ионов других щелочных металлов (Na+ и K+).
