The Stimulation of Fracture Zone Neoangiogenesis to Improve Reparative Processes and Reduce the Time of Bone Tissue Regeneration in the Fracture Zone
The Stimulation of Fracture Zone Neoangiogenesis to Improve Reparative Processes and Reduce the Time of Bone Tissue Regeneration in the Fracture Zone
Abstract
The research is dedicated to the solution of one of the topical issues of medicine, namely, the acceleration of bone fracture healing by stimulation of neoangiogenesis, which improves blood supply in the area of bone injury. We propose to apply the domestic drug "Neovasculgen" belonging to the group of endothelial cell proliferation stimulators. We will carry out experimental work on animals (rats), which will be injected in the place of the fracture this drug. Three weeks later the animals will be withdrawn from the experiment, the material will be collected and examined using different methods to detect the occurrence of neoangiogenesis phenomenon in relation to the control group.
1. Введение
Проблема лечения переломов костей весьма актуальна, количество травматических повреждений сохраняется на стабильно высоком уровне. В Российской Федерации, в структуре общей смертности взрослого населения внешние причины (травмы) составляют около 9% и занимают третье место после заболеваний сердечно-сосудистой системы и онкологических заболеваний.
В настоящее время за медицинской помощью по поводу травматических повреждений обращается каждый 12 больной, в абсолютных цифрах это около полутора миллионов только переломов костей конечностей. Показатель травматизма у городского населения превышает в два раза количество случаев в сельских регионах. В расчете на 100 тысяч населения количество переломов составляет 1055,3 из них переломов костей нижних конечностей – 711,6.
Существует большое количество способов и методик лечения переломов, но, несмотря на все достижения медицинской науки, остаются нерешенными многие вопросы, в частности, сроки заживления травмированных костей [1], [2], [3], [4]. Средние сроки нетрудоспособности на сегодня составляют от 50 до 200 дней. Сроки заживления костной травмы во многом зависят от кровотока в зоне перелома, и методика стимуляции кровотока с помощью препарата «НЕОВАСКУЛГЕН» представляется весьма перспективной.
Травматизм является не только медицинской проблемой, но и имеет значительную социально-экономическую значимость, а также оказывает влияние на демографические факторы.
2. Методы и принципы исследования
Проводилось исследование бедренных костей крыс (300-350 грамм, линия – белые чистые лабораторные). На операции фрезой проводилось повреждение костной ткани в виде продольного пропила от кортикального слоя до костномозгового канала в диафизе бедренной кости длиной 8-10 мм. В группе исследования применялся препарат, стимулирующий неоангиогенез «Неоваскулген». В контрольной группе введение стимулятора неоангигенеза не проводилось. Крысы обеих групп содержались в идентичных условиях. Животные выводились из эксперимента через 4 недели после операции. Забор оперированных (левых) бедренных костей проводился у обеих групп с последующей стандартной фиксацией тканей в растворе формалина. Полученные фрагменты костной ткани подвергались декальцинации, стандартной гистологической проводке и заливались в парафиновые блоки. Для каждого показателя вычисляли минимальное (Min) и максимальное (Max) значения, среднюю арифметическую (М) и ошибку средней (m) [2], [3].
3. Основные результаты и обсуждение
Известно, что восстановление костей требует согласованной активности нескольких различных клеточных механизмов. Хотя выздоровление переломов может произойти без каких-либо рубцов, значительный процент переломов не заживает должным образом [1], [2], [5]. Среди прочего, ангиогенез, стимулируемый сосудистым эндотелиальным фактором роста (VEGF), является основным ангиогенным фактором, который играет важную роль в хрящевой костной мозоли, а также перекрывает щель перелома и минерализованное образование кости во время эндохондральной оссификации в развитии кости [2], [3]. Различные исследования in vitro подтвердили способность VEGF стимулировать развитие эндотелиальных клеток сосудов, происходящих из артерий, вен и лимфатических сосудов [2], [4], [6], [8]. Его ингибирование обработкой растворимым рецептором VEGF снижает ангиогенез, а также образование и восстановление трабекулярной кости.
Впервые в РФ будет применен с целью стимуляции неоангиогенеза в зоне перелома костей отечественный препарат «Неоваскулген» (стимулятор пролиферации клеток эндотелия, способствующий реваскуляризации при окклюзионном поражении периферических артерий). Несмотря на то, что анализ периодических изданий показывает, что за рубежом имеется опыт использования препаратов данной группы для стимуляции васкулогенеза при переломе трубчатых костей, в отечественной литературе подобные исследования отсутствуют, а препарат «Неоваскулген» в лечении переломов костей не используется.
Основная функция костного скелета заключается в обеспечении прочной поддерживающей и механически крепкой структуры для мягких тканей и мышц. Скелетная система защищает грудно-брюшные внутренности [7] и служит «домом» для костного мозга [8]. Кости играют ключевую роль в кроветворении и метаболизме кальция [7]. Костные кристаллы являются основным резервуаром кальция, фосфора и необходимых ионов для метаболических и физиологических процессов [9]. Кость представляет собой сложную структуру и включает клетки, внеклеточный матрикс (ECM) и липиды [8]. Около 20% костей состоит из воды, а сухой вес составляет 30-35% органические и 65-70% неорганических веществ [10]. Клеточные компоненты кости включают остеобласты, остеоциты, остеокласты и остеогенные клетки-предшественники (мезенхимальные остеопрогенитальные клетки) [6], [7]. Ученые используют специфическую терминологию для определения остеобластов, такую как «мезенхимальные остеобласты» и «поверхностные остеобласты» [1], [4], [5]. Остеобласты продуцируют коллаген [6]. Другими функциями этих клеток являются синтез, регуляция, отложение и минерализация ECM [6], [8], [9]. Кроме того, эти клетки играют важную роль в гомеостазе кальция в крови и действуют как механосенсор для костей [10].
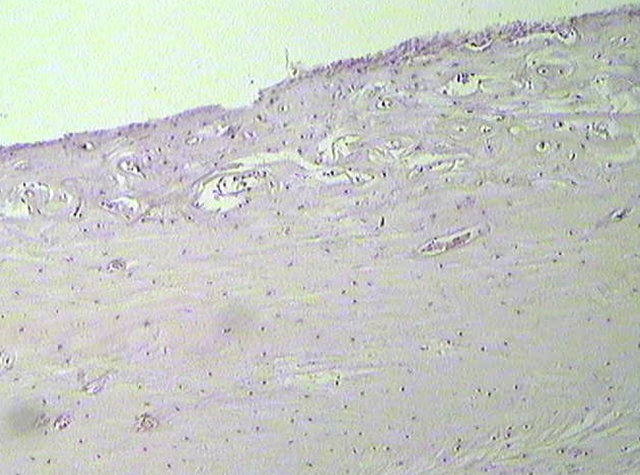
Рисунок 1 - Срез костной ткани с увеличенным количеством сосудов микроциркуляторного русла
Примечание: группа исследования; гематоксилин-эозин; ×100
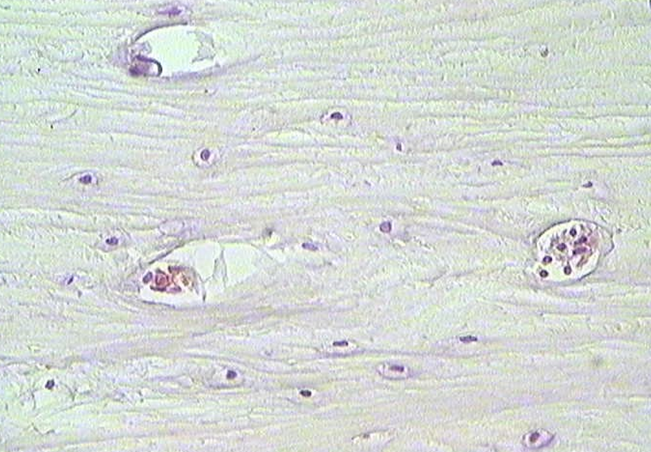
Рисунок 2 - Срез костной ткани на увеличении
Примечание: ×400; стрелками отмечены сосуды микроциркуляторного русла; группа исследования; гематоксилин-эозин
В контрольной группе на микропрепаратах видна сформированная пластинчатая костная ткань, с типичной структурой, содержащей клетки остеопластического дифферона, но с менее развитым сосудистым руслом. При увеличении ×400 сосуды встречаются не во всех полях зрения и не более одного сосуда одновременно.
Развитие костной ткани происходит за счет двух механизмов, а именно внутримембранозного и эндохондрального формирования кости. При внутримембранозной форме формирование кости происходит без посредничества хрящевой фазы, и клетки, способствующие этому, присутствуют во внутреннем надкостничном остеогенном слое. При формировании эндохондральной кости за первоначальным синтезом хряща следует эндохондральная последовательность формирования кости [4], [8], [10].
4. Заключение
При морфометрическом исследовании было выявлено следующее содержание кровеносных сосудов на единицу площади костной ткани. В исследуемой группе средняя площадь сечения сосудов микроциркуляторного русла в поле зрения при увеличении ×100 составила 817,8±2,8 мкм2. В группе сравнения этот показатель составил 651,4±2,9 мкм2. Проверка показала статистическую достоверность различий.
