The Effect of Renin-Angiotensin System Blockers on the Course of Coronavirus Infection in Patients with Comorbid Hypertension
The Effect of Renin-Angiotensin System Blockers on the Course of Coronavirus Infection in Patients with Comorbid Hypertension
Abstract
The work presents the results of a retrospective analysis of 60 medical records of inpatients with coronavirus infection. The effect of renin-angiotensin system blockers on the course of COVID-19 in patients with concomitant hypertension who continue taking these drugs (the main group) was studied. Patients in the control group were taking calcium ion antagonists for hypotensive purposes. There were no significant differences between the groups in most of the studied criteria of infection severity (average duration of bed-days of hospitalization, all laboratory and radiological criteria of COVID-19 severity). Only one criterion showed significant differences: patients taking renin-angiotensin system blockers required oxygen support longer and more frequently.
1. Введение
Пандемия COVID-19 затронула около 600 млн. человек во всем мире и привела к более чем 6 млн. смертей по состоянию на август 2022 года [1]. Заболеванию подвержены люди всех возрастов, однако смертность на фоне инфекции значительно выше среди людей старших возрастных групп, что связывают с большей коморбидностью таких пациентов [2], [3], [4]. Особую роль играют сердечно-сосудистые заболевания (гипертоническая болезнь (ГБ), хроническая сердечная недостаточность) и сахарный диабет, т.е. заболевания, характеризующиеся повышением активности эффекторов ренин-ангиотензиновой системы (РАС) [5]. Высокой активностью ангиотензина-II (АТ-II) обусловлено развитие воспаления в сосудистой стенке, оксидативный стресс, гипертрофия миокарда и сосудистой стенки, антидиуретический эффект и усиление синтеза альдостерона в коре надпочечников [6]. Известно, что вирус SARS-CoV-2 проникает в организм человека через слизистые оболочки ротовой полости, используя в качестве рецептора ангиотензинпревращающий фермент 2 типа (АПФ 2). Кроме того, вирус может снижать экспрессию АПФ2 в тканях, что приводит к накоплению в них АТ-II. Таким образом, SARS-CoV-2 и РАС тесно взаимодействуют как во время инфицирования организма, так и в процессе инфекции [6], [7], [8]. Применение блокаторов РАС (ингибиторов АПФ, антагонистов рецепторов АТ-II 1 типа (АРА)) для лечения сердечно-сосудистых заболеваний и сахарного диабета у пациентов с новой коронавирусной инфекцией вызвало серьезные опасения. Существуют наблюдения, свидетельствующие о возможном влиянии блокаторов РАС на уровень АПФ 2, в частности, о повышении экспрессии АПФ 2 в тканях под влиянием этих препаратов [7], [8]. В таком случае ИАПФ и АРА могут способствовать более высокой вирусной нагрузке и более тяжелому течению вирусной инфекции. Вместе с тем имеется немало свидетельств об отсутствии влияния блокаторов РАС на активность АПФ 2. Более того, высокий уровень плазменного АПФ 2 может играть защитную роль при проникновении вируса в клетку, т.к. плазменная форма АПФ 2, связываясь с вирусом в кровотоке, препятствует его взаимодействию с мембраносвязанной формой фермента и проникновению вируса внутрь клетки человека [8]. Учитывая исключительно широкое применение ингибиторов АПФ и АРА в терапевтической практике, проблема их применения во время COVID-19 остается актуальной.
Цель исследования – изучение влияния блокаторов РАС на течение COVID-19 у больных с сопутствующей ГБ.
2. Методы и принципы исследования
Материалом исследования послужили медицинские карты стационарных больных, находившихся на лечении в ГБУЗ РМ «Республиканская инфекционная клиническая больница» в период с сентября по ноябрь 2021 г. Изучены медицинские карты 60 женщин в возрасте 61-69 лет с коронавирусной инфекцией. У всех пациентов при поступлении в стационар была диагностирована пневмония средней степени тяжести. Критерием включения пациентов в исследование послужило наличие у них ГБ 2-3 степени в качестве сопутствующего заболевания. Сформированы 2 группы пациентов: основная (30 человек) и контрольная (30 человек). В основной группе для лечения ГБ использовались блокаторы РАС (эналаприл, каптоприл, лозартан). В контрольной группе для лечения ГБ использовались блокаторы кальциевых каналов. Анализу подвергнуты следующие показатели: средняя продолжительность койко-дня; средняя продолжительность и частота использования кислородной поддержки при лечении больных, максимальный уровень С-реактивного белка (СРБ), минимальный уровень тромбоцитов, минимальный уровень лимфоцитов, максимальный уровень соотношения нейтрофилы/лимфоциты в анализах крови, максимальная площадь поражения легочной ткани и динамика рентгенологической картины по результатам компьютерной томографии за время нахождения больных в стационаре.
Статистическая обработка результатов проводилась с применением стандартных алгоритмов вариационной статистики. Оценка достоверности различий между группами проводилась по t-критерию Стьюдента. При p<0,05 различия считались достоверными.
3. Основные результаты
Средняя длительность пребывания пациента в стационаре при легких формах коронавирусной инфекции составляет 12 дней, при среднетяжелых 14 дней. Тяжелые и крайне тяжелые случаи рассчитаны на 17- и 24-дневную госпитализацию соответственно. Продолжительность лечения в стационаре может косвенно свидетельствовать о тяжести коронавирусной инфекции. В нашем исследовании продолжительность стационарного лечения в основной группе составила 14,93±0,91 койко-дней, в контрольной – 14,1±0,55, р=0,43.
На сегодняшний день нет четких статистических данных о продолжительности респираторной поддержки, необходимой больным COVID-19. Кислородную терапию начинают при снижении сатурации <92% и продолжают до достижения SpO2 96-98% [1, C. 74-75]. Длительность оксигенотерапии может свидетельствовать о тяжести коронавирусной инфекции. В основной группе кислородная поддержка потребовалась 63±8,8% больных, в контрольной – 33±8,5%, р=0,019 (см. рисунок 1).
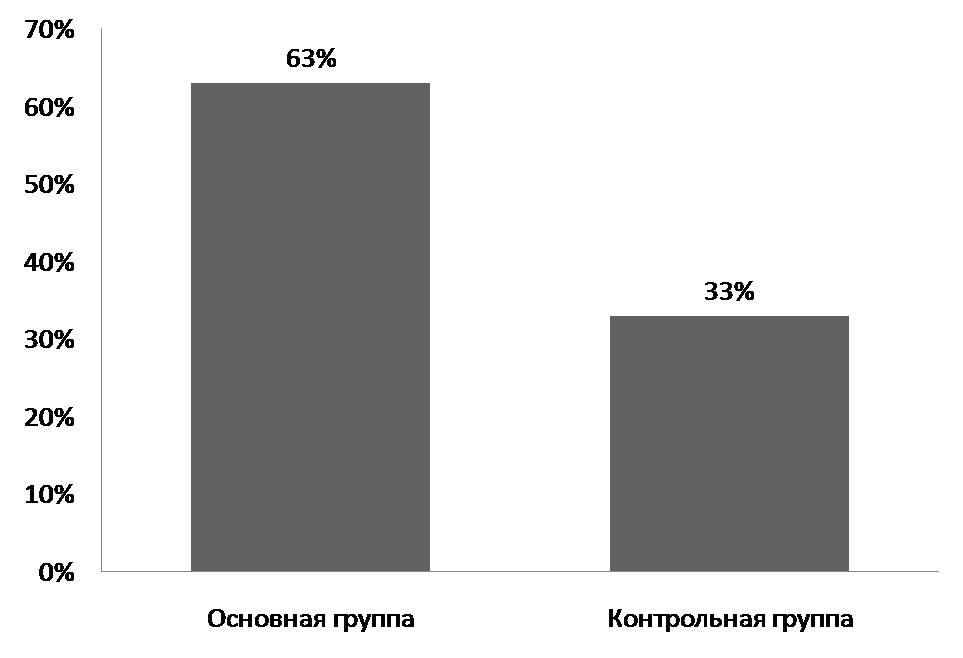
Рисунок 1 - Количество пациентов, нуждавшихся в кислородной поддержке, в основной и контрольной группах
Примечание: р<0,05
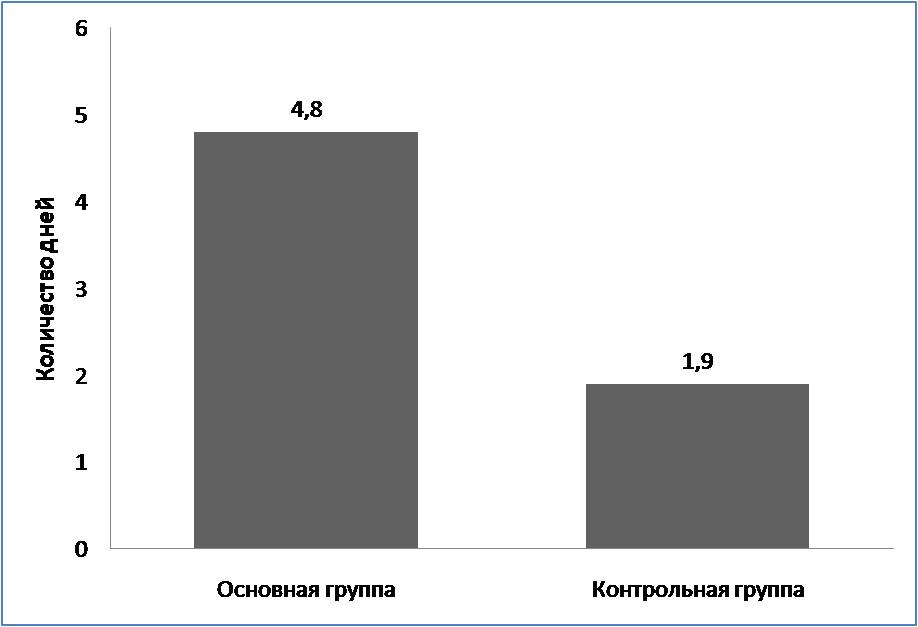
Рисунок 2 - Продолжительность оксигенотерапии в основной и контрольной группах
Примечание: р<0,05
Ещё одним лабораторным критерием тяжести COVID-19 является цитопения. Тромбоцитопения обусловлена как прямым угнетением гематопоэтических клеток костного мозга SARS-CoV-2, так и увеличением потребления тромбоцитов, поскольку повреждение легочной ткани сопровождается активацией, агрегацией и удержанием тромбоцитов в местах повреждения, образованием тромбов. В основной группе минимальный уровень тромбоцитов составил 151,29±10,7*109/л, в контрольной – 170,63±8,54, р=0,16. Лимфоцитопения развивается у 80 % пациентов с COVID-19. Существует прямая связь между степенью лимфоцитопении и вероятностью развития острого респираторного дистресс-синдрома. Факторами, способствующими снижению уровня лимфоцитов при COVID-19, являются: лизис клеток (непосредственное влияние вируса SARS-CoV-2 на лимфоциты); апоптоз клеток (этому способствует повышенный уровень интерлейкина); снижение лимфопоэза в костном мозге (при гиперактивации иммунной системы и продукции противовоспалительных цитокинов). В основной группе минимальный уровень лимфоцитов составил 0,96±0,09*109/л, в контрольной – 1,31±0,1, р=0,72.
Повышенный показатель соотношения нейтрофилы/лимфоциты может рассматриваться как прогрессирование COVID-19. Соотношение более 3,13 расценивается как неблагоприятный признак с высоким риском летального исхода. Соотношение нейтрофилы/лимфоциты в основной группе составило 0,34±0,06, в контрольной – 0,40±0,04, р=0,42.
Объем пораженной легочной ткани и тяжесть болезни находятся в непосредственной зависимости. Рентгенологическими признаками пневмонии вирусного генеза являются многочисленные двусторонние округлые участки уплотнения по типу «матового стекла» в глубине легочной ткани или расположенные субплеврально. В нашем исследовании максимальная площадь поражения легочной ткани в основной и контрольной группах была сопоставимой: 36,6±3,02 и 32,1±3,1% соответственно, р=0,3. Динамика КТ-картины в легких за время нахождения в стационаре в основной группе –8±3,45%, в контрольной –5±3,05, р=0,28.
Результаты исследования сведены в таблицу (см. таблицу 1).
Таблица 1 - Клинические, лабораторные и рентгенологические критерии тяжести болезни в основной и контрольной группах больных
Критерии тяжести болезни | Контрольная группа | Основная группа | Значимость различий между показателями в группах |
Средняя продолжительность стационарного лечения, койко-день | 14,1±0,55 | 14,93±0,91 | р=0,43 |
Средняя продолжительность кислородной поддержки (дни) | 1,9±0,75 | 4,8±1,02 | р=0,02 |
Количество больных, которым потребовалась кислородная поддержка, % | 33±8,5 | 63±8,8 | р=0,019 |
Максимальный уровень СРБ, мг/л | 43,7±8,63 | 38,47±6,92 | р=0,64 |
Минимальный уровень тромбоцитов, 109/л | 170,63±8,54 | 151,29±10,7 | р=0,16 |
Минимальный уровень лимфоцитов, % | 1,31±0,1 | 0,96±0,09 | р=0,72 |
Максимальный уровень соотношения нейтрофилы/лимфоциты | 0,40±0,04 | 0,34±0,06 | р=0,42 |
Максимальная площадь поражения легких, % | 32,1±3,1 | 36,6±3,02 | р=0,3 |
Динамика КТ-картины в легких, % | –5±3,05 | –8±3,45 | р=0,28 |
Примечание: n=30
Результаты нашей работы согласуются с данными современных клинических исследований и рекомендациями международных медицинских обществ, которые дают основание считать, что негативные последствия приема ингибиторов РАС на тяжесть течения COVID-19 не доказаны. В то же время иАПФ и АРА продолжают обеспечивать защиту дыхательной, сердечно-сосудистой системы и почек у пациентов с диагнозом COVID-19 [9], [10].
4. Заключение
Блокаторы РАС не оказывали достоверного влияния на большинство изученных критериев оценки тяжести COVID-19 у больных, принимающих и не принимающих эти препараты. Не было достоверных различий между группами по средней продолжительности койко-дней нахождения пациента в стационаре, по всем лабораторным и томографическим критериям тяжести COVID-19. Только по одному критерию выявлены достоверные различия: больные, принимающие блокаторы РАС, дольше и чаще нуждались в кислородной поддержке по сравнению с пациентами, не принимающими эти препараты. Отсутствие негативных воздействий блокаторов РААС на большинство изученных критериев тяжести COVID-19 позволяет сделать вывод об обоснованности антигипертензивной терапии иАПФ и АРА у больных коронавирусной инфекцией.
