AN ANALYSIS OF A CLINICAL CASE OF SUCCESSFUL THERAPY OF COMMUNITY-ACQUIRED POLYSEGMENTAL PNEUMONIA COMPLICATED BY ACUTE INFECTIOUS-TOXIC MYOCARDITIS
АНАЛИЗ КЛИНИЧЕСКОГО СЛУЧАЯ УСПЕШНОЙ ТЕРАПИИ ВНЕБОЛЬНИЧНОЙ ПОЛИСЕГМЕНТАРНОЙ ПНЕВМОНИИ, ОСЛОЖНЕННОЙ ОСТРЫМ ИНФЕКЦИОННО-ТОКСИЧЕСКИМ МИОКАРДИТОМ
Научная статья
Гетман С.И.1, *, Чепель А.И.2, Кушнарев С.В.3, Тегза В.Ю.4
1 Военный институт физической культуры МО РФ, Санкт-Петербург, Россия;
2 ,3, 4 Военно-медицинская академия имени С.М. Кирова МО РФ, Санкт-Петербург, Россия
* Корреспондирующий автор (sig.spb[at]mail.ru)
АннотацияВ статье описан клинический случай с пациентом, поступившего в терапевтический стационар для лечения внебольничной полисегментарной пневмонии. На 8 сутки от начала заболевания, у больного появились перебои в работе сердца и учащенное сердцебиение в утренние часы. Проведено суточное мониторирование электрокардиограммы по Холтеру. Зарегистрирован синусовый ритм с частой наджелудочковой экстрасистолией — 1084 в сутки, 122 эпизода бигеминии, 76 эпизодов тригеминии и 143 мономорфных желудочковых экстрасистол в сутки, (ранее суточное мониторирование электрокардиограммы по Холтеру не проводилось). Ишемических изменений не выявлено. Пауз не зафиксировано. Данные изменения были трактованы в рамках перенесенного острого инфекционного миокардита. Для уточнения диагноза взят биохимический анализ крови (КФК, КФК-МВ, тропонин) — показатели в норме. Выполнена магнитно-резонансная томография (МРТ) сердца с контрастным усилением гадолинием. Заключение: МР-признаки диффузного отека миокарда желудочков, что может быть признаком миокардита. Признаков повреждения миокарда или фиброзных изменений в нем не выявлено. Пациент прошел полноценное лечение миокардита и был направлен на реабилитацию. Таким образом, значимую роль в возникновении миокардита играют вирусная инфекция и аутоиммунные факторы. Пациентам при подозрении на инфекционный миокардит с частой желудочковой и наджелудочковой экстрасистолией целесообразно включать в план обследования такой высокотехнологичный метод диагностики, как магнитно-резонансная томография сердца с контрастным усилением гадолинием.
Ключевые слова: пневмония, миокардит, экстрасистолия, магнитно-резонансная томография сердца, гадолиний.
AN ANALYSIS OF A CLINICAL CASE OF SUCCESSFUL THERAPY OF COMMUNITY-ACQUIRED POLYSEGMENTAL PNEUMONIA COMPLICATED BY ACUTE INFECTIOUS-TOXIC MYOCARDITIS
Research article
Getman S.I.1, *, Chepel A.I.2, Kushnarev S.V.3, Tegza V.YU.4
1 Military Institute of Physical Culture of Ministry of Defense of the Russian Federation, St. Petersburg, Russia;
2, 3, 4 S. M. Kirov Military Medical Academy of the Ministry of Defense of the Russian Federation, Saint Petersburg, Russia
* Corresponding author (sig.spb[at]mail.ru)
AbstractThe article describes a clinical case with a patient admitted to a therapeutic hospital for the treatment of community-acquired polysegmental pneumonia. On the 8th day from the onset of the disease, the patient had heart failure and palpitations in the morning. Daily monitoring of the Holter electrocardiogram was carried out. A sinus rhythm with frequent supraventricular extrasystole was recorded - 1084 per day, 122 episodes of bigeminal pulse, 76 episodes of trigeminal pulse and 143 monomorphic ventricular extrasystoles per day, (previously, daily monitoring of the Holter electrocardiogram was not carried out). No ischemic changes were detected. No pauses are recorded. These changes were interpreted within the framework of acute infectious myocarditis. To clarify the diagnosis, a biochemical blood test (CPK, CPK-MV, troponin) was taken — the indicators were normal. CardiacMRI was performed with gadolinium contrast enhancement. Conclusion: MR signs of diffuse edema of the ventricular myocardium, which may be a sign of myocarditis. There were no signs of myocardial damage or fibrous changes in it. The patient underwent full treatment of myocarditis and was sent for rehabilitation. This concludes that viral infection and autoimmune factors play a significant role in the occurrence of myocarditis. For patients with suspected infectious myocarditis with frequent ventricular and supraventricular extrasystole, it is advisable to include in the examination plan such a high-tech diagnostic method as cardiac magnetic resonance imaging with gadolinium contrast enhancement.
Keywords: pneumonia, myocarditis, extrasystole, cardiac magnetic resonance imaging, gadolinium.
ВведениеВ 1749 г. французский врач Жан-Батист Сенак впервые описал феномен воспаления сердца и трудности в его распознавании в своем труде «Traite des Maladies du Coeur» («Трактат о болезни сердца»).
До 1980-х годов, помимо собственно воспалительных поражений миокарда, этот термин подразумевал и другие поражения миокарда, включая кардиомиопатии при ишемической болезни сердца и гипертонической болезни (гипертоническое сердце) [1], [2].
На сегодняшний день под термином «миокардит» понимают совокупность клинических и морфологических изменений тканей сердца (клеток проводящей системы, соединительнотканных структур, кардиомиоцитов), когда доказаны или обоснованно предполагаются воспалительные изменения миокарда (инфильтрация мононуклеарными клетками) аутоиммунной или инфекционной природы, которые выявляются гистологическими или иммуногистохимическими методами [3].
Современные представления об эпидемиологии миокардита носят разрозненный характер и не позволяют сформировать целостную картину [4]. Частота встречаемости миокардита серьезно недооценивается из-за неспецифических симптомов его проявления и зачастую бессимптомного течения. В недавнем эпидемиологическом исследовании установлена глобальная распространенность миокардита — 22 100 000 больных ежегодно [5]. Причинами миокардита являются инфекционные агенты, включая бактерии, вирусы, риккетсии, хламидии, простейшие, грибы, а также неинфекционные триггеры (аутоантитела, токсины). Самыми распространенными причинами развития миокардитов считаются вирусные инфекции. Из них наиболее часто в образцах эндомиокардиальной биопсии (ЭМБ) с помощью анализа на основе полимеразной цепной реакции (ПЦР) и вирус-специфической гибридизации определяют парвовирус В19 (PVB19), энтеровирус, вирус гриппа А, аденовирус, вирус Эпштейна — Барр, цитомегаловирус, вирус герпеса человека, вирус гепатита С и ВИЧ-инфекцию [6].
Нельзя обойти стороной ситуацию, связанную с новой коронавирусной инфекцией COVID-19. Мы знаем, что эта проблема коснулась всего мира и практически каждого из нас. Роль вирусной инфекции как этиологического фактора миокардита приобретает в нынешних условиях пандемии COVID-19 особое значение и высокую актуальность. Можно предположить, что заболеваемость миокардитом будет расти на фоне новой коронавирусной инфекции COVID-19, что связано с высокой тропностью вируса к системе кровообращения. В связи с этим важно своевременно выявлять заболевших острым вирусным миокардитом для полноценного и в полном объеме лечения.
Однако существуют нерешенные проблемы касательно точной диагностики миокардита. Это обусловлено разнообразием клинических проявлений этого заболевания и недостатками современных методов выявления миокардита.
Уровень лейкоцитов, С-реактивного белка считаются маркерами воспалительного ответа в организме. Однако они неспецифичны для миокардита и указывают лишь на наличие воспалительного процесса. Для выявления повреждения миокарда (некроза) могут использоваться биомаркеры некроза миокарда (тропонины, креатин-фосфокиназа МВ-фракции). Однако, они также неспецифичны.
Электрокардиография (ЭКГ) для выявления миокардита обладает низкой диагностической ценностью, поскольку ЭКГ-изменения у пациентов с подтвержденным миокардитом имеют неспецифический характер (транзиторные смещения сегмента ST, отрицательный зубец Т).
Эхокардиография (ЭхоКГ) помогает определить толщину стенок сердца, размеры полостей, диастолическую и систолическую функции миокарда, но не наличие миокардита.
В современных условиях для исследования аппарата кровообращения начинают активно использовать такой высокотехнологичный метод исследования как магнитно-резонансная томография сердца с контрастным усилением гадолинием. До недавнего времени магнитно-резонансная томография (МРТ) сердца в основном применялась для обнаружения значительно сниженной фракции выброса (ФВ) левого желудочка (ЛЖ) и уточнения аномалий движения стенки миокарда. Более чувствительной методикой для выявления миокардита и зон повреждения миокарда у пациентов с острым миокардитом является магнитно-резонансная томография сердца с контрастным усилением. Данными гистологического анализа при эндомиокардиальной биопсии (ЭМБ) подтверждается, что чувствительность и специфичность МРТ с контрастированием в отношении миокардита составляют 100 и 90% соответственно [7]. При остром миокардите участки миокарда с контрастным усилением определяются в боковой стенке эпикардиальной поверхности миокарда ЛЖ, тогда как в случае ишемизированного миокарда контрастное усиление будет чаще выявляться в субэндокардиальных слоях миокарда.
Эндомиокардиальная биопсия считается «Золотым стандартом» диагностики миокардита [8]. При выявлении лимфоцитарной инфильтрации миокарда в сочетании с некрозом кардиомиоцитов результат ЭМБ расценивают как положительный (Далласские критерии) [9]. В пользу миокардита свидетельствует обнаружение в поле зрения более 14 лимфоцитов при 400-кратном увеличении микроскопа. Однако, как известно, ЭМБ в существующей практике используют исключительно при отсутствии ответа на медикаментозное лечение и в неясных клинических случаях. И связано это с тем, что её выполнение требует серьёзного обоснования и технических навыков, кроме того, для морфологического подтверждения диагноза необходимо взять не менее трех биоптатов. А при очаговых поражениях сердечной мышцы чувствительность метода значительно снижается и составляет от 17 до 34 % [6].
Анализ клинического случая из практики врача-терапевта.
Пациент Р. 42 года поступил 14 мая 2019 г. в пульмонологическое отделение клиники ТУВ 1 (Терапия усовершенствования врачей) ВМедА им. С.М. Кирова, г. Санкт-Петербург с диагнозом направившего лечебного учреждения: Внебольничная полисегментарная пневмония с локализацией в верхней доле (S1,2,3) правого легкого нетяжелого течения. SMRT — CO 0 баллов. Без дыхательной недостаточности.
Заболел остро, в ночь на 12 мая 2019 г. Заболевание связывает с переохлаждением на фоне физической нагрузки (ремонт в квартире), а также контактом с супругой и дочерью, переносящими острую респираторную вирусную инфекцию (ОРВИ).
При поступлении в клинику пациент предъявлял жалобы на кашель с отделением вязкой, трудноотделяемой мокроты, общую слабость, повышение температуры тела до фебрильных значений, озноб, выраженную потливость.
Из анамнеза: военнослужащий по контракту. В детстве перенес закрытую черепно-мозговую травму (ЗЧМТ); компрессионный перелом позвоночника; операции по поводу варикоцеле (1996 г.); септумоперацию (1999 г.), лапароскопическую холецистэктомию, папиллосфинктеротомию по поводу желчнокаменной болезни (2018 г.). Страдает хроническим панкреатитом; остеохондрозом позвоночника, хронической пояснично-крестцовой радикулопатией L5 — S1; ожирением III ст. Наследственность не отягощена. Аллергические реакции и непереносимость лекарств отрицает. Вредные привычки: с января 2018 г. не курит (ранее курил с 1996 года по 1 пачке в сутки). Со слов пациента алкоголь, наркотические и психотропные средства не употребляет.
При объективном обследовании в клинике: общее состояние удовлетворительное, сознание ясное. В своей личности и окружающей обстановке ориентирован правильно. Рост — 180 см., масса тела — 130 кг (индекс массы тела = 40,1 кг/м2), избыточного питания. Кожные покровы и видимые слизистые физиологической окраски и повышенной влажности, чистые, внешние повреждения отсутствуют. Температура тела 38,7 0С. Периферические л/у при пальпации не увеличены, подвижные, безболезненные. Периферических отеков нет.
Границы сердца не расширены: верхняя граница на уровне III ребра, правая граница — по правому краю грудины, левая — по срединно-ключичной линии. Тоны сердца приглушены, ритмичные, акцент II тона на аорте. Пульс ритмичный с частотой 103 в минуту. Артериальное давление 135/70 мм рт. ст. на правой руке и 140/80 мм рт. ст. на левой руке.
Грудная клетка правильной формы. Симметрично участвует в акте дыхания. При перкуссии — проведение звука затруднено из-за избыточной подкожно-жировой клетчатки. Аускультативно — ослабление дыхания в проекции верхней доли правого легкого, хрипы не выслушиваются. Частота дыхательных движений — 18 в минуту.
Язык суховат, обложен желто-серым налетом у корня. Живот увеличен в объеме за счет избыточной подкожно-жировой клетчатки, при пальпации мягкий, безболезненный. Печень и селезенка не пальпируются.
Симптом поколачивания по поясничной области с обеих сторон отрицательный. Стул оформленный, без патологических примесей, 1 раз в день. Мочеиспускание самостоятельное, диурез, со слов, не затруднен.
Результаты инструментальных методов обследования
На рентгенографии органов грудной клетки от 14.05.2019. — В нижней доле правого легкого усиление легочного рисунка.
На компьютерной томографии (КТ) грудной клетки от 14.05.2019. — КТ-картина смешанной пневмонической инфильтрации S1,2,3 правого легкого, лимфоаденопатия правой бронхопульмональной группы узлов.
На ЭКГ от 14.05.2019. — QRS 120 мс, QT 327 мс, P 96 мс, синусовая тахикардия, частота сердечных сокращений 103 в минуту, горизонтальное расположение электрической оси сердца. Локальные нарушения внутрижелудочковой проводимости.
Общий анализ крови (ОАК) от 15.05.2019. — Лейкоциты 9,3 × 109/ л, СОЭ 44 мм/ч; эритроциты 5,48 × 1012/л; Hв 159 г/л; тромбоциты 150 × 109/ л; п/я 4%; с/я 77 %; эозинофилы 2 %; базофилы 0 %; лимфоциты 7 %; моноциты 10 %.
Общий анализ мокроты и на ВК от 15.05.2019. — Мокрота желтого цвета, вязкая, гнойная, без запаха. Эпителий плоский — 2-3-5 в поле зрения; мерцательный — 1-1-2 в поле зрения; лейкоциты — 80-100-120 в поле зрения; эозинофилы — 3-5-10 в поле зрения.
Микроскопическое исследование мокроты: нейтрофилы — 93%, лимфоциты — 2 %, эозинофилы — 5 %. Грам (+) микрофлора в умеренном количестве (кокки). МБТ — микобактерии туберкулеза не обнаружены. Присутствуют спирали Куршмана, кристаллы Шарко—Лейдена.
Для лечения пневмонии назначена антибактериальная терапия: цефепим 2 г. 2 раза в день внутримышечно, клацид 500 мг 2 раза в день перорально. Муколитическая терапия: ацетилцистеин 600 мг в сутки в виде шипучих таблеток. Гастропротективная терапия.
На фоне комбинированной антибактериальной и муколитической терапии состояние пациента начало улучшаться.
Обследование в клинике продолжалось.
Биохимический анализ крови от 15.05. 2019. — С-реактивный белок — 84,75 мг/л; глюкоза — 5,28 ммоль/л; холестерин 5,01 ммоль/л; триглицериды 0,92 ммоль/л; ЛПВП — 1,48 ммоль/л; ЛПОНП — 0,42 ммоль/л; ЛПНП — 3,11 ммоль/л; коэффициент атерогенности — 2,39; общий белок — 71,4 г/л; альбумины — 41,9 г/л; глобулины — 29,5 г/л; А/Г — 1,42; К — 4,11 ммоль/л; Nа — 140,9 ммоль/л; г/л; ПТИ — 98%, МНО — 1,02 ед.; фибриноген — 7,79 г/л; креатинин — 100,4 мкмоль/л; мочевина — 5,7 ммоль/л; мочевая кислота — 322,3 ммоль/л; общий билирубин — 17,9 ммоль/л; АЛТ — 62,3; АСТ — 66; ГГТ — 307,1; щелочная фосфотаза — 97,4; ЛДГ — 279; КФК — 153,5.
Спирография легких 16.05.2019. — ЖЕЛ — 103%, ФЖЕЛ — 108%, ОФВ1 — 118 %, ОФВ1/ ФЖЕЛ — 88,7 %. Заключение: вентиляционные показатели в норме.
19.05.2019 г. пациент пожаловался на перебои в работе сердца в утренние часы и периодическое учащенное сердцебиение, в связи с чем, 22.05.2019 было проведено суточное мониторирование ЭКГ по Холтеру. Зарегистрирован синусовый ритм с частой наджелудочковой экстрасистолией — 1084 в сутки, 122 эпизода бигеминии и 76 эпизодов тригеминии и 143 мономорфных желудочковых экстрасистол в сутки, (ранее суточное мониторирование ЭКГ не проводилось). Ишемических изменений не выявлено. Пауз не зафиксировано.
Данные изменения были трактованы в рамках перенесенного острого инфекционного миокардита. Для уточнения диагноза взят биохимический анализ крови (КФК, КФК-МВ, тропонин) — показатели в норме.
30.05.2019 г. выполнена эхокардиография сердца: левый желудочек (ЛЖ) не расширен. Толщина межжелудочковой перегородки — 1 см. Толщина задней стенки — 1 см. Левое предсердие (ЛП) не увеличено. Миокард правого желудочка утолщен — 0,6 см. Стенки аорты, створки аортального клапана и митрального клапана уплотнены. Фракция выброса (ФВ) — 60 %. Индекс массы миокарда (ИММ) — 69 гр/м2. Заключение: гипертрофия правого желудочка. Стенки аорты, створки аортального клапана и митрального клапана уплотнены.
31.05.2019 г. Выполнена магнитно-резонансная томография сердца (МРТ) сердца. Заключение: МР-признаки диффузного отека миокарда желудочков, что может быть признаком миокардита. Признаков повреждения миокарда или фиброзных изменений в нем не выявлено.
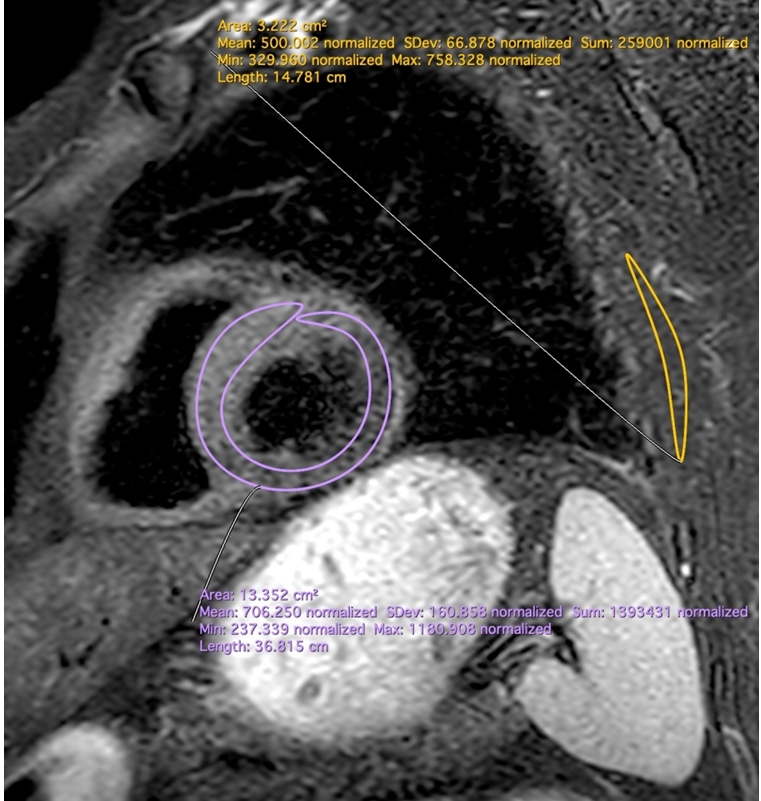
Рис. 1 – Отек в области базальных сегментов левого желудочка
Примечание: на изображении продемонстрирована разница интенсивности сигнала от миокарда левого желудочка (область интереса – изображена в круге и выделена фиолетовым цветом) по отношению к интенсивности сигнала от зубчатой мышцы (область интереса – изображена в треугольнике и выделена желтым цветом)
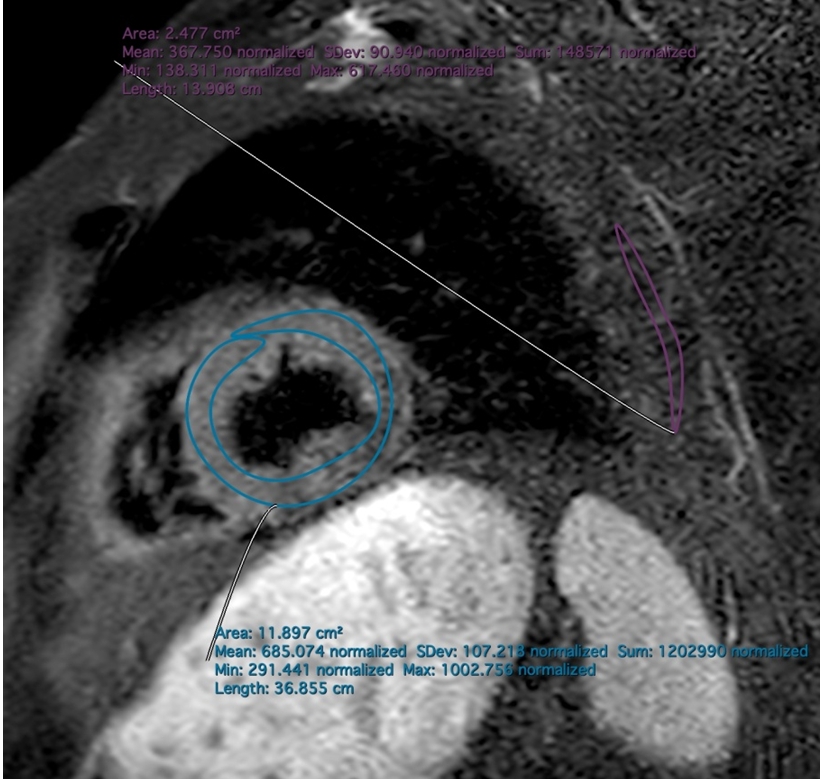
Рис. 2 – Отек в области средних сегментов миокарда левого желудочка
Примечание: на изображении продемонстрирована разница интенсивности сигнала от миокарда левого желудочка (область интереса – изображена в круге и выделена голубым цветом) по отношению к интенсивности сигнала от зубчатой мышцы (область интереса – изображена в треугольнике и выделена фиолетовым цветом)
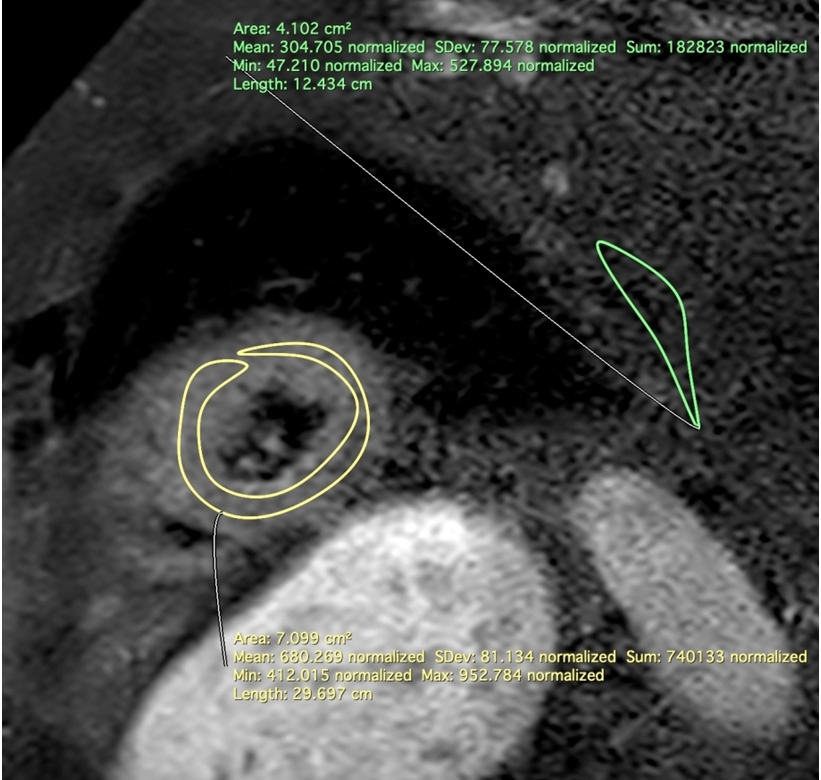
Рис. 3 – Отек в области апикальных сегментов миокарда левого желудочка
Примечание: на изображении продемонстрирована разница интенсивности сигнала от миокарда левого желудочка (область интереса – изображена в круге и выделена желтым цветом) по отношению к интенсивности сигнала от зубчатой мышцы (область интереса – изображена в треугольнике и выделена зеленым цветом)
Пациенту рекомендовано проведение эндомиокардиальной биопсии. Однако от исследования больной отказался.
Таким образом, в процессе стационарного обследования пациента был диагностирован острый инфекционно-токсический миокардит.
На фоне комбинированной антибактериальной, муколитической, бронхолитической терапии пневмония разрешилась, снизилась активность миокардита.
На рентгенографии органов грудной клетки от 24.05.2019. — Инфильтрация справа разрешилась, в S3 сегменте сохраняется незначительное усиление легочного рисунка, как остаточные изменения перенесенной пневмонии. Плевральные синусы свободны. Сердце, аорта и диафрагма в пределах нормы.
Общий анализ крови (ОАК) от 24.05.2019. — Лейкоциты 5,9 × 109/ л, СОЭ 17 мм/ч; эритроциты 5,75 × 1012/л; Hв 164 г/л; тромбоциты 305 × 109/ л; п/я — 1 %; с/я — 72 %; эозинофилы — 1 %; базофилы — 0 %; гранулоциты 86,5 %; лимфоциты 29 %; моноциты 2 %.
Биохимический анализ крови от 24.05.2019. — С-реактивный белок — 1,47 млг/л; глюкоза — 4,66 ммоль/л; К — 4,83 ммоль/л; Nа — 140,2 ммоль/л; фибриноген — 3,44 г/л; общий билирубин — 10,9 мкмоль/л; АЛТ — 34,6 Ед/л; АСТ — 21,6 Ед/л; ГГТ — 212,7 Ед/л; КФК — 147,3 Ед/л; КФК-МБ — 15 Ед/л; Тропонин Т — 0,006 нг/мл.
Окончательный диагноз 10.06.2019
Основной диагноз: Внебольничная полисегментарная пневмония с локализацией в верхней доле (S1,2,3) правого легкого нетяжелого течения. SMRT — CO 0 баллов. Без дыхательной недостаточности.
Осложнение основного заболевания: Острый инфекционно-токсический миокардит легкой степени тяжести без сердечной недостаточности.
Сопутствующие заболевания: Ожирение III степени, алиментарно-конституциональное, стабильная стадия. Хронический панкреатит, фаза ремиссии. Желчнокаменная болезнь. Состояние после лапароскопической холецистэктомии, папиллосфинктеротомии (27.08.2018 г.). Хроническая пояснично-крестцовая радикулопатия L5 — S1. Остеохондроз позвоночника.
От проведения реабилитации в санатории пациент отказался. В связи с выявленным заболеванием, предусматривающим категорию годности к военной службе «Г» — временно не годен к военной службе, направлен на медицинское освидетельствование для определения годности к военной службе.
Заключение
Проведенное нами научное исследование позволило сделать выводы:
- Миокардит остается одним из серьезных заболеваний системы кровообращения, которое значительно ухудшает прогноз и качество жизни пациентов.
- Значимую роль в возникновении миокардита играют вирусная инфекция и аутоиммунные факторы. На фоне пандемии новой коронавирусной инфекции COVID-19 можно ожидать роста заболеваемости миокардитом.
- Магнитно-резонансную томографию сердца с контрастным усилением гадолинием целесообразно включать в план обследования больных, страдающих частой желудочковой и наджелудочковой экстрасистолией, особенно при подозрении на миокардит.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Моисеев В.С. Кардиомиопатии и миокардиты / В.С. Моисеев, Г.К. Киякбаев. М.: Гэотар-Медиа. – 2012. – 350 с.
- Fung, G. Myocarditis / G. Fung, H. Luo, Y. Qiu [et al.] // Circulation Research. – 2016. – Vol. 118. – P. 496–514.
- Richardson, P. Report of the 1995 Worid Health Organization/international Society and Federation of Cardiology Task Force on the Definition and Classification of cardiomyopathies / P. Richardson, W. McKenna, M. Bristow [et al.] // Circulation. – 1996. – Vol. 93. – P. 841–842.
- Клинические рекомендации по диагностике и лечению миокардитов. – 2019. – 133 с.
- GBD 2013 Risk Factors Collaborators; Forouzanfar, M.N. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: A systematic analysis for the global burden of diseases study 2013 / M.N. Forouzanfar, L. Alexander, H.R. Global // Lancet. – 2015. – Vol. 386. – 743–800.
- Caforio, A.L. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases / A. L. Caforio [et al.] // Eur. Heart J. – 2013. – Vol. 34. – № 33. – Р. 2636–2648.
- Stensaeth, K.H. Cardiac magnetic resonance visualizes acute and chronic myocardial injuries in myocarditis / K.H. Stensaeth [et al.] // Int. J. Cardiovasc. Imaging. – 2012. – Vol. 28. – № 2. – Р. 327–335.
- Leone, O. 2011 Consensus statement on endomyocardial biopsy from the Association for European Cardiovascular Pathology and the Society for Cardiovascular Pathology / O. Leone [et al.] // Cardiovascular Pathology. – 2012. – Vol. 21. – Р. 245–274.
- Grun, S. Long-term follow-up of biopsy-proven viral myocarditis predictors of mortality and incomplete recovery / S. Grun [et al.] // J. Am. Coll. Cardiol. – 2012. – Vol. 59. – Р. 1604–1615.
Список литературы на английском языке / References in English
- Moiseev V.S. Kardiomiopatii i miokardity [Cardiomyopathy and myocarditis] / V.S. Moiseev, G.K. Kiyakbayev. M.: Geotar-Media. - 2012. - 350 p. [in Russian]
- Fung, G. Myocarditis / G. Fung, H. Luo, Y. Qiu [et al.] // Circulation Research. – 2016. – Vol. 118. – P. 496–514.
- Richardson, P. Report of the 1995 Worid Health Organization/international Society and Federation of Cardiology Task Force on the Definition and Classification of cardiomyopathies / P. Richardson, W. McKenna, M. Bristow [et al.] // Circulation. – 1996. – Vol. 93. – P. 841–842.
- Klinicheskie rekomendacii po diagnostike i lecheniju miokarditov [Clinical recommendations for the diagnosis and treatment of myocarditis]. - 2019. - 133 p. [in Russian]
- GBD 2013 Risk Factors Collaborators; Forouzanfar, M.N. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: A systematic analysis for the global burden of diseases study 2013 / M.N. Forouzanfar, L. Alexander, H.R. Global // Lancet. – 2015. – Vol. 386. – 743–800.
- Caforio, A.L. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases / A. L. Caforio [et al.] // Eur. Heart J. – 2013. – Vol. 34. – № 33. – Р. 2636–2648.
- Stensaeth, K.H. Cardiac magnetic resonance visualizes acute and chronic myocardial injuries in myocarditis / K.H. Stensaeth [et al.] // Int. J. Cardiovasc. Imaging. – 2012. – Vol. 28. – № 2. – Р. 327–335.
- Leone, O. 2011 Consensus statement on endomyocardial biopsy from the Association for European Cardiovascular Pathology and the Society for Cardiovascular Pathology / O. Leone [et al.] // Cardiovascular Pathology. – 2012. – Vol. 21. – Р. 245–274.
- Grun, S. Long-term follow-up of biopsy-proven viral myocarditis predictors of mortality and incomplete recovery / S. Grun [et al.] // J. Am. Coll. Cardiol. – 2012. – Vol. 59. – Р. 1604–1615.
