STRUCTURE AND CLINICAL SIGNIFICANCE OF THYROID PATHOLOGY IN CASE OF TISSUE DYSPLASIA AND HPERMOBILITY SYNDROME
Санеева Г.А.
Кандидат медицинских наук, Ставропольский государственный медицинский университет
СТРУКТУРА И КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ ТИРЕОИДНОЙ ПАТОЛОГИИ В АСПЕКТЕ ДИСПЛАЗИИ СОЕДИНИТЕЛЬНОЙ ТКАНИ ПРИ ГИПЕРМОБИЛЬНОМ СИНДРОМЕ
Аннотация
У 80 пациентов с синдромом гипермобильности суставов изучены характер и распространенность тиреоидной патологии. Установленные особенности тиреоидного статуса при гипермобильном синдроме в виде гипотироксинемии, аутоиммунных тиреопатий диктуют необходимость целенаправленной диагностики нарушений функции щитовидной железы и применения активных стратегий индивидуальной йодпрофилактики у молодых пациентов.
Ключевые слова: синдром гипермобильности суставов, костное ремоделирование, тиреоидные гормоны, тиреопатии.
Saneeva G.A.
MD, Stavropol State medical University
STRUCTURE AND CLINICAL SIGNIFICANCE OF THYROID PATHOLOGY IN CASE OF TISSUE DYSPLASIA AND HPERMOBILITY SYNDROME
Abstract
We examined 80 patients with hypermobility syndrome in joints and studied the nature and prevalence of thyroid pathology. The features of thyroid pathology and hypermobility syndrome include: Hypothyroxinemia and autoimmune thyropathies which require targeted diagnosis of the thyroid function defect and the use of active strategies of individual iodine treatment among young patients.
Keywords: joint hypermobility syndrome, bone remodeling, thyroid hormones, thyroid disease.
Костно-мышечная патология и заболевания соединительной ткани рассматриваются как актуальная медицинская и социальная проблема вследствие распространенности среди населения, включая лиц молодого и трудоспособного возраста, возрастающих расходов системы здравоохранения на лечение локомоторных патологических состояний и их осложнений, а также высокого рейтинга в ряду причин первичного выхода на инвалидность. Большое внимание в означенном контексте уделяется разработке и внедрению программ своевременной диагностики, эффективной курации и профилактики метаболической костной патологии.
К числу состояний, доказано приводящих к развитию остеопороза и переломов, относят ряд генетических синдромов, ассоциированных с наследственными нарушениями соединительной ткани – несовершенный остеогенез, синдромы Марфана и Элерса-Данло [2]. Однако общность патогенетических механизмов соединительнотканной дисплазии с системностью вовлечения предполагают включение в стратегии целенаправленной диагностики и других клинико-функциональных диспластических проявлений, в том числе полигенно-мультифакториальных, с возможностью коррекции метаболической костной патологии.
К весьма распространенным в практической деятельности терапевта и ревматолога вариантам соединительнотканной дисплазии у лиц молодого возраста относят синдром гипермобильности суставов (СГМС) [4]. Облигатность клинико-морфологических проявлений костно-хрящевой дисплазии при СГМС актуализирует исследование процессов костного метаболизма характеристик с установлением особенностей гормонального регулирования остеогенеза.
Ведущее регуляторное действие в цикле ремоделирования принадлежит гормональным агентам, обеспечивающим гомеостаз основных остеотропных минералов [7]. Однако, помимо регуляторов обмена фосфора и кальция ‒ паратиреоидного гормона и кальцитриола, на клеточные линии ремоделирующей единицы осуществляют воздействие множественные юкста-, паракринные и эндокринные эффекторы. Удержание сбалансированности последовательных процессов остеорезорбции и остеосинтеза не нуждается в прямых гормональных воздействиях, а непосредственно подчинено межклеточным и тканевым пептидам-медиаторам. Наряду с этим кость, являясь акцептором гормональных влияний, испытывает регуляторные эффекты гуморального комплекса. Система гормонального контроля способна изменять выживаемость и функционально-активную способность клеток в костной ремоделирующей единице, инициировать костно-анаболическую реакцию на физические нагрузки.
Одними из важнейших факторов, обеспечивающих физиологически гармоничные линейный рост и созревание скелета, являются тиреоидные гормоны [1, 8]. Рецепторы к тиреотропному гормону непосредственно экспрессируются в кости. Функциональное значение гормонов щитовидной железы в качестве ростовых пермиссоров состоит в синергизме облигатному эффектору ‒ соматотропину. Полноценное биологическое действие последнего становится возможным только при их нормальном содержании. Физиологические концентрации тиронинов требуются и для осуществления генетически запрограммированных дифференцировки, роста и созревания на клеточно-тканевом и на органно-системном уровне. В различных видах соединительной ткани биологические эффекты тиреоидных гормонов сопровождаются угнетением пролиферации фибробластов и хондроцитов [3, 8]. Тиронины также способствуют синтезу в костях коллагена I типа и остеокальцина [1, 3]. Как известно, именно коллаген I типа, имеет наибольшую репрезентативность в тканях организма, в том числе, коже и костях. С процессами мутации в его структуре моногенного или мультифакториального характера связано возникновение системных соединительнотканных дисплазий (синдромов Марфана, Элерса-Данло несовершенного остеогенеза), а также несиндромальных диспластических вариантов. Известным фактором формирования остеопенического синдрома является персистенция сверхфизиологических количеств тиреоидных гормонов за счет усиления резорбции кости и разобщения процессов костного ремоделирования. Таким образом, изучение частоты и характера дисфункции щитовидной железы при СГМС представляется важным для уточнения патогенетического значения в нарушении регуляции костно-хрящевого метаболизма.
Цель исследования. Установление распространенности и спектра тиреоидной патологии у пациентов с гипермобильным синдромом.
Материал и методы. Проведена лабораторная оценка плазменного содержания тиреоидных гормонов у 80 пациентов (34 мужчин и 46 женщин) с СГМС в возрасте от 18 до 30 лет (средний возраст 22,9±3,8 лет). Гипермобильный синдром устанавливали согласно действующим критериям с применением шкалы Р. Beighton [4]. Больные с моногенными наследственными синдромами в исследовании не участвовали Иммунохимическими методами определяли содержание тиреотропного гормона (ТТГ), свободной фракции тироксина (сТ4), трийодтиронина (Т3), а также антител к тиреоидным антигенам (тиреопероксидазе) – АТ к ТПО.
Контрольная группа состояла из 25 человек, сопоставимых по полу и возрасту (средний возраст 22,3±3,6 лет), без гипермобильного синдрома.
Статистическая обработка проведена с помощью пакета статистических программ. Достоверность различий между группами оценивали на основании t-критерия Стьюдента. Достоверность различий качественных признаков подтверждали с использованием критерия χ2. Достоверными считали различия при p≤0,05.
Результаты и обсуждение. Распределение пациентов в соответствии с выраженностью суставной гиперподвижности продемонстрировало преобладание умеренных степеней гипермобильности. Так в 43,8% наблюдений расширенный объем движений в суставах соответствовал 5 баллам, еще у 20% больных данный показатель составил 3 балла, а 4-балльную сверподвижность имели 26,2% обследуемых. Выраженные степени гипермобильности отмечены у 10% пациентов: по 7 и 9 баллов установлено у 2,5% и 7,5% в исследуемой группе.
Полученные данные лабораторных тестов продемонстрировали ряд иммунно-гормональных дезадаптивных состояний щитовидной железы у пациентов с СГМС (рис. 1).
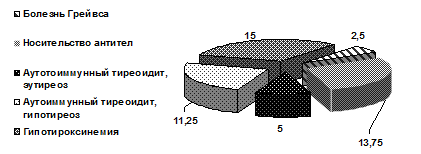
Рис. 1 - Структура тиреоидной патологии у пациентов с СГМС (%)
Из особенностей тиреоидного статуса в исследуемой группе чаще всего отмечались изолированная гипотироксинемия, бессимптомное носительство антител к тиреоидной пероксидазе (р>0,05).
Как известно, снижение уровня сТ4 на фоне нормальных показателей ТТГ, нередко встречается у женщин во время беременности (изолированная гестационная гипотироксинемия) [6]. В группу пациентов с СГМС, включавшую 46 женщин, беременные не входили. Лабораторный феномен умеренного снижения показателей сТ4 или их низконормального диапазона при одновременном повышении уровня Т3 и сохраненном референсном ТТГ также наблюдается в районах, эндемичных по недостаточному содержанию йода в почве и воде [5]. Случаи изолированной гипотироксинемии у больных СГМС можно расценить в качестве снижения адаптивно-приспособительных механизмов в условиях существующей географически йодной эндемии легкой степени выраженности. Активной медикаментозной коррекции установленные особенности не требуют, однако актуализируют использование стратегий индивидуальной йодной профилактики у молодых пациентов с СГМС.
Следующим по частоте в спектре тиреопатий явилось бессимптомное носительство АТ к ТПО, зарегистрированное у 13,75% обследуемых с гипермобильным синдромом. Обособленное увеличение титра антител к компонентам щитовидной железы без нарушения ее функции и известных ультразвуковых или гистологических феноменов, выявляется у 5-10% здоровой популяции, чаще всего среди лиц женского пола [5], рассматриваясь как предиктор развития аутоиммунных и деструктивных тиреопатий и формирования стойкого гипотиреоза.
У 4 (5%) больных СГМС повышение титра АТ к ТПО сочеталось с характерными ультразвуковыми феноменами. При условии эутиреоидного статуса пациентов это послужило диагностике у них аутоиммунного тиреоидита без нарушения функции щитовидной железы, требующей лишь соответствующего контроля в динамике.
Всего же повышенный титр антитиреоидных антител установлен у 24 (30%) пациентов с СГМС, характеризуя превышение среднепопуляционных показателей (р≤0,05). Таким образом, повышение риска развития аутоиммунных тиреопатий определяет целесообразность скрининга тиреоидной дисфункции у лиц с гипермобильным синдромом.
Из клинически значимых нарушений функции щитовидной железы при гипермобильном синдроме верифицированы гипотиреоз на фоне аутоиммунного тиреоидита и гипертиреоидные варианты болезни Грейвса-Базедова. Развернутая клиническая картина тиреоидита Хашимото, с развитием манифестного или субклинического гипотиреоза у иммуннокомпетентных лиц, отмечена в 11,25% наблюдений (р>0,05). Значимость гипотиреоза при СГМС объясняется утратой ингибирующих влияний на синтез фибробластами гиалуронатов, фибронектина и других структур коллагена; под действием тиреоидных гормонов тормозятся процессы синтеза фибробластами кожи гликозаминогликанов и коллагена. При гипотиреозе снижение уровней тиронинов ведет к активации данных синтетических процессов и развитию микседемы. Представляется интересным, что фибробласты лиц с синдромом Марфана также синтезируют повышенные количества гликозаминогликанов и коллагена с формированием состояний подобных гипотиреоидному тканевому муцинозному отеку [3]. Кроме того, геномные влияния, относящиеся к физиологическим эффектам Т3, модулируют состояние скелетной мускулатуры, включая периартикулярные мышцы. В плане костного обмена ТТГ способен оказывать непосредственное влияние на остеобластогенез и тормозить пролиферацию остеокластов, а это лежит в основе увеличения плотности костей при гипотиреозе.
В случаях выявленного гипотиреоза, включая субклинические его варианты, с учетом молодого возраста пациентов была назначена стандартная заместительная терапия Левотироксином.
Значимость персистирующего манифестного и субклинического эндогенного тиреотоксикоза для костно-метаболического статуса состоит в их отрицательном воздействии на качество кости в виду массивной периферической конверсии нативных гормонов щитовидной железы под действием тканевых дейодиназ с высокой активностью костно-резорбтивных процессов. Болезнь Грейвса, как причина тиреотоксикоза, зарегистрирована у 2 (2,5%) пациентов с СГМС, что соответствует популяционной распространенности нозологии [5]. Очевидно, тиреотоксикоз при гипермобильном синдроме не может рассматриваться в качестве сугубо специфического фактора, ухудшающего качественные характеристики костной ткани и способствующего нарушению процессов костного метаболизма.
Установление особенностей системной и многофакторной регуляции костного обмена с определением самостоятельного значения дисфункции пермиссивных гормональных систем расширяют представления о патогенезе формирования остеопенических нарушений у пациентов с СГМС и механизмах дисрегуляции костно-хрящевого ремоделирования при дисплазии соединительной ткани.
Заключение. Таким образом, проведенное исследование установило повышенный риск развития гипотироксинемии, аутоиммунных тиреопатий при гипермобильном синдроме. Это диктует необходимость целенаправленной диагностики нарушений функции щитовидной железы и применения активных стратегий индивидуальной нутритивной йодпрофилактики у молодых пациентов с СГМС.
Список литературы/ References
- Белая, Ж. Е. Современные представления о действии тиреоидных гормонов и тиреотропного гормона на костную ткань / Ж.Е. Белая, Л. Я. Рожинская, Г. А. Мельниченко // Проблемы эндокринологии – 2006. – Т. 52. –№ 2. С. 48–54.
- Лесняк О.М. Остеопороз / Под ред. О.М. Лесняк, Л.И. Беневоленской. 2-е изд. М.: ГЭОТАР-Медиа, 2012. 272 с.
- Муджикова, О.М. Соединительная ткань, соматотип и щитовидная железа / О.М. Муджикова, Ю.И. Строев, Л.П. Чурилов // Вестник Санкт-Петербургского университета.- 2009.- № 2 (11). – С. 35-46.
- Национальные рекомендации Российского научного медицинского общества терапевтов по диагностике, лечению и реабилитации пациентов с дисплазиями соединительной ткани // Медицинский вестник Северного Кавказа. –- № 1 (11). – С. 2-76.
- Петунина, Н. А. Болезни щитовидной железы: рук./ Н.А. Петунина, Л.В. Трухина – М.: ГЭОТАР-Медиа, 2011 – 216 с.
- Фадеев, В.В. По материалам клинических рекомендаций по диагностике и лечению заболеваний щитовидной железы во время беременности и в послеродовом периоде американской тиреоидной ассоциации / В.В. Фадеев // Клиническая и экспериментальная тиреоидология.- 2012.- №1 (8).- С. 7-18.
- Levine, M.A. Normal mineral homeostasis. Interplay of parathyroid hormone and vitamin D/ M.A. Levine // Endo Dev. ––Vol. 6. – Р. 14.
- Zhang, J. The mechanism of action of thyroid hormones / Zhang, J., Lazer M. A. //Ann. Rev. Physiol. – 2000. Vol. 62. – Р. 439–466.
Список литературы на английском языке / References in English
- Belaya Zh.E. Sovremennye predstavleniya o deystvii tireoidnyh gormonov i tireotropnogo gormona na kostnuyu tkan [Modern views on the action of thyroid hormones and thyroid stimulating hormone to bone tissue] / Zh.E. Belaya, L.Ya. Rozhinskaya, G.A. Melnichenko// Problemy endokrinologyi [The Problems of Endocrinology]. – 2006.- №2 (52).- P. 48–54. [in Russian]
- Lesnyak O.M. Osteoporoz. 2-e izd. [Osteoporosis. 2nd edition] / O.M. Lesnyak, L.I. Benevolenskoja /Moskva: GEOTAR-Media.- 2012.- 272 p.
- Mudzhikova O.M., Stroev Yu.I., Churilov L.P. Soyedinitelnaya tkan, somatotip i schitovidnaya zheleza. [Connective tissue, somatotype and thyroid gland]/ Vestnik Sankt-Peterburgskogo Universiteta – [Bulletin of St. Petersburg State University]. – - №2(11).-P. 35-46. [in Russian]
- Natsionalnye rekomendatsii Rossiyskogo nauchnogo meditsinskogo obschestva terapevtov po diagnostike, lecheniyu i reabilitatsii patsientov s displasiyami soyedinitelnoy tkani. [National recommendations of the Russian scientific society of internal medicine for diagnostics, treatment and rehabilitation of patients with connective tissue dysplasia] // Meditsinskiy Vestnik Severnogo Kavkaza. [Medical News of North Caucasus]. - 2016.- № 1 (11).- P 2-76. [in Russian]
- Petunina N.A. Bolesni schitovidnoy zhelezy. [Thyroid diseases]/ N.A.Petunina, L.V. Trukhina / Moskva: GEOTAR-Media.- 2011.- 216 p. [in Russian]
- Fadeev V.V. Po materialam klinicheskih rekomendacij po diagnostike i lecheniyu zabolevanij shchitovidnoj zhelezy vo vremya beremennosti i v poslerodovom periode amerikanskoj tireoidnoj associacii. [Guidelines of the American Thyroid Association for the Diagnosis and Management of Thyroid Disease During Pregnancy and Postpartum]/ V.V. Fadeev // Klinicheskaya i ehksperimental'naya tireoidologiya. [Clinical and Experimental Thyroidology]. 2012.- № 1 (8): P. 7-18. [in Russian]
- Levine, M.A. Normal mineral homeostasis. Interplay of parathyroid hormone and vitamin D/ M.A. Levine // Endo Dev. ––Vol. 6. – Р. 14. [in English]
- Zhang, J. The mechanism of action of thyroid hormones / Zhang, J., Lazer M. A. //Ann. Rev. Physiol. – 2000. Vol. 62. – Р. 439–466. [in English]
