ЭНДОГЕННАЯ И ЭКЗОГЕННАЯ РЕГУЛЯЦИЯ МИКРОРАЗМНОЖЕНИЯ ЧЕРЕШНИ
Корнацкий С.А.
Доцент, кандидат сельскохозяйственных наук, Российский университет дружбы народов
ЭНДОГЕННАЯ И ЭКЗОГЕННАЯ РЕГУЛЯЦИЯ МИКРОРАЗМНОЖЕНИЯ ЧЕРЕШНИ
Аннотация
Обсуждаются проблемы выращивания черешни в нетрадиционных зонах возделывания культуры. Рассматриваются приемы получения корнесобственных растений черешни с использованием метода in vitro и предлагается технология доращивания микрорастений с моделированием периода покоя.
Ключевые слова: черешня, клональное микроразмножение, растительные гормоны, корнесобственная культура.
Kornatskiy S.A.
Associate Professor, PhD in Agriculture, Russian Peoples' Friendship University
ENDOGENOUS AND EXOGENOUS REGULATION OF MICROPROPAGATION SWEET CHERRIES
Abstract
The problems of growing sweet cherries in non-traditional areas of cultivation culture are discussed. Methods for the own-rooted plants with cherries by in vitro are considered and technology of microplants rearing with modeling dormancy period is proposed..
Keywords: sweet cherry, micropropagation, plant hormones, own rooted culture.
Черешня как плодовая культура чрезвычайно популярна за счет ранней сезонной продукции с высокими вкусовыми качествами. Общепризнанно, что культура это южная, однако ситуация с ареалом распространения ее достаточно сильно изменилась в последнее время. Результативная селекционная работа позволила создать ряд сортов, которые удалось районировать даже в Нечерноземье - зоне с весьма суровыми, в отдельные годы, климатическими условиями.
Основой создания продуктивных черешневых насаждений, безусловно, является качественный посадочный материал. И, наиболее очевидная проблема в средней полосе России в этой связи – отсутствие высоко технологичного подвоя, который в питомнике давал бы выровненные рослые сеянцы, обеспечивающие высокий выход качественных саженцев. Поэтому в качестве подвоев с разной степенью успешности используют сеянцы культурных сортов черешни, сеянцы сильнорослых сортов вишни и сильнорослые клоновые подвои.
В то же время существует еще один вариант получения саженцев черешни – вегетативное размножение. Корнесобственная культура косточковых растений известна достаточно давно на примере вишни и сливы, технологически процесс детально прорабатывался в отечественной практике в середине прошлого века [1]. Однако, низкая укореняемость зеленых черенков не позволила тогда решить вопрос выращивания корнесобственного материала черешни. С разработкой принципиально нового метода вегетативного размножения – клонального микроразмножения ситуация коренным образом изменилась.
Начало работ по клональному микроразмножению черешни положено в лаборатории культуры тканей ВСТИСП (п. Измайлово, Московская обл.) в 2001-2004 годах и продолжено в биотехнологической лаборатории аграрного факультета РУДН (г. Москва) в 2012-2015 годах.
Целью изучения был подбор уровней и соотношений экзогенных и эндогенных факторов культивирования, обеспечивающих эффективную пролиферацию культур и получение растений-регенерантов in vitro.
В качестве объектов исследований использовали сорта селекции ВСТИСП – Фатеж, Чермашная и селекции ВНИИЛ - Ревна. Для культивирования применяли питательную среду Murashige и Skoog (1962). Поверхностная стерилизация исходного материала обеспечивалась 0,1%-ным раствором сулемы или 1%-ным раствором азотнокислого серебра. Введение в культуру проводили в марте, после пробуждения вегетативных почек на однолетних ветвях, прошедших период покоя. На этапе пролиферации в питательную среду добавляли 6-бензиламинопурин (6-БАП) в концентрации 1,0-2,0 мг/л, для укоренения микропобегов - β–индолилмасляную кислоту (ИМК) в концентрации 0,5-1,0 мг/л и β–индолилуксусную кислоту (ИУК) в концентрации 1,0-1,5 мг/л. Перед укоренением проводили элонгацию побегов на среде с содержанием 6-БАП 0,05 – 0,1 мг/л. При высадке микрорастений на адаптацию использовали автоклавированный субстрат на основе торфа. Культивационные сосуды (пробирки, колбы) с растениями помещали в культуральную комнату с заданным режимом (интенсивность освещения 5,0–6,5 клк, 16 часовой фотопериод и температура 24±1ºС).
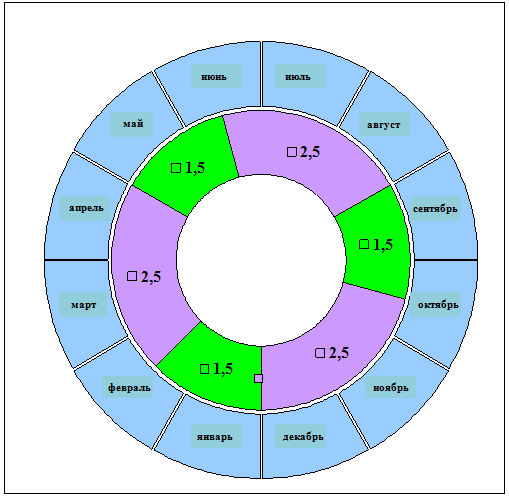
Введение в культуру проходило достаточно стандартно, сходно вишней. Наиболее успешным оказалось введение в культуру сорта Фатеж по числу продолживших развитие эксплантов. Выпады эксплантов отмечали по разным причинам, включая развитие скрытой патогенной микрофлоры, в пределах 10-30%. Из них удалось получить устойчиво пролиферирующие культуры. Конгломераты почек и побегов сорта Фатеж после 6-го пассажа были пересажены на среду для элонгации, что позволило через месяц получить достаточное количество микропобегов длиной 2,5-3,5 см, которые отбирали для укоренения. Лучшие результаты по укоренению микропобегов были получены при использовании ИМК в концентрации 1,0 мг/л и при использовании ИУК в концентрации 1,5 мг/л. Укореняемость составила 64,7% и 66,1% соответственно, но развитие корневой системы не имело какого-либо единообразия и в конечном итоге не играло существенной роли в приживаемости растений. Все укорененные растения были высажены на адаптацию по схеме, отработанной ранее с вишней. Использование автоклавированного субстрата и индивидуальный подход к каждому растению позволили обеспечить 100%-ный выход адаптированных растений. В ходе адаптации, по мере развития корневой системы растений в объеме субстрата, отмечался рост их надземной части, который составил в пределах 2,7 - 3,4 см. Спустя 6 нед. после высадки микрорастений на адаптацию рост окончательно прекратился и растения впали в состояние, аналогичное состоянию покоя в естественных условиях. Наиболее встречаемой рекомендацией в литературе является приурочивание адаптации микрорастений к началу вегетационного периода в естественных условиях. Доращивание растений до размеров, позволяющих высадить их на постоянное место, таким образом, затягивается на 2 года, что в совокупности с потерями растений значительно снижает эффективность процесса размножения. Учитывая эти обстоятельства, нами была разработана схема адаптации микрорастений и первичного их доращивания, позволяющая обеспечить практически полную сохранность растительного материала и сокращение на год доращивания растений, полученных in vitro, которая успешно была применена при получении корнесобственных растений черешни [ 2 ]. Руководствуясь оптимальными для прохождения периода покоя температурами, адаптированые и закончившие рост растения, выдерживали в течение 2,5 месяцев в специально оборудованной камере. В январе растения возвратили в светокомнату, где через 2-3 дня у растений наблюдалось синхронное активное начало развития и последующий рост, что позволило получить у исходных 5-7 см растений прирост 20 - 30 см в течение 2-3 недель. Спустя месяц рост снова замедлился и растениям повторно моделировали условия периода покоя до конца апреля, практически до момента, когда их можно было высадить в открытый грунт. Использование данной схемы позволило вырастить полученные микрорастения черешни до высоты 70-110 см уже в первую вегетацию, то есть за 1 год (Рис.1).
Рис. 1 - Диаграмма соотнесения роста и покоя растений (в мес.) с календарными месяцами в году, ![]() - покой растений,
- покой растений, ![]() - рост растений
- рост растений
Литература
- Тарасенко, М.Т. Зеленое черенкование садовых и лесных культур/ М.Т. Тарасенко // М. Изд. МСХА. - 1991. - 272 с.
- Корнацкий, С.А. Особенности получения и возможности использования корнесобственной черешни / С.А. Корнацкий, В.В. Введенский// Вестник МичГау. - Мичуринск . – 2012. - 3. - с.74-77
References
- Tarasenko, M.T. Zelenoe cherenkovanie sadovyh i lesnyh kul'tur/ M.T. Tarasenko // M. Izd. - 1991. - 272 s.
- Kornatskiy, S.A. Osobennosti poluchenija i vozmozhnosti ispol'zovanija kornesobstvennoj chereshni / S.A. Kornatskiy, V.V. Vvedenskiy// Vestnik MichGau. - Michurinsk . – 2012. - 3. - s.74-77