ЭКСПРЕСС-ОЦЕНКА КАЧЕСТВА МЁДА С ПОМОЩЬЮ ХЕМИЛЮМИНЕСЦЕНТНОГО АНАЛИЗА
ЭКСПРЕСС-ОЦЕНКА КАЧЕСТВА МЁДА С ПОМОЩЬЮ ХЕМИЛЮМИНЕСЦЕНТНОГО АНАЛИЗА
Научная статья
Лесовская М.И. 1,*, Игошин А.С.2
1, 2 Красноярский государственный аграрный университет, Красноярск, Россия
* Корреспондирующий автор: (lesmari[at]rambler.ru)
АннотацияС помощью хемилюминесцентного (ХЛ) анализа выявлены достоверные различия между образцами натурального мёда с гарантированным качеством и обезличенными образцами из торговой сети. Образцы натурального мёда проявляли однотипные антиоксидантные свойства в умеренной степени, снижение продукции свободных радикалов относительно контроля не превышало 20–40%. Образцы из торговой сети обладали либо прооксидантными свойствами, либо аномально высокой антиоксидантной активностью. Результаты ХЛ-анализа хорошо согласовались с данными традиционного лабораторного исследования и имели преимущества в скорости, наглядности и воспроизводимости.
Ключевые слова: мёд, качество, фальсификация, свободные радикалы, антиоксиданты, прооксиданты, хемилюминесценция.
RAPID HONEY QUALITY CONTROL BY MEANS OF CHEMILUMINESCENT ANALYSIS
Research article
Lesovskaia M. I. 1,*, Igoshin A. S.2
1, 2 Krasnoyarsk State Agrarian University, Krasnoyarsk, Russia
* Corresponding author: (lesmari[at]rambler.ru)
AbstractThrough chemiluminescent analysis, a significant difference was found between the samples of pure honey of guaranteed quality and de-identified samples taken from distributing facilities. The samples of pure honey demonstrated same-type anti-oxidant character moderately, decrease in producing the free radicals in comparison with the control group was no more than 20–40%. The samples taken from distributing facilities demonstrated either pro-oxidant character or abnormally high anti-oxidant activity. The results of chemiluminescent analysis comply with the data obtained through traditional laboratory analysis, and got the advantage of speed, being illustrative, and repeatability.
Keywords: honey, quality, falsification, free radicals, anti-oxidant, pro-oxidant, chemiluminescence.
ВведениеМёд занимает уникальное положение в ряду природных нутриентов как продукт животного происхождения, созданный без антропогенных технологий, посредством пчелиных биофабрик. Помимо натуральных моносахаридов, в его составе содержатся многочисленные биологически активные соединения (водорастворимые витамины, минеральные компоненты, органические кислоты, гликозиды, биофлавоноиды, ферменты, короткоцепочечные пептиды с гормональными эффектами и др.), которые в подобном сочетании и компонентном соотношении не встречаются ни в каком другом природном субстрате [1]. Несмотря на химическое разнообразие, все эти компоненты объединены общей функциональной способностью регулировать скорость и направленность протекания окислительно-восстановительных процессов [2]. Данные процессы лежат в основе поддержания гомеостаза на всех уровнях биологической организации. При этом процессы с участием молекулярного кислорода включают стадии, связанные с образованием свободных радикалов. Нарушение равновесия их образования и элиминации, т.е. редокс-баланса, является ключевой причиной нарушения нормального метаболизма клеток и тканей, а следовательно, включает механизмы патогенеза [3].
Показано, что полиморфные природные комплексы биологически активных компонентов в зависимости от условий способны стимулировать или тормозить продукцию свободных радикалов [4, с. 31]. Поэтому можно предположить, что сортозависимые сочетания большого числа компонентов в составе мёда, в зависимости от биохимических условий стимулирующих или тормозящих продукцию свободных радикалов, формируют антиоксидантную или прооксидантную способность данного вида мёда в целом. Оценка такой способности является необходимым компонентом интегральной биологической ценности данного продукта.
В соответствии с действующим ГОСТ 19792-2017, биологическую ценность мёда определяют в рамках полипараметрического подхода, когда состав и содержание химических компонентов определяют по отдельности (сахароза, редуцирующие сахара, свободная кислотность и др.) [5]. Данный подход, как и органолептический анализ, не позволяет судить о функциональной активности мёда в отношении свободных радикалов. В то же время именно этот параметр необходим для определения биологической ценности мёда для выявления фальсификатов, число которых в торговой сети беспрепятственно увеличивается при отсутствии надёжных инструментальных методов контроля качества.
Таким образом, актуальной проблемой является поиск экспрессных информативных методов определения качества мёда, выявления и отбраковки фальсификатов. Решение данной проблемы может быть осуществлено с использованием хемилюминесцентного (ХЛ) анализа. Принцип метода состоит в оценке изменения уровня продукции свободных радикалов в ходе реакции Фентона, сущность которой заключается в распаде пероксида водорода под влиянием ионов Fe2+ [6]. В присутствии люминола C8H7N3O2 химическая энергия цепной реакции преобразуется в энергию световых квантов, подсчёт которых производится с помощью биохемилюминометра. Исходная гипотеза заключалась в том, что с помощью хемилюминесцентного анализа скрининг образцов мёда для выявления фальсификатов можно проводить намного эффективнее с получением воспроизводимых результатов.
Целью настоящей работы было сопоставление двух методических подходов (традиционный полипараметрический и инновационный монопараметрический) для определения информативности хемилюминесцентного метода при экспресс-оценке качества мёда.
Объекты и методы исследования
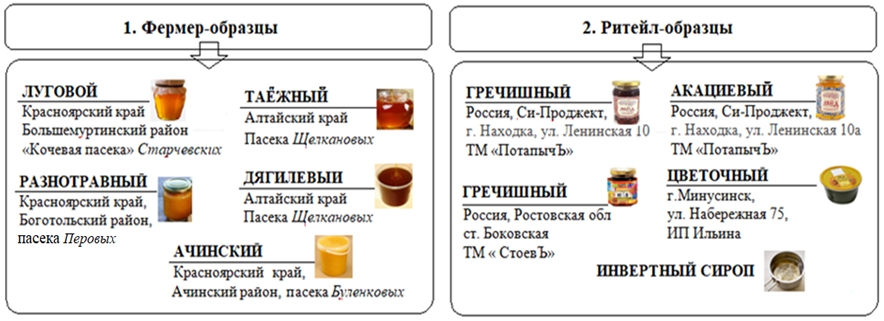
Объектами исследования были две группы образцов мёда (рис. 1). Первая группа включала пять образцов фермерского мёда от индивидуальных производителей. Натуральное происхождение и качество этих сортов было гарантировано поручительством конкретных пасечников. Вторая группа объединяла четыре образца, приобретённых в торговой сети (ритейл-образцы), качество которых не было надёжно гарантировано. Кроме того, в эту группу в качестве «нулевого контроля» был включён инвертный сироп, приготовленный общеизвестным способом из сахарозы с добавлением лимонной кислоты [7].
В рамках полипараметрического подхода в соответствии с действующим ГОСТ 19792-2017 определяли суммарный уровень органических кислот (активная кислотность) методом кислотно-щелочного титрования; содержание сахарозы – методом рефрактометрии; общий белок – биуретовым методом; уровень аскорбиновой кислоты методом колориметрии по реакции с метиленовым синим; суммарное количество восстановителей – методом перманганатометрического титрования [8].
Рис. 1 – Характеристика исследуемых образцов
Для определения суммарного количества антиоксидантов или прооксидантов использовали хемилюминесцентный анализ, который проводили с использованием РС-управляемого биохемилюминометра БХЛМ-3606. Методика исследования описана [9]. Реакционную модельную смесь, в которой проходила генерация свободных радикалов, получали соединением 100 мкл пероксида водорода, 150 мкл люминола, 50 мкл сульфата железа (добавляли непосредственно перед началом измерения). В смесь вносили 100 мкл 3%-ного раствора тестируемого образца мёда в дистиллированной воде, в контроле – равное количество дистиллированной воды. При проведении ХЛ-анализа фиксировали параметры: высока пика (I, имп/с), площадь под кинетической кривой (S, тыс.имп.). Продолжительность записи кинетики в каждой повторности составляло 480 с, каждое измерение проводили не менее чем в трёх повторностях. Массив полученных данных проверяли на соответствие закону нормального распределения и равенства дисперсий независимых выборок. Для оценки достоверности межвыборочных различий результаты обрабатывали статистически с использованием t-критерия Стьюдента. Различия принимались значимыми при р<0,05.
Результаты и их обсуждение
Результаты измерения кислотных компонентов в каждой группе образцов отображены на рис. 2; на рис. 2а показано содержание суммы органических кислот (активная кислотность), на рис. 2б – уровень аскорбиновой кислоты, выполняющей специфичные функции в регуляции редокс-баланса. Из приведённых результатов видно, что значения в группе ритейл-образцов оказались выше как по уровню общей кислотности (p<0,05), так и по индивидуальному содержанию витамина С.
Рис. 2 – Содержание органических кислот и витамина С в фермерских и ритейл-образцах мёда
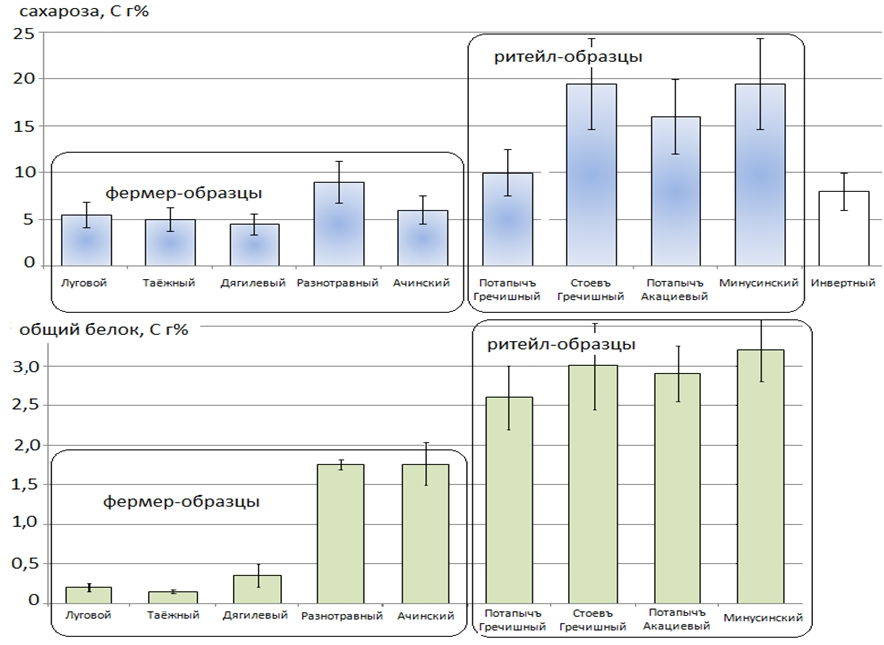
Ещё более выраженные межгрупповые различия были выявлены по уровням сахарозы и пептидов (рис. 3).Рис. 3 – Содержание сахарозы и общего белка в фермерских и ритейл-образцах мёда
Из приведённых результатов видно, что в ритейл-образцах достоверно выше содержание сахарозы и белковых соединений, что вполне согласуется с имеющимися данными о наиболее распространённых способах фальсификации мёда, направляемого в торговую сеть, к которым относится замещение части продукта, в частности, инвертным сиропом и мучной суспензией или сывороткой [10]. Повышенное содержание сахарозы в составе мёда может быть следствием нарушения технологии пчеловодства (незрелый мёд; искусственные подкормки пчёл и т.д.) Общим результатом при этом будет снижение пищевой и биологической ценности мёда, т.е. потеря природного качества продукта.
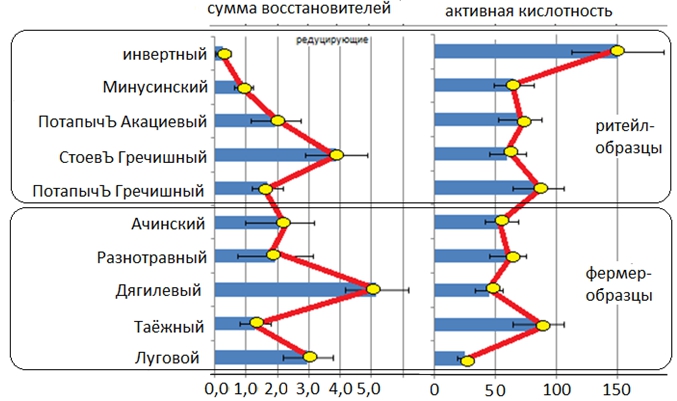
На рис. 4 показаны результаты определения суммы редуцирующих соединений в составе анализируемых образцов.
Рис. 4 – Содержание восстановителей и кислотных эквивалентов в фермерских и ритейл-образцах мёда
В перманганатометрическом определении восстановителей использовали тирование сильным окислителем, а в описанном выше ацидиметрическом (при определении активной кислотности) – титрование сильным основанием. Поэтому результаты, полученные в этих определениях, должны комплементарно соответствовать друг другу. Действительно, высокому содержанию кислотных эквивалентов соответствововало низкое содержание восстановителей, и наоборот. Полученные результаты подтвердили методическую валидность проведённых измерений. В то же время выявление подобных фильсификаций в производственной практике представляет реальные трудности, будучи связаным с лабораторными исследованиями, затратами времени и дополнительными издержками, что делает экономически невыгодным выявление фальсификатов с помощью лабораторной аналитики.
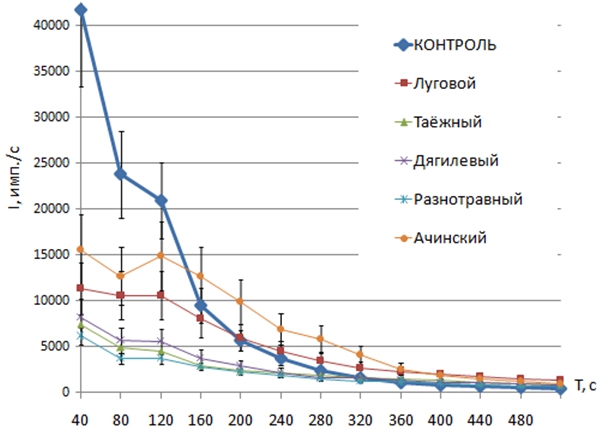
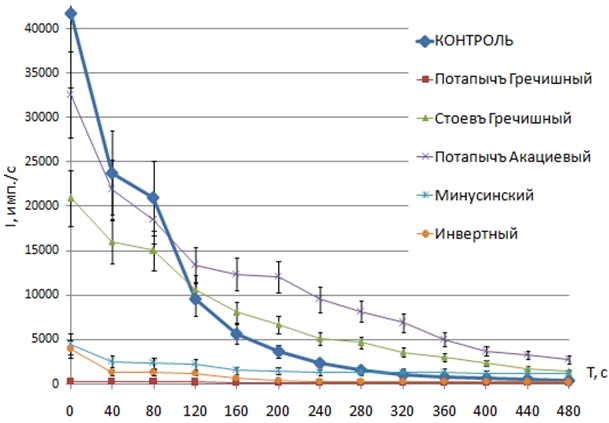
Выявление фальсифицированных образцов может быть ускорено и упрощено с помощью хемилюминесцентного анализа, результаты которого приведены на рис. 5–7. Суммарному содержанию антиоксидантов в исследуемом материале соответствует величина снижения уровня свободных радикалов относительно контроля на кинетических кривых (рис. 5, 6) и на гистограмме, отображающей светосумму за время наблюдения процесса (рис. 7).
Рис. 5 – Снижение продукции свободных радикалов под влиянием фермер-образцов мёда
Рис. 6 – Снижение продукции свободных радикалов под влиянием ритейл-образцов мёда и инвертного сиропа
Из рис. 5 и 6 видно, что в контроле, где реакционная среда не содержит антиоксидантов, торможение продукции свободных радикалов происходит с максимальной скоростью. При этом элиминация частиц идёт по самому простому механизму – рекомбинация и деактивация [11]. В присутствии тестируемых образцов характер кинетики усложняется в связи с внесением в реакционную среду комплекса органических соединений, способных регулировать скорость редокс-процесса с помощью различных механизмов. По высоте пика, светосумме и общему профилю кинетики можно судить о суммарном содержании антиоксидантов либо прооксидантов в образце, а также о доминирующем способе регулирования цепных процессов.
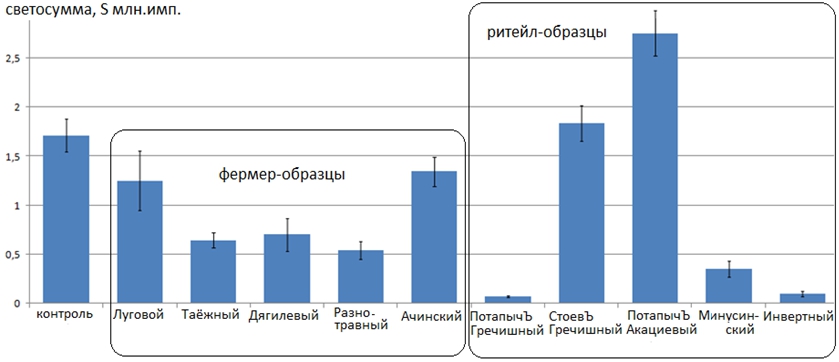
Рис. 7 – Снижение светосуммы хемилюминесценции под влиянием образцов мёда и инвертного сиропа
На рис. 7 отображены результаты измерения светосуммы под влиянием фермер-образцов, в присутствии которых продукция свободных радикалов однонаправленно снижалась, хотя и в различной степени. Так, наименьшим содержанием антиоксидантов характеризовались «Ачинский» и «Луговой» (снижение светосуммы относительно контроля на 26 и 21%, соответственно). У остальных образцов натурального мёда выявлено высокое содержание антиоксидантов, снижение светосуммы относительно контроля составило 62, 59 и 68%, соответственно. Наиболее высоким уровнем антиоксидантов среди них характеризовался мёд «Разнотравный». Судя по характеру кинетограмм, в составе этих образцов содержатся антиоксиданты однонаправленного механизма действия, тогда как в составе «Ачинского» и «Лугового» присутствуют регуляторы-антагонисты. Так, мёд «Луговой» характеризовался высоким содержанием не только аскорбиновой кислоты, но и ионов железа, под влиянием которого аскорбиновая кислота быстро теряет свои восстановительные свойства. Мёд «Ачинский» отличался от других образцов более высоким содержанием белковых соединений, которые переходят в состав мёда из цветочных субстратов в основном в виде ферментов-цитохромов. Их регуляторная способность имеет узкий функциональный интервал, чем, по-видимому, и объясняется невысокая антиоксидантная активность образца.
Результаты ХЛ-анализа ритейл-образцов значительно отличались от предыдущей группы и характеризовались контрастным внутригрупповым полиморфизмом. Так, у двух образцов («Потапов Акациевый», «СтоевЪ Гречишный») выявлены отчётливые прооксидантные свойства, т.к. под их влиянием продукция свободных радикалов возрастала на 60% и 7%, соответственно. У двух других образцов продукция свободных радикалов, напротив, снижалась до аномально низких значений, светосумма снизилась на 95% («ПотаповЪ Гречишный») и 80% («Минусинский»). На фоне уровня антиоксидантной активности у образцов натурального мёда с гарантированным качеством подобные пиковые значения у ритейл-образцов заставляют обоснованно сомневаться в их технологической чистоте.
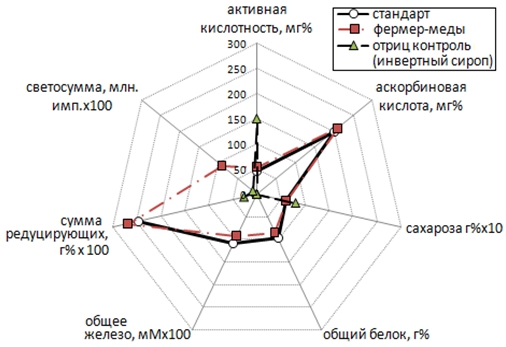
На рис. 8 и 9 приведены лепестковые диаграммы по каждой группе образцов, где результаты всех измерений, включая ХЛ-анализ, соединены общей линией (пунктир) и сопоставлены с усреднёнными справочными данными по составу натурального мёда (стандарт, сплошная линия).
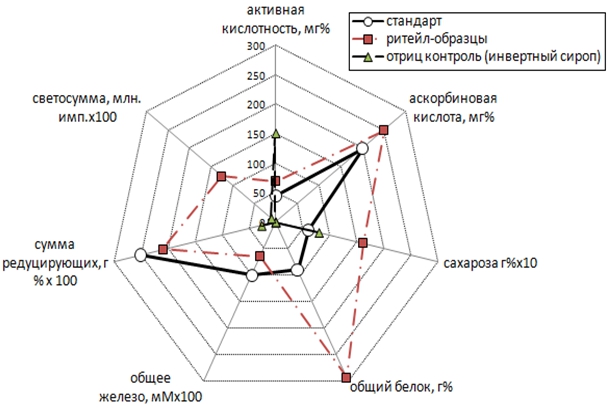
Рис. 8 – Содержание редокс-активных компонентов в образцах мёда (ритейл-образцы)
Рис. 9 – Содержание редокс-активных компонентов в образцах мёда (фермер-образцы)
Из рис. 8 видно, что ритейл-образцы не выдерживают сравнения со стандартом, максимальное расхождение наблюдается по величинам общего белка и сахарозы. Напротив, в группе фермер-образцов со стандартом совпали результаты всех проведённых традиционных измерений (рис. 9), с которыми хорошо согласовались данные ХЛ-анализа. Можно заключить, что ХЛ-анализ является весьма перспективным методом для первичного скрининга образцов мёда с негарантированным качеством, в первую очередь по признаку технологической фальсификации. При этом длительность анализа составляет считанные минуты; используемые реагенты легкодоступны и нетоксичны; результаты предъявляются в легко читаемом виде, не требующем длительного анализа.
ЗаключениеТаким образом, ХЛ-анализ пригоден для распознавания образцов мёда с негарантированным качеством. Единственным маркёрным признаком при этом является направленность и диапазон влияния на продукцию свободных радикалов. Длительность проведения анализа исчисляется минутами; число одновременно измеряемых проб – десятками экземляров; воспроизводимость результатов обеспечивается в максимальной степени; для получения критерия оценки качества не требуется суммировать множественные разнородные показатели, единым критерием является антиоксидантная (или прооксидантная) активность. Данный показатель по своей природе является интегральным и результирует большое число разнонаправленных редокс-процессов.
| Благодарности Авторы выражают благодарность фермерам, предоставившим для исследования образцы натурального мёда с собственных пасек. | Acknowledgement The authors thank the farmers who provided samples of natural honey from their own apiaries for research. |
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Корпачев В.В. Целебная фауна /В.В. Корпачев/. М.: Наука, 1989. – 204 с.
- Макарова Н.В. Антиоксидантные вещества различных сортов мёда / Н.В. Макарова, В.С. Лиманова, В.П. Бординова // Известия вузов. Пищевая технология. – 2011. – №1. – С. 18–20.
- Владимиров Ю.А. Свободные радикалы и клеточная хемилюминесценция / Ю.А. Владимиров, Е.В. Проскурина // Успехи биологической химии. – 2009. – Т. 49. – С. 341–388.
- Лесовская М.И. Методические проблемы тестирования биологической активности нутриентов / М.И. Лесовская / В кн.: Влияние нутриентов на свободнорадикальный баланс крови in vitro. – М., 2015. – 94 с.
- ГОСТ 19792-2017. Мёд натуральный. Технические условия (с поправкой): [Электронный ресурс] http://docs.cntd.ru/document/1200157439.
- Аристова Н.А. Механизмы хемилюминесценции в реакции Фентона / Н.А. Аристова, И.П. Иванова, С.В. Трофимова, И.М. Пискарёв, О.Е. Бурхина, О.О. Сошникова // Исследовано в России: электронный научный журнал. – 909 http://zhurnal.ape.relarn.ru/articles/2011/067.pdf
- Матов В.А. Способ производства инвертного сиропа. RU2188869 C1 /В.А. Матов, З.Г. Скобельская, В.А. Васькина, А.И. Драгилев, В.А. Алымов, А.В. Куров / Опубл. 09.10
- Васильев В.П. Аналитическая химия в 2-х томах, том 2. Физико-химические методы анализа /В.П. Васильев /– Москва: Дрофа, 2004. – 384 с.
- Хасанов В.В. Методы исследования антиоксидантов /В.В. Хасанов, Г.Л. Рыжова, Е.В. Мальцева // Химия растительного сырья. – №3. – С. 63–75.
- Фальсификация меда: виды, способы и методы определения: [Электронный ресурс] / FB.ru: https://fb.ru/article/380586/falsifikatsiya-meda-vidyi-sposobyi-i-metodyi-opredeleniya
- Денисов Е.Т. Физико-химические аспекты изомеризации свободных радикалов /Е.Т. Денисов, Т.Г. Денисова // Усп. хим., 2004. – Т. 73. – Вып. 11. – С 1181–1209.
Список литературы на английском языке / References in English
- Korpachev V.V. Celebnaya fauna [Healing fauna] /V.V. Korpachev / – М.: Nauka, 1989. – 204 p. [in Russian]
- Makarova N.В. Antioxidantniye veschestva razlichnich ssortov meda [Antioxidant substances of various varieties of honey] / N.В. Маkarova, V.S. Limanova, V.P. Bordinova // Isvestiya vuzov. Pichevaya technologia [University News. Food technology]. – 2011. – №1. – P. 18–20. [in Russian]
- Vladimirov Y.A. Svobodnie radikali I kletochnaya chemiluminescencia [Free radicals and cell chemiluminescence ]/ Y.А. Vladimirov, Е.V. Proskurina // Usrechi Biologichescoj Chimii [Advances in Biological Chemistry]. – 2009. – Т. 49. – P. 341–388. [in Russian]
- Lesovskaya М.I. Metodicheskie problemi testirovanija biologicheskoi aktivnosti nutrientov [Methodological problems of testing the biological activity of nutrients] / М.L. Lesovskaya/ In.: Vliyanie nutrientov na svobodnoradikalniy balans krovi in vitro [The effect of nutrients on the free radical balance of blood in vitro]. – М., 2015. – 94 p. [in Russian]
- GОSТ 19792-2017. Med naturalnij. Technicheskie uslovia (s popravkoi) [Natural honey. Specifications (as amended)]: [Electronic resource] http://docs.cntd.ru/document/1200157439. [in Russian]
- Aristova N.А. Mechanizmi chemiluminescencii v reakcii Fentona [Mechanisms of chemiluminescence in the Fenton reaction] / N.А. Aristova, I.P. Ivanova, S.V. Тrofimova, I.М. Piskarjiev, О.Е. Burchina, О.О. Sochnikova // Issledovano v Rossii: electronnij nauchnij zhurnal [Investigated in Russia: an electronic scientific journal]. – 909 http://zhurnal.ape.relarn.ru/articles/2011/067.pdf [in Russian]
- Matov V.А. Sposob proizvodstva invertnogo siropa [Method for the production of invert syrup]. RU2188869 C1 / /V.A. Matov, Z.G. Skobelskaya, V.A. Vaskina, A.I. Dragilev, V.A. Alymov, A.V. Kurov / Publ. 2002.09.10 [in Russian]
- Vasiliev V.П. Analiticheskaya chimia v 2 tomah, tom 2. Phisiko-chimicheskie metodi Analisa [Analytical chemistry in 2 volumes, volume 2. Physical and chemical methods of analysis] /V.P. Vasiliev/– M.: Drofa, 2004. – 384 p. [in Russian]
- Hasanov V.V. Metodi issledovania antioxidantov [Antioxidant Research Methods] /V.V. Hasanov, G.L. Rizhova, Е.V. Maltzeva // Chimia rastitelnogo sirja растительного сырья [Chemistry of plant raw materials]. – 2004. – №3. – P. 63–75. [in Russian]
- Falsifikacia meda: vidi, sposobi i metodi opredelenia: [Electronnij resurs] [The falsification of honey: types, methods and methods of determination: [Electronic resource] ] / FB.ru: https://fb.ru/article/380586/falsifikatsiya-meda-vidyi-sposobyi-i-metodyi-opredeleniya [in Russian]
- Denisov Е.Т. Phiziko-chimicheskie aspect isomerizacii svobodnich radikalov [Physicochemical aspects of free radical isomerization] /Е.Т. Denisov, Т.G. Denisova// Uspehi chimii [Success of chemistry]. – 2004. – V. 73. – Issue 11. – P. 1181–1209. [in Russian]