Лобулярная капиллярная гемангиома кожного покрова: от патогенетических гипотез к совершенствованию диагностики и стратегии лечения (обзор литературы)
Лобулярная капиллярная гемангиома кожного покрова: от патогенетических гипотез к совершенствованию диагностики и стратегии лечения (обзор литературы)
Аннотация
Целью статьи является анализ источников литературы и изложение этиологических факторов, возможных патогенетических механизмов развития лобулярной капиллярной гемангиомы кожного покрова с обоснованием методов диагностики и обзором применяемых методов лечения. В связи с не до конца изученным этиопатогенезом создаются трудности для определения оптимальной лечебной тактики и профилактики возникновения осложнений. Лобулярная капиллярная гемангиома демонстрирует интенсивный рост в течение нескольких недель, для нее характерны отсутствие фаз стабилизации, спонтанной регрессии, отмечены кровотечение при минимальной травматизации и склонность к рецидивированию. Кровотечение возникает часто и в ряде случаев носит профузный характер, что является причиной обращения за неотложной медицинской помощью.
В ходе исследования проанализированы статьи в информационно-поисковых и электронных библиотечных базах данных PubMed, eLIBRARY, Google Scholar, специализированная литература с фокусом на педиатрических пациентов. Отмечено, что консервативные методы могут быть рассмотрены как терапия первой линии, при ограниченности других методов, с целью уменьшения объема последующего хирургического пособия и не применимы при осложнениях. Показано, что полнослойное хирургическое иссечение опухоли предоставляет материал для гистопатологического исследования, при этом не исключает рецидив и не дает достичь приемлемого косметического результата. В связи с развитием применения методов лазерной фотодеструкции, требуется проведение дальнейших исследований, направленных на минимизацию рецидива. Необходим точный подбор параметров воздействия луча, чтобы предотвратить избыточное термическое повреждение тканей, актуальными остаются риск рецидива, отсутствие надежного гемостаза при крупном питающем сосуде, гиперпигментация кожи. В заключении авторы указывают, что при выборе терапевтического подхода необходимо учитывать ангиоархитектонику лобулярной капиллярной гемангиомы; терапия должна быть направлена на устранение питающего базального сосуда.
1. Введение
Лобулярная капиллярная гемангиома (ЛКГ), или пиогенная гранулема, представляет собой приобретенную доброкачественную сосудистую опухоль согласно классификации Международного общества по изучению сосудистых аномалий (ISSVA, пересмотр 2025 г.). Характерными особенностями ЛКГ являются интенсивный рост в течение нескольких недель или месяцев, склонность к изъязвлению и кровотечение при минимальной травматизации .
На коже ЛКГ манифестирует в виде единичной плотной красно-багровой папулы или узла диаметром 0,5–1,0 см, имеет экзофитный тип роста в виде сидячей бляшки или образования на ножке с широким основанием. Преимущественная локализация — кожа головы, шеи, верхних конечностей и слизистые оболочки. У детей до 77% случаев ЛКГ обнаруживаются в области лица и шеи .
Данная опухоль диагностируется как у взрослых, так и в детском возрасте. В педиатрической практике на нее приходится порядка 0,5% всех кожных узлов и 5–10% сосудистых новообразований кожи. У детей средний возраст манифестации составляет 6–10 лет с преобладанием мальчиков , .
Несмотря на доброкачественный характер опухоли и отсутствия сообщений о малигнизации, ЛКГ демонстрирует отдельные признаки агрессивного поведения, а именно: интенсивный быстрый рост, отсутствие фаз стабилизации (плато), спонтанной регрессии, характерна склонность к рецидивированию. Согласно данным различных авторов, частота рецидивов составляет до 7,7% случаев на кожных покровах и до 15% – на слизистых оболочках. Другое осложнение, проявляющееся обильным кровотечением в связи с патологически расширенным сосудом в основании образования, встречается в 7,5–26% случаев. Кровотечение возникает часто при незначительной травматизации образования и в ряде случаев может быть профузным, что служит причиной обращения за неотложной медицинской помощью , .
2. Этиологические факторы
Потенциальными предрасполагающими факторами ЛКГ могут быть: травматическое повреждение, хроническое раздражение, повышенный уровень женских половых гормонов, инфекционные агенты, вирусные онкогены, а также наличие микроскопических артериовенозных анастомозов.
Несмотря на то, что травма рассматривается в качестве возможного триггерного фактора, анамнестические указания на возникновение ЛКГ в зоне травматического повреждения отмечают лишь у 7–25% пациентов. Тем не менее, при околоногтевой локализации локальная травма (например, острая механическая травма, неоднократные манипуляции с ногтевой пластиной) была зафиксирована в 58% случаев .
Предполагается, что женские половые гормоны усиливают экспрессию ангиогенных факторов, включая фактор роста эндотелия сосудов, основной фактор роста фибробластов и интерлейкин. Количество прогестерона и эстрогена значительно увеличивается во время беременности и, следовательно, может оказывать большее воздействие на эндотелий. Зафиксированы случаи разрешения патологии после родов. Однако, как указывается, количество рецепторов прогестерона и эстрогена не является регулирующим фактором в патогенезе этого заболевания .
Описаны случаи связи развития ЛКГ, ассоциированные с приемом определенных лекарственных препаратов при терапии иммунодефицитных состояний и неопластических процессов. Так, сообщается что околоногтевые пиогенные гранулемы могут развиваться через 2–12 месяцев после начала антиретровирусной терапии ламивудином или индинавиром. Однако окончательное улучшение обычно требует отмены вызывающего заболевание препарата . Помимо этого, имеются клинические наблюдения возникновения пиогенной гранулемы у пациентов с меланомой после начала таргетной и иммунной терапии селективными ингибиторами BRAF (вемурафениб, энкорафениб, даброфиниб) и как результат токсических эффектов, вызванных ингибиторами MEK . Также описаны случаи развития пиогенной гранулемы полости рта и кожи у пациентов после трансплантации почки, в том числе у подростка 14 лет, получавших иммуносупрессивную терапию циклоспорином и такролимусом .
Сообщается о развитии околоногтевых пиогенных гранулем у подростков, получающих терапию системным изотретиноином по поводу акне .
Существует предположение, что ЛКГ может формироваться как реакция тканей на незначительную травму и/или хроническое раздражение, что потенциально может способствовать инвазии неспецифических микроорганизмов, несмотря на редкое их выявление в очаге поражения. Согласно данным, у части пациентов с пиогенной гранулемой были идентифицированы дерматотропный парапоксвирус (вирус контагиозного пустулезного дерматита, Orf-вирус) и вирус папилломы человека 2-го типа (ВПЧ-2) . Было высказано предположение, что ангиопоэтины и эфрин B2 в других сосудистых опухолях и состояниях пролиферации сосудов, таких как Bartonella hanselae, Bartonella Quintana и вирус герпеса человека 8 типа (ВГЧ-8), играют роль в развитии рецидивирующих форм .
В литературе также представлены единичные сообщения о развитии пиогенной гранулемы после коронавирусной инфекции COVID-19 и вакцинации против данной инфекции , .
Дополнительными предрасполагающими факторами могут выступать уже существующие сосудистые мальформации .
3. Патогенез
Патогенез ЛКГ остается недостаточно изученным. Указывается роль дисбаланса между проангиогенными и антиангиогенными факторами. Причины активации ангиогенеза остаются невыясненными. Следует подчеркнуть, эндотелий представляет собой один из ключевых участков контроля апоптоза при повреждении сосудов и процесса ангиогенеза.
M.G.Blackwell et al. (2016) выявили в ткани пиогенной гранулемы маркеры эмбриональных стволовых клеток в эндотелиальных клетках, что предполагает васкулогенез de novo из примитивных стволовых клеток. Yüksel E. İ. et al. (2023) высказывают о роли сигнального пути Wnt1/β-катенин, активируемого макрофагами, в опухолевом ангиогенезе в эндотелиальных клетках сосудов. Считается, что ингибирование этого пути также ингибирует экспрессию факторов стволовых клеток .
Исследование методом полного экзомного секвенирования 40 очагов пиогенной гранулемы выявило соматические мутации гена HRAS в четырех образцах, что подтверждает вовлеченность сигнального пути RAS-MAPK в развитии данной патологии . Мутации RAS объясняются проангиогенным эффектом на эндотелиальные клетки. Мутации генов HRAS и BRAF также были обнаружены при спорадической кожной форме при исследовании 15 образцов у детей, что противоречит классификации пиогенной гранулемы как реактивной гиперплазии .
Установлено, что факторы роста фибробластов (FGFs) играют важную роль в процессах ангиогенеза, васкулогенеза и репарации, стимулируя миграцию, пролиферацию и дифференцировку клеток. FK.Yuan et al.(2000) подчеркнули роль усилителей ангиогенеза — фактора роста эндотелия сосудов (VEGF) и b-фактора роста фибробластов (bFGF) и ингибиторов ангиогенеза — тромбоспондина-1 (TSP-1) и ангиостатина в механизме воспалительного ангиогенеза. Факторы сосудистого морфогенеза — тирозинкиназа с иммуноглобулин-подобными и ЭФР-подобными доменами-2 (Tie-2), ангиопоэтин-1, ангиопоэтин-2, эфрин-B2 и эфрин-B4 — были обнаружены в состоянии повышенной регуляции в ткани пиогенной гранулемы полости рта по сравнению со здоровой десной . Помимо того, к факторам, участвующим в ангиогенезе и влияющим на скорость роста пиогенной гранулемы, относятся индуцибельная NO-синтетаза (iNOS), b-FGF, циклооксигеназа-2 (ЦОГ-2), интерлейкин-10 (ИЛ-10) . Также стоит отметить экспрессию iNOS и низкую скорость апоптоза регуляторных белков Bax/Bcl-2 в пиогенных гранулемах .
bFGF опосредует процессы неоваскуляризации посредством проангиогенных цитокинов, в первую очередь, VEGF. Уровень VEGF, патологически повышенный при злокачественных новообразованиях с целью стимуляции ангиогенеза и поддержания опухолевого роста, также возрастает при доброкачественных патологиях, включая пиогенную гранулему . Однако при разрешении пиогенной гранулемы, в том числе после проведения местной терапии, происходит нормализация уровня VEGF. В отличие от доброкачественных состояний, при злокачественных опухолях возникает необходимость в проведении системной анти-VEGF терапии для контроля прогрессирования заболевания .
Со своей стороны, медиатор тучных клеток — триптаза — индуцирует активацию фибробластов, отложение коллагена и фиброз. На начальной стадии поражения наблюдаются инфильтрация воспалительными клетками, сосудистая пролиферация, а также появление миофибробластов и коллагена III типа в ответ на повреждение и процессы репарации. По мере развития поражения соединительная ткань представляется плотно упакованными волокнами коллагена I типа при отсутствии воспалительной инфильтрации, а миофибробласты подвергаются редукции, что указывает на процесс заживления .
Гистологически ЛКГ представляет собой беспорядочные скопления сосудов артериального и венозного типов, содержащие многочисленные запустевающие и кавернозно расширенные сосудистые полости различных размеров и формы, расположенные среди фиброзированной стромы. Выраженность стромального окружения варьирует от тонких прослоек до обширных очагов плотной фиброзной ткани с высоким содержанием сульфатированных гликозамингликанов . Формируемая соединительнотканными перегородками структура ЛКГ приобретает дольчатый вид. В периферической части каждой подобной «дольки» располагается сосуд крупного диаметра с утолщенной склерозированной и, зачастую, гиалинизированной стенкой, формируя структуру «сосудистой ножки» .
4. Диагностика
Диагностика ЛКГ основывается на клинических данных. При «настораживающем» диагнозе необходимо проведение гистологического и иммуногистохимического исследований для исключения заболеваний, имеющих мимикрию с ЛКГ, что требует получения биопсийного материала.
Дерматоскопическое исследование позволяет визуализировать элементы ЛКГ при увеличении. Наличие красноватых бесструктурных участков наряду с пересекающимися толстыми белыми линиями и полосатое шелушение являются характерными признаками для данной опухоли .
При ультразвуковом исследовании ЛКГ визуализируется как четко отграниченное экзофитное гипоэхогенное неоднородное солидное образование, занимающее эпидермис и дерму, с эхоструктурой, отражающей дольчатое строение; при допплерографии обычно лоцируется подходящий к основанию образования единичный питающий сосуд, имеющий вертикальную линейную ориентацию. Отмечается, что сохранение данного сосуда при удалении опухоли может служить причиной рецидива , , .
В литературе обсуждается роль высокочастотного дерматологического ультразвукового исследования для дифференциации сосудистых аномалий. При этом существуют противоречия в описании ультразвуковой картины ЛКГ. Так, C.Gonzalez et al. (2024) описывают пиогенную гранулему как четко отграниченное, экзофитное или полиповидное гипоэхогенное образование с выраженным артериальным кровотоком, выявляемым при допплерографии . В отличие от этого, P.Pilat et al. (2019) характеризуют ее как гиперэхогенное образование, расположенное непосредственно под входной зоной дермы, с четкими ровными контурами, содержащее гиперэхогенные тяжи и пятна в структуре центральной части . T.Nozaki et al. (2013) также регистрируют гиперэхогенность образования и выявляют выраженный кровоток на цветовом допплеровском картировании . V.Cantisani et al. (2014) определяют пиогенную гранулему как плохо очерченное полидольчатое гипоэхогенное поражение с полидольчатыми краями с выраженной артериальной и венозной васкуляризацией и периферической кальцификацией . J.Prajapat et al. (2022) указывают, что для пиогенной гранулемы не характерны четкие границы, а при цветовом допплеровском картировании обнаруживаются рассеянные центральные и периферические сосудистые сигналы . Кроме того, A.Kikusawa et al.(2012), а также G.K.Lee et al.(2010) наряду с высокой васкуляризацией визуализировали расширенную питающую артерию , .
Таким образом, представленные данные свидетельствуют о необходимости стандартизации методики проведения и обеспечения качества дерматологических, ультразвуковых исследований.
5. Лечение
Выбор стратегии ведения пациентов с ЛКГ определяется индивидуальными характеристиками каждого случая. Описаны отдельные клинические наблюдения регресса кожных поражений у пациентов после отмены провоцирующей терапии, а также у беременных женщин после родоразрешения. Однако, в большинстве случаев, в связи с высокой частотой рецидивирующих кровотечений, трудно поддающихся контролю, ЛКГ требует лечения .
Консервативные методы лечения включают: использование бета-адреноблокаторов системно и местно в виде раствора, мази, крема, кортикостероидная терапия, использование имиквимода, крема алитретиноина, ингенола мебутата, нитрата серебра, фенола, прессотерапия и другие.
Эффективность бета-адреноблокаторов в отношении ЛКГ, в отличие от младенческой гемангиомы, выражена слабее, вероятной причиной этого является сниженная экспрессия бета-адренорецепторов на поверхности ЛКГ . Тем не менее, в литературе описаны случаи успешного применения неселективных антагонистов β-адренорецепторов, таких как тимолол (местно) и пропранолол (местно или системно).
Местная форма пропранолола используется в лечении пиогенной гранулемы в виде 1%, 4% мази, крема или геля. Имеются также сообщения о системном применении пропранолола в составе комбинированной терапии диссеминированной пиогенной гранулемы . В небольшом сравнительном исследовании (n=30, по 10 пациентов в группе) применение 1% пропранолола и 0,5% тимолола в форме крема дважды в день в течение двух месяцев продемонстрировало полный регресс поражения лишь в 30% случаев, при этом существенных различий между группами лечения отмечено не было .
Тимолола малеат в форме геля является наиболее распространённой для местного применения формой бета-адреноблокаторов, используемой как на коже, так и при пиогенных гранулемах конъюнктивы. Для кожных поражений повышение эффективности лечения может быть достигнуто за счёт применения окклюзионной терапии (гидроколлоидные повязки) и использования более высоких концентраций препарата. Однако, согласно данным Angela Filoni et al. (2021), такие подходы могут быть безопасны и переносимы при лечении небольших по размеру и поверхностных форм . При этом частота полного регресса поражений на фоне терапии тимололом варьировала от 30% до 50% . Кроме того, для достижения значительного уменьшения размеров или полного регресса пиогенной гранулемы при таком лечении может потребоваться от 4 недель до 6 месяцев и более .
Описаны случаи применения местных форм глюкокортикостероидов (клобетазол, галобетазол, бетаметазон) у детей дважды в день в течение 5 недель под окклюзионной повязкой. При этом частота случаев, потребовавших последующего хирургического иссечения пиогенной гранулёмы, оказалась несколько ниже по сравнению с местным применением 0,5% тимолола в форме гельобразующего раствора (в среднем 6 недель), составив 43% и 56% соответственно .
В местной консервативной терапии также применяется имиквимод — агонист TLR-7/8, относящийся к имидазохинолиновым соединениям и обладающий иммунорегуляторным, противоопухолевым и антиангиогенным действием. Описан случай полного регресса суборбитальной пиогенной гранулемы у ребёнка через 8 недель применения 5% крема имиквимода и отсуствие рецидивов в течение 15 месяцев наблюдения . В другом исследовании эффективность имиквимода была продемонстрирована при лечении пиогенной гарнулемы в области лица (размером 3–6 мм) у 8 детей в возрасте от 2 месяцев до 12 лет: средняя продолжительность терапии до достижения эффекта составила 10,8 недель, рецидивы отсутствовали в течение 9,6 месяцев наблюдения. При этом двум пациентам потребовалось хирургическое вмешательство из-за отсутствия ответа на терапию имиквимодом .
Также сообщены в терапии пиогенной гранулемы: прижигание нитратом серебра у различной возрастной группы пациентов, успешное лечение ребенка 0,015% кремом ингенола мебутата, применение 98% раствора фенола еженедельно и единичные отчеты о случаях применения поваренной соли в виде аппликации пластырем, а также в виде нанесения раствора соли дважды в день в течение 2-х недель , , .
Таким образом, методы консервативного лечения показывают различную успешность терапии, могут быть рассмотрены как терапия первой линии, при ограниченности других методов лечения с целью уменьшения объема последующего хирургического пособия и не применимы при осложненном течении заболевания.
В терапии ЛКГ также применяются методы внутриочаговой терапии, включающие инъекции в толщу опухоли глюкокортикостероидов, полидоканола, блеомицина, абсолютного этанола и других агентов. В одном клиническом сообщении описано успешное лечение 11-летнего ребёнка с рецидивирующей после многократных иссечений пиогенной гранулемы полости рта: применено двукратное внутриочаговое введение триамцинолона ацетонида (10 мг/мл) с интервалом в 2 недели в сочетании с местной терапией 0,05% мазью бетаметазона дважды в день . Однако терапия кортикостероидами может сопровождаться осложнениями, такими как липоатрофия, некроз кожи, развитие кушингоидных признаков и задержка роста . При обзоре применения инъекций моноэтаноламида олеата сообщалось о боли во время процедуры и поствоспалительной гиперпигментации. Склеротерапия полидоканолом ассоциирована с такими побочными эффектами, как отёк, лихорадка и кожная сыпь .
Криохирургия с использованием углекислого газа описана у детей как доступный вариант в условиях ограниченных ресурсов. В рандомизированном исследовании (n=89) пациентов различных возрастных групп, сравнивавшем криотерапию жидким азотом (один цикл замораживания-оттаивания) и кюретаж с электродиссекцией основания, установлено следующее: полный регресс поражений диаметром менее 15 мм достигнут после 1–3 сеансов (в среднем 1,42) в группе криотерапии и после 1–2 сеансов (в среднем 1,03) в группе кюретажа. При этом косметический результат в группе кюретажа оказался более благоприятным в отношении формирования рубца и гипопигментации .
Хирургическое лечение в виде полнослойного иссечения новообразования остается методом выбора при неконтролируемом кровотечении из ЛКГ, при сомнительном диагнозе, позволяющий получить материал для гистологического исследования. Данный метод у ребенка может требовать проведение наркоза. Однако рубцевание является основным недостатком, особенно на таких участках как лицо, где косметический результат является важным . Стоит отметить, что частота рецидива после полнослойного иссечения до здоровых тканей с линейным закрытием составляет около 3,8% .
В терапии ЛКГ распространено использование различных видов лазерного излучения (CO2, PDL, Nd:YAG, эрбиевый лазер, полупроводниковый лазер, KTP-лазер и другие). Кожные хромофоры (гемоглобин, оксигемоглобин, вода и меланин) селективно поглощают разные длины волн. Глубина целевого хромофора, а также конкретная длина волны, поглощаемая этим хромофором, должны быть приняты во внимание при выборе лазера (Рис.1). Согласно теории селективного фототермолиза, предложенной R. Anderson и D. Parrish длина волны, длительность импульса и плотность потока лазера должны быть подобраны так, чтобы привести к селективной деструкции образования, при этом не повреждая окружающие ткани .
Излучение непрерывно-волнового лазера на диоксиде углерода (CO2-лазер) преимущественно воздействует на воду в тканях кожи посредством ее хромофорных свойств, значительно менее активно затрагивает меланин и практически не влияет на гемоглобин. При этом существует определенный риск образования рубцов из-за неспецифической коагуляции в непрерывном режиме. С.Raulin et al. (2002) сообщили об успешном применении CO2-лазера у 98 пациентов, где только у 2 наблюдался рецидив, при этом отмечая использование комбинации режимов с последующей коагуляции основания пиогенной гранулемы для предотвращения рецидива. Тем не менее, стоит отметить, что в 2 случаях отмечены атрофические рубцы, в 12 случаях транзиторные гипер- и гипопигментации (длительностью до 6 месяцев), процесс заживления области коагуляции занимал от 1 до 3 недель .
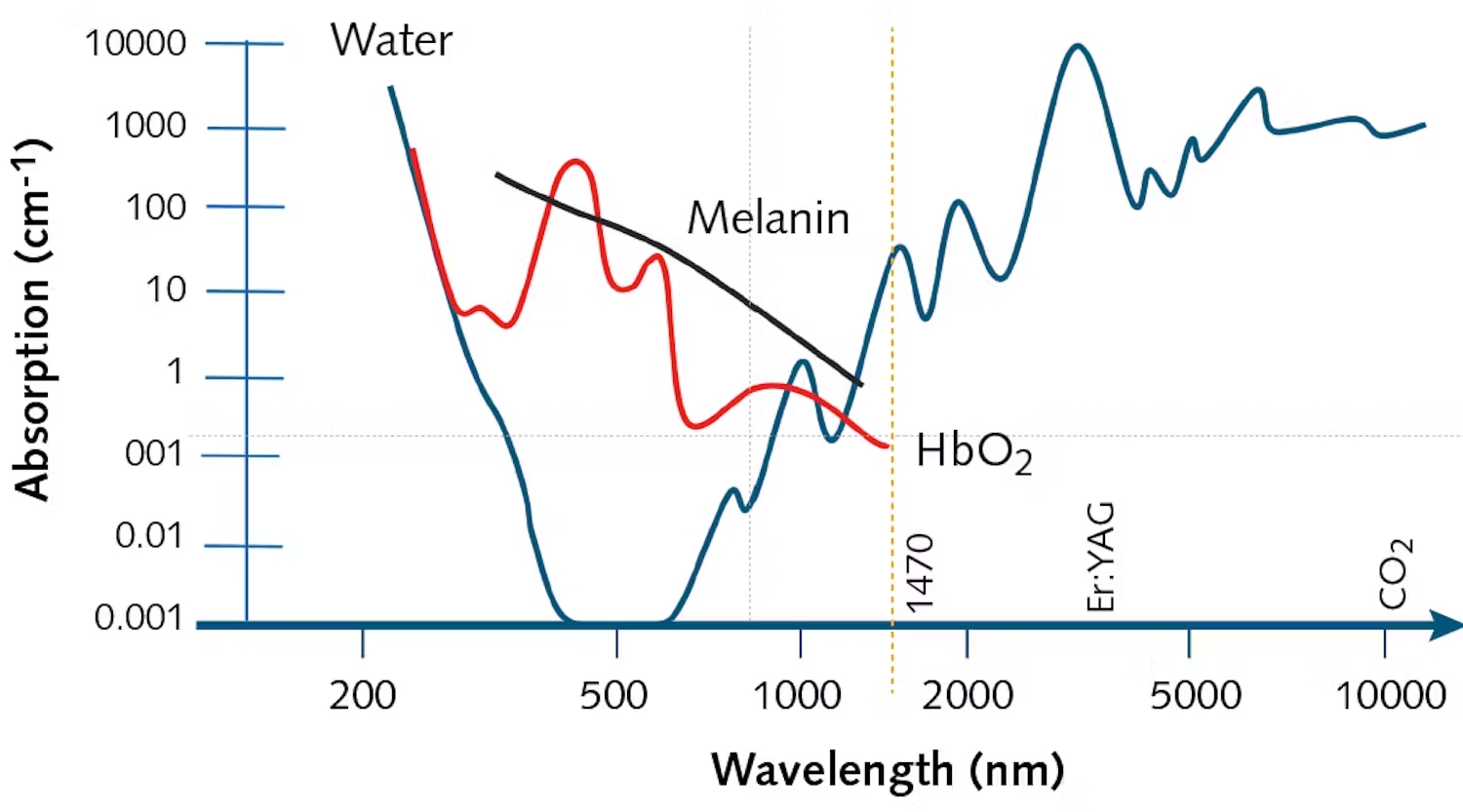
Рисунок 1 - Спектры поглощения лазерного излучения водой, меланином и гемоглобином
Примечание: источник: https://www.laserfocusworld.com/home/contact/14199342/osier-wu
Впервые операция с использованием лазерных аппаратов на алюмоиттриевом гранате с неодимом (Nd:YAG) была продемонстрирована J.E.Geusic et al. в 1964 году . Nd:YAG имеют самую высокую глубину проникновения среди сосудисто-селективных лазеров и самое низкое поглощение эпидермального меланина. Коэффициент поглощения крови при 1064 нм составляет 0,4/мм, что намного выше, чем у окружающей дермы (0,05/мм) при той же длине волны. Эта разница в коэффициентах поглощения обеспечивает селективность лечения глубже расположенных кровеносных сосудов . Проникая на глубину 4–7 мм, возможна эффективная коагуляция ЛКГ большего размера, хороший внутренний гемостаз. Те не менее, необходим точный подбор параметров воздействия луча, чтобы предотвратить избыточное термическое повреждение тканей, результатом чего может быть возникновение грубых рубцов .
Обобщая, стоит отметить, к недостаткам лазерной терапии можно отнести риск рецидива заболевания, отсутствие надежного гемостаза при крупном питающем сосуде, избыточную травматизацию кожи, приводящую к формированию рубцовой деформации, гиперпигментацию кожи и другие.
6. Заключение
Большинство исследований, сравнивающих терапевтические подходы, представлены в виде описаний клинических случаев или серий случаев; количество рандомизированных исследований остается недостаточным. Это создает трудности для критической оценки эффективности различных методов терапии ЛКГ и определения оптимальной лечебной тактики. При выборе терапевтического подхода необходимо учитывать ангиоархитектонику ЛКГ; терапия должна быть направлена на устранение питающего базального сосуда.
