ИЗУЧЕНИЕ ДЕПОЛЯРИЗАЦИИ КОРЫ ГОЛОВНОГО МОЗГА ПРИ ОЧАГОВОЙ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ У КРЫС В ЭКСПЕРИМЕНТЕ В УСЛОВИЯХ КОНТРОЛИРУЕМОЙ ТЕМПЕРАТУРЫ
ИЗУЧЕНИЕ ДЕПОЛЯРИЗАЦИИ КОРЫ ГОЛОВНОГО МОЗГА ПРИ ОЧАГОВОЙ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ У КРЫС В ЭКСПЕРИМЕНТЕ В УСЛОВИЯХ КОНТРОЛИРУЕМОЙ ТЕМПЕРАТУРЫ
Научная статья
Коробков Д.М.1, *, Вечканова Н.А.2, Ляпина С.А.3, Ивашин А.А.4, Миронова Е.А.5, Селькин В.В.6, Прокофьев Д.А.7
1-7 Национальный исследовательский Мордовский государственный университет им. Н.П. Огарёва, Саранск, Россия
* Корреспондирующий автор (doctordmk [at]mail.ru)
АннотацияРоль ишемической деполяризации при очаговой ишемии головного мозга неизвестна. Однако имеются косвенные доказательства того, что ишемическая деполяризация способна усугубить ишемическое повреждение клеток. В своем исследовании мы постарались показать, что количество эпизодов ишемической деполяризации, возникающих во время фокальной церебральной ишемии, пропорционально степени ишемического повреждения клеток. Для этого мы провели моделирование очаговой церебральной ишемии у 30 крыс. Животные были разделены на три группы: 1) нормотермия (n = 10), 2) гипотермия (n = 10), 3) гипертермия (n = 10).Нами выявлена статистически значимая корреляция между температурой тела животного и количеством эпизодов деполяризаций (r = 0,87, p<0,001). Среднее число отклонений потенциала постоянного тока у животных с гипертермией было статистически значимо выше, чем у животных с нормотермией (p<0,05). Температурные колебания оказывают физиологические и биохимические эффекты на ткани, статистически значимая корреляция между эпизодами деполяризаций при ишемии головного мозга и процент поражения мозга после ишемии не всегда находятся в причинно-следственных отношениях.
Ключевые слова: ишемия, деполяризация, корковая депрессия.TO STUDY THE DEPOLARIZATION OF THE CEREBRAL CORTEX IN FOCAL CEREBRAL ISCHEMIA IN RATS IN AN EXPERIMENT UNDER CONTROLLED TEMPERATURE CONDITIONS
Research article
Korobkov D.M.1, *, Vechkanova N.A.2, Lyapina S.A.3,Ivashin A.A.4, Mironova E.A.5, Selkin V.V.6, Prokofyev D.A.7
1-7 N.P. Ogarev National Research Mordovian State University, Saransk, Russia
*Corresponding author (doctordmk [at]mail.ru)
AbstractThe role of ischemic depolarization in focal cerebral ischemia is unknown. However, there is indirect evidence that ischemic depolarization can exacerbate ischemic cell damage. The current article attempts to show that the number of episodes of ischemic depolarization occurring during focal cerebral ischemia is proportional to the degree of ischemic cell damage. In order to achieve this, the authors conducted a simulation of focal cerebral ischemia in 30 rats. The animals were divided into three groups: 1) normothermia (n = 10), 2) hypothermia (n = 10), 3) hyperthermia (n = 10). The authors found a statistically significant correlation between the body temperature of the animal and the number of depolarization episodes (r = 0.87, p The average number of DC potential deviations in animals with hyperthermia was statistically significantly higher than in animals with normothermia (p Temperature fluctuations have physiological and biochemical effects on tissues, while a statistically significant correlation between episodes of depolarization in cerebral ischemia and the percentage of brain damage after ischemia do not always have causal relationships.
Keywords: ischemia, depolarization, cortical depression. АктуальностьОбщеизвестный факт, что очаговая церебральная ишемия приводит к множественным электрофизиологическим изменениям в пораженной ткани [1], [2], среди которых микроскопические клеточные события: перераспределение ионных частиц, электрическая деполяризация мембран, сопровождающаяся высвобождением биологически активных веществ [3], но стоит отметить, что этот вопрос по-прежнему не до конца изучен. Кроме того, во время фокальной церебральной ишемии возникают макроскопические консолидированные события, такие как деполяризация коры головного мозга, которая включает распространяющуюся корковую депрессию.
Роль ишемической деполяризации при очаговой ишемии головного мозга неизвестна. Однако имеются косвенные доказательства того, что ишемическая деполяризация способна усугубить ишемическое повреждение клеток. Депрессия корковых структур напрямую связана с таким патологическим явлением, как нарушение перфузии. В условиях ишемии, когда возникает энергетический коллапс, корковая депрессия может спровоцировать накопление внутриклеточных ионов Са2+ и, следовательно, инициирует апоптоз. Корковая депрессия — это не просто изолированная электрическая дисфункция, на фоне фокальной ишемии, корковая депрессия сама может стать инициирующим фактором в развитии ишемического повреждения клеток.
Мы в своем исследовании постарались показать, что количество эпизодов ишемической деполяризации, возникающих во время фокальной церебральной ишемии, пропорционально степени ишемического повреждения клеток. Повреждение тканей в результате очаговой ишемии головного мозга коррелирует с температурными колебаниями тела. Снижение температуры тела при очаговой церебральной ишемии приводит к уменьшению размера зоны ишемии, а как следствие и инфаркта головного мозга, и наоборот, небольшое повышение температуры тела приводит к увеличению площади инфаркта мозга.
Материалы и методы
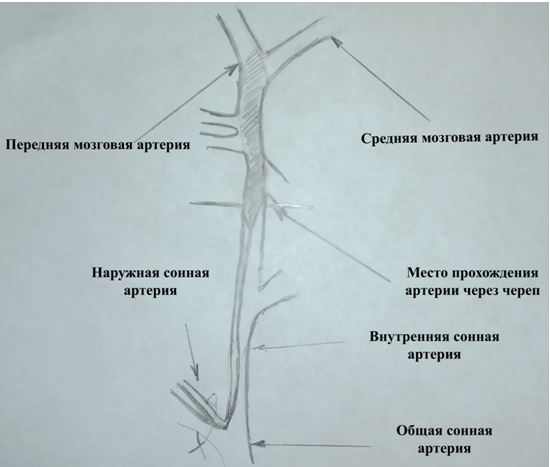
Исследование выполнено на 30 нелинейных белых крысах обоего пола массой 250-300 г. Все манипуляции с животными проводились в соответствии с Руководством по содержанию и использованию лабораторных животных [5]. Животные были разделены на три группы: 1-я нормотермия (n = 10), 2-я гипотермия (n = 10), 3-я гипертермия (n = 10).При нормотермии внутреннюю температуру поддерживали на уровне 37,0 ± 0,89°С, гипотермия поддерживалась на уровне 30,0 ± 0,2°С, гипертермия поддерживалась на уровне 40,0 ± 0,2°C. Для обеспечения гипотермии животных обкладывали емкостями с охлажденным раствором и укрывали теплоизоляционным одеялом, а также дополнительно вводили в латеральную хвостовую вену охлажденный 0,9% раствор NaCl. Для согревания животных обкладывали емкостями с горячим раствором и укрывали теплоизоляционным одеялом для поддержания оптимальной температуры в условиях эксперимента. Животным проводилось анестезиологическое пособие, включающее интраперитонеальное введение препаратов: «Золетил 100» и «Ксилазин» по стандартной методике [1]. Производилась респираторная поддержка. После чего животным выполнялась окклюзия средней мозговой артерии (СМА) по методике KoizumiJ. еtal (1986) (рис. 1) [4].
Рис.1 – Схема окклюзии СМА по методике KoizumiJ. еtal (1986)
Период окклюзии составил 90-минут. Затем осуществлялась реперфузия, путем перерезки лигатуры на наружной сонной артерии. На аппаратном комплексе «BIOPAC» регистрировалась ЭЭГ, проводилось измерение температуры в соответствии со стандартными методиками [6].
Окклюзия СМА выполнялась после того, как внутренняя температура животного достигала заданного уровня (30, 37 или 40°C соответственно). Гипо- или гипертермию поддерживали в течение всего периода эксперимента и спустя 60 минут после реперфузии. Затем животным давали возможность восстановить физиологический уровень температуры (этот период в среднем занимал 30 минут). На следующем этапе производилось морфологическое исследование. Головной мозг извлекался из черепной коробки, происходила фиксация в 10% нейтральном формалине, с дальнейшей проводкой в спиртах, затем происходило получение парафиновых блоков, выполнялось определение площади поражения [4], затем окрашивание срезов гематоксилином и эозином.
Для статистической обработки данных, полученных в ходе эксперимента, был применен пакет программ «Statistica 6.0». Был применен критерий Крускала-Уоллиса. Различия принимались за статистически значимые при p<0,05. Корреляции между переменными были проанализированы с использованием критерия Спирмена. Результаты принимались за статистически значимые при p<0,01.
Результаты и обсуждение
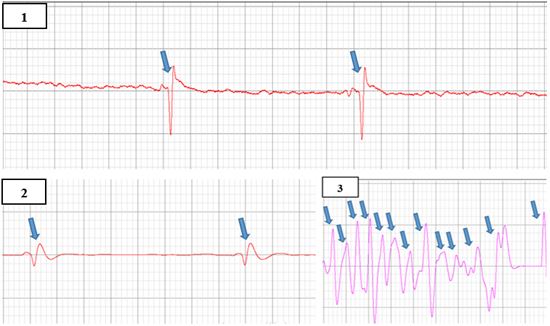
На рис. 2 представлены репрезентативные записи коркового потенциала постоянного тока у животных, подвергшихся окклюзии СМА во всех исследуемых группах. Всего у всех животных, подвергшихся ишемии в условиях контролируемой температуры, при анализе ЭЭГ нами отмечено 124 отклонения уровня потенциала постоянного тока; они были зарегистрированы в период окклюзии СМА, за исключением 6 эпизодов при которых, поляризация были зафиксирована в течение 5 минут после реперфузии.
Рис.2 – Репрезентативная запись коркового потенциала постоянного тока у животных, подвергшихся окклюзии СМА:
1 – нормотермия;2 – гипотермия; 3 – гипертермия
В начале и в течение 60 минут реперфузии корковой депрессии не наблюдалось. Первые зарегистрированные эпизоды отклонения потенциала постоянного тока в группе гипертермии наступало статистически значимо раньше, чем в группах нормо- и гипотермии (p<0,05) (таблица 1).
Таблица 1 – Время регистрации первых эпизодов деполяризаций, количество зарегистрированных эпизодов, временные интервалы между эпизодами деполяризаций и площадь инфаркта головного мозга в исследуемых группах
| Группа животных | Время регистрации первых эпизодов деполяризации, m±SD, мин | Количество зарегистрированных эпизодов деполяризации при ишемии, m±SD | Временной интервал между эпизодами деполяризации при ишемии, m±SD, мин | Площадь инфаркта головного мозга, m±SD, % поражения |
| Нормотермия (n=10) | 8,95±11,14 | 2,7±0,96 | 19±10,89 | 13,2±12,3 |
| Гипотермия (n=10) | 12,24±6,41 | 2,01±0,61 | - | 0±0 |
| Гипертермия (n=10) | 1,17±0.27 | 13,17±3,84 | 15±10,32 | 36,5±3,4 |
У животных с гипертермией первые эпизоды поляризации возникали уже через одну минуту после окклюзии СМА, а у нормо- и гипотермичных животных время варьировалось от 20 до 30 минут. Амплитуда волны первых отклонений потенциала постоянного тока обычно отличалась от последующих во всех экспериментальных группах (рис. 2). Появление деполяризации сопровождалось общим сдвигом потенциала постоянного тока, который не возвращался к исходному уровню, наиболее заметен этот феномен в группе животных с гипертермией. Пиковые отклонения потенциала постоянного тока коры головного мозга на двух противоположных участках происходили с разницей во времени от десятых доли секунды до одной минуты. Отклонение обычно происходило раньше на электроде, расположенном на 5 мм латеральнее, чем на 2 мм латеральнее брегмы. В группе гипотермии у животных зарегистрировано 2,01±0,61 эпизода отклонения потенциала постоянного тока. Напротив, множественные отклонения потенциала постоянного тока наблюдались как у нормо-, так и у гипертермичных животных (таблица 1). Нами выявлена статистически значимая корреляция между температурой тела животных и количеством эпизодов деполяризаций (r = 0,87, p< 0,001). Среднее число отклонений потенциала постоянного тока у животных с гипертермией было статистически значимо выше, чем у животных с нормотермией (p<0,05). У животных с гипотермией была обнаружена минимальная площадь ишемического повреждения клеток, ограниченное изолированным очаговым клеточным некрозом в стриатуме и отсутствием измеримой зоны инфаркта. В группах нормотермии и гипертермии наблюдалась четко разграниченная зона инфаркта головного мозга. Ишемическое поражение в группе нормотермии охватывало гиппокамп, а также полосатое тело, как и в группе гипертермии. Объемы инфаркта во всех трех группах статистически значимо отличались друг от друга (p<0,05). Выявлена статистически значимая корреляционная связь между площадью инфаркта и температурой тела (r = 0,95, p< 0,001). Выявлена статистически значимая корреляция между объемом инфаркта головного мозга и числом деполяризаций (r = 0,90, p< 0,001).
В настоящем исследовании мы непрерывно регистрировали изменения потенциала постоянного тока до, во время окклюзии СМА и спустя 90 мин после окклюзии СМА. Наши данные показывают, что количество отклонений потенциала постоянного тока, наблюдаемые в течение 90 минут очаговой церебральной ишемии, сильно коррелирует с площадью инфаркта. Отклонения потенциала постоянного тока и время задержки между началом эпизода деполяризации не поддаются количественному подсчету в виду артефактов, выходящих за пределы измерений.
Данные этого исследования дополнительно подтвердили, что во время ишемического инсульта возникают множественные эпизоды деполяризации. Без точной информации о положении деполяризующего источника практически невозможно рассчитать скорость распространяющейся волны. Первоначальное отклонение постоянного тока имело некоторые уникальные особенности по сравнению с последующими деполяризациями. Начальный пик напряжения наблюдался у всех животных вместе с общим сдвигом потенциала постоянного тока, который не возвращался к исходному уровню. Начальный пик был единственным, и наблюдался у всех животных в группе с гипотермией. Хорошо известно, что гипотермия практически полностью подавляет возникновение корковой депрессии, но не влияет на аноксическую деполяризацию.
Таким образом, можно предположить, что начальные отклонения на электроэнцефалограмме во время окклюзии СМА вызываются аноксической деполяризацией, а не корковой депрессией. У большинства животных во время реперфузии не наблюдалось деполяризации головного мозга, также как, и корковой депрессии во время реперфузии. Восстановление мозгового кровотока и восстановление ионного гомеостаза не вызывают электрофизиологических изменений, приводящих к явлениям деполяризации.
Температура животного во время ишемии также оказывает сильное влияние на исход. Для интерпретации этого эффекта можно выделить несколько возможных механизмов: пониженная температура мозга снижает потребность в энергии и, следовательно, может уменьшить последствия, вызванные энергетическим сбоем во время ишемического инсульта [7], [9]; гипотермия может уменьшить или даже полностью подавить высвобождение глутамата и дофамина, оба из которых связаны с постишемическим повреждением нейронов [8], [10].
Выводы
Наше исследование показало, что количество эпизодов ишемической деполяризации во время очаговой церебральной ишемии коррелирует с площадью инфаркта головного мозга. Выявлена статистически значимая корреляционная связь между площадью инфаркта и температурой тела (r = 0,95, p< 0,001). Выявлена статистически значимая корреляция между объемом инфаркта головного мозга и числом деполяризаций (r = 0,90, p< 0,001). Температурные колебания оказывают физиологические и биохимические эффекты на ткани, статистически значимая корреляция между эпизодами деполяризаций при ишемии головного мозга и процент поражения мозга после ишемии не всегда находятся в причинно-следственных отношениях.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
- Korobkov D.M. The study of the features of total brain ischemia in combination with hyperglycemia under controlled temperature conditions in rats in the experiment/ D.M. Korobkov, N.A. Vechkanova, A.A. Ivashin et al. // International Research Journal.-2021.-V.113.-№11.-Р. 172 – 174.DOI: 10.23670/IRZH.2021.113.11.065
- Wu X.The effectiveness of early prophylactic hypothermia in adult patients with traumatic brain injury: A systematic review and meta-analysis/ Х.Wu, Y. Tao, L. Marsons et al. // Australian Critical Care. -2021.-V.34.-№1.-Р.83-91. DOI: 10.1016/j.aucc.2020.05.005.
- Anrather J. Inflammation and Stroke: An Overview / J. Anrather, C. Ladecola// Neurotherapeutics. -2016. -№ 13. –Р. 661–670. DOI: 10.1007/s13311-016-0483-x
- Koizumi, J. Experimental studies of ischemic brainedema. I: a new experimental model of cerebral embolism in rats in which recirculation can be introduced in the ischemic area / J. Koizumi et al. // Jаpаn. Journal of Stroke. - 1986.- № 8. -P. 1-8.
- Annex A. To The European Convention On The Protection Of Spine Animals Used For Experiments And Other Scientific Purposes (Ets №. 123) Guidelines For The Maintenance And Care Of Laboratory Morals (Laboratory). 2006. [Electronic resource]. URL:http://conventions.coe.int/Treaty/EN/Treaties/PDF/123- Arev. pdf (accessed: 15.12.2021).
- Reference Manual for AcqKnowledge 4.4 Software & MP150/MP36R, BioHarness, B-Alert Mobita or Stellar Hardware/Firmware on Windows 10, 8, 7 or Vista, or Mac OS X 10.5-10.9 [Electronic resource]. URL: https://www.biopac.com/wp-content/uploads/BSL-PRO-3_7-Manual.pdf (accessed: 15.12.2021).
- Vahidy F.S. Systematic review and meta-analysis of bone marrow-derived mononuclear cells in animal models of ischemic stroke/ F.S. Vahidy, M.H. Rahbar, H. Zhu et al. // Stroke.- 2016. №47. –Р.1632-1639.
- Singh V. HMGB1 as a key mediator of immune mechanisms in ischemic stroke/ V.Singh, S. Roth, R. Veltkamp et al. // Antioxid Redox Signal. -2016.-№24.-Р.635-651.
- Petrovic-Djergovic D. Inflammatory disequilibrium in stroke/ D. Petrovic-Djergovic, S.N. Goonewardena, D.J. Pinsky // Circulation Research. -2016.-№119.-Р.142-158.
- Shi H. Mild hypothermia improves brain injury in rats with intracerebral hemorrhage by inhibiting IRAK2/NF-kappaB signaling pathway/Н.Shi, Z. Su, Н. Su et al. // Brain and Behavior.-2021.- V.11.-№1. DOI: 10.1002/brb3.1947.