ЭФФЕКТИВНОСТЬ ТАРГЕТНОЙ ТЕРАПИИ МУКОВИСЦИДОЗА У ДЕТЕЙ СТАВРОПОЛЬСКОГО КРАЯ, СРАВНИТЕЛЬНЫЙ АНАЛИЗ С ДАННЫМИ РЕГИСТРА
ЭФФЕКТИВНОСТЬ ТАРГЕТНОЙ ТЕРАПИИ МУКОВИСЦИДОЗА У ДЕТЕЙ СТАВРОПОЛЬСКОГО КРАЯ, СРАВНИТЕЛЬНЫЙ АНАЛИЗ С ДАННЫМИ РЕГИСТРА
Аннотация
В представленной статье проводится анализ влияния таргетной терапии на нутритивный статус, значение потовой пробы, функцию внешнего дыхания у детей с муковисцидозом, проживающих в Ставропольском крае. Основной целью исследования является сравнительный анализ полученных данных с информацией, содержащейся в Национальном регистре больных муковисцидозом за 2022 год.
В рамках исследования были оценены показатели физического развития, потовой пробы, функции внешнего дыхания у 30 пациентов в возрасте от 3 до 18 лет. Участники были разделены на три группы в зависимости от типа получаемой терапии: таргетная терапия с использованием препаратов «Оркамби», «Трикафта» и «Трилекса», а также контрольная группа, получающая стандартную базисную терапию.
Основные результаты исследования включают детальный анализ динамики изменения параметров физического развития, результатов потовой пробы, функции внешнего дыхания на различных этапах терапевтического вмешательства.
Статистический анализ данных проводился с использованием программного обеспечения AtteStat и STATISTICA v.10.0. Минимальный уровень статистической значимости различий верифицировали при р<0,05 (использовался U-критерий Манна-Уитни). Нами проанализированы: среднее значение (М), ошибка среднего (m), медиана (Ме), минимальное (Min) и максимальное (Max) значения.
Исследование представляет значительный интерес для специалистов в области педиатрии и медицинской генетики, задействованных в лечении муковисцидоза. Полученные результаты могут способствовать оптимизации терапевтических стратегий и улучшению качества жизни пациентов с данным заболеванием.
1. Введение
Муковисцидоз (далее МВ) или кистозный фиброз — тяжелое генетическое заболевание, которое передается по аутосомно-рецессивному типу, характеризуется поражением всех экзокринных желез, а также жизненно важных органов и систем , .
В Российской Федерации частота муковисцидоза по данным ФГБНУ «Медико-генетического научного центра им. акад. Н.П. Бочкова» составляет 1 на 9 тыс. новорожденных , . Среди народов Кавказа муковисцидоз встречается гораздо чаще — 1 случай на 2500 живорождений , . По разным оценкам, муковисцидозом страдают от 70 до 100 тыс. человек во всем мире. Тяжесть заболевания и вариабельность клинической картины зависят от разнообразия генетических мутаций и разного характера их проявлений , .
Очень важным результатом развития фармакотерапии МВ стало открытие малых молекул, восстанавливающих работу неполноценного белка Cystic Fibrosis Transmembrane conductance Regulator (далее CFTR) , .
Эти препараты называются CFTR-модуляторами. Среди них выделяют корректоры и потенциаторы , . CFTR-модуляторы эффективны в отношении только некоторых патологических последовательностей гена CFTR , , . В связи с этим необходимо учитывать региональные особенности генетики МВ, в частности, в соответствии с национальным регистром частоту встречаемости гена delF508 при которой эффективность таргетной терапии ниже на Северном Кавказе , , .
По данным анализа литературных источников описаны следующие результаты применения таргетной терапии при муковисцидозе:
1. Благодаря включению в терапию препаратов, изменяющих функцию поврежденного белка CFTR, даже за короткий период лечения улучшаются показатели нутритивного статуса (за счет массы тела) , ;
2. Более значимые изменения (прибавка массы, субъективное улучшение состояния, тенденция к нормализации показателей потовой пробы) отмечены в группе пациентов, получающих трехкомпонентную таргетную терапию , .
Наиболее эффективными в лечении МВ являются комбинированные препараты, в состав которых входят как потенциаторы, так и корректоры . В настоящее время в РФ зарегистрированы и разрешены для использования в педиатрической практике 3 таргетных препарата , :
1. «Оркамби» (Ивакафтор+Лумакафтор) — для детей с 2 лет.
2. «Трикафта» (Ивакафтор+Тезакафтор+Элексакафтор) — для детей с 6 лет.
3. «Трилекса» (Ивакафтор+Тезакафтор+Элексакафтор) (дженерик оригинального препарата «Трикафта», зарегистрирован в России 15 ноября 2024 года) — для детей с 6 лет.
По данным национального регистра больных муковисцидозом (2022 год) в Ставропольском крае насчитывается 48 ребенок с данным диагнозом .
По данным национального регистра в СКФО насчитывается 174 ребенка больных муковисцидозом .
Суммарно в РФ насчитывается 2802 ребенка больных муковисцидозом .
Цель работы: проанализировать влияния таргетной терапии на нутритивный статус, значение потовой пробы, функцию внешнего дыхания детей с муковисцидозом в Ставропольском крае в сравнении с данными национального регистра за 2022 год.
2. Материалы и методы исследования
Был проведен анализ литературных источников, анализ данных из историй болезни, статистическая обработка материала. Были проанализированы стационарные карты 30 детей, больных МВ, в возрасте от 3 до 18 лет (n=30), проживающих в Ставропольском крае и находившихся на лечении в отделении пульмонологии ГБУЗ СК «Краевая детская клиническая больница» в период с 2020 г. по 2025 г.
В данном исследовании оценивались следующие параметры:
1. Показатели физического развития (Z-Score массы тела, Z-Score роста; Z-Score индекса массы тела) — при помощи программного обеспечения ВОЗ Anthro для персональных компьютеров.
2. Показатели функции внешнего дыхания: объём форсированного выдоха за первую секунду (далее ОФВ1), форсированная жизненная ёмкость лёгких (далее ФЖЕЛ).
3. Показатели значения потовой пробы – при помощи приборов «Нанодакт» и «Макродакт».
В данном исследовании был проанализирован генетический спектр мутаций среди отобранных пациентов.
Были проанализированы стационарные карты 30 детей, больных МВ, в возрасте от 3 до 18 лет (n=30), проживающих в Ставропольском крае. Из них 14 (46%) мальчиков м 16 (54%) девочек. Средний возраст составил 11,5 ± 0,8 лет. Контингент исследованных был разделен на 3 группы:
1. Первая — состоит из 6 детей (n=6), получающих таргетную терапию препаратом «Оркамби». Их них 1 (16,7%) мальчик и 5 (83,3%) девочек.
2. Вторая — состоит из 8 детей (n=8), получающих таргетную терапию препаратом «Трикафта». Из них 5 (62,5%) мальчиков, 3 (37,5 %) девочек. К данной группе также относится 2 ребенка, получающие терапию препаратом «Трилекса». Из них 1 мальчик (50,0%), 1 девочка (50%)»
3. Третья — «контрольная группа» насчитывает 14 детей (n=14), получающих базисную терапию (основой препарат «Дорназа альфа»). Их них 6 (42,8%) мальчиков и 8 (57,2%) девочек.
Нами было проведено динамическое наблюдение за анализируемыми параметрами в трёх контрольных точках:
1. На старте терапии.
2. На 6 мес. непрерывной терапии.
3. На 12 мес. непрерывной терапии.
Пациенты исследуемых групп на фоне базисной терапии и на терапии «Оркамби» были сопоставимы по возрасту (9,4 ± 0,8 лет и 8,8 ± 0,6 лет соответственно). Пациенты, получающие «Трикафту» были несколько старше (14,8 ± 0,9 лет), что связано с ограничением по возрасту при назначении препарата.
По данным национального регистра 53,1% детей в РФ получают терапию CFTR-модуляторами, а по СКФО 15,2% больных детей.
Статистический анализ результатов исследования проводили с использованием пакета программ AtteStat, STATISTICA v.10.0. Минимальный уровень статистической значимости различий верифицировали при р<0,05 (использовался U-критерий Манна-Уитни). Нами проанализированы: среднее значение (М), ошибка среднего (m), медиана (Ме), минимальное (Min) и максимальное (Max) значения.
3. Результаты исследования и их обсуждение
Повозрастная структура детей с муковисцидозом представлена на рис. 1. Исходя из представленных данных мы делаем вывод, что контингент детей, больных МВ в Северо-Кавказском федеральном округе (далее СКФО), моложе чем в общероссийской статистике.
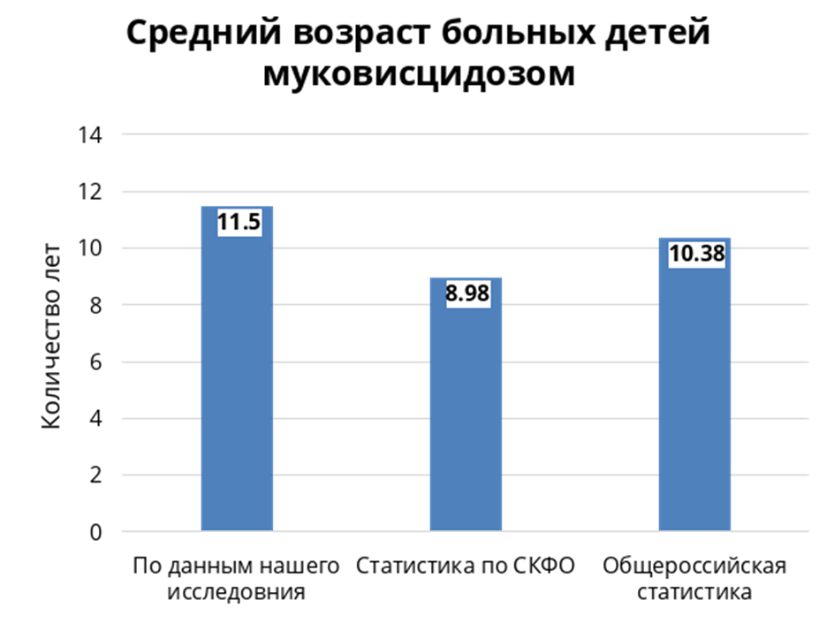
Рисунок 1 - Средний возраст детей больных муковисцидозом
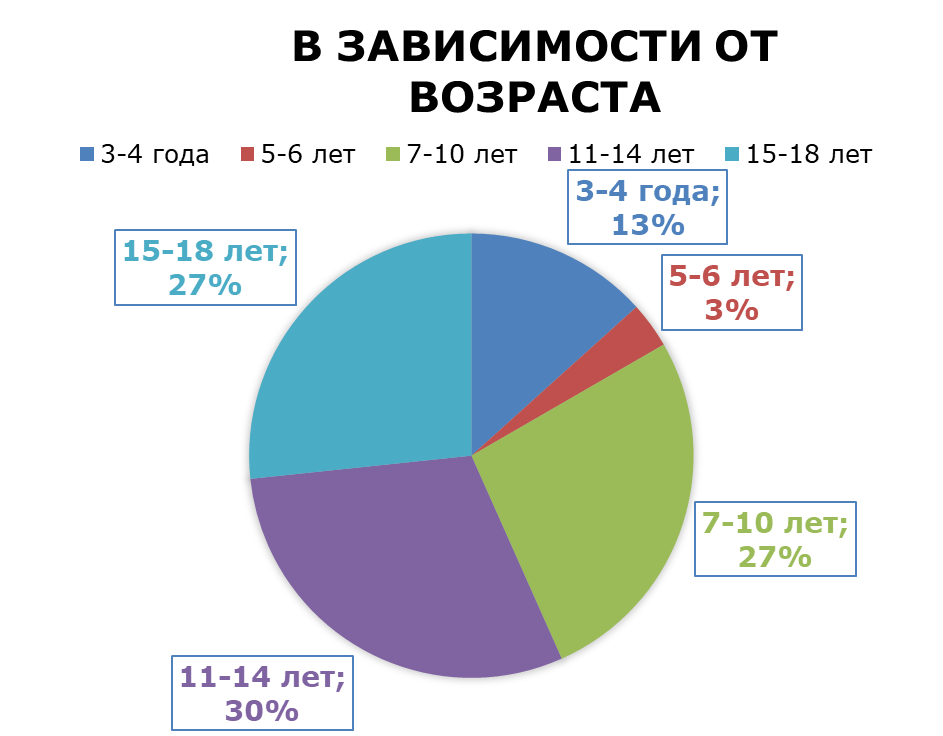
Рисунок 2 - Структура детей больных МВ в зависимости от возраста

Рисунок 3 - Структура детей больных МВ в зависимости от генетического варианта мутации в гене CFTR
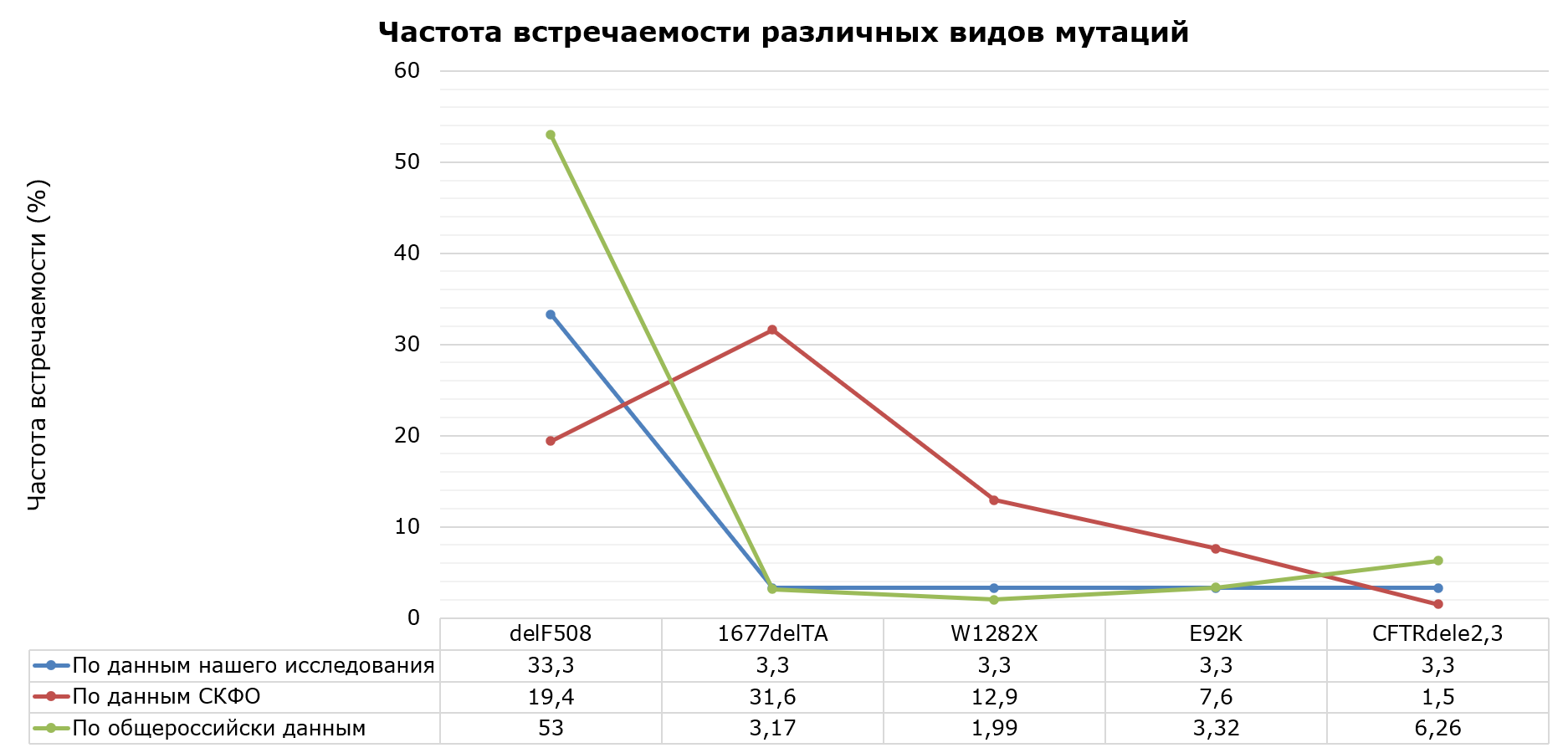
Рисунок 4 - Частота встречаемости различных видом мутации в гене CFTR у детей больных МВ
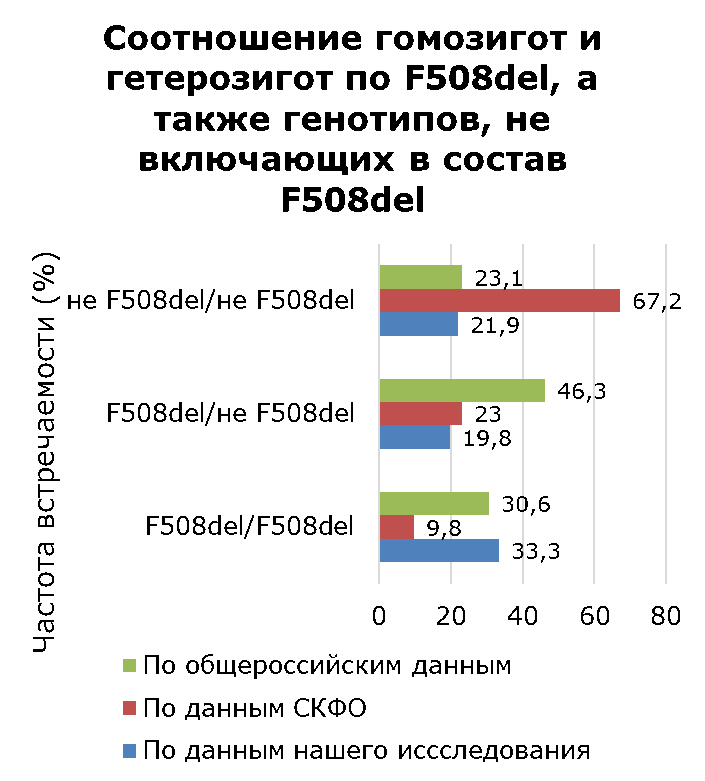
Рисунок 5 - Частота встречаемости различных видов мутаций в гене delF508 у детей больных МВ
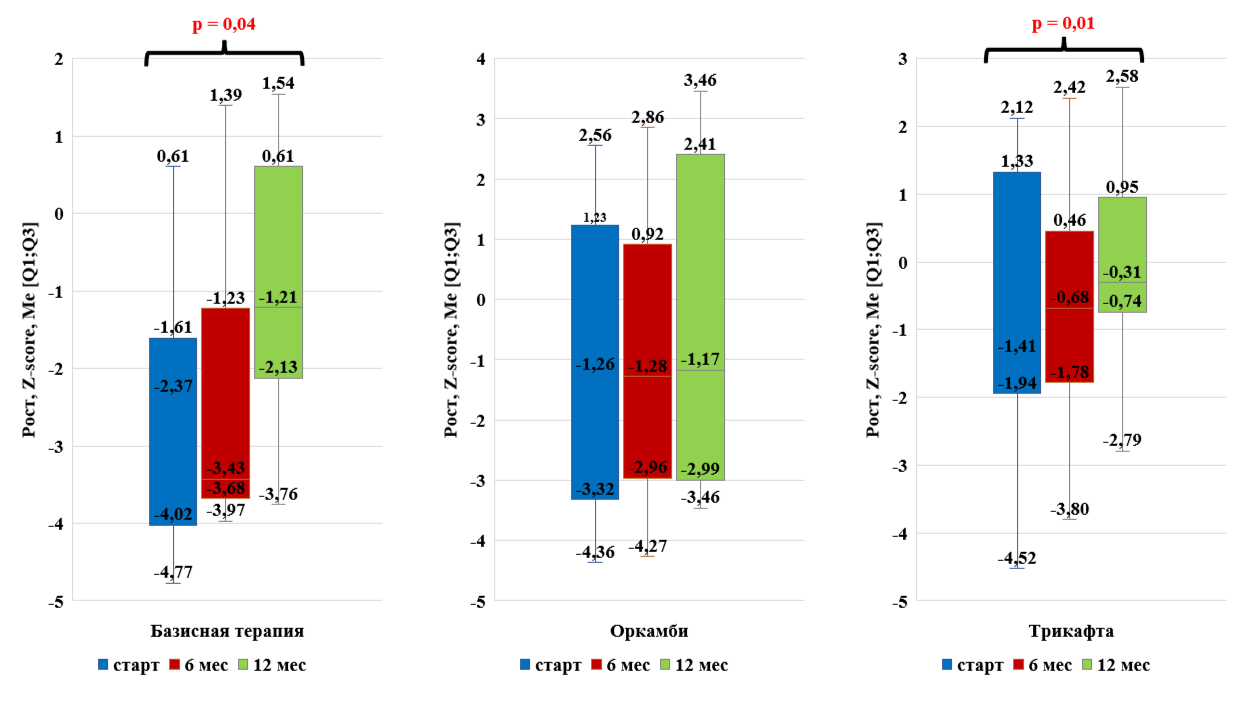
Рисунок 6 - Динамика физического развития (рост) на фоне таргетной терапии
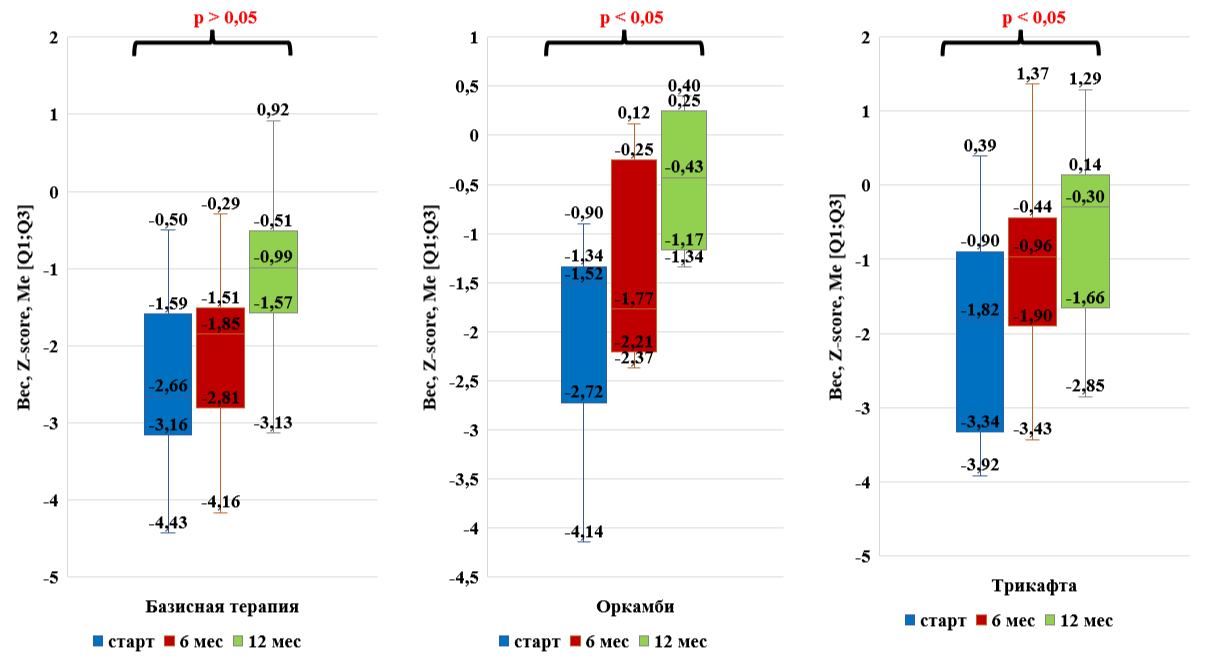
Рисунок 7 - Динамика физического развития (масса тела) на фоне таргетной терапии
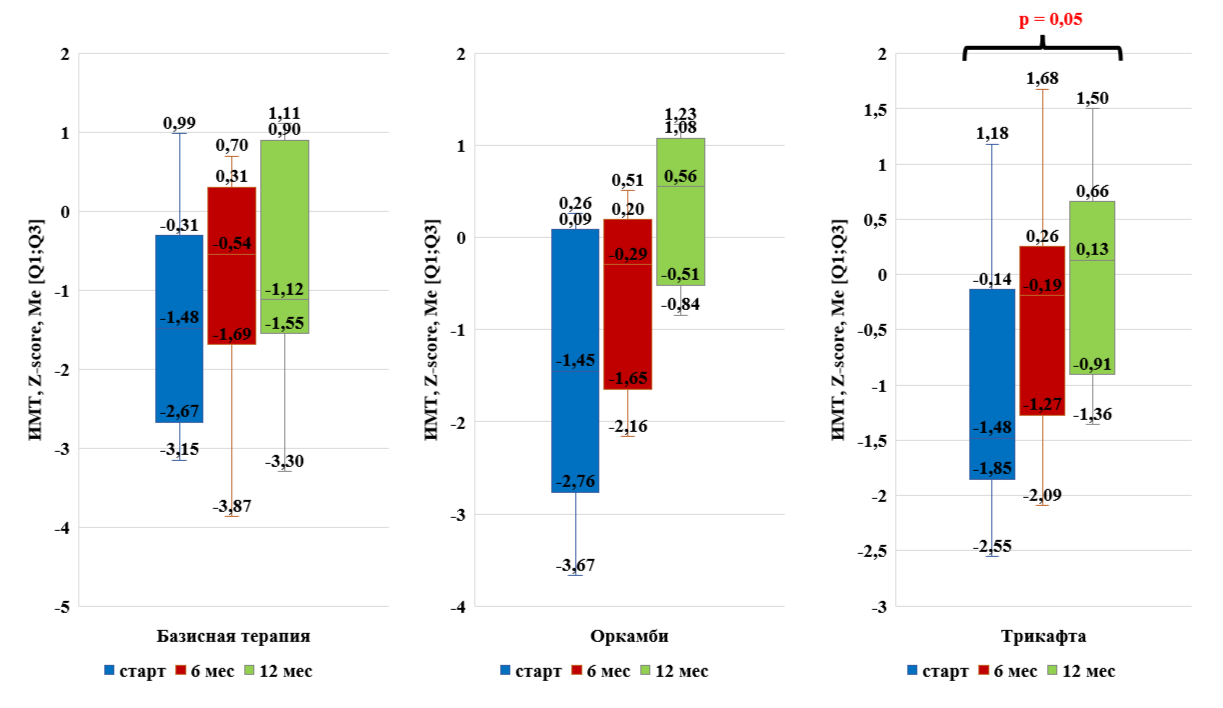
Рисунок 8 - Динамика физического развития (индекс массы тела) на фоне таргетной терапии
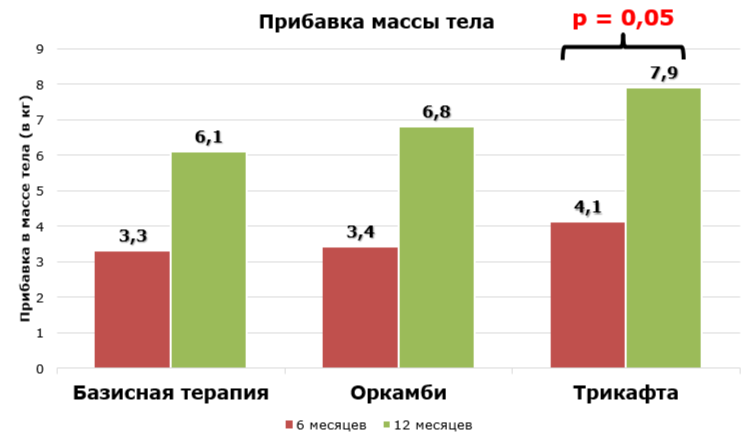
Рисунок 9 - Динамика физического развития на фоне таргетной терапии
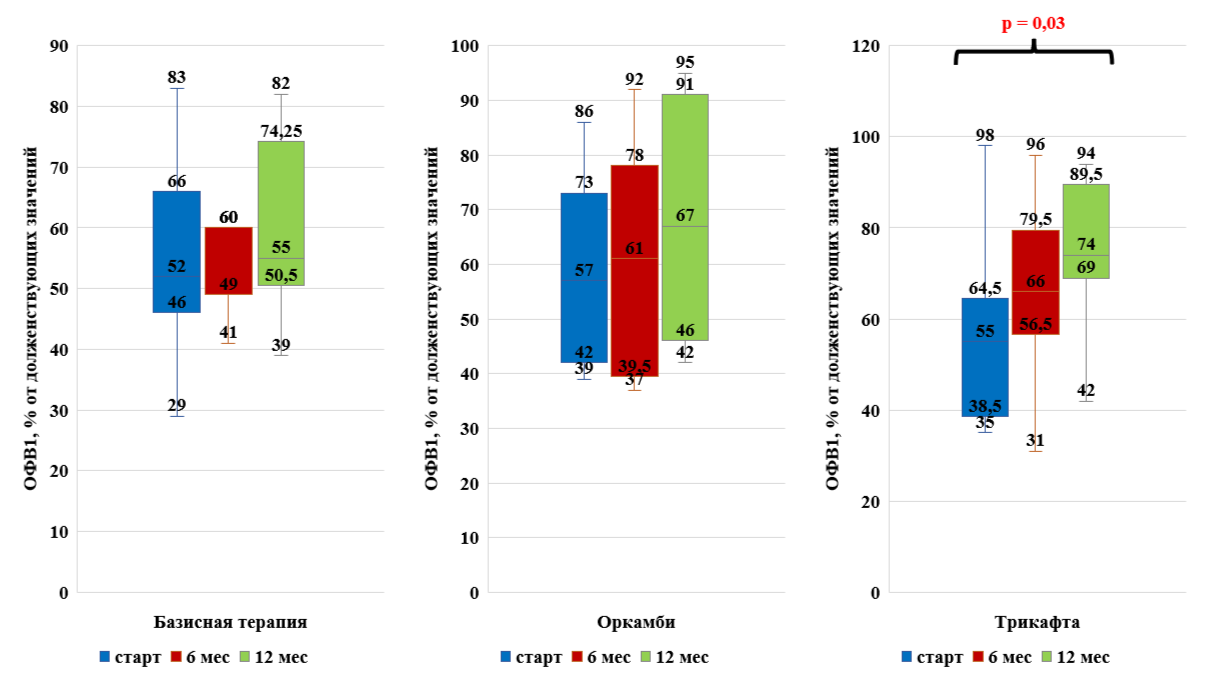
Рисунок 10 - Динамика показателей внешнего дыхания (ОФВ1) на фоне таргетной терапии
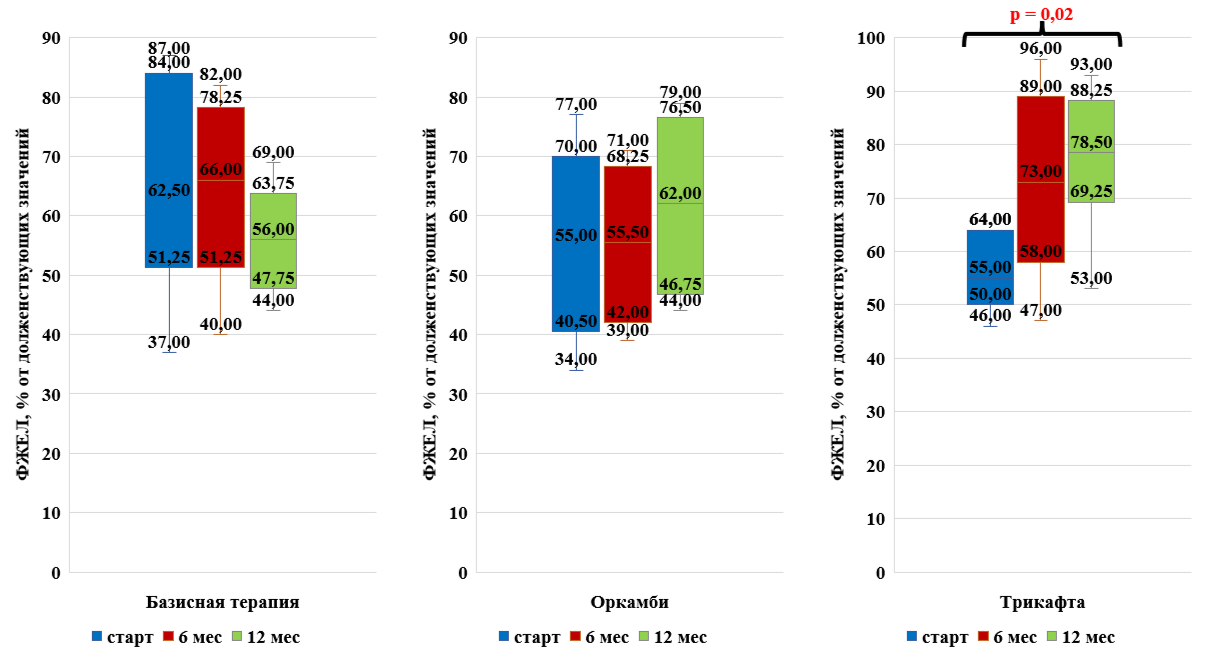
Рисунок 11 - Динамика показателей внешнего дыхания (ФЖЕЛ) на фоне таргетной терапии
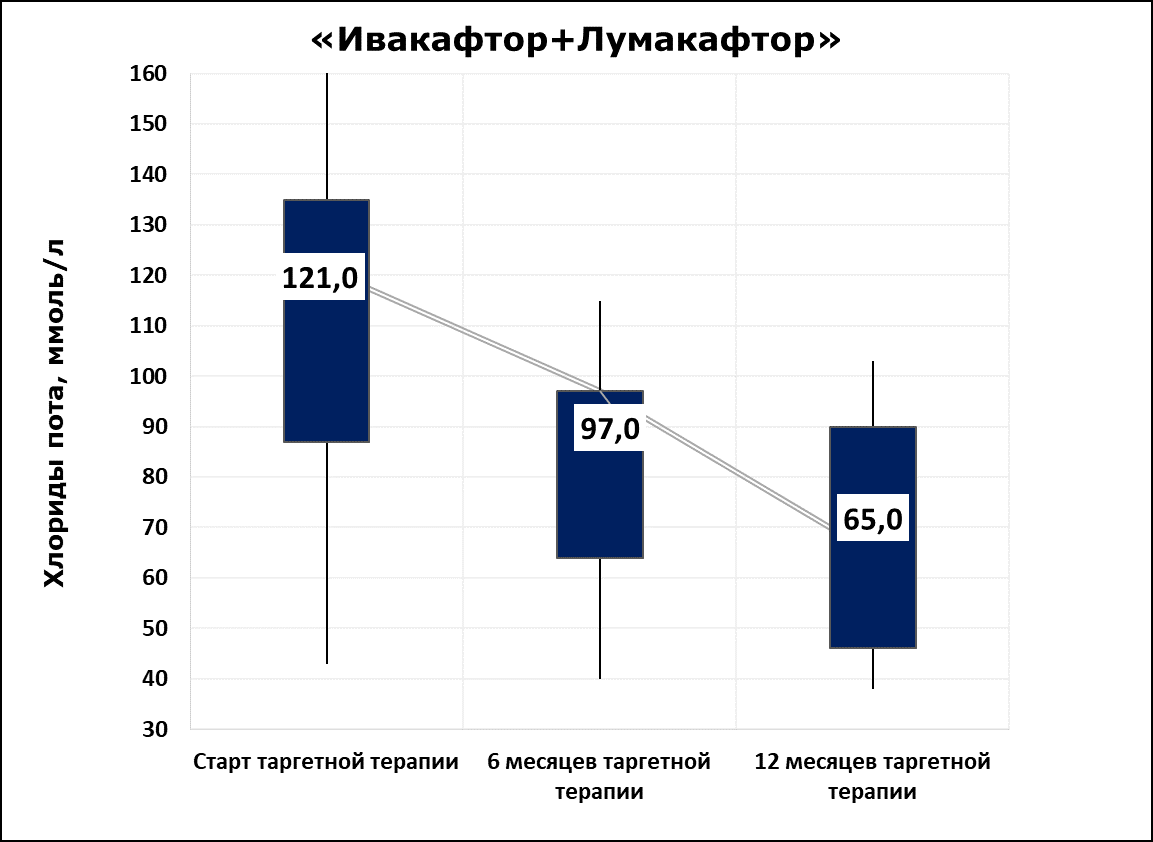
Рисунок 12 - Динамика потовой пробы на фоне таргетной терапии препаратом «Оркамби»
Примечание: Ивакафтор+Лумакафтор
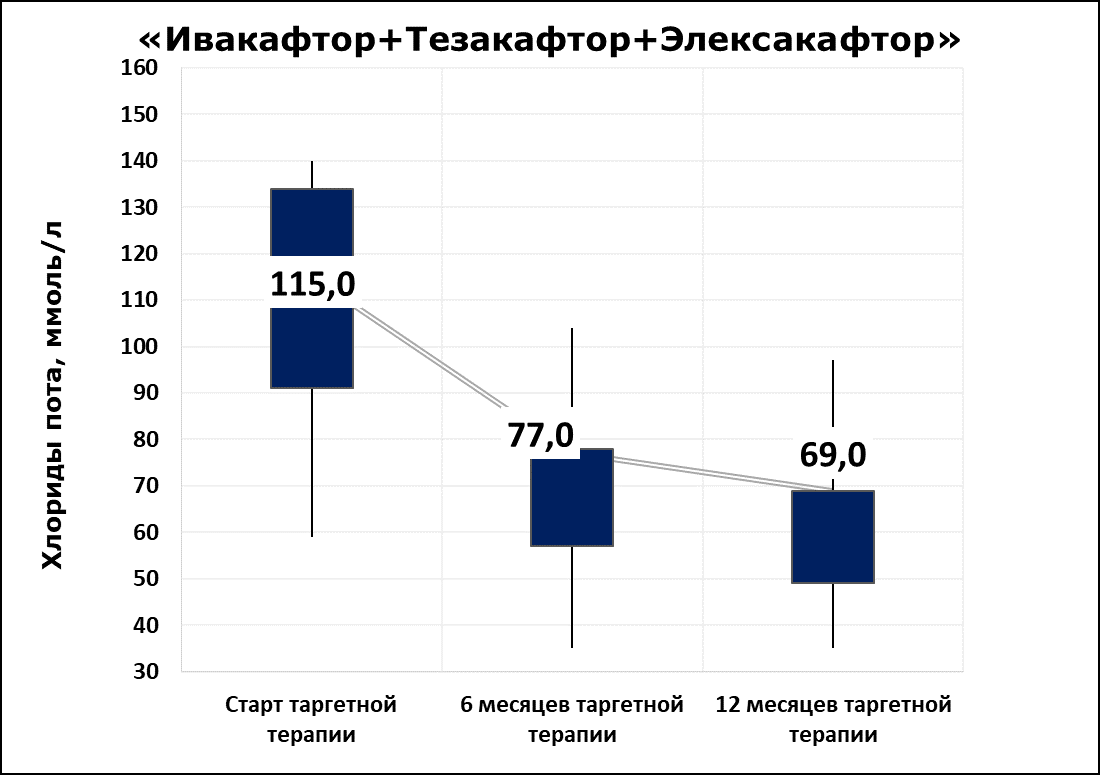
Рисунок 13 - Динамика потовой пробы на фоне таргетной терапии препаратом «Трикафта»
Примечание: Ивакафтор+Тезакафтор+Элексакафтор
4. Заключение
Уровень хлоридов пота значимо снижался у пациентов с муковисцидозом как на таргетной терапии препаратом «Оркамби», так и на таргетной терапии препаратом «Трикафта», что свидетельствует об эффективности терапии у большинства обследованных пациентов.
Пациенты с муковисцидозом детского возраста на фоне 12-месячной терапии препаратом «Трикафта» имели значимо более высокие показатели физического развития, чем пациенты на базисной терапии.
Пациенты, получающие таргетную терапию препаратом «Оркамби», имели тенденцию к улучшению показателей физического развития.
Улучшение показателей физического развития на фоне таргетной терапии, вероятно, обусловлены снижением частоты и тяжести бронхолегочных обострений и возможностью эрадикации бактериальных патогенов дыхательных путей, что показано в ряде исследований, и в меньшей степени связано с улучшением экскреторной функции поджелудочной железы .
