АДСОРБЦИЯ КОМПОНЕНТОВ БИНАРНОЙ СИСТЕМЫ Na-Cs В ЖИДКОМ И ТВЕРДОМ СОСТОЯНИЯХ
АДСОРБЦИЯ КОМПОНЕНТОВ БИНАРНОЙ СИСТЕМЫ Na-Cs В ЖИДКОМ И ТВЕРДОМ СОСТОЯНИЯХ
Аннотация
В сообщении приводятся результаты расчетов адсорбции компонентов (Na, Cs и молекул химического соединения Na2Cs) сплавов бинарной системы Na-Cs, полученных по разработанной авторами методике как в жидком, так и твердом состояниях. Величины адсорбций цезия и квазимолекулярного образования Na2Cs определяются в жидком и в твердом состояниях раствора с использованием экспериментальных данных по работе выхода электрона (РВЭ) чистых металлов и их сплавов. Установлено, что вторичные системы Na-Na2Cs и Na2Cs-Cs при температуре 183К более близки к идеальным, чем исходная бинарная система Na-Cs при температуре 300К. Показано, что адсорбции химсоединения Na2Cs и цезия в твердом состоянии сплавов меньше адсорбции цезия в жидком состоянии сплавов бинарной системы Na-Cs, что авторы связывают со значительным уходом цезия в межкристаллитное пространство в твердом поликристаллическом сплаве.
1. Введение
Сплавы и различные изделия из них используются в технике в основном в твердом состоянии , . Многие свойства сплавов, определяющие их эксплуатационные свойства зависят от состава или содержания компонентов в сплаве , , , . Особенно представляют интерес для техники такие поверхностные свойства сплавов, как смачивание , , микротвердость, коэффициент трения, износостойкость, различные виды электронной эмиссии, отражательная способность электромагнитных волн и т.д. Эти свойства сплавов тесно связаны не только с содержанием компонентов сплава в объеме, но и в его поверхностном слое , , , . Для изучения поверхностных свойств сплавов в жидком состоянии разработана прекрасная и достаточно информативная методика на основе термодинамики Гиббса , . При этом измеряемым в экспериментах параметром поверхности является поверхностное натяжение (ПН, σ(x)) в зависимости от состава xi , . Однако при переходе к изучению сплавов в твердом состоянии указанную выше методику использовать, к сожалению, не возможно из-за отсутствия надежного способа определения ПН или поверхностной энергии (ПЭ) растворов в твердом состоянии , , .
Для выхода из этой ситуации в 60-70-х годах прошлого столетия было рекомендовано (Б.В. Лазаревым, С.Н. Задумкиным и др. , ) измерить работу выхода электрона (РВЭ) в зависимости от состава xi или построить изотерму РВЭ (φ(x)) , , , . Однако, появились трудности с аналитическим описанием концентрационной зависимости не только ПН (σ(x)) , но и РВЭ (φ(x)) , , , . Во второй половине прошлого столетия С.Н. Задумкину и М.А. Кривоглазу теоретически, а затем Б.В. Лазареву и Ю.И. Малову , С.И. Попелю и В.К. Семенченко удается получить выражения зависимости РВЭ и ПН от состава раствора, а также уравнения связи между ПН и РВЭ , , , , работающие в узкой области составов – в основном для слабо концентрированных растворов, в приближении идеальных растворов.
Поиски в данном направлении были прекращены в 70-80-х годах прошлого столетия и с новой силой возобновились с получением достаточного количества экспериментальных изотерм для анализа и систематизации ПН (σ(x)) , и РВЭ (φ(x)) . Из анализа и систематизации экспериментальных изотерм ПН и РВЭ , были получены уравнения изотерм ПН и РВЭ, работающие во всем концентрационном интервале которые были использованы для расчетов поверхностных характеристик бинарных систем. В было получено уравнение, связывающее ПН (σ(x)) с РВЭ(φ(x)), описывающее концентрационную зависимость связи ПН с РВЭ во всей области составов. В настоящей работе предпринята попытка показать работоспособность полученных в , , аналитических выражений на примере надежно изученной бинарной системы Na-Cs , , , как в жидком, так и в твердом состояниях. Эти вопросы становятся еще более актуальными при переходе к малоразмерным объектам , , . Изучение РВЭ в зависимости от состава может стать одним из способов контроля качества поверхности изделия из сплава , .
Изотермы поверхностного натяжения и работы выхода электрона бинарной системы Na-Cs изучены в , , . С использованием данных в был сделан расчет адсорбции компонентов системы Na-Cs в жидком состоянии. Представляет определенный интерес оценить величину адсорбции компонентов этой же системы в твердом состоянии и сравнить результаты с данными . С другой стороны, компоненты бинарной системы Na-Cs при температуре 267 К в результате перитектической реакции между жидким раствором состава 0,7 ат.д. Cs и выпавшими кристаллами Na могут образовать химическое соединение Na2Cs . Интересно знать, как ведут себя молекулы Na2Cs в твердых растворах системы Na-Cs. Рассмотрению этих задач посвящена настоящая работа.
2. Расчет адсорбции компонентов бинарной системы Na-Cs в жидком и в твердом состояниях
Расчет адсорбции компонентов системы Na-Cs в жидком состоянии проводили в с использованием известной формулы , ,
которая, с учетом зависимости поверхностного натяжения от состава x
где σА, σВ – поверхностные натяжения чистых компонентов бинарной системы А-В, а А и В – компоненты системы, β0 и F – постоянные параметры уравнения (2), принимает для жидких растворов следующий вид
Для растворов, как в жидком, так и в твердом состояниях, когда измеряемым параметром является работа выхода электрона
где φА, φВ – работа выхода электрона чистых компонентов бинарной системы А-В, а А и В – компоненты системы, α0 – постоянный для данной бинарной системы параметр уравнения (4), уравнение (1) с учетом (4) принимает вид
Уравнения (3) и (5) позволяют вычислить адсорбцию без применения недостаточно точного способа графического дифференцирования изотерм поверхностного натяжения и работы выхода электрона с большей точностью, чем традиционный графический способ .
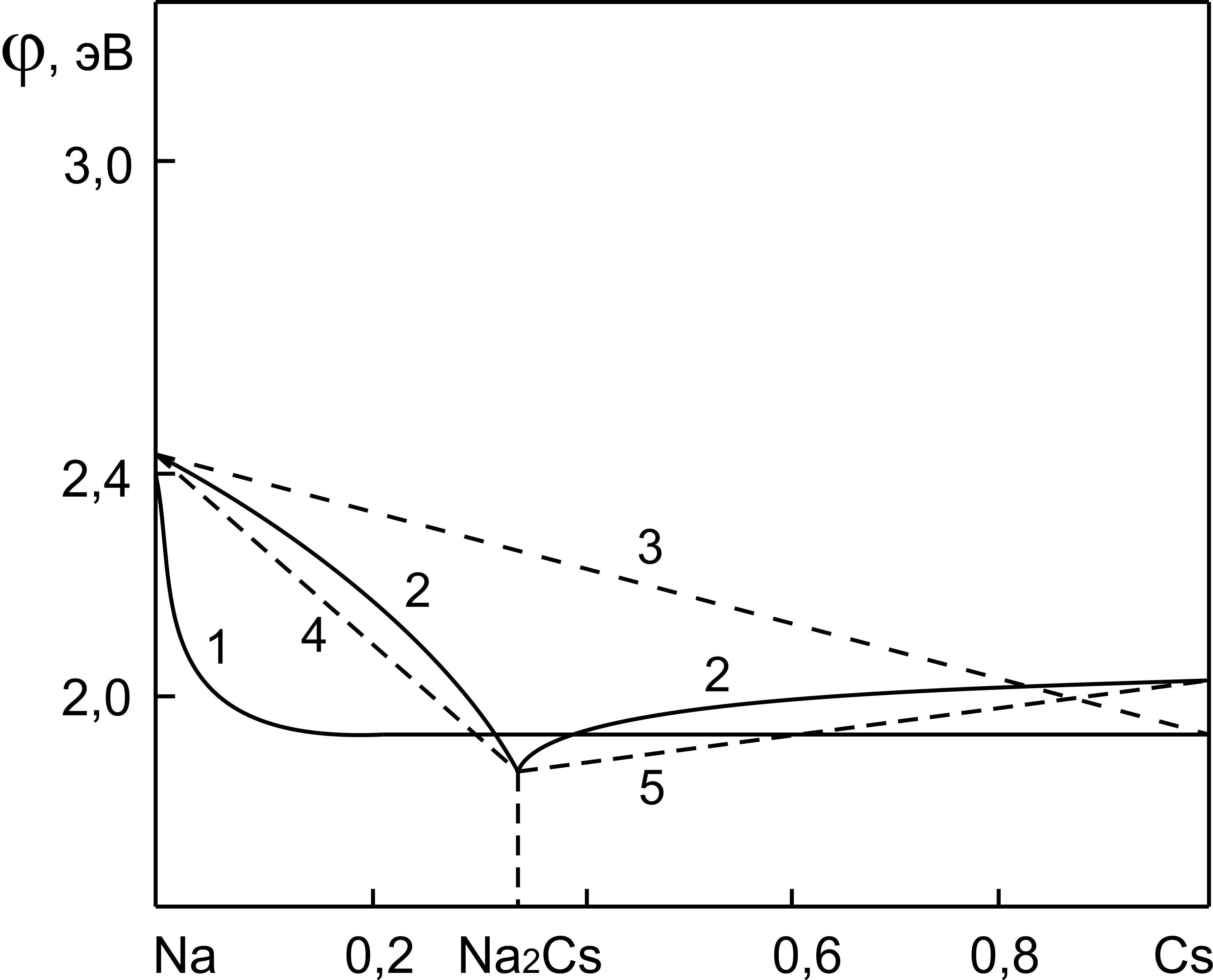
Рисунок 1 - Изотермы работы выхода электрона бинарной системы Na-Cs в жидком (1) и твердом (2) состояниях:
1, 2 - получены как результат обработки данных экспериментов; 3-5 - аддитивные прямые изотерм работы выхода электрона основной 3 (Na-Cs) и вторичных изотерм РВЭ 4 (Na-Na2Cs) и 5 (Na2Cs-Cs) систем
Примечание: по ист. [18], [25]
3. Методика расчета адсорбции компонентов системы A-B c химическим соединением A_mB_n
Для расчета адсорбции компонентов бинарной системы A-B в жидком состоянии воспользуемся известной формулой определения адсорбции в N-варианте Гуггенгейма- Адама
где
Здесь ωA и ωB – мольные площади компонентов рассматриваемой бинарной системы A-B.
Новым в данном случае в методике расчета адсорбции компонентов является то, что величину F – константу адсорбционного равновесия в настоящей работе определяют по методике
с использованием уравнения изотермы работы выхода электрона (5), представленного в видегде
Здесь
При расчетах адсорбции компонентов системы Na-Cs в твердом состоянии мы разбивали систему Na-Cs на вторичные Na-Na2Cs и Na2Cs-Cs. Для каждой вторичной системы, нами использованы выражения (4)-(6) отдельно. При этом допускали, что состав x=0,33 соответствует чистому химическому соединению Na2Cs и все добавляемые в раствор атомы цезия вступают в химическую реакцию с атомами натрия. Об этом свидетельствует резкий излом на изотерме работы выхода электрона (см. кривые 2, Рис. 1.) .
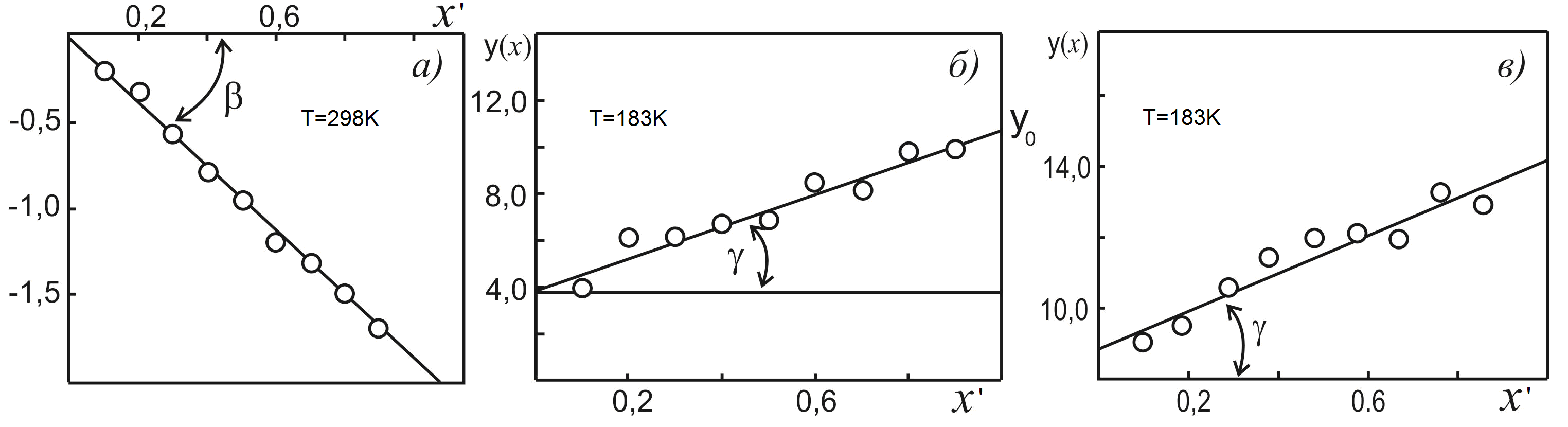
Рисунок 2 - Прямые (7) для системы Na-Cs при 298К (а) и для вторичных систем Na-Na2Cs и Na2Cs-Cs при 183К (б) и (в)
Как видно из Рис. 2, экспериментальные точки y(xi') выстраиваются в прямые линии, что свидетельствует о справедливости уравнения (4) для системы Na-Cs и вторичных систем Na-Na2Cs и Na2Cs-Cs.
Определенные из графиков Рис. 2 значения α0 и F представлены в Таблице 1.
Таблица 1 - Значения α0 и F для основной, 1 и вторичных систем 2 и 3 Na-Cs
№ | Система | α0 (тверд) | F (тверд) | β0 (жидк) | F (жидк) | Т, К |
1 | Na-Cs,РВЭ, (ПН) | -0,4 | 42,6 | -125 | 27,7 | 300(375) |
2 | Na-Na2Cs, РВЭ | 0,15 | 1,6 | — | — | 300 |
3 | Na2Cs-Cs,РВЭ | 0,19 | 1,62 | — | — | 300 |
Входные данные для расчетов для металлов ωmi(x) приведены в Таблице 2.
Таблица 2 - Входные данные для расчетов ωmi(x) для бинарных систем А-В
Металл | ρТ, кг/м3 | ρж, кг/м3 | M×103 кг/моль |
Cs | 1873 | 1802 | 132,91 |
Na | 968 | 925 | 22,99 |
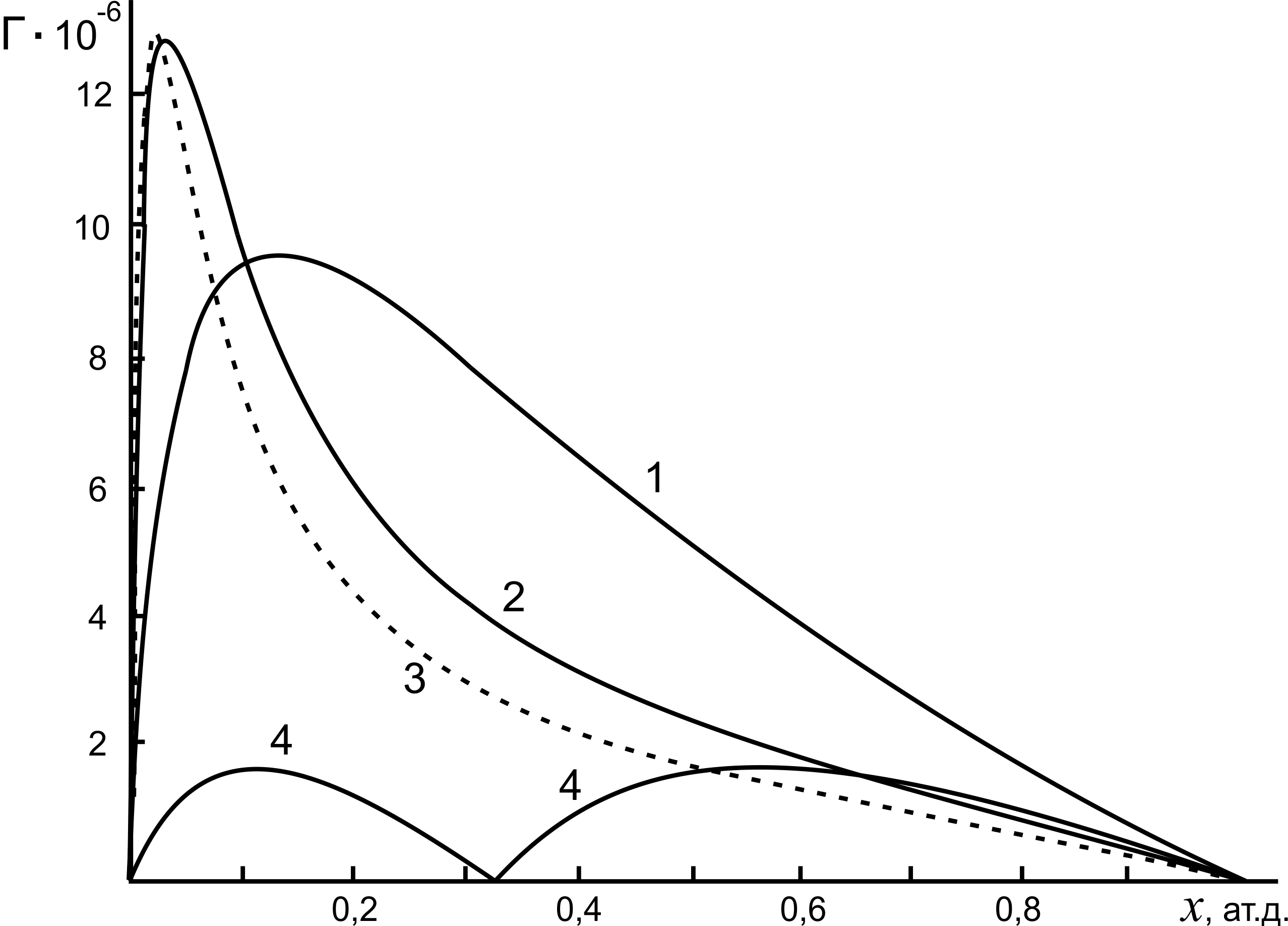
Рисунок 3 - Результаты расчетов адсорбции компонентов системы Na-Cs в твердом и жидком состояниях:
1 - адсобрция цезия в жидком состоянии в приближении реального раствора (расчет по (6)); 2 - адсобрция цезия в жидком состоянии в приближении идеального раствора (расчет по (3)); 3 - адсорбция цезия в жидком состоянии (расчет по (5)); 4 - адсорбция молекул Na2Cs и атомов цезия на поверхности твердого раствора (расчет по (6))
В твердом состоянии молекулы химического соединения Na2Cs ведут себя как самостоятельный компонент сплава : молекулы Na2Cs поверхностно-активны по отношению к Na, тогда как они же инактивны по отношению к Сs. Величины адсорбции молекул Na2Cs и атомов Cs в твердом состоянии значительно меньше адсорбции цезия в жидком состоянии (сравнить кривые 1 и 4) что, по-видимому, связано с тем, что в твердом состоянии большее количество цезия по сравнению с жидким состоянием уходит (адсорбируется) в межкристаллитное пространство твердого сплава.
4. Заключение
1. Результаты расчетов адсорбции цезия в системе Na-Cs, полученные в приближении идеальных растворов с использованием данных по поверхностному натяжению и работе выхода электрона совпадают удовлетворительно, что говорит о применимости разработанной методики расчетов адсорбции ПА компонента жидкого бинарного раствора с использованием экспериментальных данных по работе выхода электрона. Небольшая разница значений адсорбций цезия в средней области составов, по-видимому, связана с различными экспериментальными условиями получения данных σNa, σCs, φNa, φCs. Необходимо получить такие данные в одном эксперименте.
2. Сравнение результатов расчетов адсорбции цезия, полученных в приближении реальных растворов с данными, полученными в приближениях идеальных растворов, показывает, как и ожидалось, удовлетворительное их совпадение в областях с малым содержанием компонентов. А в областях, богатых компонентами эти различия значительные, что связано с ярко выраженной неидеальностью бинарной системы Na-Cs.
3. Использование уравнения изотермы поверхностного натяжения для расчетов адсорбции компонентов возможно только для жидких растворов. Уравнение изотермы работы выхода электрона может быть использовано как для жидких растворов, так и для растворов в твердом состоянии.
4. Адсорбции компонентов Na, Cs, Na2Cs в твердых растворах вторичных систем значительно ниже адсорбции цезия в жидком и в твердом состоянии растворов. Это означает, что вторичные системы Na-Na2Cs и Na2Cs-Cs более близки к идеальным, чем исходная бинарная система Na-Cs.
5. Квазимолекулярные образования (КМО) типа AmBn, которые могут быть образованы в бинарных системах, ведут себя как отдельные компоненты, способствуя разделению исходной системы А-В на составляющие вторичные системы А-AmBn и AmBn-В. К каждой вторичной системе, для описания поверхностных характеристик, может быть применено уравнение изотермы поверхностного натяжения, или работы выхода электрона.
Обнаружен интересный результат. Параметр Fдля твердого состояния (Fтв=42,6) больше параметра F для жидкого состояния (Fж=27,7). А адсорбция цезия в твердом состоянии меньше адсорбции цезия в жидких растворах. Очевидно, это связано с разными скоростями протекания процессов в поверхностном слое жидкого и твердого раствора. Процесс адсорбции в жидком растворе протекает легко и быстро. А в твердом растворе процесс перераспределения компонентов затруднен и протекает медленнее, в результате чего в системе не наступает состояниt полного равновесия, а профиль распределения компонентов в приповерхностном слое может быть другим. Для понимания таких результатов, очевидно, необходимы специальные исследования.
