ПРИМЕНЕНИЕ РАЗЛИЧНЫХ КОСТНОПЛАСТИЧЕСКИХ МАТЕРИАЛОВ ПРИ ПРОВЕДЕНИИ КОСТНОЙ ПЛАСТИКИ АЛЬВЕОЛЯРНОГО ОТРОСТКА У ПАЦИЕНТОВ С ВРОЖДЕННЫМИ РАСЩЕЛИНАМИ ВЕРХНЕЙ ГУБЫ, АЛЬВЕОЛЯРНОГО ОТРОСТКА И НЕБА
Карачунский Г.М.¹, Сипкин А.М.2, Тонких-Подольская О.А.3
1ORCID: 0000-0003-2639-0986, кандидат медицинских наук, н.с. отделения челюстно-лицевой хирургии,
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского.
2ORCID: 0000-0001-8287-741X, доктор медицинских наук, профессор кафедры челюстно-лицевой хирургии и хирургической стоматологии ФУВ ГБУЗ МО МОНИКИ им. М. Ф. Владимирского,
ведущий научный сотрудник отделения челюстно-лицевой хирургии ГБУЗ МО МОНИКИ.
3ORCID: 0000-0001-8098-9629, очный аспирант кафедры челюстно-лицевой хирургии и хирургической стоматологии, ФУВ ГБУЗ МО МОНИКИ им. М. Ф. Владимирского
ПРИМЕНЕНИЕ РАЗЛИЧНЫХ КОСТНОПЛАСТИЧЕСКИХ МАТЕРИАЛОВ ПРИ ПРОВЕДЕНИИ КОСТНОЙ ПЛАСТИКИ АЛЬВЕОЛЯРНОГО ОТРОСТКА У ПАЦИЕНТОВ С ВРОЖДЕННЫМИ РАСЩЕЛИНАМИ ВЕРХНЕЙ ГУБЫ, АЛЬВЕОЛЯРНОГО ОТРОСТКА И НЕБА
Аннотация
Врожденные расщелины верхней губы, альвеолярного отростка и неба составляют более 86% аномалий челюстно-лицевой области и 13% всех врожденных пороков развития.
Важным этапом комплексного лечения пациентов с врожденными расщелинами верхней губы, альвеолярного отростка и неба, является костная пластика альвеолярного отростка, направленная на стабилизацию фрагментов верхней челюсти, достигнутого предоперационного ортодонтического результата, а также создание условий, направленных на восстановление зубного ряда.
В данной статье будут рассмотрены различные виды костнопластических материалов, применяемые при костной пластике альвеолярного отростка у пациентов с врожденными расщелинами.
Ключевые слова: врожденная патология челюстно-лицевой области, расщелина альвеолярного отростка, костная пластика, хирургическое лечение.
Karachunskiy G.M.¹, Sipkin A.M.2, Tonkikh-Podolskaya O.A.3
1ORCID: 0000-0003-2639-0986 – MD, Research Associate of the Department of Oral Surgery of SBHI of Moscow Regional Research and Clinical Institute named after M.F. Vladimirsky
2ORCID: 0000-0001-8287-741X – MD, Professor of the Department of Oral Surgery and Surgical Dentistry of SBHI of Moscow Regional Research and Clinical Institute named after M.F. Vladimirsky, Leading Research Assistant of the Department of Oral Surgery of SBHI of Moscow Regional Research and Clinical Institute named after M.F. Vladimirsky
3ORCID: 0000-0001-8098-9629 – Postgraduate Student of the Department of Oral Surgery and Surgical Dentistry of SBHI of Moscow Regional Research and Clinical Institute named after M.F. Vladimirsky
USE OF VARIOUS OSTEOPLASTIC MATERIALS IN OSTEOPLASTY OF ALVEOLAR BONE AMONG PATIENTS WITH CONGENITAL GAPS OF THE UPPER LIP, ALVEOLAR BONE AND PALATE
Abstract
Congenital gaps of the upper lip, alveolar bones and palate account for more than 86% of oral surgery anomalies and 13% of all congenital malformations.
The osteoplasty of the alveolar bone aimed at stabilizing the fragments of the maxilla, achieving preoperative orthodontic result and creating conditions for dentition restoration is an important stage in the complex treatment of patients with congenital gaps of the upper lip, alveolar bone and palate.
In this article, we consider various types of osteoplastic materials used in osteoplasty of the alveolar bone among patients with congenital gap.
Keywords: congenital pathology of the oral surgery area, alveolar bone gap, osteoplasty, surgical treatment.
Врожденные расщелины верхней губы, альвеолярного отростка и неба составляют более 86% аномалий челюстно-лицевой области и 13% всех врожденных пороков развития [4, С. 233–234], [8, С. 127], [26, С. 14–17], [36, С. 1773–1785].
Как всем известно, расщелины появляются на четвертом этапе внутриутробного развития (на 28-55 день эмбриогенеза). Место их появления определяется участками, где не произошло сращение различных лицевых отростков. Поскольку сращение медианного носового отростка в процессе формирования первичного неба создает губу и область альвеолярного отростка, содержащую центральные и боковые резцы, расщелина губы сопровождает расщелину альвеолярного отростка, даже если расщелины неба не наблюдается [8, С. 127], [26, С. 14–17], [27, С. 22–26].
У пациентов с врожденной расщелиной альвеолярного отростка, имеется ряд клинико-анатомических особенностей, значительно затрудняющих возмещение костного дефекта, таких как: уплощение фронтального отдела верхней зубной дуги, поворот по оси центрального резца, граничащего с расщелиной, врожденная адентия латерального резца или наличие сверхкомплектных зубов в области расщелины, смещение фрагментов верхней челюсти относительно друг друга, значительный диастаз между фрагментами верхней челюсти, истончение краев фрагментов. При врожденной полной двусторонней расщелине губы, альвеолярного отростка и неба на ряду с выше изложенными особенностями отмечается также смещение передних участков боковых фрагментов верхней челюсти медиально, что ведет к симметричной деформации верхней челюсти и ее сужению. Таким образом, при лечении пациентов с данной патологией, основными задачами хирурга при проведении костной пластики альвеолярного отростка являются: восстановление целостности альвеолярного отростка, стабилизация ортодонтического результата, создание объема для последующей дентальной имплантации в рамках восстановления зубного ряда, восстановление формы грушевидного отверстия в области апикального базиса альвеолярного отростка верхней челюсти для опоры крыльев носа перед корригирующей ринохейлопластикой [1, С. 95–96], [5, С. 24–27], [7, С. 248–249], [8, С. 127].
В настоящее время остается обсуждаемым возраст проведения данного оперативного вмешательства. Многие авторы сходятся во мнении, что возраст 8-12 лет является наиболее оптимальным для проведения костной пластики альвеолярного отростка в области расщелины, так как способствует прорезыванию постоянного клыка в область регенерата в правильном положении. Исследования отдаленных результатов показали, что при проведении костной пластики альвеолярного отростка в период сменного прикуса (до прорезывания клыка), у 90% детей происходит самостоятельное закрытие дефекта. В тоже время у 10% этих пациентов закрытие дефекта невозможно из-за недоразвитости средней зоны лица, вызванной недостаточным ростом верхней челюсти, или отсутствием более одного зуба в области расщелины и связанных с этим проблем с адекватной ортодонтической опорой [3, С. 151–155], [10, С. 113], [38, С. 156].
Для достижения успешного результата при проведении костной пластики альвеолярного отростка необходимо соблюдение основных хирургических принципов, которые включают: достаточный объем мягких тканей для сопоставления краев раны без натяжения; применение костных блоков при значительном дефекте альвеолярного отростка (при диастазе более 4 мм); наличие спонтанного; стабилизация положения трансплантата; максимальная конгруэнтность трансплантата и реципиентного ложа; отграничение костнопластического материала от мягких тканей [21, С. 284–290].
Механизм регенерации костнопластического материала
В течение первых трех–четырех недель после пересадки трансплантата протекают процессы остеогенеза и остеокондукции. [13, С. 388–428].Остеокласты инициируют замещение неорганизованной рыхлой кости на более минерализованную и структурно более организованную кость. В ходе данного цикла формируется надкостница и эндостальная прослойка, и трансплантат замещается плотной, губчатой структурой [21, С. 284–290].Различные костнопластические материалы содержат различные факторы роста, обладают остеокондуктивными и остеоиндуктивными свойствами, а так же содержат различный объем губчатой и кортикальной костной ткани, соответственно образование регенерата из костнопластического материала происходит разными механизмами регенерации [13, С. 388-428].Аутогенные костные содержат стволовые клетки, факторы роста и дифференциации, вступающие в химические связи с белками аутогенной костной матрицы. Таким образом, использование аутогенной кости в виде стружки обеспечивает большую площадь поверхности для миграции клеток-предшественников, что считается оптимальным [41, С. 636–641], [43, С. 195–229].
Биологическая интеграция неваскуляризованных костных блоков характеризуется их полным разрушением остеокластами и образованием новой костной ткани в результате деятельности остеобластов. Axhausen, Urist и Von Arx называют этот процесс наползающим замещением [13, С. 388-428], [17, С. 136–159], [21, С. 284–290].
В настоящее время золотым стандартом являются трансплантаты гребня подвздошной кости, так как они отличаются большим объемом остеогенных клеток, обеспечивающих высокий регенеративный потенциал. Из данной кости можно получить трансплантат большого объема кости. Однако в этой области преобладает губчатая ткань, кортикально-губчатые трансплантаты гребня подвздошной кости сопоставимы с типом кости D3/D4 по классификации Misch и резорбция трансплантатов подвздошной кости происходит также быстрее, даже при функциональной нагрузке со стороны имплантатов и может продолжаться несколько лет [21, С. 284–290]. Так же в раннем послеоперационном периоде отмечается нарушение походки пациента и выраженный болевой синдром.
Другой донорской зоной является область ветви нижней челюсти, в данной области можно получить достаточный объем костного (так как можно производить забор с обеих сторон челюсти), аутотрансплантат содержит достаточный объем кортикального вещества и факторов роста [19, С. 1320-1326], [20, С. 536-542], [34, C. 3–9], [41, С. 28].
При использовании в качестве донорской зоны области подбородочного симфиза костный трансплантат обычно получают с помощью трепанов (7-12 мм) и формируют до четырех цилиндрических трансплантатов. Забор аутокости в данной области может сопровождаться относительно выраженным болевым синдромом, количество доступной кости в этой зоне, как правило, ограниченно, а риск повреждения резцовой ветви нижнего альвеолярного нерва очень высок.
Взятие трансплантата из области бугра верхней челюсти сопровождается меньшей болезненностью, но эффективность костных трансплантатов из этой зоны пока недостаточно изучена, а качество и количество доступной кости часто не удовлетворяют клиническим требованиям.
Кортикальная пластинка костей черепа характеризуется наиболее высокой плотностью костной ткани по сравнению с другими костями скелета. Трансплантат чаще получают из теменной кости по обе стороны от сагиттального шва, он представляет собой каркас только из очень плотной кортикальной кости, которая не подвергается значительной резорбции. [18, С. 56]. Кортикальная кость содержит много факторов роста и костных морфогенетических протеидов, включенных в костный матрикс. Тем не менее забор кости в данной области может быть связан с жизнеугрожающими осложнениями [40, С. 28].
В качестве аллогенного костнопластического материала чаще всего используют деминирализованный фрагмент свода, содержащий остеокондуктивные материалы, биологическая активность которых зависит от способа его стерилизации. При использовании неаутогенного костного материала, необходимо учитывать, что в некоторых случаях может возникнуть асептическая воспалительная реакция, что в свою очередь стимулирует деятельность макрофагов, регулирующих иммунный ответ [11, С. 79].
В случаях, когда пациенты принципиально предпочитают синтетические материалы, можно использовать двухфазный гидроксиапатит с трикальцийфосфатом. Оба указанных материала обладают остеокондуктивными свойствами, т.е. способствуют медленному аппозиционному росту кости по направлению от костных стенок дефекта в толщу сгустка [29, С. 24]. Эффективность этого процесса зависит от возможности прорастания кровеносных сосудов между частицами материала [30, С. 752–760]. Однако аппозиционный рост кости спонтанно прекращается на расстоянии нескольких миллиметров от стенок дефекта. Для увеличения глубины врастания сосудов в костный материал и создания условий для последующей оссификации необходимо использовать мембраны [22, С. 185-191]. С целью придания используемому материалу остеоиндуктивных свойств, необходимо добавление аутогенной костной стружки [15, С. 78], [16, С. 441], [29, С. 24].
Не менее обсуждаемым вопросом является необходимость применения мембран, с целью минимизирования воздействия мягких тканей. Хотелось бы отметить, что по данным литературы мембрана не только обеспечивает барьерную функцию, но и способствует стабилизации кровяного сгустка и костных материалов в пространстве дефекта [28, С. 487-498]. Кроме того, она замедляет поверхностную резорбцию трансплантата [22, С. 185-191], препятствуя проникновению предшественников остеокластов со стороны надкостницы и стимулируют внутреннее ремоделирование костного блока [45, С. 10].
Ниже приводятся характеристики мембран применяемых при костной пластике:
Материалом для нерезорбируемой мембраны является расширенный политетрафторэтилен (ПТФЭ). Данная мембрана - жесткая, что способствует фиксации костно-пластического материала и минимизированию давления на него мягких тканей [29, С. 24]. Данный материал не подвергаются резорбции, в связи, с чем необходимо ее удаление между 21-м и 25-м днём, но не позже, чем через 28 дней после операции. При применении данных мембран отмечается высокий риск преждевременного прорезывания, а также провоцирование расхождения краев раны и инфицирование ее [18, С. 1065–1073].
Резорбируемая коллагеновая мембрана свиного происхождения без перекрестных сшивок, характеризуется выраженной гидрофильностью и хорошо взаимодействует с фибрином кровеносного сгустка. Кроме того, быстрое пропитывание мембраны облегчает ее клиническое применение [23, С. 203–213], [42, С. 359–366], поскольку устраняет необходимость фиксации кнопками или винтами. По сравнению с мембранами из расширенного политетрафторэтилена (р-ПТФЭ) при использовании коллагеновых мембран края раны расходятся реже [29, С. 24], но данные мембраны имеют недостаточную жесткость. В связи с этим для поддержки мембраны под нее рекомендуется вводить наполнитель. Также к недостаткам коллагеновых мембран можно отнести довольно высокую скорость резорбции (4-8 недель), в результате непрерывной активности протеолитических ферментов), поэтому некоторые авторы рекомендуют устанавливать их в два слоя [14, С. 420–432.].
Целью данной статьи является сравнение костнопластических материалов применяемых при костной пластике альвеолярного отростка у пациентов с врожденными расщелинами верхней губы, альвеолярного отростка и неба.
Материалы и методы
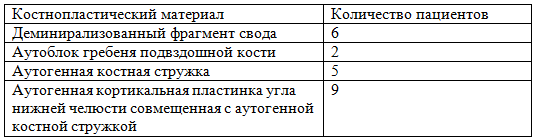
В период с 2011 по 2017 г. в отделении челюстно-лицевой хирургии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского проведено 21 оперативное вмешательство – костная пластика альвеолярного отростка у 19 пациентов, у 17 пациентов отмечалась односторонняя расщелина, 2 пациентов двухсторонняя расщелина альвеолярного отростка [табл.1]. Возраст больных составил от 8 до 22 лет.
В случае двухсторонних расщелин оперативное лечение проводилось в два этапа, с промежутком в 6 месяцев. В качестве костнопластического материала применялся: Деминирализованный фрагмент свода, Аутоблок гребеня подвздошной кости, Аутогенная костная стружка, а также аутогенная кортикальная пластинка угла нижней челюсти, совмещенная с аутогенной костной стружкой и использование PRF аутомембраны.
Таблица 1 – Костнопластические материалы применявшиеся при костной пластике альвеолярного отростка у пациентов с врожденной расщелиной верхней губы, альвеолярного отростка и неба
Предоперационное обследование пациентов включало: Наблюдение и лечение ортодонта. клинический осмотр, лабораторное обследование (общий анализ крови, биохимический анализ крови, общий анализ мочи, электрокардиограмма). Рентгенологическое обследование (компьютерная томография лицевого скелета).
После предоперационного обследования в условиях стационара пациентам проводилась костная пластика альвеолярного отростка по классическому протоколу.
Послеоперационный контроль включал компьютерную томографию через 6 месяцев, 1 год и более после операции [табл.2].
Результат
Отличным оценивался результат, при условии, что степень резобции костнопластического материала составляла менее 20% , хорошим считался результат, если степень резорбции костнопластического материала составляла от 20% до 70%. Данные результаты отмечались в 10 клинических случаях: в качестве костнопластического материала применялась аутогенная кортикальная пластинка угла нижней челюсти, с последующим заполнением остаточного дефекта совмещенной измельченной аутокостью с гранулированным бета трикальций фосфата, после чего производилось отграничение от мягких тканей посредствам мембраны - в 9 клинических случаях. В 1 клиническом случае в качестве костнопластического материала применялся гребень подвздошной кости.
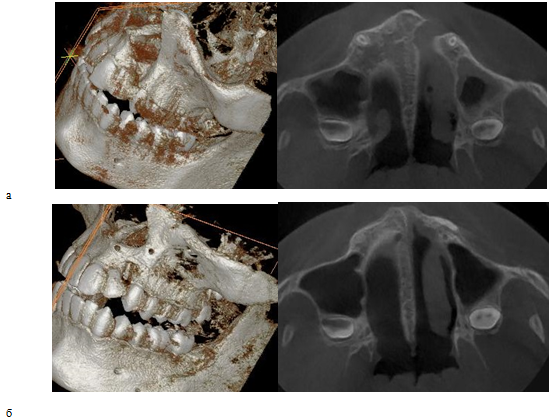
Рис. 1 – Пациент Ш. 16 лет. а) Клиническая картина перед костной пластикой альвеолярного отростка. б) послеоперационный контроль через 6 месяцев после костной пластики альвеолярного отростка, в качестве костнопластического материала использовалась аутогенная кортикальная пластинка угла нижней челюсти, совмещенная с измельченной аутокостью
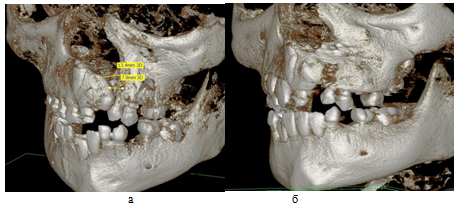
Рис. 2 – Пациентка С. 6 лет а) Клиническая картина перед костной пластикой альвеолярного отростка;
б) послеоперационный контроль через 6 месяцев после костной пластики альвеолярного отростка, в качестве костнопластического материала использовался аутогенная кортикальная пластинка угла нижней челюсти, совмещенная с измельченной аутокостью
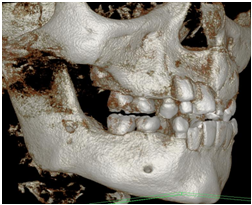
Рис. 3 – Область взятия аутогенной кортикальной пластинки угла нижней челюсти, через 6 месяцев после операции
Удовлетворительным оценивался результат при условии, что степень резобции костнопластического материала составляла от 70% до 90% и наблюдался в 5 клинических случаях: в качестве костнопластического материала применялась измельченная аутокость смешанная с гранулированным бета трикальций фосфата в 4 клинических случаях, и фрагмент свода черепа в 1 клиническом случае.
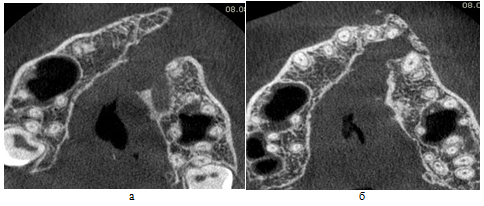
Рис. 4 – Пациентка 16 лет. а) клиническая картина перед костной пластикой альвеолярного отростка;
б) послеоперационный контроль через 3 года после костной пластики альвеолярного отростка, в качестве костнопластического материала использовался деминирализованный свод черепа
Неудовлетворительным оценивался результат при условии, что степень резобции костнопластического материала составляла более 90% до полной резорбции костнопластического материала, данный результат отмечался в 6 клинических случаях. В качестве костнопластического материала применялась деминирализованный фрагмент свода черепа - в 4 клинических случаях, и измельченная аутокость смешанная с гранулированным бета трикальций фосфата - в 1 клиническом случае.
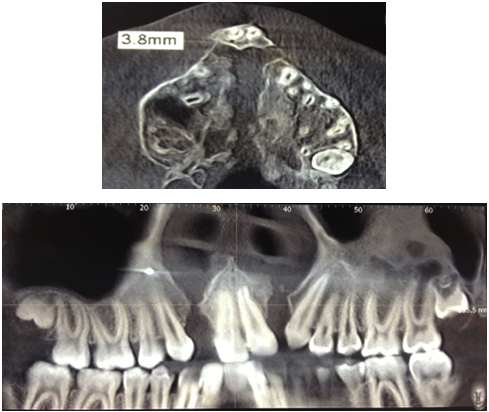
Рис. 5 – Пациент П. 17 лет послеоперационный контроль через 3 года после костной пластики альвеолярного отростка, в качестве костнопластического материала использовался деминирализованный свод черепа слева и справа
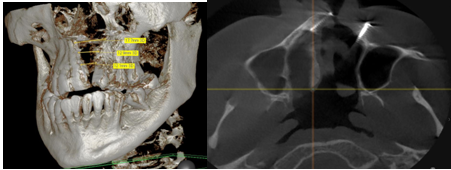
Рис. 6 – Пациентка К. 21 год. Послеоперационный контроль через 3 года после костной пластики альвеолярного отростка, в качестве костнопластического материала использовался фрагмент деминирализованного свода черепа
Отторжение костнопластического материала отмечалось в 2 клинических случаях: в 1 случае в качестве костнопластического материала применялся деминирализованный фрагмент свода черепа, в 1 клиническом случае аутогенный гребень подвздошной кости, данные случаи были оценены и отнесены к неудовлетворительному результату.
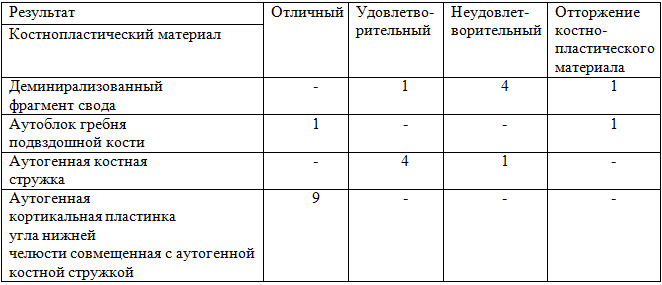
Таблица 2 – Степень резорбции различных костнопластических материалов при проведении костной пластике у пациентов с врожденной расщелиной верхней губы, альвеолярного отростка и неба
Выводы
Таким образом на основании данных проведенного после операционного клинико-инструментального обследования, через 3,6 месяцев и более после операции, а так же на основании проведенного анализа литературы, наиболее эффективно применение в качестве костно-пластического материала, в ходе костной пластики альвеолярного отростка верхней челюсти у пациентов с расщелинами верхней губы, альвеолярного отростка и неба, аутогенной кортикальной пластинки угла нижней челюсти, обладающей высокой плотностью костной ткани, с последующем заполнением остаточного дефекта измельченной аутокостью совмещенной с гранулированным бета трикальций фосфата (данная смесь обладает остеокондуктивными и остеоиндуктивными свойствами), с последующим отграничением костнопластического материала по средствам мембран.
Список литературы/ References
- Арсенина О.И., Ортодонтические мероприятия в комплексном лечении пациентов с врожденной расщелиной губы и неба / Арсенина О.И., Пащенко Е.И. //Материалы Всерос. конф. «Функционально-эстетическая реабилитация больных с врожденными расщелинами лица».- 2002.- С. 95–96.
- Коротких Д. В, Парфенова А. А. Удар по кризису A-PRF / Коротких Д. В, Парфенова А. А. // Практика имплантологa - 2015.-№9-С.60-63.
- Мамедов Ад.А. Алгоритм реабилитации детей с врожденной расщелиной верхней губы и неба / Мамедов Ад.А. // Врожденная и наследственная патология головы, лица и шеи у детей: актуальные вопросы комплексного лечения. - 2002.- С. 151-155.
- Никитин А.А. Лечение детей раннего возраста с расщелинами верхней губы, альвеолярного отростка и неба аппаратом с устройством из металла с памятью формы./ Никитин А.А., Егорова М.В., Карачунский Г.М. // Материалы III Всерос. научно-практ. конф. «Врожденная и наследственная патология головы, лица и шеи у детей: актуальные вопросы комплексного лечения» (8–10 сентября 2009 г.). МГМСУ -2009.- С.233–234.
- Польма JI.B. Коррекция неправильного положения языка у пациентов с врожденной расщелиной языка, альвеолярного отростка и неба./ Польма JI.B., Киселева Е.В., Агаева В.Е., Надточий А.Г. // Ортодонтия. – 2004. 2(26) - С.24- 27.
- Рубцова Н.В. Сравнительная оценка результатов хирургического лечения детей с врожденными односторонними сквозными расщелинами неба./ Рубцова Н.В. //Автореф. дис. .канд. мед. наук. - 2006. – С.24-27.
- Рягузова Е.Н.Применение модифицированного несъемного аппарата Latham R.A. при врожденной протрузии межчелюстной кости у детей с врожденной полной двусторонней расщелиной верхней губы и неба. / Рягузова Е.Н., Матюнин В.В., Дьякова С.В. //Материалы III Всерос. научнопаркт. конф.: «Врожденная и наследственная патология головы, лица и шеи у детей: актуальные вопросы комплексного лечения» (8–10 сентября 2009 г.). МГМСУ -2009.- С.248–249.
- Старикова Н.В. Раннее ортопедическое лечение детей с врожденной двусторонней расщелиной верхней губы и неба / Старикова Н.В. // Автореф. дис. канд. мед. наук.- 2006.- С.127.
- Цепколенко В. PRP- стимуляция синтеза коллагена I типа в коже человека: плацебо-контролируемое исследование in vivo / Цепколенко В., Суровяк П. // Вестник эстетической медицины. – 2012. – Т. 11.- № 3. – С.17–24.
- Чуйкин С.В. Реабилитация детей с врожденной расщелиной верхней губы и неба / Чуйкин С.В., Давлетшин Н.А. // Автореф. дис. .канд. мед. наук. - 2009. –C. 113.
- Anderson G. C. et al. Research diagnostic criteria for temporomandibular disorders: Future directions //Journal of orofacial pain. – 2010. – V. 24. – №. 1. – P. 79.
- Anitua E. Effectiveness of autologous preparation rich in growth factors for the treatment of chronic cutaneous ulcers / Anitua E. et al. //Journal of Biomedical Materials Research Part B: Applied Biomaterials. – 2008. – V. 84. – №. 2. – P. 415-421.
- Axhausen G. Histologische Untersuchungen über Knochentransplantation am Menschen / Axhausen G. //Dtsch Z Chir. – 1907. – V. 91. – P. 388-428
- Buser D. et al. Lateral ridge augmentation using autografts and barrier membranes: a clinical study with 40 partially edentulous patients / Buser D. //Journal of oral and maxillofacial surgery. – 1994. – V. 54. – №. 4. – P. 420-432.
- Buser D., Dahlin C., Schenk R. K. Guided bone regeneration //Chicago Quintessence. – 1994.
- Buser D. Early implant placement following single-tooth extraction in the esthetic zone: biologic rationale and surgical procedures / Buser D. et al. //The International journal of periodontics & restorative dentistry. – 2008. – V. 28. – №. 5. – P. 441.
- Chiapasco M. Augmentation procedures for the rehabilitation of deficient edentulous ridges with oral implants / Chiapasco M., Zaniboni M., Boisco M. //Clinical oral implants research. – 2006. – V. 17. – №. 2. – P. 136-159.
- Chiapasco M. Long term outcome of implants placed with guided bone regeneration (GBR) using resorbable and non resorbable membranes after 12–14 years / Chiapasco M., Jung R. E. et al //Clinical Oral Implants Research. – 2013. – V. 24. – №. 10. – P. 1065-1073.
- Cordaro, L. Mandibular bone harvesting for alveolar reconstruction and implant placement: subjective and objective cross sectional evaluation of donor and recipient site up to 4 years./ Cordaro, L., Torsello, F., Tindara Miuccio, M., Mirisola di Torresanto, V., & Eliopoulos, D. //Clinical oral implants research.-2011. V 22(11).- P.1320-1326.
- Cordaro L. Single unit attachments improve periimplant soft tissue conditions in mandibular overdentures supported by four implants. / Cordaro L. et al. //Clinical oral implants research. – 2013. – V. 24. – №. 5. – P. 536-542.
- Cordaro L. ITI Treatmen Guide / Cordaro L., Terheyden H. //Ridge augmentation Procedures in Implant Patients. A Staged Approach. Chen S, Buser D, Wismeijer. – 2014.-V. 7.-P.284-290.
- Donos N.Alveolar ridge augmentation by combining autogenous mandibular bone grafts and non resorbable membranes./ Donos N., Kostopoulos L., Karring T. //Clinical Oral Implants Research. – 2002. – V. 13. – №. 2. – P. 185-191.
- Donos N. Alveolar ridge augmentation using a resorbable copolymer membrane and autogenous bone grafts / Donos N., Kostopoulos L., Karring T. //Clinical Oral Implants Research. – 2002. – V. 13. – №. 2. – P. 203-213.
- Ehrenfest D. Classification of platelet concentrates: from pure platelet!rich plasma (P-PRP) to leucocyte- and platelet-rich fibrin (L-PRF) / Ehrenfest D., Rasmusson L, Albrektsson T. // Trends Biotechnol. – 2009. –V 27 (3). – P. 158-67.
- Ehrenfest D.M.In search of a consensus terminology in the field of platelet concentrates for surgical use: platelet-rich plasma (PRP), platelet-rich fibrin (PRF), fibrin gel polymerization and leukocytes / Ehrenfest D.M., Bielecki T., Mishra A., et.al. //Current pharmaceutical biotechnology. – 2012. – V. 13. – №. 7. – P. 1131-1137.
- Heinrich A.Prenatal diagnostics of cleft deformities and its significance for parent and infant care./ Heinrich A., Proff P., Michel Т., Ruhland F., Kirbschus A., Gedrange T. // J. of CranioMaxiillofac.Surg. 2006. - V.34. -P. 14- 17.
- Hemprich A. The functionally based Leipzig concept for the treatment of patients with cleft lip, alveolus and palate./ Hemprich A., Frerich В., Hierl Т., Dannhauer K.-H. // J. of CranioMaxiillofac.Surg.- 2006. - V.34. - №.2. - P. 22 - 26.
- Hockers T. The combined use of bioresorbable membranes and xenografts or autografts in the treatment of bone defects around implants. A study in beagle dogs / Hockers T. et al. //Clinical oral implants research. – 1999. – V. 10. – №. 6. – P. 487-498.
- Jensen S. S. Bone augmentation procedures in localized defects in the alveolar ridge: clinical results with different bone grafts and bone-substitute materials / Jensen S. S., Terheyden H. //International Journal of Oral & Maxillofacial Implants. – 2009. – V 24.
- Karageorgiou V. Porosity of 3D biomaterial scaffolds and osteogenesis / Karageorgiou V., Kaplan D. //Biomaterials. – 2005. – V. 26. – №. 27. – P. 5474-5491
- Keyhan S.Use of Platelet-Rich Fibrin and Platelet- Rich Plasma in Combination With Fat Graft: Which Is More Effective During Facial Lipostructure? / Keyhan S., Hemmat S.,Badri A., Khiabani K. // J. Oral Maxillofac Surg. – 2013. – V. 71. – P. 610–621.
- Krasna M. Platelet gel stimulates proliferation of human dermal fibroblasts in vitro / Krasna M., Domanović D., Tomsic A., Svajger U. et al. // Act. Dermatovenerol. Alp. Panonica Adriat. – 2007. – V.16 (3). – P. 105–110.
- Leitner G. C. Platelet content and growth factor release in platelet‐rich plasma: a comparison of four different systems / Leitner G. C. et al. //Vox sanguinis. – 2006. – V. 91. – №. 2. – P. 135-139.
- Marx R. E. A comparison of particulate allogeneic and particulate autogenous bone grafts into maxillary alveolar clefts in dogs / Marx R. E. et al. //Journal of Oral and Maxillofacial Surgery. – 1984. – V. 42. – №. 1. – P. 3-9.
- Marx R. Platelet- rich plasma: growth factor enhancement for bone grafts / Marx R., Carlson E., Eichstaedt R., Schimmele S. et al.// Oral Surg Oral Med Oral Pathol Oral Radiol Endod. – 1998. – V. 85. – P. 638–646.
- Mossey P. A. Cleft lip and palate / Mossey P. A. et al. //The Lancet. – 2009. – Т. 374. – №. 9703. – P. 1773-1785.
- Matras H. The use of fibrin sealant in oral and maxillofacial surgery / Matras H. //J. Oral Maxillofac Surg. – 1982. – V40. – P. 617.
- Ross R. B. Treatment variables affecting growth in unilateral cleft lip and palate. / Ross R. B. //Part 5: timing of palate repair. – 2006.-P. 156
- Sammartino, G. Use of autologous plateletrich plasma (PRP) in periodontal defect treatment after extraction of impacted mandibular third molars / Sammartino, G., Tia M., Marenzi G., di Lauro A., et al. // J. OralMaxillofac Surg. – 2005. – V.63. – P. 766.
- Scheerlinck E. Donor site complications in bone grafting: comparison of iliac crest, calvarial, and mandibular ramus bone / Scheerlinck E. et al. //International Journal of Oral & Maxillofacial Implants. – 2013. – №. 1.-.P. 28.
- Schwartz-Arad D. Intraoral autogenous block only bone grafting for extensive reconstruction of atrophic maxillary alveolar ridges / Schwartz-Arad D., Levin L. //Journal of periodontology. – 2005. – V. 76. – №. 4. – P. 636-641.
- Von Arx T. Horizontal ridge augmentation using autogenous block grafts and the guided bonebregeneration technique with collagen membranes/ A clinical study with 42 patients / Von Arx T, Buser D. // Clin Oral Implants Res /-2006.- V 17(4). – P. 359-366
- Von Arx T. Guited bone regeneration and autogenous block grafts for gorizontal augmentation: a staged approach / Von Arx T., Buser D. // In : Buser D: 20 years of guided bone regeneration in implant dentistry, 2nd ed. Chicago: Quintessence. -2009.- P.195-229
- Wrotniak M. Current opinion about using the plateletrich gel in orthopaedics and trauma surgery / Wrotniak M., Bielecki T., Gaździk T.S. // Ortop Traumatol Rehabil. – 2007. – V.9. - P. 227–238.
- Zhang Y. Membranes for guided tissue and bone regeneration / Zhang Y. et al. //Annals of Oral & Maxillofacial Surgery. – 2013. – V. 1. – №. 1. – P. 10.
Список литературы на английском языке / References in English
- Arsenina O.I. Ortodonticheskie meroprijatija v kompleksnom lechenii pacientov s vrozhdennoj rasshhelinoj guby i neba. [Orthodontic events in the complex treatment of patients with congenital cleft lip and palate]./ Arsenina O.I., Pashhenko E.I. // Materialy Vseros. konf. «Funkcional'no-jesteticheskaja reabilitacija bol'nyh s vrozhdennymi rasshhelinami lica»[ Materials of all-Russian conference. « Functional and aesthetic rehabilitation of patients with congenital cleft face »].- 2002; Р. 95–96. [in Russian]
- Korotkih D. V. Udar po krizisu – A-PRF. [A blow to the crisis – A-PRF.] / Korotkih D. V, Parfenova A. A. //Praktika implantologija. [Practice implantology].- 2015.-№9. -Р.60-63. [in Russian]
- Mamedov Ad.A. Algoritm reabilitacii detej s vrozhdennoj rasshhelinoj verhnej guby i neba. [Algorithm of rehabilitation of children with congenital cleft lip and palate]/ Mamedov Ad.A. // Vrozhdennaja i nasledstvennaja patologija golovy, lica i shei u detej: aktual'nye voprosy kompleksnogo lechenija [Congenital and hereditary pathology of the head, face and neck in children: current issues of comprehensive treatment]. - 2002. - Р. 151-155. [in Russian]
- Nikitin A.A. Lechenie detej rannego vozrasta s rasshhelinami verhnej guby, al'veoljarnogo otrostka i neba apparatom s ustrojstvom iz metalla s pamjat'ju formy. [Treatment of young children with clefts and palate apparatus with a device made of metal with shape memory]./ Nikitin A.A., Egorova M.V., Karachunskij G.M. // Materialy III Vseros. nauchno-prakt. konf. «Vrozhdennaja i nasledstvennaja patologija golovy, lica i shei u detej: aktual'nye voprosy kompleksnogo lechenija» [Proceedings of the III all-Russia. scientific-practical conference "Congenital and hereditary pathology of the head, face and neck in children: current issues of comprehensive treatment]. (8–10 september 2009 g.). M: MGMSU - 2009. - Р. 233–234.[in Russian]
- Pol'ma L.V. Korrekcija nepravil'nogo polozhenija jazyka u pacientov s vrozhdennoj rasshhelinoj jazyka, al'veoljarnogo otrostka i neba. [Correction of incorrect position of the tongue in patients with cleft, alveolar ridge and palate]. / Pol'ma L.V., Kiseleva E.V., Agaeva V.E., Nadtochij A.G. // Ortodontija// [Оrthodontics]. – 2004. – V 2(26) -Р.24- 27. [in Russian]
- Rubcova N.V. Sravnitel'naja ocenka rezul'tatov hirurgicheskogo lechenija detej s vrozhdennymi odnostoronnimi skvoznymi rasshhelinami neba. [Comparative evaluation of results of surgical treatment of children with congenital unilateral cross cleft palate.] / Rubcova N.V. //Avtoref. dis. .kand. med. nauk. M.[ Abstract. dis. .C.M.] - 2006. – V. 24. - Р. 7. [in Russian]
- Rjaguzova E.N. Primenenie modificirovannogo nesemnogo apparata Latham R.A. pri vrozhdennoj protruzii mezhcheljustnoj kosti u detej s vrozhdennoj polnoj dvustoronnej rasshhelinoj verhnej guby i neba. [The application of the modified fixed camera Latham R. A. congenital protrusion of maxillary bones in children with bilateral cleft lip and palate]./ Rjaguzova E.N., Matjunin V.V., D'jakova S.V. // Materialy III Vseros. nauchnoparkt. konf.: «Vrozhdennaja i nasledstvennaja patologija golovy, lica i shei u detej: aktual'nye voprosy kompleksnogo lechenija»[ Proceedings of the III all-Russian scientific-practical conference «Congenital and hereditary pathology of the head, face and neck in children: current issues of comprehensive treatment»] (8–10 September 2009 ) MGMSU.- 2009. - Р. 248–249. [in Russian]
- Starikova N.V. Rannee ortopedicheskoe lechenie detej s vrozhdennoj dvustoronnej rasshhelinoj verhnej guby i neba. [Early orthopedic treatment of children with congenital bilateral cleft lip and palate]./ Starikova N.V. // Avtoref. dis. kand. med. nauk. .[ Abstract. dis. .C.M.]/ - 2006. - Р. 127. [in Russian]
- Cepkolenko V. PRP- stimuljacija sinteza kollagena I tipa v kozhe cheloveka: placebo-kontroliruemoe issledovanie in vivo. [PRP - stimulation of the synthesis of type I collagen in human skin: a placebo-controlled study in vivo]./ Cepkolenko V., Surovjak P. //. Vestnik jesteticheskoj mediciny.[ Bulletin of aesthetic medicine.] – 2012. – V. 11. - № 3. – Р.17–24. [in Russian]
- Chujkin S.V. Reabilitacija detej s vrozhdennoj rasshhelinoj verhnej guby i neba. [Rehabilitation of children with congenital cleft of upper lip and her palate]./ Chujkin S.V., Davletshin N.A. //Avtoref. dis. .kand. med. nauk. M.[ Abstract. dis..C.M.] - 2005. – Р. 113.
- Anderson G. C. et al. Research diagnostic criteria for temporomandibular disorders: Future directions //Journal of orofacial pain. – 2010. – V. 24. – №. 1. – P. 79.
- Anitua E. Effectiveness of autologous preparation rich in growth factors for the treatment of chronic cutaneous ulcers / Anitua E. et al. //Journal of Biomedical Materials Research Part B: Applied Biomaterials. – 2008. – V. 84. – №. 2. – P. 415-421.
- Axhausen G. Histologische Untersuchungen über Knochentransplantation am Menschen / Axhausen G. //Dtsch Z Chir. – 1907. – V. 91. – P. 388-428
- Buser D. et al. Lateral ridge augmentation using autografts and barrier membranes: a clinical study with 40 partially edentulous patients / Buser D. //Journal of oral and maxillofacial surgery. – 1994. – V. 54. – №. 4. – P. 420-432.
- Buser D., Dahlin C., Schenk R. K. Guided bone regeneration //Chicago Quintessence. – 1994.
- Buser D. Early implant placement following single-tooth extraction in the esthetic zone: biologic rationale and surgical procedures / Buser D. et al. //The International journal of periodontics & restorative dentistry. – 2008. – V. 28. – №. 5. – P. 441.
- Chiapasco M. Augmentation procedures for the rehabilitation of deficient edentulous ridges with oral implants / Chiapasco M., Zaniboni M., Boisco M. //Clinical oral implants research. – 2006. – V. 17. – №. 2. – P. 136-159.
- Chiapasco M. Long term outcome of implants placed with guided bone regeneration (GBR) using resorbable and non resorbable membranes after 12–14 years / Chiapasco M., Jung R. E. et al //Clinical Oral Implants Research. – 2013. – V. 24. – №. 10. – P. 1065-1073.
- Cordaro, L. Mandibular bone harvesting for alveolar reconstruction and implant placement: subjective and objective cross sectional evaluation of donor and recipient site up to 4 years./ Cordaro, L., Torsello, F., Tindara Miuccio, M., Mirisola di Torresanto, V., & Eliopoulos, D. //Clinical oral implants research.-2011. V 22(11).- P.1320-1326.
- Cordaro L. Single unit attachments improve periimplant soft tissue conditions in mandibular overdentures supported by four implants. / Cordaro L. et al. //Clinical oral implants research. – 2013. – V. 24. – №. 5. – P. 536-542.
- Cordaro L. ITI Treatmen Guide / Cordaro L., Terheyden H. //Ridge augmentation Procedures in Implant Patients. A Staged Approach. Chen S, Buser D, Wismeijer. – 2014.-V. 7.-P.284-290.
- Donos N.Alveolar ridge augmentation by combining autogenous mandibular bone grafts and non resorbable membranes./ Donos N., Kostopoulos L., Karring T. //Clinical Oral Implants Research. – 2002. – V. 13. – №. 2. – P. 185-191.
- Donos N. Alveolar ridge augmentation using a resorbable copolymer membrane and autogenous bone grafts / Donos N., Kostopoulos L., Karring T. //Clinical Oral Implants Research. – 2002. – V. 13. – №. 2. – P. 203-213.
- Ehrenfest D. Classification of platelet concentrates: from pure platelet!rich plasma (P-PRP) to leucocyte- and platelet-rich fibrin (L-PRF) / Ehrenfest D., Rasmusson L, Albrektsson T. // Trends Biotechnol. – 2009. –V 27 (3). – P. 158-67.
- Ehrenfest D.M.In search of a consensus terminology in the field of platelet concentrates for surgical use: platelet-rich plasma (PRP), platelet-rich fibrin (PRF), fibrin gel polymerization and leukocytes / Ehrenfest D.M., Bielecki T., Mishra A., et.al. //Current pharmaceutical biotechnology. – 2012. – V. 13. – №. 7. – P. 1131-1137.
- Heinrich A.Prenatal diagnostics of cleft deformities and its significance for parent and infant care./ Heinrich A., Proff P., Michel Т., Ruhland F., Kirbschus A., Gedrange T. // J. of CranioMaxiillofac.Surg. 2006. - V.34. -P. 14- 17.
- Hemprich A. The functionally based Leipzig concept for the treatment of patients with cleft lip, alveolus and palate./ Hemprich A., Frerich В., Hierl Т., Dannhauer K.-H. // J. of CranioMaxiillofac.Surg.- 2006. - V.34. - №.2. - P. 22 - 26.
- Hockers T. The combined use of bioresorbable membranes and xenografts or autografts in the treatment of bone defects around implants. A study in beagle dogs / Hockers T. et al. //Clinical oral implants research. – 1999. – V. 10. – №. 6. – P. 487-498.
- Jensen S. S. Bone augmentation procedures in localized defects in the alveolar ridge: clinical results with different bone grafts and bone-substitute materials / Jensen S. S., Terheyden H. //International Journal of Oral & Maxillofacial Implants. – 2009. – V 24.
- Karageorgiou V. Porosity of 3D biomaterial scaffolds and osteogenesis / Karageorgiou V., Kaplan D. //Biomaterials. – 2005. – V. 26. – №. 27. – P. 5474-5491
- Keyhan S.Use of Platelet-Rich Fibrin and Platelet- Rich Plasma in Combination With Fat Graft: Which Is More Effective During Facial Lipostructure? / Keyhan S., Hemmat S.,Badri A., Khiabani K. // J. Oral Maxillofac Surg. – 2013. – V. 71. – P. 610–621.
- Krasna M. Platelet gel stimulates proliferation of human dermal fibroblasts in vitro / Krasna M., Domanović D., Tomsic A., Svajger U. et al. // Act. Dermatovenerol. Alp. Panonica Adriat. – 2007. – V.16 (3). – P. 105–110.
- Leitner G. C. Platelet content and growth factor release in platelet‐rich plasma: a comparison of four different systems / Leitner G. C. et al. //Vox sanguinis. – 2006. – V. 91. – №. 2. – P. 135-139.
- Marx R. E. A comparison of particulate allogeneic and particulate autogenous bone grafts into maxillary alveolar clefts in dogs / Marx R. E. et al. //Journal of Oral and Maxillofacial Surgery. – 1984. – V. 42. – №. 1. – P. 3-9.
- Marx R. Platelet- rich plasma: growth factor enhancement for bone grafts / Marx R., Carlson E., Eichstaedt R., Schimmele S. et al.// Oral Surg Oral Med Oral Pathol Oral Radiol Endod. – 1998. – V. 85. – P. 638–646.
- Mossey P. A. Cleft lip and palate / Mossey P. A. et al. //The Lancet. – 2009. – Т. 374. – №. 9703. – P. 1773-1785.
- Matras H. The use of fibrin sealant in oral and maxillofacial surgery / Matras H. //J. Oral Maxillofac Surg. – 1982. – V40. – P. 617.
- Ross R. B. Treatment variables affecting growth in unilateral cleft lip and palate./ Ross R. B. //Part 5: timing of palate repair. – 2006.-P. 156
- Sammartino, G. Use of autologous plateletrich plasma (PRP) in periodontal defect treatment after extraction of impacted mandibular third molars / Sammartino, G., Tia M., Marenzi G., di Lauro A., et al. // J. OralMaxillofac Surg. – 2005. – V.63. – P. 766.
- Scheerlinck E. Donor site complications in bone grafting: comparison of iliac crest, calvarial, and mandibular ramus bone / Scheerlinck E. et al. //International Journal of Oral & Maxillofacial Implants. – 2013. – №. 1.-.P. 28.
- Schwartz-Arad D. Intraoral autogenous block only bone grafting for extensive reconstruction of atrophic maxillary alveolar ridges / Schwartz-Arad D., Levin L. //Journal of periodontology. – 2005. – V. 76. – №. 4. – P. 636-641.
- Von Arx T. Horizontal ridge augmentation using autogenous block grafts and the guided bonebregeneration technique with collagen membranes/ A clinical study with 42 patients / Von Arx T, Buser D. // Clin Oral Implants Res /-2006.- V 17(4). – P. 359-366
- Von Arx T. Guited bone regeneration and autogenous block grafts for gorizontal augmentation: a staged approach / Von Arx T., Buser D. // In : Buser D: 20 years of guided bone regeneration in implant dentistry, 2nd ed. Chicago: Quintessence. -2009.- P.195-229
- Wrotniak M. Current opinion about using the plateletrich gel in orthopaedics and trauma surgery / Wrotniak M., Bielecki T., Gaździk T.S. // Ortop Traumatol Rehabil. – 2007. – V.9. - P. 227–238.
- Zhang Y. Membranes for guided tissue and bone regeneration / Zhang Y. et al. //Annals of Oral & Maxillofacial Surgery. – 2013. – V. 1. – №. 1. – P. 10.
