ПАТОГЕНЕТИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ ДЖИНУРЫ ПРОКУМБЕНС ДЛЯ ПРОФИЛАКТИКИ РАЗВИТИЯ НЕАЛКОГОЛЬНОГО СТЕАТОЗА ПЕЧЕНИ (ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ)
ПАТОГЕНЕТИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ ДЖИНУРЫ ПРОКУМБЕНС ДЛЯ ПРОФИЛАКТИКИ РАЗВИТИЯ НЕАЛКОГОЛЬНОГО СТЕАТОЗА ПЕЧЕНИ (ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ)
Научная статья
Гуляева И.Л.1, *, Мифтахова А.М.2, Булатова И.А.3, Курцев Б.В.4
1 ORCID: 0000-0001-7521-1732;
3 ORCID: 0000-0002-7802-4796;
1, 2, 3 Пермский государственный медицинский университет им. академика Е.А. Вагнера, Пермь, Россия;
4 Via Vitae Estate Ltd., Лимассол, Кипр
* Корреспондирующий автор (pimenova774[at]yandex.ru)
АннотацияНеалкогольная жировая болезнь печени является одним из самых распространенных заболеваний гепатобилиарной системы, приводящих к ухудшению качества жизни, инвалидизации и смерти. Изучение патогенеза, поиск новых средств профилактики и лечения неалкогольной жировой болезни печени является важной задачей современной медицины. Джинура прокумбенс – лекарственное растение, все части которого содержат большое количество биологически активных веществ и используются как пищевой продукт, так и для лечения различных заболеваний в традиционной медицине. Доказаны антигипергликемическая, антигиперлипидемическая, антиоксидантная, противовоспалительная активности Джинуры прокумбенс, что предположительно может обусловливать саногенетические и профилактические эффекты при неалкогольном стеатозе печени.
Целью исследования явилось изучение гепатопротекторного действия водного экстракта Джинуры прокумбенс при неалкогольном стеатозе печени в эксперименте. Исследование проводилось на 25-ти белых нелинейных крысах, разделенных на 3 группы: контроль (интактные животные), «Стеатоз» (животные с стеатозом печени, смоделированном в лабораторных условиях) и «Стеатоз+Джинура прокумбенс», где животные с первого дня моделирования стеатоза получали интрагастрально водный экстракт Джинуры. Методы исследования: гистологические, биохимические (АЛТ, АСТ, щелочная фосфатаза, общий белок, альбумин, глюкоза), измерение концентрации интерлейкина-6. В ходе исследования было установлено, что саногенетический эффект курсового профилактического введения экстракта Джинуры проявляется снижением выраженности синдромов цитолиза и холестаза, положительными изменениями в липидном спектре и улучшением белковосинтетической функции печени, что позволяет сделать вывод о целесообразности дальнейшего изучения возможного применения водного экстракта этого растения для профилактики и лечения неалкогольного стеатоза печени.
Ключевые слова: неалкогольная жировая болезнь печени, стеатоз, гепатопротекторное действие, экспериментальное моделирование, Джинура прокумбенс.
A PATHOGENETIC JUSTIFICATION OF THE USE OF GYNURA PROCUMBENS FOR THE PREVENTION OF THE DEVELOPMENT OF NON-ALCOHOLIC LIVER STEATOSIS (AN EXPERIMENTAL STUDY)
Research article
Gulyaeva I.L.1, *, Miftakhova A.M.2, Bulatova I.A.3, Kurtsev B.V.4
1 ORCID: 0000-0001-7521-1732;
3 ORCID: 0000-0002-7802-4796;
1, 2, 3 Perm State Medical University, Perm, Russia;
4 Via Vitae Estate Ltd., Limassol, Cyprus
* Corresponding author (pimenova774[at]yandex.ru)
AbstractNon-alcoholic fatty liver disease is one of the most common diseases of the hepatobiliary system, leading to a deterioration in the quality of life, disability and death. The study of the pathogenesis and the search for new means of prevention and treatment of non-alcoholic fatty liver disease is an important task of modern medicine. Gynura procumbens is a medicinal plant, all parts of which contain a large amount of biologically active substances and are used as a food product and for the treatment of various diseases in traditional medicine. The study proves the antihyperglycemic, antihyperlipidemic, antioxidant, anti-inflammatory activity of Gynura procumbens, which presumably can cause sanogenetic and preventive effects in non-alcoholic liver steatosis.
The aim of the study was to study the hepatoprotective effect of the aqueous extract of Gynura procumbens in non-alcoholic liver steatosis in an experiment. The study was conducted on 25 white non-pedigree rats divided into 3 groups: control (intact animals), "Steatosis"(animals with liver steatosis modeled in laboratory conditions) and " Steatosis+Gynura procumbens", where animals received intragastric aqueous extract of Gynura from the first day of steatosis modeling. Methods of investigation include histological, biochemical (ALT, AST, alkaline phosphatase, total protein, albumin, glucose), and the measurement of the concentration of interleukin-6. The results of the study showed that the sanogenetic effect of the course of preventive administration of the Gynura extract is manifested by a decrease in the severity of cytolysis and cholestasis syndromes, positive changes in the lipid spectrum and improvement of the protein-synthetic function of the liver, which allowed the authors to conclude that it is advisable to further study the possible use of an aqueous extract of this plant for the prevention and treatment of non-alcoholic liver steatosis.
Keywords: non-alcoholic fatty liver disease, steatosis, hepatoprotective effect, experimental modeling, Gynura procumbens.
Введение
Неалкогольная жировая болезнь печени (НАЖБП) – одна из наиважнейших проблем современной медицины во всем мире в связи с её широкой распространенностью и тенденцией к росту. Она наблюдается у 20–33% взрослого населения различных стран, занимая лидирующую позицию среди заболеваний печени [1]. НАЖБП – это спектр заболеваний, включающий в себя стеатоз, неалкогольный стеатогепатит и цирроз. Согласно результатам открытого многоцентрового проспективного исследования-наблюдения DIREG L 01903, проведенного в Российской Федерации, НАЖБП была выявлена у 27% обследованных, при этом в подавляющем большинстве случаев был установлен стеатоз (у 80,3% пациентов), у 16,8% — стеатогепатит, у 2,9% - цирроз [2]. Углубленное изучение патогенеза, своевременная диагностика НАЖБП, ее профилактика и лечение остаются актуальными задачами медицины. Учитывая, что механизмы развития НАЖБП сопряжены с целым ряд метаболических нарушений, современная терапия должна быть комплексной, направленной на коррекцию всех звеньев, вовлеченных в патологический процесс: нормализацию липидного профиля, повышение антиоксидантной защиты, снижение интенсивности оксидативного стресса, уменьшение активности воспалительного процесса, цитокин-индуцированного повреждения, предупреждение избыточного апоптоза и некроза гепатоцитов [3]. Современный арсенал средств с гепатопротекторной активностью достаточно большой. Он включает как синтетические лекарственные препараты, так и лекарственные формы растительного происхождения. В то же время для НАЖБП, особенно на стадии стеатоза, нет утвержденной терапии [4]. Это делает проблему поиска новых эффективных, безопасных и патогенетически обоснованных лекарственных средств для профилактики и лечения НАЖБП чрезвычайно актуальной.
Джинура прокумбенс (Gynura procumbens) (семейство Астровые) является лекарственным растением, обычно встречающимся в странах Восточной Азии и Китая. Листья Джинуры используются как пищевой продукт, так и для лечения целого ряда заболеваний в традиционной медицине. Интерес ученых к этому растению многократно вырос после того, как появились научные данные о том, что все части Джинуры прокумбенс (ДП) содержат большое количество биологически активных веществ: полифенолов, алкалоидов, флавоноидов, кофеилхиновых кислот, каратиноидов, эфирных масел и др. [5], [6].
Было показано, что это растение в связи с высоким содержанием кверцитина, фенолов и флавоноидов обладает выраженным антигипергликемическим эффектом [7], [8]; благодаря содержанию кофеилхиновых кислот, в частности, хлорогеновой кислоты, проявляет высокую антиоксидантную активность и способно оказывать антигиперлипидемическое действие с значительным снижением общего холестерина, триглицеридов, липопротеинов низкой плотности (ЛПНП), липопротеинов очень низкой плотности (ЛПОНП) и увеличением уровня липопротеинов высокой плотности (ЛПВП) [9]. Полифенолы и стероиды, содержащиеся во всех частях ДП, обеспечивают противовоспалительный эффект [6]. Можно предположить, что большинство из перечисленных активностей этого растения должны обусловливать его гепатопротекторное действие, однако данных о эффективности применения ДП для профилактики и лечения неалкогольного стеатоза печени нет.
Материалы и методы
Исследование проводилось на неинбредных половозрелых белых крысах-самцах. Возраст животных составлял 7 месяцев, масса тела - 400-530 г. Животные содержались в стандартных условиях вивария ЦНИЛ ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера Минздрава России в соответствии с Директивой № 63 от 22 сентября 2010 года Президиума и Парламента Европы «О защите животных, используемых для научных исследований» и приказом Минздрава России №199н от 01.04.2016 г. «Об утверждении правил надлежащей лабораторной практики», основываясь на принципах гуманного обращения с подопытными животными. Проведение исследований одобрено локальным этическим комитетом ПГМУ до начала эксперимента.
Животные содержались в стандартных клетках, предназначенных для содержания грызунов в лаборатории, по 4-5 особей в клетке при температуре 20-22oС. Световой режим соответствовал схеме: с 08.00. до 20.00 (12 часов) – свет («день»); с 20.00 до 08.00 (12 часов) – темнота («ночь»). Доступ к пище и воде не ограничивался.
Были сформированы 3 группы животных:
- «Контроль» (группа 1) (n=9) – здоровые, интактные животные. Для кормления этой группы использовался полноценный сбалансированный стандартный гранулированный корм, одобренный для лабораторных животных (крыс и мышей) (ООО «Лабораторкорм», Россия).
- «Стеатоз» (группа 2) (n=9). Кормление осуществляли аналогично животным первой группы. Моделирование стеатоза печени проводили путем добавления в питьевую воду фруктозы на протяжении всего эксперимента [10], [11], [12]. Таким образом, использовали 15%-ый раствор фруктозы в качестве питьевой воды.
- «Стеатоз + ДП» (группа 3) (n=7) – крысы, у которых моделировали стеатоз печени аналогично тому, как это осуществлялось в группе «Стеатоз печени». Одновременно, с первого дня исследования, через один час после начала светового периода, проводили ежедневное интрагастральное введение водного экстракта листьев Джинуры прокумбенс (производство Via Vitae Estate, Кипр), из расчета 0,5 г на 1 кг веса животного в день, однократно, на протяжении 30 суток [13].
Ежедневно производились осмотр животных, оценка их поведения, состояния шерсти, активности, аппетита; осуществлялось измерение массы тела. В конце эксперимента, на 30-й день, крыс подвергали эфирному наркозу путем их помещения в эксикатор с парами эфира, производили вскрытие и прямой забор крови из правого предсердия.
У животных контрольной группы и группы «Стеатоз» печеночная ткань подвергалась гистологическому исследованию.
Лабораторное обследование экспериментальных животных включало в себя определение ряда биохимических показателей: аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы (ЩФ), общего белка, альбумина, глюкозы, общего холестерина, триглицеридов, ЛПВП, ЛПНП, ЛПОНП. Эти параметры исследовали в сыворотке крови на автоматическом анализаторе «Mindray» (Китай) с использованием реагентов этой же фирмы. Концентрацию интерлейкина-6 (ИЛ-6) определяли методом иммуноферментного анализа на аппарате Stat Fax 2100 (Awareness Technology, США) с использованием наборов «VEGF-ИФА-БЕСТ», «Интерлейкин-6-ИФА-БЕСТ» (ЗАО «Вектор-Бест», г. Новосибирск).
Гистологический анализ тканей печени проводился с окраской срезов гематоксилином и эозином по общепринятой методике. Для подтверждения наличия нейтральных липидов в цитоплазме гепатоцитов и уточнения степени стеатоза в группе «Стеатоз» пять образцов были исследованы с помощью окраски замороженных срезов суданом III, без докраски гематоксилином и эозином.
Статистическая обработка полученных данных проводилась на ПК с использованием встроенного пакета анализа табличного процессора Excel® 2016 MSO (© Microsoft, 2016), авторского (© В.С. Шелудько, 2001-2016) пакета прикладных электронных таблиц (ППЭТ) "Stat2015" [14]. Для анализа количественных признаков применялись медиана (Me) и квартили (Q1, Q3).
Для сравнения двух групп между собой использовали критерий Манна-Уитни (U). Различия между выборками считали статистически значимыми при р<0,05.
Результаты и обсуждение
Результаты гистологического исследования показали, что у животных в группе «Стеатоз» при окраске гематоксилином и эозином определяются гепатоциты с признаками мелко- и крупнокапельной жировой дистрофии в виде оптически пустых вакуолей в цитоплазме клеток, распространенной преимущественно центролобулярно и на периферии печеночных долек (20-25%, индекс стеатоза - 1). При окраске замороженных срезов суданом III верифицируются еще более выраженные изменения: в цитоплазме гепатоцитов выявляются округлые вакуоли различных размеров оранжевато-желтого цвета, соответствующие нейтральным липидам (до 40-50% объема паренхимы органа, индекс стеатоза - 2) (см. рисунок 1). В контрольных образцах при окраске суданом III в цитоплазме гепатоцитов накопления нейтральных липидов не отмечается (индекс стеатоза – 0).
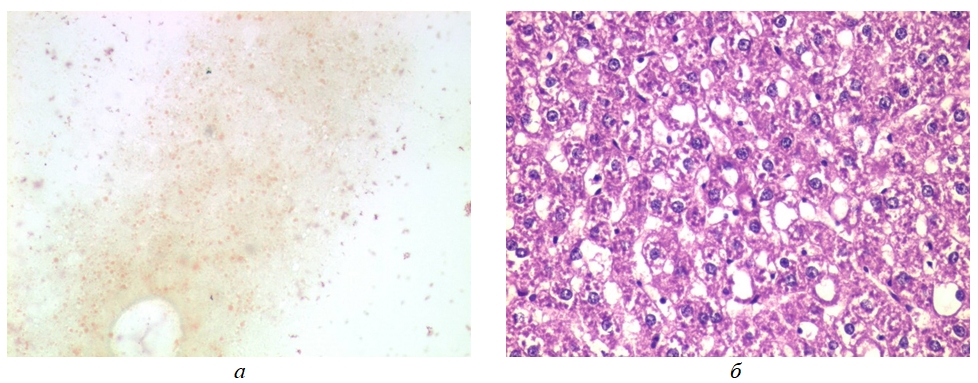
Рис. 1 – Изменения в ткани печени у животных из группы 2 с характерными признаками стеатоза, гистологические срезы:
а – окраска суданом III; б – окраска гематоксилином и эозином
Примечание: увеличение х400
Описанная структурная реорганизиция печени подтверждает развитие стеатоза у животных и адекватность использованного способа моделирования данного заболевания.
Известно, что в патогенезе НАЖБП значимую роль играют провоспалительные цитокины, в частности, ИЛ-6 [15]. Интерлейкин-6 способен индуцировать синтез острофазных белков, таких как фибриноген и С-реактивный белок, играя тем самым центральную роль в индуцировании воспаления; участвует в регуляции работы иммунной системы. Кроме того, известно, что ИЛ-6 стимулирует процессы липогенеза в печени, что является одним из центральных механизмов развития стеатоза [16].
При проведении сравнительного анализа содержания маркера системного воспаления ИЛ-6 в цитоплазме животных разных групп установлено, что при моделировании стеатоза печени концентрация этого цитокина статистически значимо увеличивается по сравнению с контролем (р1-2= 0,006).
Профилактическое введение Gynura Procumbens не оказало противовоспалительного эффекта. Содержание ИЛ-6 у животных этой группы по сравнению с контролем статистически значимо больше (р1-3= 0,018), в то время, как при сравнении с группой «Стеатоз» значимых различий не наблюдалось (р2-3=0,751).
По данным лабораторных тестов уровень АЛТ в сыворотке крови животных не имел значимых различий, в то время, как показатель АСТ в группе 3 был статистически ниже, чем в группе 2 (р2-3=0,003), что свидетельствует о цитопротекторном эффекте водного экстракта ДП в отношении паренхиматозных клеток печени. Профилактическое введение Джинуры эффективно предотвращало рост ферментативной активности ЩФ: уровень этого энзима в группе «Стеатоз» достоверно выше, чем у животных третьей группы, получавших ДП, – 257,50 (192,50–332,60) Ед/л и 134,4 (72,5–179,9) Ед/л, соответственно (р2-3=0,002). Статистически значимое увеличение содержания общего белка в плазме крови животных группы 3 (медиана – 73,8 г/л) по сравнению с контролем (медиана – 66,3 г/л, р1-3=0,001) и группой 2 (медиана – 66,7 г/л, р2-3=0,001) свидетельствует о улучшении белковосинтетической функции печени при курсовом введении животным водного экстракта ДП. Уровень глюкозы статистически значимо не отличался в сравниваемых группах (см. таблицу 1).
Таблица 1 – Сравнительный анализ биохимических показателей крови животных в исследуемых группах
| Показатель | Группа 1 n=9, Ме (хj – xk) | Группа 2 n=9, Ме (хj – xk) | Группа 3 n=7, Ме (хj – xk) | р |
| АЛТ, Ед/л | 62,1 (51,0–78,6) | 64,80 (53,70–77,50) | 56,8 (36,7–90,3) | р1-2=0,825 р1-3=0,560 р2-3=0,427 |
| АСТ, Ед/л | 114,1 (98,3–165,6) | 140,20 (118,10–161,30) | 98,9 (85,6–122,9) | р1-2=0,102 р1-3=0,223 р2-3=0,003 |
| Щелочная фосфатаза (Ед/л) | 219,8 (152,9–363,9) | 257,50 (192,50–332,60) | 134,4 (72,5–179,9) | р1-2=0,566 р1-3=0,007 р2-3=0,002 |
| Общий белок (г/л) | 66,3 (64,3–67,7) | 66,70 (61,80–68,90) | 73,8 (71,0–76,4) | р1-2=0,825 р1-3=0,001 р2-3=0,001 |
| Альбумин (г/л) | 30,8 (29,7–32,0) | 31,40 (29,30–32,70) | 31,5 (29,1–34,8) | р1-2=0,508 р1-3=0,397 р2-3=0,525 |
| Глюкоза (ммоль/л) | 17,2 (13,2–20,7) | 20,53 (16,60–25,00) | 21,5 (14,7–25,0) | р1-2=0,085 р1-3=0,125 р2-3=0,874 |
При сравнительном анализе показателей липидограммы обнаружено, что при формировании стеатоза печени у животных второй группы развивается дислипидемия, проявляющаяся достоверно более выраженными триглицеридемией (р1-2=0,012), ЛПОНП-емией (р1-2=0,008) и статистически значимым снижением концентрации ЛПВП (р1-2=0,001), что согласуется с данными литературы [16]. Курсовое профилактическое введение экстракта ДП оказывает определенное положительное влияние на метаболизм липидов. Так, уровень общего холестерина в группе 3 стал значимо меньше, чем в контроле: 2,0 (1,6–2,1) и 1,4 (1,0–1,7) ммоль/л, соответственно (р1-3=0,004). Также имеется тенденция к снижению содержания тригицеридов в плазме крови животных, получавших ДП, по сравнению с группой «Стеатоз» (1,9 (0,7–2,6) и 3,20 (1,86–5,00) ммоль/л, соответственно), однако достоверных различий не выявлено, что, возможно, связано с малым количеством выборки. Надо отметить, что наряду с указанными положительными изменениями в липидном спектре при применении ДП не произошло нормализации показателя ЛПВП (р2-3=0,672) (см. таблицу 2).
Таблица 2 – Сравнительный анализ показателей липидограммы животных в исследуемых группах
| Показатель | Группа 1 n=9, Ме (хj – xk) | Группа 2 n=9, Ме (хj – xk) | Группа 3 n=7, Ме (хj – xk) | р |
| Общий холестерин (ммоль/л) | 2,0 (1,6–2,1) | 1,63 (1,42–2,08) | 1,4 (1,0–1,7) | р1-2=0,185 р1-3=0,004 р2-3=0,185 |
| Триглицериды (ммоль/л) | 1,5 (1,2–2,3) | 3,20 (1,86–5,00) | 1,9 (0,7–2,6) | р1-2=0,012 р1-3=0,711 р2-3=0,064 |
| ЛПНП (ммоль/л) | 0,6 (0,5–0,8) | 0,59 (0,51–0,66) | 0,5 (0,4–0,7) | р1-2=0,270 р1-3=0,064 р2-3=0,290 |
| ЛПВП (ммоль/л) | 1,0 (1,0–1,2) | 0,75 (0,66–0,91) | 0,7 (0,4–1,0) | р1-2=0,001 р1-3=0,002 р2-3=0,672 |
| ЛПОНП (ммоль/л) | 0,7 (0,6–1,0) | 1,45 (0,84–2,27) | 0,9 (0,3–1,2) | р1-2=0,008 р1-3=0,459 р2-3=0,057 |
Таким образом, при моделировании неалкогольного жирового гепатоза формируются соответствующие морфологические изменения, которые подтверждаются гистологическими исследованиями; увеличивается содержание ИЛ-6, что свидетельствует о развитии воспалительной реакции; нарушается липидный обмен (повышается уровень холестерина, триглицеридов, ЛПНП, ЛПОНП; снижается содержание ЛПВП в плазме крови). Саногенетический эффект курсового профилактического интрагастрального введения водного экстракта ДП проявляется снижением выраженности синдромов цитолиза и холестаза, положительными изменениями в липидном спектре и улучшением белковосинтетической функции печени, что позволяет сделать вывод о целесообразности дальнейшего изучения возможного применения водного экстракта ДП для профилактики и лечения неалкогольного стеатоза печени.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Ивашкин В.Т. Клинические рекомендации по диагностике и лечению неалкогольной жировой болезни печени Российского общества по изучению печени и Российской гастроэнтерологической ассоциации / В.Т. Ивашкин, М.В. Маевская, Ч.С. Павлов и др.//Российский журнал гастроэнтерологии, гепатологии и колопроктологии. – 2016. – №2. – С.24-42.
- Драпкина О.М. Эпидемиологические особенности неалкогольной жировой болезни печени в России (результаты открытого многоцентрового проспективного исследования-наблюдения DIREGL 01903) / О.М. Драпкина, В.Т. Ивашкин // Российский журнал гастроэнтерологии, гепатологии и колопроктологии. – 2014. – №4. – С. 32-38.
- Pei K. An Overview of Lipid Metabolism and Nonalcoholic Fatty Liver Disease / K. Pei , T. Gui, D. Kan et al. // BioMed Research International. – 2020. – Vol. 2020. – P. 12. DOI:10.1155/2020/4020249
- EASL–EASD–EASO Clinical Practice Guidelines for the Management of Non-Alcoholic Fatty Liver Disease // J. Hepatol. – 2016. – Vol. 64. – 1388–1402. DOI:10.1016/j.jhep.2015.11.004.
- Пестренин Л.Д. Джинура Прокумбенс: обзор биологических эффектов и их возможных механизмов / Л.Д. Пестренин, Б.В. Курцев, И.Л. Гуляева и др. // Современные проблемы науки и образования. – 2020. – №3. – С. 146.
- Herawan Timotius K., Rahayu I. Overview of Herbal Therapy with Leave of Gynura procumbens (Lour.) Merr / K. Herawan Timotius, I. Rahayu // Journal of Young Pharmacists. – 2020. – Vol. 12(3). – P. 201-206. DOI: 10.5530/jyp.2020.12.61
- Guo S. Exploring the protective effect of Gynura procumbensagainst type 2 diabetes mellitus by network pharmacology and validation in C57BL/KsJ db/db mice / H. Ouyang, W. Du, J. Li et al. // Food Funct. – 2021. – Vol. 12(4). – P. 1732-1744. DOI: 10.1039/d0fo01188f.
- Гуляева И.Л. Изучение эффективности применения отвара листьев растения Джинура Прокумбенс у пациентов с сахарным диабетом 2 типа с недостаточным контролем гликемии на фоне терапии сахароснижающими препаратами / И.Л. Гуляева // Наука, техника и образование. – 2014. - № 5(5). [Электронный ресурс]. URL: http://scienceproblems.ru/izuchenie-effektivnosti-primenenija-otvara-listev.html (дата обращения: 22.07.2021).
- Ahmad Nazri K.A. Gynura Procumbens standardised extract reduces cholesterol levels and modulates oxidative status in postmenopausal rats fed with cholesterol diet enriched with repeatedly heated palm oil / K.A. Ahmad Nazri, N.M. Fauzi, F. Buang et al. // Evid Based Complement Alternat Med. – 2019. – Vol.2019. – P. 7246756. DOI: 10.1155/2019/7246756.
- Брус Т.В. Моделирование неалкогольной жировой болезни печени различной степени тяжести у лабораторных крыс и возможности ее коррекции : автореферат дис. ... канд. мед. наук : 14.03.03 : защищена 05.06.2018 / Брус Татьяна Викторовна. – СПб., 2018. – 21 с.
- Roeb E. Fructose and Non-Alcoholic Steatohepatitis / E. Roeb, R. Weiskirchen // Frontiers in Pharmacology. – 2021. – Vol. 12. – P. 634344. DOI: 10.3389/fphar.2021.634344
- Shojaei Zarghani S. Comparison of Three Different Diet-Induced Non Alcoholic Fatty Liver Disease Protocols in Rats: A Pilot Study / S. Shojaei Zarghani, H. Soraya, L. Zarei et al. // Pharmaceutical Sciences. – 2016. – Vol. 22. – P. 9-15. DOI: 10.15171/PS.2016.03.
- Hassan Z. Antidiabetic properties and mechanism of action of Gynura procumbens water extract in streptozotocin-induced diabetic rats / Z. Hassan, M.F. Yam, M. Ahmad et al. // Molecules. – 2010. Vol.15. – P. 9008-9023. DOI: 10.3390/molecules15129008.
- Шелудько В.С. Теоретические основы медицинской статистики (статистические методы обработки и анализа материалов научно-исследовательских работ: учеб.-метод. пособие. Изд 3-е, исправл. и доп. / В.С Шелудько, Г.И. Девяткова. – Пермь: ФГБОУ ВО ПГМУ им. академика Е.А. Вагнера Минздрава России; Саратов: Амирит, 2019. – 96 с.
- Пестренин Л.Д. Активность сывороточных цитокинов и маркера повреждения эндотелия у пациентов со стеатозом, фиброзом и циррозом печени / Л.Д. Пестренин, И.А. Булатова, И.Л. Гуляева // Здоровье и образование в XXI веке. – 2017. – №19(7). – С. 116-120.
- Гуляева И.Л. Взаимосвязь дислипидемии, провоспалительных цитокинов и маркера дисфункции эндотелия у пациентов с неалкогольным жировым гепатозом / И.Л. Гуляева, И.А. Булатова, Л.Д. Пестренин //Смоленский альманах. – 2018. – №4. – С. 183-185.
Список литературы на английском языке / References in English
- Ivashkin V.T. Klinicheskie rekomendacii po diagnostike i lecheniju nealkogol'noj zhirovoj bolezni pecheni Rossijskogo obshhestva po izucheniju pecheni i Rossijskoj gastrojenterologicheskoj associacii [Clinical guidelines for the diagnosis and treatment of non-alcoholic fatty liver disease of the Russian Society for the Study of the Liver and the Russian Gastroenterological Association] / V.T. Ivashkin M.V. Maevskaja, Ch.S. Pavlov et al. // Rossijskij zhurnal gastrojenterologii, gepatologii i koloproktologii [Russian Journal of Gastroenterology, Hepatology and Coloproctology]. – 2016. – №2. – P.24-42. [in Russian]
- Drapkina O.M. Jepidemiologicheskie osobennosti nealkogol'noĭ zhirovoĭ bolezni pecheni v Rossii (rezul'taty otkrytogo mnogocentrovogo prospektivnogo issledovanija-nabljudenija DIREGL 01903) [Epidemiological features of non-alcoholic fatty liver disease in Russia (results of an open multicenter prospective observation study DIREGL 01903)] / O.M. Drapkina, V.T. Ivashkin // Rossijskij zhurnal gastrojenterologii, gepatologii i koloproktologii [Russian Journal of Gastroenterology, Hepatology and Coloproctology]. – 2014. – №4. – P. 32-38. [in Russian]
- Pei K. An Overview of Lipid Metabolism and Nonalcoholic Fatty Liver Disease / K. Pei , T. Gui, D. Kan et al. // BioMed Research International. – 2020. – Vol. 2020. – P. 12. DOI:10.1155/2020/4020249
- EASL–EASD–EASO Clinical Practice Guidelines for the Management of Non-Alcoholic Fatty Liver Disease // J. Hepatol. – 2016. – Vol. 64. – 1388–1402. DOI:10.1016/j.jhep.2015.11.004.
- Pestrenin L.D. Dzhinura Prokumbens: obzor biologicheskih jeffektov i ih vozmozhnyh mehanizmov [Gynura Procumbens: an overview of biological effects and their possible mechanisms] / L.D. Pestrenin, B.V. Kurcev, I.L. Guljaeva et al. // Sovremennye problemy nauki i obrazovanija [Modern problems of science and education]. – 2020. – №3. – P. 146. [in Russian]
- Herawan Timotius K., Rahayu I. Overview of Herbal Therapy with Leave of Gynura procumbens (Lour.) Merr / K. Herawan Timotius, I. Rahayu // Journal of Young Pharmacists. – 2020. – Vol. 12(3). – P. 201-206. DOI: 10.5530/jyp.2020.12.61
- Guo S. Exploring the protective effect of Gynura procumbensagainst type 2 diabetes mellitus by network pharmacology and validation in C57BL/KsJ db/db mice / H. Ouyang, W. Du, J. Li et al. // Food Funct. – 2021. – Vol. 12(4). – P. 1732-1744. DOI: 10.1039/d0fo01188f.
- Guljaeva I.L. Izuchenie jeffektivnosti primenenija otvara list'ev rastenija Dzhinura Prokumbens u pacientov s saharnym diabetom 2 tipa s nedostatochnym kontrolem glikemii na fone terapii saharosnizhajushhimi preparatami [The study the effectiveness of the use of decoction of the leaves of the Jinura Procumbens plant in patients with type 2 diabetes mellitus with insufficient glycemic control against the background of therapy with hypoglycemic drugs] / I.L. Guljaeva // Nauka, tehnika i obrazovanie. – 2014. - № 5(5). [Electronic resource]. URL: http://scienceproblems.ru/izuchenie-effektivnosti-primenenija-otvara-listev.html (accessed: 22.07.2021). [in Russian]
- Ahmad Nazri K.A. Gynura Procumbens standardised extract reduces cholesterol levels and modulates oxidative status in postmenopausal rats fed with cholesterol diet enriched with repeatedly heated palm oil / K.A. Ahmad Nazri, N.M. Fauzi, F. Buang et al. // Evid Based Complement Alternat Med. – 2019. – Vol.2019. – P. 7246756. DOI: 10.1155/2019/7246756.
- Brus T.V. Modelirovanie nealkogol'noj zhirovoj bolezni pecheni razlichnoj stepeni tjazhesti u laboratornyh krys i vozmozhnosti ee korrekcii [Modeling non-alcoholic fatty liver disease of varying severity in laboratory rats and the possibility of its correction] : avtoreferat dis. ... of PhD in Medicine : 14.03.03 : defense of the thesis 05.06.2018 / Brus Tat'jana Viktorovna. – SPb., 2018. – 21 p. [in Russian]
- Roeb E. Fructose and Non-Alcoholic Steatohepatitis / E. Roeb, R. Weiskirchen // Frontiers in Pharmacology. – 2021. – Vol. 12. – P. 634344. DOI: 10.3389/fphar.2021.634344
- Shojaei Zarghani S. Comparison of Three Different Diet-Induced Non Alcoholic Fatty Liver Disease Protocols in Rats: A Pilot Study / S. Shojaei Zarghani, H. Soraya, L. Zarei et al. // Pharmaceutical Sciences. – 2016. – Vol. 22. – P. 9-15. DOI: 10.15171/PS.2016.03.
- Hassan Z. Antidiabetic properties and mechanism of action of Gynura procumbens water extract in streptozotocin-induced diabetic rats / Z. Hassan, M.F. Yam, M. Ahmad et al. // Molecules. – 2010. Vol.15. – P. 9008-9023. DOI: 10.3390/molecules15129008.
- Shelud'ko V.S. Teoreticheskie osnovy medicinskoj statistiki (statisticheskie metody obrabotki i analiza materialov nauchno-issledovatel'skih rabot: ucheb.-metod. posobie. [Theoretical bases of medical statistics (statistical methods of processing and analysis of scientific and research materials)]. Methodic recommendations. / V.S Shelud'ko, G.I. Devjatkova. – Perm': FGBOU VO PGMU im. akademika E.A. Vagnera Minzdrava Rossii; Saratov: Amirit, 2019. – 96 p. [in Russian]
- Pestrenin L.D. Aktivnost' syvorotochnyh citokinov i markera povrezhdenija jendotelija u pacientov so steatozom, fibrozom i cirrozom pecheni [The activity of serum cytokines and a marker of endothelial damage in patients with steatosis, fibrosis and cirrhosis of the liver] / L.D. Pestrenin, I.A. Bulatova, I.L. Guljaeva // Zdorov'e i obrazovanie v XXI veke [Health and education in the 21st century]. – 2017. – №19(7). – P. 116-120. [in Russian]
- Guljaeva I.L. Vzaimosvjaz' dislipidemii, provospalitel'nyh citokinov i markera disfunkcii jendotelija u pacientov s nealkogol'nym zhirovym gepatozom [Interrelation of dyslipidemia, proinflammatory cytokines and a marker of endothelial dysfunction in patients with non-alcoholic fatty hepatosis] / I.L. Guljaeva, I.A. Bulatova, L.D. Pestrenin // Smolenskij medicinskij al'manah [Smolensk Medical Almanac]. – 2018.– №4. – P. 183-185. [in Russian]
