КОРРЕКЦИЯ ПРОДОЛЖИТЕЛЬНОЙ ГЕМОФИЛЬТРАЦИЕЙ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ ПРИ АБДОМИНАЛЬНОМ СЕПСИСЕ
DOI: https://doi.org/10.23670/IRJ.2018.75.9.024
КОРРЕКЦИЯ ПРОДОЛЖИТЕЛЬНОЙ ГЕМОФИЛЬТРАЦИЕЙ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ ПРИ АБДОМИНАЛЬНОМ СЕПСИСЕ
Научная статья
Фомин А.М.*
ORCID: 0000-0001-6010-9583,
Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского», Москва, Россия
* Корреспондирующий автор (amf05[at]mail.ru)
Аннотация
Продолжительная гемофильтрация была использована в комбинированной терапии 27 больных абдоминальным сепсисом, у которых развивалась полиорганная недостаточность или септический шок. Были исследованы показатели оксидативного стресса. Установлены усиление перекисного окисления липидов и падение содержания α-токоферола. Продолжительная гемофильтрация улучшала показатели антиоксидантной защиты. Рассчитанный коэффициент окислительного стресса «К» в сыворотке и эритроцитах, в норме приближающийся к единице, исходно увеличен в 2,8 и 2,59 раза, соответственно. В плазме и в эритроцитах после проведения продолжительной гемофильтрации этот показатель существенно улучшился, но оставался повышенным 1,28 и 1,72 раза.
Ключевые слова: абдоминальный сепсис, гемофильтрация, окислительный стресс, α-токоферол.
CORRECTION OF PROLONGED HEMOFILTRATION OF LIPID PEROXIDATION IN ABDOMINAL SEPSIS
Research article
Fomin A.M.*
ORCID: 0000-0001-6010-9583,
M.F. Vladimirsky Moscow Regional Research and Clinical Institute, Moscow, Russia
* Corresponding author (amf05[at]mail.ru)
Abstract
Continuous hemofiltration was used in combination therapy of 27 patients with abdominal sepsis, with developing multichannel insufficiency or septic shock. Indicators of oxidative stress were studied. The enhancement of lipid peroxidation and the decrease in the content of α-tocopherol are established. Continuous hemofiltration improved the performance of antioxidant protection. The calculated coefficient of oxidative "K" stress in the serum and erythrocytes, normally approaching unity, was initially increased by 2.8 and 2.59 times, respectively. This index improved significantly after prolonged hemofiltration but remained elevated 1.28 and 1.72 times in plasma and erythrocytes.
Keywords: abdominal sepsis, hemofiltration, oxidative stress, α-tocopherol.
Усиление свободнорадикальных реакций, проявляющиеся окислительным стрессом с перекисным окислением жиров и ослаблением антиоксидантной защиты, наблюдается при различных патологических состояниях человека. При тяжелых гипоксических поражениях клеток и тканей наблюдается избыточная активация перекисного окисления липидов [4,6,9]. Избыточное усиление ПОЛ было выявлено у пациентов с гнойными заболеваниями абдоминальной области [1,5]. Известно, существуют естественные системы антиоксидантной направленности, которые постепенно истощаются. Данных о влиянии продолжительной (постоянной) гемофильтрации (ГФ) на показатели оксидативного стресса и компоненты антиоксидантной системы у больных абдоминальным сепсисом в изученной литературе нам не встретилось.
Материал и методы
Продолжительная гемофильтрация использована в интенсивной терапии 27 больных, поступивших в реанимационное отделение института из стационаров подмосковного региона в связи с развитием гнойно-септических осложнений и абдоминального сепсиса. Мужчин было 18, женщин - 9. Большинство пациентов было до 50 лет, что составило 66,7%. Перечень заболеваний, осложненных абдоминальным сепсисом, отражен в таблице 1.
Таблица 1 – Перечень заболеваний с абдоминальным сепсисом
| Заболевание | Число больных | |
| Абс. | % | |
| Острый аппендицит | 11 | 40,7 |
| Акушерско-гинекологическая патология | 4 | 14,8 |
| Повреждения органов брюшной полости | 3 | 11,1 |
| Язвенная болезнь желудка и двенадцатиперстной кишки | 4 | 14,8 |
| Осложнения плановых операций | 3 | 11,1 |
| Спаечная тонкокишечная непроходимость | 1 | 3,7 |
| Панкреатит | 1 | 3,7 |
| Итого | 27 | 100 |
Острый аппендицит чаще всего сопровождается абдоминальным сепсисом. Далее по частоте развития абдоминального сепсиса и синдрома полиорганной дисфункции занимают острая акушерско-гинекологическая патология и язвенная болезнь желудка и двенадцатиперстной кишки.
При обследовании у пациентов выявлены клинико-лабораторные признаки полиорганной дисфункции. Церебральная недостаточность и острое почечное повреждение наблюдались у всех пациентов, причем у (25,9%) пациентов развилась олигоанурия. Печеночная недостаточность была у 11 (40,7 %) пациентов, дыхательная недостаточность (РДСВ) - у 5 (18,5%) больных. Острая сердечная недостаточность зарегистрирована у 6 (22,2%) пациентов абдоминальным сепсисом. Сочетанное поражение органов и систем существенным образом усиливало тяжесть состояния пациентов. У пациентов диагностирован сепсис на основании критериев «Сепсис-3» [10], септический шок развился у 6 (22,2%) пациентов.
Всем больным была выполнена релапаротомия, тщательной лаваж брюшной полости и назоинтестиналыюй интубации. В последующем применяли программную санацию брюшной полости, этиотропную антибиотикотерапию, иммунотерапию, энтеральное зондовое питание.
В раннем послеоперационном периоде применяли продолжительную гемофильтрацию (ГФ). ГФ проводили на аппарате «Окто Нова» «Asahi Kasei Medical» (Япония), используя гемофильтры «Rexeed-21A» той же фирмы. Всего проведено 67 гемофильтраций, средняя продолжительность ГФ 23 часа 15 ± 49,8 мин, средний объем ГФ – 67,2 ± 5,3 литра из расчета 35 мл/кг веса/сутки. Во всех случаях ГФ использовали вено-венозный сосудистый доступ, наиболее часто применяли трехпросветный катетер, который устанавливали в центральную вену (яремную или бедренную). При необходимости, особенно при РДСВ осуществляли дегидратацию в пределах 3 л. При всех ГФ использовали замещающий раствор вводили после гемофильтра. Для замещения применяли полиэлектролитный двухкомпонентный бикарбонатный диализный раствор «Аккусол 4+» фирмы «Nikkiso» в мешках по 5 литров.
Исследование показателей оксидативного стресса проводили у 22 пациентов перед началом гемофильтрации и при ее завершении.
Кровь забирали в пробирки с ЭДТА, центрифугировали, отделяли плазму от эритроцитарной массы. Эритроцитарную массу дважды промывали физиологическим раствором.
Уровень гидроперекисей липидов (ГП) исследовали в эритроцитах и в плазме по методике В. В. Гавриловой, М. И. Мишкорудной [3]. Там же исследовали уровень малонового диальдегида спектрофлюорометрическим методом по способу К. Yagi, уровень α-токоферол (ТФ) исследовали спектрофлюорометрическим методом по способу G.Storer [10].
Общие липиды определяли унифицированными методами. Кроме того, оценку окислительного стресса проводили с помощью расчета коэффициента окислительного стресса К по модифицированной формуле [7]:
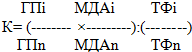
Показатель с индексом «i» равен показателям полученным у пациентов, а цифры с индексом «n» - нормальным значениям. Полученные при исследовании данные обработаны с использованием вариационной статистики.
Результаты исследования и их обсуждение
При анализе результатов исследования , приведенных в таблице № 2, у пациентов абдоминальным сепсисом выявлено развертывание окислительного стресса в крови — проявляющиеся нарастанием эритроцитарных и сывороточных показателей гидроперекисей липидов.
Если пересчитать значения гидроперекисей липидов на 1 г липидов сыворотки, физиологическая норма этого показатели составит 0,26, то у пациентов как до ГФ, так и после ГФ этот показатель будет значительно повышен и составляет 0,46 и 0,44 соответственно. При расчете уровня гидроперекисей липидов на 1 мг эритроцитов, физиологическая норма составит 1,63. У больных пациентов абдоминальным сепсисом как до ГФ, так и после ГФ этот показатель значительно повышен и составляет 2,35 и 2,19 соответственно. После ГФ наблюдается тенденция к улучшению этого показателя. Таким образом, если рассматривать состояние эритроцитарной мембраны как отражение функционального состояния клеточных мембран в других органах, то данному показателю наблюдается активация оксидативного стресса.
При рассмотрении второго вторичного продукта окислительного стресса, нарастание малонового диальдегида (МДА) видно нет его накопления и в плазме и в эритроцитах. Уменьшение значений эритроцитарного МДА после ГФ сопровождается снижением коэффициента МДА/холестерин, физиологическая норма которого составляет 1,63, этот показатель снижается при ГФ с 1,71 до1,38.
Исходное значимое накопление МДА у пациентов абдоминальным сепсисом связано с большим потреблением одного из значимых антиоксидантов α-токоферола, при этом снижены эритроцитарные и плазменные уровни. Гемофильтрация сопровождается повышением плазменного уровня α -токоферола , и это связано с перераспределением α-токоферола в организме.
Известно, что об уровне резервов в организме витамина Е можно предполагать по оценке количества α-токоферола в эритроцитах и по коэффициенту соотношения α-токоферол/общие липиды (индекс Хорвитта), полученные результаты позволяют заключить, что ГФ способствует улучшению тканевых запасов организма витамином Е и тем самым нормализации обмена в мембранах клетки.
Несомненно представляет интерес оценить вклад α-токоферола в поддержание гомеостаза окислительного стресса у пациентов с сепсисом при органной дисфункции и вклад ГФ на эти взаимоотношения. В связи с этим нами для плазмы и эритроцитов рассчитаны степени потребности и обеспеченности, где за 100% взята величина физиологической нормы.
Таблица 2 – Динамика показателей окислительного стресса при продолжительной гемофильтрации (М±m)
| Показатель | Физиологическая норма | Больные | |
| Перед гемофильтрацией | По окончании гемофильтрации | ||
| Липиды общие, г/л | 5,98±0,18 | 5,17±0,32* | 5,18±0,33* |
| Общий холестеринерин , ммоль/л | 4,9±0,09 | 2,53±0,12* | 3,12±0,09** |
| Эритроцитарный холестерин, мг/мл | 0,99±0,033 | 0,98±0,06 | 0,96±0,043 |
| Сывороточные гидроперекиси, единиц оптической плотности. | 1,56±0,11 | 2,40±0,18 | 2,27±0,15 |
| Эритроцитарные гидроперекиси, единиц оптической плотности | 1,61±0,11 | 2,30±0,25* | 2,14±0,16 |
| Сывороточный МДА (нм/л) | 3,28±0,09 | 4,17±0,23 | 3,70±0,16 |
| Эритроцитарный МДА , нм/л | 1,62±0,16 | 1,68±0,16 | 1,32±0,1* |
| Сывороточный α-ТФ, мкм/л | 21,3±0,6 | 14,9±1,2* | 19,7±1,1** |
| Эритроцитарный α-ТФ, мкм/л | 4,15±0,17 | 2,37±0,20* | 2,6±0,29* |
| α –ТФ / ОбЛип | 3,54 | 2,86* | 3,8 |
| Плазменная степень потребности в α-ТФ | 100% | 130% | 165% |
| Эритроцитарная степень потребности в α-ТФ | 100% | 249% | 210% |
| Плазменная степень обеспеченности α-ТФ | 100% | 55% | 82% |
| Эритроцитарная степень обеспеченности α-ТФ | 100% | 25% | 31% |
| Плазменная степень недостаточности α-ТФ | 0 | 45% | 18% |
| Эритроцитарная степень недостаточности α-ТФ | 0 | 75% | 69% |
| Коэффициент окислительного стресса для сыворотки | ≈ 1 | 2,80 | 1,28 |
| Коэффициент окислительного стресса для эритроцитов | ≈ 1 | 2,59 | 1,72 |
Примечание. α-ТФ- α-токоферол, ОбЛип – общие липиды, символ «*» — (р<0,05) достоверность различий между физиологической нормой и больными; ** — между значениями до и после гемофильтрации.
Степень потребности в α-токофероле оказалась повышенной для сывороточного и плазменного α-токоферола. По окончании ГФ данный показатель более значимо снизился в плазме и незначительно — в эритроцитах.
Степень обеспеченности α-ТФ оказалась более низкой в эритроцитах. По окончании гемофильтрации она заметно повысилась в плазме и очень незначительно увеличилась в эритроцитах. Отсюда степень недостаточности в α-ТФ до ГФ была почти вдвое выше в эритроцитах и почти не изменилась в них после гемофильтрации, тогда как заметно поднялась после ГФ в плазме. Последнее свидетельствует о перераспределении α-токоферола после ГФ, но не обеспечивает потребность организма в нем. Эти результаты дают основание для рекомендации о введении α-токоферола пациентам абдоминальным сепсисом как до ГФ, так и после нес.
О глубоком нарушении метаболизма холестерина свидетельствуют данные о резком снижении уровня общего холестерина в сыворотке. Вероятно, понижение уровня холестерина в плазме объясняет стабильное содержание холестерина в эритроцитах.
Рассчитанный коэффициент окислительного стресса К в сыворотке и эритроцитах, в норме приближающийся к единице, исходно увеличен в 2,8 и 2,59 раза, соответственно. После проведения продолжительной гемофильтрации этот показатель существенно улучшился, но оставался повышенным для сыворотки 1,28 и для эритроцитов 1,72 раза. Коррекция окислительного стресса более быстро происходит в сыворотке, чем в эритроцитах.
По нашему мнению, улучшение показателей оксидативного стресса у пациентов с абдоминальным сепсисом после гемофильтрации необходимо связать с тем, что при гемофильтрации наблюдается снижение метаболитов перекисного окисления. Редукция метаболитов перекисного окисления временно протезирует антиоксидантную систему пациента. Видно, что после ГФ маркеры оксидативного стресса и антиоксидантной резистентности не соответствуют физиологическим параметрам, что диктует патогенетическую необходимость назначения препаратов повышающих антиоксидантную защиту.
Раннее в исследованиях было показано, что в процессе ГФ наблюдается улучшение показателей общей и системной гемодинамики, в том числе улучшение кровоснабжения печени [2]. Мы считаем, улучшением метаболических процессов в печени объясняется факт увеличения содержания общего холестерина у пациентов с абдоминальным сепсисом после гемофильтрации.
Выводы
- У пациентов абдоминальным сепсисом наблюдаются активация перекисного окисления липидов и значимое уменьшение содержания в организме α-токоферола. Использование продолжительной гемофильтрации в интенсивной терапии больных абдоминальным сепсисом позволяет усилить антиоксидантную толерантность, но не устранить ее дефицит.
- Динамика взаимоотношений между показателями общего холестерина, показателями перекисного окисления липидов и α-токоферола демонстрирует патогенетическую целесообразность проведения гемофильтрации у больных абдоминальным сепсисом и раскрывает один из механизмов ее эффективности.
- Полученные результаты патогенетически обосновывают применение в интенсивной терапии пациентов абдоминальным сепсисом препаратов с антиоксидантной направленностью.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Абакумов М.М. Ранее применение плазмафереза в комплексной терапии медиастенита / М.М.Абакумов, И.В.Александрова, С.И.Рей и др. // Хирургия. - 2008. - №2. - С.4-9.
- Ватазин А.В. Послеоперационный перитонит. Хирургические концепции и методы экстракорпоральной гемокоррекции / А.В.Ватазин, А.М.Фомин, Е.Е.Круглов, А.Б. Зулькарнаев // М:Бином.- - 416с.
- Гаврилов В.Б. Спектрофотометрическое определение содержания гидроперекисей липидов в плазме крови / В.Б.Гаврилов, М.И.Мишкорудная //Лабораторное дело. - 1983.- №3. - С.33-36.
- Матвеев С.Б Влияние гипохлорида натрия на эндогенную интоксикацию при алкогольном абстинентном синдроме / С.Б.Матвеев, Е.А.Лужников, Е.В.Клычникова, Л.Ф.Панченко и др. // Наркология. - 2014. Т.13. -№4(148).- С.43-46.
- Матвеев С.Б Интегральная оценка эндогенной интоксикации у больных гнойным медистенитом / С.Б.Матвеев, И.В.Александрова, С.И.Рей и др. // Клиническая лабораторная диагностика. - 2008.- №8.- С.12-13.
- Панченко Л.Ф Состояние окислительного стресса у больных с хронической недостаточностью кровообращения при токсической энцефалопатии / Л.Ф.Панченко, А.П.Баранов, Б.В.Давыдов, А.В. Струтынский // Патогенез. - 2015. - Т.13.- №3. - С.23-25.
- Панченко Л.Ф., Давыдов Б.В., Теребилина Н.Н., Баронец В.Ю., Журавлева А.С. Окислительный стресс при алкогольной болезни печени/ Л.Ф.Панченко, Б.В.Давыдов, Н.Н.Теребилина и др. // Биомедицинская химия. - 2018. - Т.59. - Вып.4. - С.452-458.
- Панченко Л.Ф. Содержание маркеров эндотелиальной дисфункции и медиаторов воспаления у больных алкоголизмом с хронической сердечной недостаточностью на конечных стадиях развития / Л.Ф.Панченко, С.В.Пирожков, В.Ю.Баронец и др. // Наркология. - 2018. - Т.17. - №2. - С.20-28.
- True S.M. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)/ S.M.True, C.S.Deutschman, C.Seymour // JAMA. - 2016. - 315. - №8. - P.801-810.
- A simple fluorometric assay for type B monoamine oxidase activity in rat tissues / R.Yagi , O.Suzuki , E.Noguchi // Journal of -1976. -V.79. - №6. - P.1297.
Список литературы на английском языке / References in English
- Abakumov M.M. Raneye primeneniye plazmafereza v kompleksnoy terapii mediastenita [Eary the use of plasmapheresis in complex mediastenitis therapy] / M.M.Abakumov, I.V.Aleksandrova, S.I.Rey and others // Khirurgiya [Surgery]. - 2008. - №2. - S.4-9. [in Russian]
- Vatazin A.V. Posleoperatsionnyy peritonit. Khirurgicheskiye kontseptsii i metody ekstrakorporal'noy gemokorrektsii [Postoperative peritonitis. Surgical concepts and methods of extracorporal hemocorrection] / A.V.Vatazin, A.M.Fomin, Ye.Ye.Kruglov, A.B. Zul'karnayev // M:Binom.- - 416s. [in Russian]
- Gavrilov V.B. Spektrofotometricheskoye opredeleniye soderzhaniya gidroperekisey lipidov v plazme krovi [Spectrophotometric determination of the content of lipid hydroperoxides in blood plasma] / V.B.Gavrilov, M.I.Mishkorudnaya //Laboratornoye delo [Laboratory work]. - 1983. - №3. - S.33-36. [in Russian]
- Matveyev S.B Vliyaniye gipokhlorida natriya na endogennuyu intoksikatsiyu pri alkogol'nom abstinentnom sindrome / S.B.Matveyev, Ye.A.Luzhnikov, Ye.V.Klychnikova, L.F.Panchenko and others [Influence of sodium hypochlorite on endogenous intoxication in alcohol withdrawal syndrome] // Narkologiya [Narcology]. - 2014. - T.13. -№4 (148). - S.43-46. [in Russian]
- Matveyev S.B. Integral'naya otsenka endogennoy intoksikatsii u bol'nykh gnoynym medistenitom [Integral assessment of endogenous intoxication in patients with purulent mediastenitis] / S.B.Matveyev, I.V.Aleksandrova, S.I.Rey and others// Klinicheskaya laboratornaya diagnostika [Clinical laboratory diagnostics]. - 2008. - №8.- S.12-13. [in Russian]
- Panchenko L.F. Sostoyaniye okislitel'nogo stressa u bol'nykh s khronicheskoy nedostatochnost'yu krovoobrashcheniya pri toksicheskoy entsefalopatii [The state of oxidative stress in patients with chronic circulatory insufficiency with toxic encephalopathy] / L.F.Panchenko, A.P.Baranov, B.V.Davydov, A.V. Strutynskiy // Patogenez [Pathogenesis]. - 2015. - T.13. - №3. - S.23-25. [in Russian]
- Panchenko L.F. Zhuravleva A.S. Okislitel'nyy stress pri alkogol'noy bolezni pecheni [Oxidative stress in alcoholic liver disease]/ L.F.Panchenko, B.V.Davydov, N.N.Terebilina and others // Biomeditsinskaya khimiya [Biomedical Chemistry]. - 2018. - T.59. - Vyp.4. - S.452-458. [in Russian]
- Panchenko L.F. Soderzhaniye markerov endotelial'noy disfunktsii i mediatorov vospaleniya u bol'nykh alkogolizmom s khronicheskoy serdechnoy nedostatochnost'yu na konechnykh stadiyakh razvitiya [The content of markers of endothelial dysfunction and inflammatory mediators in patients with alcoholism and chronic heart failure at the final stages of development] / L.F.Panchenko, S.V.Pirozhkov, V.YU.Baronets and others // Narkologiya [Narcology]. - 2018. - T.17. - №2. - 20-28. [in Russian]
- True S.M. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)/ S.M.True, C.S.Deutschman, C.Seymour // JAMA. - 2016. - 315. - №8. - P.801-810.
- A simple fluorometric assay for type B monoamine oxidase activity in rat tissues / R.Yagi , O.Suzuki , E.Noguchi // Journal of -1976. -V.79. - №6. - P.1297.
