ОПРЕДЕЛЕНИЕ ДИМЕТИЛАМИНА В ВОДНЫХ ИСТОЧНИКАХ РАЗЛИЧНОГО ГЕНЕЗИСА МЕТОДОМ ВЭЖХ
ОПРЕДЕЛЕНИЕ ДИМЕТИЛАМИНА В ВОДНЫХ ИСТОЧНИКАХ РАЗЛИЧНОГО ГЕНЕЗИСА МЕТОДОМ ВЭЖХ
Научная статья
Федорова Н.Е.1, Ивченкова А.А.2, Бондарева Л.Г.3, *
1 ORCID: 0000-0001-8278-6382;
2 ORCID: 0000-0003-1342-1536;
3 ORCID: 0000-0002-1482-6319;
1, 2, 3 Федеральный научный центр гигиены им. Ф.Ф. Эрисмана Роспотребнадзора, Мытищи, Россия
* Корреспондирующий автор (bondarevalg[at]fferisman.ru)
АннотацияНа основании собственных и опубликованных ранее информации, разработан высокоэффективный метод определения концентрации вторичного алифатического амина - диметиламина в воде различного генезиса. Метод жидкостной хроматографией с флуориметрическим детектором, с предварительной дериватизацией проб воды, позволяет с высокой селективностью определять диметиламин в воде, что было подтверждено на модельных системах с внесением различных концентраций диметиламина в диапазоне от 0,005 до 0,1 мг/л. Это вполне удовлетворяет требования, предъявляемые действующими нормативными документами Российской Федерации. Метод продемонстрировал высокую эффективность ~ 97 %, при суммарной погрешности методики измерения концентраций диметиламина в воде методом высокоэффективной жидкостной хроматографии с FLD не более 25 %.
Ключевые слова: диметиламин, вода, высокоэффективная жидкостная хроматография, флуориметрический детектор.
DETERMINING DIMETHYLAMINE IN WATER SOURCES OF VARIOUS GENESIS VIA HPLC
Research article
Fedorova N.E.1, Ivchenkova A.A.2, Bondareva L.G.3, *
1 ORCID: 0000-0001-8278-6382;
2 ORCID: 0000-0003-1342-1536;
3 ORCID: 0000-0002-1482-6319;
1, 2, 3 F. F. Erisman Federal Scientific Center of Hygiene of Rospotrebnadzor, Mytishchi, Russia
* Corresponding author (bondarevalg[at]fferisman.ru)
AbstractBased on the authors' own previously published information, the article introduces a highly effective method for determining the concentration of secondary aliphatic amine - dimethylamine in water of various genesis. The method of liquid chromatography with a fluorometric detector, with preliminary derivatization of water samples, allows for determining dimethylamine in water with high selectivity, which was confirmed on model systems with the introduction of various concentrations of dimethylamine in the range from 0.005 to 0.1 mg/l. This fully meets the requirements imposed by the current regulatory documents of the Russian Federation. The method demonstrated high efficiency of ~ 97 %, with a total error of the method for measuring dimethylamine concentrations in water by high-performance liquid chromatography with FLD of no more than 25 %.
Keywords: dimethylamine, water, high-performance liquid chromatography, fluorimetric detector.
ВведениеАлифатические амины являются распространёнными составляющими растворенных органических веществ и присутствуют в повышенных концентрациях в водах различного генезиса, особенно загрязненных стоками. Короткоцепочечные алифатические амины повсеместно встречаются в водных средах из-за их широкого применения в химической и фармацевтической промышленности. Кроме того, алифатические амины являются распространенными компонентами биологических систем в качестве продуктов разложения органических материалов, таких как аминокислоты и белки [1], [2], [3]. Из-за высокой реакционной способности реакции алифатических аминов с озоном могут происходить во время озонирования воды и очистки сточных вод. В литературе описаны исследования кинетики и механизмов реакций озона с этиламином, диметиламином и триэтиламином, как модельными азотистыми соединениями [4]. Анализ показал, что все амины превращались в продукты, содержащие связь азот-кислород (например, N-оксид триэтиламина, нитроэтан, нитрозоамин) с химическим выходом в диапазоне от 64-100 % по отношению к исходным аминам. Было сделано заключение о том, что при озонировании воды, содержащей высокие уровни растворенного органического азота, образуются нитро- и нитрозо- алканы [4]. Также алкиламины могут реагировать с определенными азотсодержащими соединениями, также с образованием нитрозоаминов, которые являются канцерогенами.
Помимо проблем гигиены, из-за резкого запаха указанные соединения представляют опасность для жизни человека, поскольку являются раздражителями кожи, глаз, слизистой оболочки и дыхательных путей.
В качестве представителя вторичных алкиламинов, диметиламин широко применяется в разных областях промышленности: в синтезе инсектицидов, гербицидов, моющих средств, растворителей и лекарственных средств. Служит сырьём для производства гептила – ракетного топлива. Использовался в производстве химического оружия (табуна). Кроме того, диметиламин, как и другие вторичные амины, являются продуктами биодеградации целого ряда поверхностно-активных веществ в условиях окружающей среды [5], [6].
Содержание ряда органических аминов нормировано в питьевой воде централизованных систем питьевого водоснабжения согласно санитарным нормам [7] и в водных объектах рыбохозяйственного значения [8]. Так, например, содержание диметиламина в питьевой воде – 0,1 мг/л [7], в воде рыбохозяйственного значения – 0,005 мг/л [8].
Для определения алифатических аминов в воде, как правило, используют хроматографические методы. В частности, описан ряд методик определения аминов с помощью газовой (ГХ) [9], [10] и жидкостной хроматографии (ЖХ) [11], [12] и др. Две из которых входит в реестр методик, используемых службами Роспотребнадзора [13] и [14]. Однако же, данные методики не удовлетворяют современные требования по чувствительности, селективности, точности определения.
С учетом выше сказанного, возникла необходимость в разработке принципиально нового метода определения диметиламина, как представителя алифатических аминов в воде, отобранной в ряде водных источников, в том числе и центрального водоснабжения.
Принцип отбора и подготовка образцов воды к анализу
Воду поверхностных водоемов и из системы центрального водоснабжения отбирали в стеклянные бутылки емкостью 0,5 л. Отобранные пробы рекомендуется хранить и транспортировать при температуре не более 10 оС. В лаборатории пробы должны храниться в холодильник при температуре (2-6) оС не более 3 дней.
Непосредственно перед анализом воду перемешивали в бутылях, в которых вода хранилась. Необходимый для каждого анализа объем воды пропускают через шприцевой мембранный фильтр с размером пор 0,45 мкм.
Результаты и их обсуждениеВ качестве методов пробоподготовки используют жидкостно–жидкостную экстракцию [15], [16], твердофазную экстракцию [17], [18], ион-парную экстракцию [19] и т.д. Большинство указанных методов длительны и требуют использования значительных объемов дорогостоящих и токсичных реагентов [20].
Ранее специалистами ФБУН «ФНЦГ им. Ф.Ф. Эрисмана» Роспотребнадзора была разработана методика по определению глифосата в пробах воды и почвы методом жидкостной хроматографии с масс-спектрометрическим детектированием. В разработанной методике образцы воды очищали на патронах для твердофазной экстракции, а затем дериватизируют с использованием 0,01M раствора 9-флуоренилметилхлороформиата (FMOC) в среде боратного буфера с последующей очисткой толуолом. Данная методика показала эффективность применения дериватизации для определения аминов. Однако, диметиламин обладает малой молекулярной массой, что делает затруднительным его определение с помощью масс-детектора.
Поэтому мы решили пойти по другому пути. Предлагается следующая, как наиболее эффективная схема подготовки пробы воды для определения диметиламина. Отфильтрованная через мембранный фильтр проба воды подвергается дериватизации раствором 9-флуоренилметилхлорформиата в среде тетрабората натрия.
В ходе проведенных исследований изучалось влияние температуры на прохождение стадии дериватизации. Реакцию проводили при 50 °С и комнатной температуре. Выяснилось, что температурный режим не оказывает влияние на полноту протекания данной реакции – площадь пика диметиламина оставалась без изменений.
Для остановки дериватизации в смесь добавляли ледяную уксусную кислоту и затем реализовывали стадию отмывки от избытка дериватизирующей смеси. Для этого исследовали применение толуола и гексана. В наших экспериментах толуол давал устойчивые мутные не расслаивающиеся растворы, что требовало дополнительной стадии фильтрации и влекло потерю целевого компонента. Таких проблем не наблюдалось при использовании гексана, и он был выбран в качестве экстрагента.
Таким образом, была разработана следующая схема подготовки проб воды при определении остаточных количеств диметиламина: в стеклянную пробирку с притертой пробкой на 5 мл помещали 0,4 мл отфильтрованной пробы воды. Добавляли 0,5 мл 0,01 М раствора 9-флуоренилметилхлорформиата (FMOC) и 0,5 мл 0,025 М раствора тетрабората натрия. Помещали пробирку на 10 минут на аппарат для встряхивания (вортекс). Затем добавляли 5 мкл ледяной уксусной кислоты, интенсивно встряхивали. После чего добавляли 2 мл гексана, помещали на аппарат для встряхивания (вортекс) на 3 минуты. После расслоения фаз верхний слой гексана удаляли пипеткой. Для анализа брали нижний слой.
Кроме того, рассматривался вопрос влияния состава подвижной фазы на формирование и деление пиков. Эксперимент показал, что при содержании в подвижной фазе 0,2% ортофосфорной кислоты необходимого разделения не происходит, тогда как при замене ортофосфорной кислоты на уксусную наблюдался четкий симметричный пик целевого соединения.
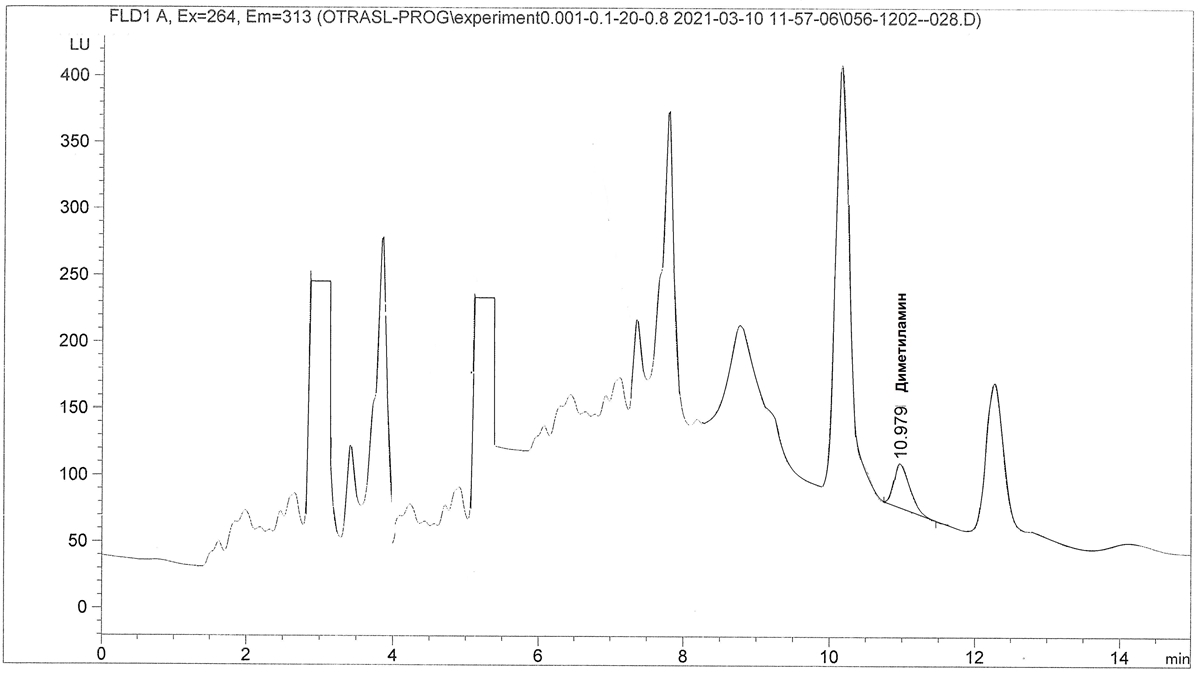
На основании проведенных экспериментов обоснованы следующие условия хроматографирования: Жидкостной хроматограф Agilent-1200 фирмы Agilent (США) с флуориметрическим детектором, колонка ZORBAX Eclipse XDB-C18 (150 мм х 4,6 мм х 5мкм), подвижная фаза: ацетонитрил - 0,2% уксусная кислота (55:45, по объему); скорость потока элюента: 0,8 см3/мин; длина волны: возбуждение 264 нм; длина волны: эмиссия 313 нм; объем вводимой пробы: 20 мм3. Ориентировочное время выхода диметиламина: 10,9-11,0 мин (рис. 1). Линейный диапазон детектирования: 0,1-2 нг.
Рис. 1 – Хроматограмма стандартного раствора диметиламина с концентрацией 0,01 мкг/мл
Диапазон определяемой концентрации диметиламина в пробах воды составил - 0,005 – 0,1 мг/л, что удовлетворяет требованиям для питьевой воды централизованных систем питьевого водоснабжения [7] и для водных объектов рыбохозяйственного значения [8].
Разработанная методика опробована при анализе проб питьевой воды и модельных растворов.
Для оценки правильности результатов использовали способ введено–найдено. В анализируемые образцы воды вводили известные объемы стандартного раствора диметиламина (табл.1).
Таблица 1 – Результаты определения диметиламина в пробах водопроводной воды (n = 5, P = 0.95)
| № | Внесено диметиламина, мг/дм3 | Найдено диметиламина, (Сср) мг/дм3 (%) | Стандартное отклонение, мг/дм3 |
| 1 | 0,005 | 0,005464 (109,3) | 3,9·10-4 |
| 2 | 0,01 | 0,010301 (103,0) | 7,07·10-4 |
| 3 | 0,02 | 0,017265 (86,3) | 7,67·10-4 |
| 4 | 0,1 | 0,089405 (89,4) | 1,64·10-3 |
Разработанный нами метод имеет хорошую эффективность – до 97 %. При этом суммарная погрешность методики измерения концентраций диметиламина в воде методом высокоэффективной жидкостной хроматографии с FLD не превышала 25 %.
ЗаключениеТаким образом, разработан порядок применения метода высокоэффективной жидкостной хроматографии для определения в воде питьевой систем централизованного, в том числе горячего, и нецентрализованного водоснабжения, в воде подземных и поверхностных водных объектов хозяйственно-питьевого и культурно-бытового водопользования, в воде плавательных бассейнов и аквапaрков массовой концентрации диметиламина в диапазоне 0,005 – 0,1 мг/дм3.
| Финансирование Работа выполнена при финансовой поддержке Государственной программы «Обеспечение химической и биологической безопасности РФ на 2021-2024 г.». | Funding This work was financially supported by the State Program of the Russian Federation "Ensuring the Chemical and Biological Safety of the Russian Federation for 2021-2024". |
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Zhao Y.Y. Determination of aliphatic amines using N-succinimidyl benzoate as a new derivatization reagent in gas chromatography combined with solid phase microextraction / Zhao Y.Y., Cai L.S., Jing Z.Z.et al. // J. Chromatogr. A. - 2003. - V. 1021. - P. 175-183.
- Psillakis E. Application of solvent microextraction to the analysis of nitroaromatic explosives in water samples / Psillakis E., Kalogerakis N. // J. Chromatogr. A. - 2001. - V. 907. - P. 211-218.
- Belloli R. Determination of toxic nitrophenols in the atmosphere by high-performance liquid chromatography / Belloli R., Barlcatta B., Bolzacchini E. et al. // J. Chromatogr. A. - 1999. - V. 846. - P. 277-288.
- LimS. Reactions of aliphatic amines with ozone: Kinetics and mechanisms / LimS., McArdell C. S., von Gunten U.// Water Res. – 2019. – 157. - P. 514-528.
- García M. T. Effect of the alkyl chain length on the anaerobic biodegradability and toxicity of quaternary ammonium-based surfactants / García M. T., Campos E., Sanchez-Leal J. et al. // Chemosphere. 1999. - V. 38. – No 15. – P. 3473–3483.
- Giolando S. T. Environmental fate and effects of DEEDMAC: a new rapidly biodegradable cationic surfactant for use in fabric softeners / Giolando S. T., Rapaport R. A., Larson R. J., et al. // Chemosphere. – 1995. - V. 30. - no. 6. – P. 1067–1083.
- СанПиН 1.2.3685-21 «Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания», утверждены Постановлением Главного государственного санитарного врача РФ от 28.01.2021, № 2.
- Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения. Приказ № 16326 Федерального агентства по рыболовству.
- Luonga J. Ultra-trace level analysis of morpholine, cyclohexylamine, and diethylaminoethanol in steam condensate by gas chromatography with multi-mode inlet, and flame ionization detection / Luonga J., Shellie R.A., Cortesa H. et al. // J. Chromatogr. A. - 2012. - V. 1229. - P. 223-229.
- Kataoka H. Derivatization reactions for the determination of amines by gas chromatography and their applications in environmental analysis / H. Kataoka // J. Chromatogr. A. - 1996. - V. 733. - P. 19-25.
- Meseguer Lloret S. Sensitive determination of aliphatic amines in water by high-performance liquid chromatography with chemiluminescence detection / Meseguer Lloret S., Molins Legua C., Verdu Andres J. et al. // J. Chromatogr. A. - 2004. - V. 1035. - P. 75-80.
- Sahasrabuddhey B. Determination of ammonia and aliphatic amines in environmental aqueous samples utilizing pre-column derivatization to their phenylthioureas and high-performance liquid chromatography / Sahasrabuddhey B., Archana Jain and Krishna K. Verma. // Analyst. - 1999. -124. - P. 1017-1021.
- МУК 4.1.1674-03. Измерение концентрации диметиламина в воде газохроматографическим методом. МинЗдрав России. – 2003.
- МУК 4.1.008-13. Методика измерений массовой концентрации диметиламина в пробах питьевых, природных, очищенных сточных и талых (снег) вод фотометрическим методом. ФМБА. - 2018.
- Weiss T. Simultaneous determination of various aromatic amines and metabolites of aromatic nitro compounds in urine for low level exposure using gas chromatography-mass spectrometry / Weiss T., Angerer J. // J. Chromatogr. B. -2002. - V. 778. - P. 179-183.
- Sarafraz Yazdi A. Liquid−liquid−liquid phase microextraction of aromatic amines in water using crown ethers by high-performance liquid chromatography with monolithic column / Sarafraz Yazdi A., Eshaghi Z. // Talanta. - 2005. - V. 66. - P. 664-670.
- Meseguer Lloret S. Preconcentration and dansylation of aliphatic amines using C18 solid-phase packings: Application to the screening analysis in environmental water samples / Meseguer Lloret S., Molins Legua C., Campins Falco P. // J. Chromatogr.A. - 2002. - V. 978. - P. 59-63.
- Abalos M. Development of a solid-phase microextraction GC-NPD procedure for the determination of free volatile amines in wastewater and sewage-polluted waters / Abalos M., Bayona J.M., Ventura F. // Anal. Chem. - 1999. - V. 71. - P. 3531-3541.
- Akyuz M. Simultaneous determination of aliphatic and aromatic amines in water and sediment samples by ion-pair extraction and gas chromatography-mass spectrometry / Akyuz M., Ata S. // J. Chromatogr. A. - 2006. - V. 1129. - P. 88-92.
- Rezaee M. Determination of organic compounds in water using dispersive liquid−liquid microextraction / Rezaee M., Assadi Y., Hosseini M.-R.M. et al. // J. Chromatogr. A. - 2006. - V. 1116. - P. 1-5.
Список литературы на английском языке / References in English
- Zhao Y.Y. Determination of aliphatic amines using N-succinimidyl benzoate as a new derivatization reagent in gas chromatography combined with solid phase microextraction / Zhao Y.Y., Cai L.S., Jing Z.Z.et al. // J. Chromatogr. A. - 2003. - V. 1021. - P. 175-183.
- Psillakis E. Application of solvent microextraction to the analysis of nitroaromatic explosives in water samples / Psillakis E., Kalogerakis N. // J. Chromatogr. A. - 2001. - V. 907. - P. 211-218.
- Belloli R. Determination of toxic nitrophenols in the atmosphere by high-performance liquid chromatography / Belloli R., Barlcatta B., Bolzacchini E. et al. // J. Chromatogr. A. - 1999. - V. 846. - P. 277-288.
- LimS. Reactions of aliphatic amines with ozone: Kinetics and mechanisms / LimS., McArdell C. S., von Gunten U.// Water Res. – 2019. – 157. - P. 514-528.
- García M. T. Effect of the alkyl chain length on the anaerobic biodegradability and toxicity of quaternary ammonium-based surfactants / García M. T., Campos E., Sanchez-Leal J. et al. // Chemosphere. 1999. - V. 38. – No 15. – P. 3473–3483.
- Giolando S. T. Environmental fate and effects of DEEDMAC: a new rapidly biodegradable cationic surfactant for use in fabric softeners / Giolando S. T., Rapaport R. A., Larson R. J., et al. // Chemosphere. – 1995. - V. 30. - no. 6. – P. 1067–1083.
- SanPiN 1.2.3685-21 «Gigienicheskie normativy i trebovanija k obespecheniju bezopasnosti i (ili) bezvrednosti dlja cheloveka faktorov sredy obitanija» ["Hygienic standards and requirements for ensuring the safety and (or) harmlessness of environmental factors for humans"], approved by the Decree of the Chief State Sanitary Doctor of the Russian Federation of 01.28.2021, No. 2. [in Russian]
- Ob utverzhdenii normativov kachestva vody vodnyh ob’ektov rybohozjajstvennogo znachenija, v tom chisle normativov predel'no dopustimyh koncentracij vrednyh veshhestv v vodah vodnyh ob’ektov rybohozjajstvennogo znachenija [On approval of water quality standards for water bodies of fishery significance, including standards for maximum permissible concentrations of harmful substances in waters of water bodies of fishery significance]. Order No. 16326 of the Federal Agency for Fisheries. [in Russian]
- Luonga J. Ultra-trace level analysis of morpholine, cyclohexylamine, and diethylaminoethanol in steam condensate by gas chromatography with multi-mode inlet, and flame ionization detection / Luonga J., Shellie R.A., Cortesa H. et al. // J. Chromatogr. A. - 2012. - V. 1229. - P. 223-229.
- Kataoka H. Derivatization reactions for the determination of amines by gas chromatography and their applications in environmental analysis / H. Kataoka // J. Chromatogr. A. - 1996. - V. 733. - P. 19-25.
- Meseguer Lloret S. Sensitive determination of aliphatic amines in water by high-performance liquid chromatography with chemiluminescence detection / Meseguer Lloret S., Molins Legua C., Verdu Andres J. et al. // J. Chromatogr. A. - 2004. - V. 1035. - P. 75-80.
- Sahasrabuddhey B. Determination of ammonia and aliphatic amines in environmental aqueous samples utilizing pre-column derivatization to their phenylthioureas and high-performance liquid chromatography / Sahasrabuddhey B., Archana Jain and Krishna K. Verma. // Analyst. - 1999. -124. - P. 1017-1021.
- MUK 4.1.1674-03. Izmerenie koncentracii dimetilamina v vode gazohromatograficheskim metodom [Measurement of the concentration of dimethylamine in water by gas chromatography]. Ministry of Health of Russia. - 2003. [in Russian]
- MUK 4.1.008-13. Metodika izmerenij massovoj koncentracii dimetilamina v probah pit'evyh, prirodnyh, ochishhennyh stochnyh i talyh (sneg) vod fotometricheskim metodom [Methods for measuring the mass concentration of dimethylamine in samples of drinking, natural, purified waste and melt (snow) waters by the photometric method]. FMBA. - 2018. [in Russian]
- Weiss T. Simultaneous determination of various aromatic amines and metabolites of aromatic nitro compounds in urine for low level exposure using gas chromatography-mass spectrometry / Weiss T., Angerer J. // J. Chromatogr. B. -2002. - V. 778. - P. 179-183.
- Sarafraz Yazdi A. Liquid−liquid−liquid phase microextraction of aromatic amines in water using crown ethers by high-performance liquid chromatography with monolithic column / Sarafraz Yazdi A., Eshaghi Z. // Talanta. - 2005. - V. 66. - P. 664-670.
- Meseguer Lloret S. Preconcentration and dansylation of aliphatic amines using C18 solid-phase packings: Application to the screening analysis in environmental water samples / Meseguer Lloret S., Molins Legua C., Campins Falco P. // J. Chromatogr.A. - 2002. - V. 978. - P. 59-63.
- Abalos M. Development of a solid-phase microextraction GC-NPD procedure for the determination of free volatile amines in wastewater and sewage-polluted waters / Abalos M., Bayona J.M., Ventura F. // Anal. Chem. - 1999. - V. 71. - P. 3531-3541.
- Akyuz M. Simultaneous determination of aliphatic and aromatic amines in water and sediment samples by ion-pair extraction and gas chromatography-mass spectrometry / Akyuz M., Ata S. // J. Chromatogr. A. - 2006. - V. 1129. - P. 88-92.
- Rezaee M. Determination of organic compounds in water using dispersive liquid−liquid microextraction / Rezaee M., Assadi Y., Hosseini M.-R.M. et al. // J. Chromatogr. A. - 2006. - V. 1116. - P. 1-5.