Biochemical aspects of non-carious lesions of dental hard tissues occurring during odontogenesis
Biochemical aspects of non-carious lesions of dental hard tissues occurring during odontogenesis
Abstract
The article presents a literature review that examines the biochemical aspects of the occurrence of non-carious lesions of teeth associated with the influence of exogenous or endogenous factors during the mineralization of dental rudiments and the formation of enamel and dentin. A key role in the process of mineralization of dental hard tissues is played by specific proteins containing phosphoserine, glutamate and aspartate residues, which bind calcium ions, contributing to the formation of apatite crystals. Excess fluoride ingested by pregnant women and infants leads to the development of fluorosis. At high concentrations of fluoride inhibits the proliferation of ameloblasts, disrupts the formation of phosphoserine. Fluoride is also able to bind to the active centre of serine proteinases, inhibiting limited proteolysis of high molecular weight proteins of enamel matrix. Negative impact of factors causing changes in mineral and protein metabolism leads to enamel and dentin hypoplasia due to impaired synthesis and functioning of regulatory proteins and enzymes such as enamelins, amelogenins, ameloblastin, amelotin, taftelin, dentinsialophosphoprotein, kallikrein-4 and MMP-20. The intake of tetracycline antibiotics by pregnant women and young children leads to the occurrence of "tetracycline teeth", as tetracyclines inhibit protein synthesis in the 70S ribosome, causing pathological changes in the development of dental tissues. Thus, clinicians face a particularly acute issue of prevention of non-carious lesions and the choice of safe pharmacotherapy, taking into account the impact of external and internal factors affecting biochemical processes during odontogenesis.
1. Введение
Формирование постоянных зубов – это сложный и многоэтапный процесс, начиная с момента закладки зачатков зубов и заканчивая прорезыванием зубов в ротовой полости на различных стадиях морфогенеза зубных тканей
. Воздействие негативных эндогенных и экзогенных приводит к уменьшению толщины эмали, изменению размера и формы кристаллов гидроксиапатита (ГАП), а также к увеличению массы органического матрикса . Многообразными факторы (экзогенные и эндогенные) являются причинами нарушения развития зачатков зубов. К числу эндогенных факторов относят генетические отклонения, сопряженные с наследственным недоразвитием эктодермальных и мезодермальных тканей зародыша, а также эндокринные заболевания . Между тем, выделяют экзогенные причины, к которым относят: проживание беременных женщин в неблагоприятных экологических условиях, травмы, полученные при родах, осложнения детских инфекций и приём лекарственных препаратов во время развития и минерализации твердых тканей зубов , . Множество лекарственных препаратов, таких как гормональные препараты, салицилаты и некоторые витамины при регулярном и длительном применении могут нарушать минеральный обмен и, в конечном итоге, явиться причиной возникновения некариозных поражений зубов .На сегодняшний день, изучение воздействия внешних и внутренних факторов на развитие зачатков зубов и их роли в возникновении некариозных поражений постоянных зубов является актуальной темой стоматологических исследований, в этом вопросе особый интерес представляют биохимические аспекты данного вопроса
.2. Основная часть
К некариозным поражениям, которые возникают на различных этапах формирования зуба, относят системную гипоплазию, флюороз, гиперплазию зубов и «тетрациклиновые зубы»
, . В России, согласно эпидемиологическому стоматологическому обследованию, 43% некариозных поражений возникают в период развития твердых тканей зубов . Особенно уязвимым периодом для появления некариозной патологии является период минерализации зачатков зубов и амелогенез (процесс формирования эмали), а также период недостаточной минерализации эмали, который длится до трех лет после прорезывания зубов , .Белки, являющиеся основой твердых тканей зуба, играют важную роль в построении органической матрицы, регулируя их минерализацию
. Все белки минерализованных тканей содержат остатки аспарагиновой и глутаминовой аминокислот, а также фосфосерин, связывающие Са2+для формирования кристаллов ГАП . В процессе развития эмали энамелобласты вырабатывают высокомолекулярные гликофосфопротеины, подвергающиеся ограниченному протеолизу при помощи ферментов: энамелизинов (ММП-20), калликреинов и матриксных сериновых протеиназ, превращаясь в низкомолекулярные . 75% неорганических компонентов эмали представлено ГАП Ca10(PO4)6(OH)2, 12% составляет карбонатный апатит Ca10(PO4)6(СО3)2(OH)2, доля фторапатита Ca10(PO4)6F2 -1%, а также встречаются иные формы апатитов, которые связаны с органической матрицей . Фторапатит образуется вследствие равных ионных радиусов фтор-иона и гидроксил-иона, одинакового заряда и равных степеней гидратации, ввиду этого происходит изменение структуры кристалла (см. рис. 1):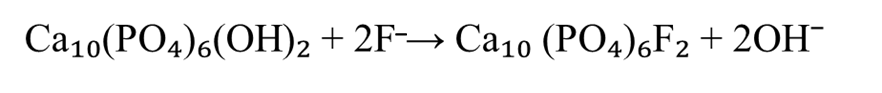
Рисунок 1 - Структура кристалла фторапатита
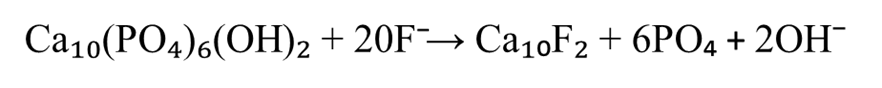
Рисунок 2 - Образование фторида кальция
Избыточная концентрация фторидов, поступающая в организм беременной женщины и ребенка, угнетает пролиферацию амелобластов, к тому же, фтор может вступать в реакцию с гидроксильными группами серина, входящего в состав полипептидных цепей белков, блокируя образование фосфосерина, принимающего участие в процессе минерализации твердых тканей зуба
. Также необходимо отметить, что в высоких концентрациях F связывается с активным центром сериновых протеиназ, при этом ингибируется частичный протеолиз высокомолекулярных белков эмалевого матрикса до низкомолекулярных. Поэтому в эмали прорезавшегося зуба пациентов с эндемическим флюорозом отмечается более высокая концентрация воды и белков, сопутствующее снижением содержания кальция, сопровождающегося изменением проницаемости эмали, а также снижением ее микротвердости .Проведение микрорентгеноспектрального анализа у пациентов с флюорозом позволило обнаружить молекулярные изменения в кристаллической решетке гидроксиапатита (ГАП) и нарушения процесса минерализации эмали. При оптическом микроскопическом исследовании заметно, что даже при легкой стадии флюороза, периферические участки эмали выглядят разрывистыми и узкими меловидными полосками
. Однако, при очень тяжелых формах флюороза, при использовании электронного микроскопа, можно выявить фокусы полного распада эмали, чередующиеся с участками аморфной структуры, содержащей кристаллы различных размеров и формы ГАП . Интересно отметить, что среди них присутствуют и кристаллы ГАП с нормальным строением. В основном, морфологические изменения эмали, которые можно обнаружить на поверхностном слое, являются необратимыми .К необратимым изменениям, нарушающим формирование эмали, помимо вышеперечисленных патологий, относят гипоплазию зубов
. Причиной данной патологии является негативное действия на организм эмбриона или ребенка разнообразных факторов в период закладки зачатков зубов, которые способствуют нарушениям в минеральном обмене и обмене белков . Воздействие внешних или внутренних факторов на метаболизм только энамелобластов приводит к возникновению гипоплазии эмали, при одновременном поражении энамелобластов и одонтобластов, диагностируется гипоплазия эмали и дентина. Нарушения синтеза и деятельности регуляторных белков и ферментов лежат в основе биохимических аспектов гипоплазии. К ним относят: энамелины, амелогенины, амелобластин, калликреин-4, энамелизин, амелотин, тафтелин и дентинсиалофосфопротеин (фосфофорин) . Впоследствии происходит нарушение минерализации и созревания эмали, приводящие к её истончению, изменению цвета и уменьшению размера, а также к появлению в области коронковой части зуба бороздок, ямок и углублений .По данным исследователей, гипоплазия во временном прикусе является следствием сбоев в организме беременной женщины, а причиной гипоплазии постоянных зубов является ряд заболеваний (например, острые инфекционные заболевания, алиментарная дистрофия, болезни желудочно-кишечного тракта, рахит у детей и др.)
. Вышеперечисленными патологиями ребенок заболевает в период формирования и минерализации зубов, на которых появились очаги гипоплазии. Гипопластические дефекты зубов остаются на протяжении всей жизни .С середины XX века началось использование препаратов тетрациклиновой группы, что в 1956 года привело к обнаружению нового вида гипоплазии эмали – «тетрациклиновые зубы». Ученые установили, что данное заболевание возникает при приёме беременными женщинами и детьми младшего возраста антибиотиков тетрациклинового ряда в период развития молочных зубов или зубов постоянного прикуса . Тетрациклины, широко используемые в клинической практике, оказались ингибиторами синтеза белка в 70S рибосоме
. Тетрациклины свободно проникают через мембраны клеток, замедляют связывание аминоацил-тРНК с аминоацильным центром в 50S субчастице рибосомы. Нарушение синтеза белка приводит к патологическим изменениям на ранних этапах развития тканей зуба и к возникновению дефектов минерализованных тканей. К ним относят: уменьшение толщины эмали, изменение размеров и формы кристаллов ГАП и увеличении массы органического матрикса . Это происходит потому, что тетрациклины блокируют связывание аминоацил-тРНК с А-центр рибосомы, вследствие этого происходит нарушение элонгации полипептидной цепи. Нарушения в синтезе белка негативно сказывается на образовании первичных кристаллов ГАП в эмали и дентине. Применение тетрациклинов в третьем триместре беременности приводит к изменению цвета молочных зубов, в первую очередь затрагивая резцы и жевательную поверхность моляров. При приеме препаратов тетрациклинового ряда на девятом месяце беременности окрашиваются молочные зубы и жевательная поверхность шестых зубов постоянного прикуса . При назначении тетрациклиновых препаратов ребенку в первые дни и недели после рождения, окрашивание затрагивает ту часть молочных зубов и первых постоянных моляров, которые в это время активно минерализуются . Окрашивание зубов препаратами тетрациклинового ряда обусловлено его способностью проникать через плацентарный барьер и накапливаться в дентине и в эмали зубов. Предполагается, что критическая доза тетрациклина для окрашивания зубов составляет от 22 до 26 мг/кг и более. Под действием ультрафиолетовых лучей образуется тетрациклин-кальций-ортофосфатный комплекс, который придает зубам более темную окраску. Тетрациклины имеют свойство образовывать нерастворимые комплексы с многовалентными ионами (Са²⁺, Mg²⁺, AIᶾ⁺, Fe²⁺, Feᶾ⁺), что позволяет им накапливаться в развивающихся зубах и костной ткани, приводя к возникновению несовершенного амелогенеза и дентиногенеза , . После приема тетрациклинов зубы приобретают светло-желтый или темно-желтый цвет, причем коронковая часть зуба окрашивается не полностью, а затрагивает только минерализующаяся область коронки.Для лечения инфекционных болезней применяются лекарственные средства, являющиеся ингибиторами синтеза ДНК и РНК или других белков
. Использование ингибиторов матричных биосинтезов оказывает как положительное, так и отрицательное воздействие. С одной стороны, они оказывают положительный эффект при лечении инфекционных заболеваний, замедляя рост и размножения патогенных микроорганизмов, а с другой стороны, ингибиторы матричных биосинтезов негативно сказываются на нормальных биологических процессах в организме .В список фармакологических препаратов, являющихся ингибиторами матричных биосинтезов относят: ингибиторы транскрипции (рифампицин), ингибиторы репликации и транскрипции (актиномицин D, номермицин, новобиоцин, дауномицин, доксорубицин), ингибиторы трансляции (стрептомицин, эритромицин, левомицетин, тетрациклины)
.Тетрациклин-бактериостатический антибиотик, поэтому беременным женщинам и кормящим женщинам рекомендуется принимать препараты с аналогичным действием . В эту группу входят макролиды. Следует также помнить, что помимо тетрациклина ингибиторы матричного синтеза могут оказывать токсическое воздействие на другие органы или создавать ситуации, опасные для жизни беременной женщины и новорожденного. Например, использование рифамицина в последние недели беременности увеличивает риск кровотечений у новорожденных и матерей в послеродовом периоде, а хлорамфеникол противопоказан во время беременности и лактации, также его не рекомендуется применять у новорожденных, так как это может вызвать развитие «серого синдрома», проявляющийся сердечно-сосудистой недостаточностью, метеоризмом, тошнотой, снижением температуры тела, сизым оттенком кожи, прогрессирующей одышкой. Стрептомицин способен проникать через плацентарный барьер и оказывать нефротоксическое воздействие на эмбрион. У детей грудного возраста, матери которых принимали стрептомицин во время беременности, высокий риск возникновения глухоты. Применение других антибиотиков во время беременности, в частности, аминогликозидов (в том числе неомицина), может привести к повреждению восьмой пары черепно-мозговых нервов у плода
.Рацион беременной женщины и ребенка играет первостепенную роль в возникновении патологии твердых тканей зубов. Например, если в рационе превышена суточная норма углеводов, это способствует аккумулированию селена в минерализованных тканях
. Избыток селена в организме изменяет активность ферментов в пульпе зуба, приводя к гипоминерализации эмали и дентина и, впоследствии к кариесу зубов .По данным ученых, генетические нарушения могут стать причиной несовершенного амелогенеза, связанный с дефектом гена АМЕLX в участках хромосом энамелобластов
. Изменение первичной структуры амелогенинов влечет за собой нарушение роста кристаллов ГАП на органическом матриксе .При гипоксии плода возникают нарушения метаболизма, происходит недостаточное синтезирование АТФ, что оказывает влияние на фосфорилирование амелогенинов и других белков эмали, вследствие этого затрудняется связывание кальция с белковым матриксом эмали
. Несовершенный дентиногенез характеризуется нарушением развития дентина. Между тем, эмаль остается без изменений, и клинически патология не проявляется. На этапе инициации минерализации важная роль отводится ионам, находящимся в телах одонтобластов . Активный транспорт ионов Са²⁺, К⁺, Nа⁺ происходит при функционировании транспортных ионов Са²⁺, К⁺, Nа⁺-АТФаз, локализованных в комплексе Гольджи и кристах митохондрий по дистальному краю тел одонтобластов. Na⁺ накапливаются в цитозоле и в матриксных пузырьках одонтобластов, а ионы Са²⁺ в митохондриях и цитоплазме . Концентрация Са²⁺ во внеклеточной жидкости превышает их концентрацию в клетках, по этой причине, Са²⁺-АТФаза транспортирует Са²⁺ путем первично-активного транспорта против градиента концентрации, в то же время происходит пассивный перенос Nа⁺ и К⁺ в клетки пульпы и из неё. Транспортные Nа⁺, К⁺-АТФазы препятствуют повышению осмотического давления в клетках пульпы зубов. Поступление ионов происходит во время развития дентина и продолжается после прорезывания зуба, поддерживая минеральный состав зрелого дентина.В современной стоматологии наиболее часто используют классификацию несовершенного дентиногенеза по Shields, который выделял 3 типа данной патологии. По данным автора, первый тип характеризуется нормальной структурой эмали, но наблюдается гипоминерализация дентина. Преколлагеновые волокна не превращаются в коллагеновые, вследствие чего зубы окрашиваются в серый цвет. Второй тип, названный синдромом Стентона-Капдепона, проявляется нарушением структуры эмали, уменьшением ее толщины, неоднородностью структуры дентина, прогрессирующей кальцификацией пульповой камеры и дегенеративными изменениями в цементе. При данной патологии наблюдается снижение количества дентинных трубочек и минеральных веществ, что приводит к коричневому окрашиванию зубов. Третий тип несовершенного дентиногенеза характеризуется неоднородной структурой околопульпарного дентина, расширением пульповой камеры, и изменением цвета зубов от желто-коричневого до серо-голубого
, .3. Заключение
Литературные данные свидетельствуют об увеличении частоты встречаемости некариозных поражений твердых тканей зубов, возникающих в период одонтогенеза, ввиду этого, для эффективной профилактики возникновения некариозных поражений твердых тканей зубов, необходимо более детально изучить их биохимические аспекты. Механизм действия тетрациклинов до сих пор остается недостаточно изученным. Известно, что нарушение или выпадение любого звена, задействованного в синтезе белка, зачастую приводит к развитию заболевания, причем клинические проявления болезни будут определяться природой и функцией белка, синтез которого нарушается. Вследствие этого, перед врачами особенно остро возникает проблема выбора безопасной фармакотерапии во время лечения беременных и кормящих женщин. Все это указывает на необходимость осторожного применения препаратов, влияющих на матричный биосинтез. Новейшие достижения в медицине позволяют заменить тетрациклин безопасными для матери и ребенка антибиотиками из группы макролидов. Врачу следует подробно объяснить пациенту о возможных побочных эффектах лекарственных препаратов, влияющих на разные стадии зубного развития, и назначить соответствующую фармакотерапию.
