THE EFFECT OF INSOLATION ON THE BIOACCESSIBILITY OF DISSOLVED ORGANIC MATTER AND RELATED METALS IN THE WATER OF THE SENGA RIVER
ВЛИЯНИЕ ИНСОЛЯЦИИ НА БИОДОСТУПНОСТЬ РАСТВОРЕННОГО ОРГАНИЧЕСКОГО ВЕЩЕСТВА И СВЯЗАННЫХ С НИМ МЕТАЛЛОВ В ВОДЕ РЕКИ СЕНЬГА
Научная статья
ORCID: 0000-0003-3460-0197,
Московский государственный университет им. М.В. Ломоносова, Москва, Россия
* Корреспондирующий автор (lis.aleshina[at]yandex.ru)
АннотацияРастворенное органическое вещество (РОВ) играет важную роль в химическом составе природных вод бореальных экосистем. Основными факторами трансформации РОВ являются солнечный свет и микробный комплекс.
Проведение натурного эксперимента с водой реки Сеньга позволило выявить влияние инсоляции на биодеградацию исходного растворенного органического вещества и связанных с ним металлов. Было показано, что биодеградации подвергаются в основном низкомолекулярные соединения. При инсоляции примерно треть РОВ перешло в более высокомолекулярную форму (>0,22 мкм) или было минерализовано до СО2 и НСО3-. В результате фото- и биодеградации образуются крупные (>0,22 мкм) органо-минеральные соединения, представленные гидроксидами железа, стабилизированными гуминовыми веществами, с которыми также могут соосаждаться Al, V, Mn, Co, Cu, Zn, Cd, Pb. В то же время, увеличились содержания низкомолекулярных (<1 кДа) и, следовательно, более биодоступных соединений Co и Ni.
Ключевые слова: растворенное органическое вещество, поверхностные воды, инсоляция, фотодеградация, биодеградация, металлы.
THE EFFECT OF INSOLATION ON THE BIOACCESSIBILITY OF DISSOLVED ORGANIC MATTER AND RELATED METALS IN THE WATER OF THE SENGA RIVER
Research article
Aleshina A.R.*
ORCID: 0000-0003-3460-0197,
Moscow State University, Moscow, Russia
* Corresponding author (lis.aleshina[at]yandex.ru)
AbstractDissolved organic matter (DOM) plays an important role in the chemical composition of natural waters of boreal ecosystems. The main factors of DOM transformation are sunlight and the microbial complex.
Conducting a full-scale experiment with the water of the Senga River allowed for identifying the effect of insolation on the biodegradation of the initial dissolved organic matter and related metals. The study demonstrates that mainly low-molecular compounds undergo biodegradation. During insolation, about a third of the DOM passed into a higher molecular weight form (>0.22 microns) or was mineralized to CO>2 and HCO3-. As a result of photo-and biodegradation, large (>0.22 microns) organo-mineral compounds are formed as iron hydroxides, stabilized humic substances, with which Al, V, Mn, Co, Cu, Zn, Cd, Pb can also be co-deposited. At the same time, the content of low-molecular (<1 kDa) and therefore more bioaccessible compounds Co and Ni are observed to be on the increase.
Keywords: dissolved organic matter, surface water, insolation, photodegradation, biodegradation, metals.
ВведениеРастворенное органическое вещество (РОВ, размер соединений <0,22 мкм) играет важную роль в водных экосистемах. Исследования взаимодействий органического вещества с ионами металлов актуальны для прогнозирования процессов перераспределения гуминовых соединений и тяжелых металлов в окружающей среде, формирования качества природных вод, токсичности и биодоступности металлов [1]. Основными факторами трансформации РОВ являются фото- и биодеградация [2].
Фотохимическая трансформация растворенных веществ в поверхностных водах может происходить путем прямого фотолиза (когда поглощение солнечного излучения молекулой вызывает ее изменение) или косвенного (когда образуются химически активные переходные формы) [3]. Фотодеградация может трансформировать молекулярные структуры РОВ в более биодоступные формы [4], что может приводить к увеличению их биодеградации в природных системах.
Фотолиз также оказывает влияние на металлы в поверхностных водах, которые часто связаны в органические и органо-минеральные коллоиды [5]. Однако поведение многих микроэлементов при фото- и биодеградации РОВ остается слабоизученным за исключением нескольких работ [6], [7].
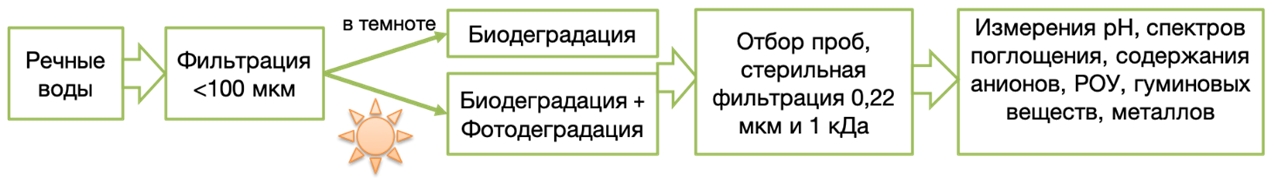
Методы исследованияЭксперимент с пробами природных вод реки проводился в следующих вариантах (рис. 1):
- биодеградация и фотодеградация: пробы вод, пропущенные через сетку с размером ячеек 100 мкм (для отделения крупного материала), с нативным микробным комплексом облучались солнечным светом;
- биодеградация: пробы вод, пропущенные через сетку с размером ячеек 100 мкм, с нативным микробным комплексом находились в темноте.
Контрольный вариант эксперимента поставлен со «стерильными» (пропущенными через фильтры с размером пор 0,22 мкм, FiTreM®, INNIT) образцами природных вод без доступа света. Фильтрация через 0,22 мкм позволяет удалить более 99,5% бактерий [8].
Рис. 1 – Схема экспериментов
Для исследования были выбраны богатые гумусовыми веществами воды реки Сеньга (Sводосбора = 163 км2, средний расход ок. 0,6 м3/с), расположенной во Владимирской области (центральная Россия, бореальная зона). Эксперимент проводился в июле на протяжении 10 суток. Образцы исследуемых вод помещались в кварцевые герметично закрытые стаканы и помещались либо под солнечное излучение, либо хранились в темноте. В ходе экспериментов в определенные промежутки времени отбирались пробы, которые позволили отследить динамику протекающих в растворах процессов. Для дальнейших анализов все образцы пропускались через стерильные фильтры с размером пор 0,22 мкм и 1 кДа.
Значения рН растворов измерены рН-метром Hanna HI 9025. Концентрации РОУ определены на жидкостном элементном анализаторе (LiquiTOC trace, Elementar). Концентрации металлов в пробах измерены методом ИСП-МС (Element-2, Thermo Finnigan). Содержания неорганических анионов определены методом ионной хроматографии (Dionex ICS-2000). Щелочность измерена по методу титрования [9]. Концентрацию гуминовых веществ (ГВ) в образцах определяли по реакции их связывания с толуидиновым синим [10]. Количество выделяющегося СО2 измеряли абсорбционным методом с 0,05 М КОН в качестве поглотителя.
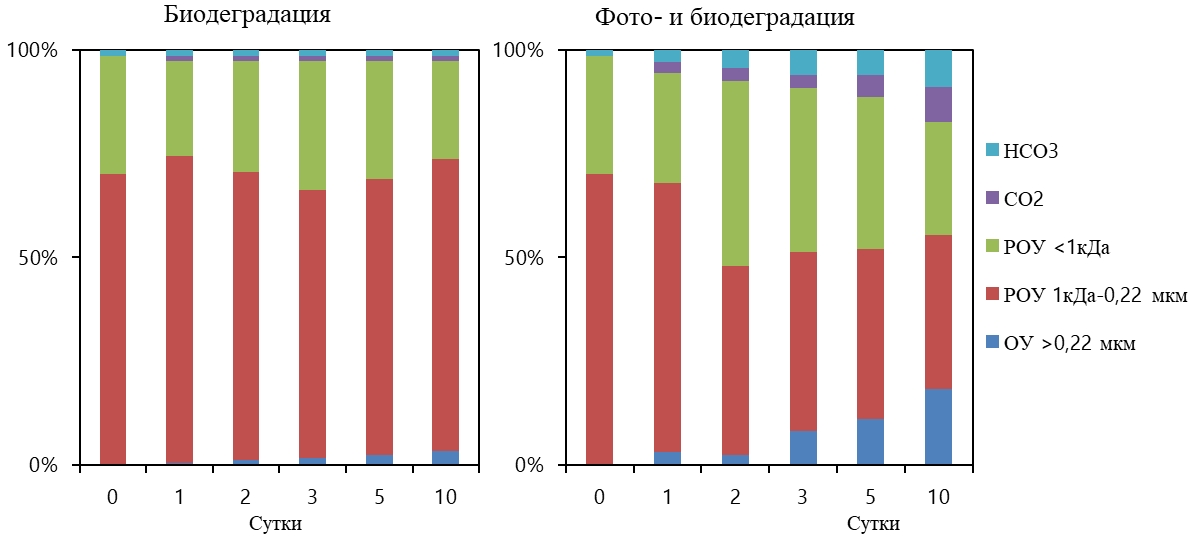
Основные результатыВ ходе эксперимента наблюдалось снижение концентрации растворенного органического углерода (РОУ) как в результате биодеградации в темноте, так и при инсоляции. Часть РОУ перешло в неорганическую форму (гидрокарбонаты и углекислый газ). Снижение содержания органического углерода в фильтратах 0,22 мкм обусловлено также процессом образования более высокомолекулярных органических соединений, которые удаляются из раствора при перефильтрации проб (рис. 2).
Рис. 2 – Изменение форм углерода в ходе экспериментов
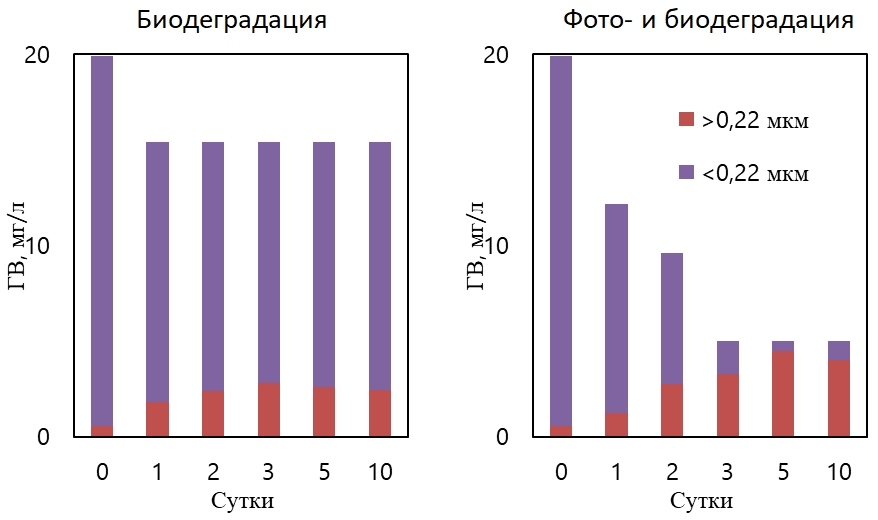
Содержание гуминовых веществ во фракции <0,22 мкм снизилось на 33% в результате биодеградации и на 95% в результате совместного влияния фото- и биодеструкции (рис. 3).
Рис. 3 – Изменение форм нахождения гумусовых веществ (ГВ) в ходе экспериментов
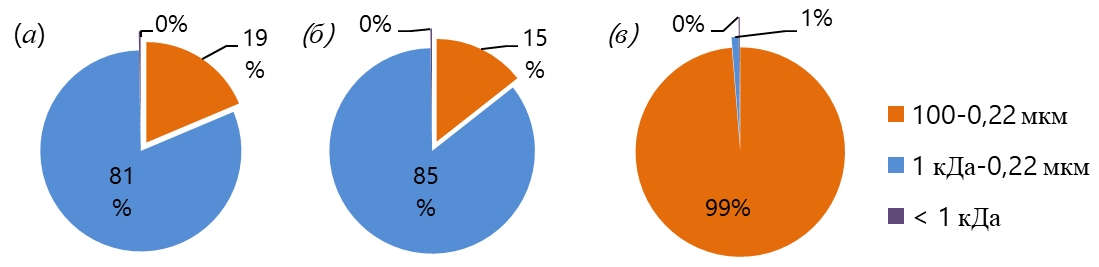
В речных водах исходно большая часть железа находится во фракции 1 кДа – 0,22 мкм, лишь пятая часть всех соединений железа превышает в размере 0,22 мкм (рис. 4). Биодеградация практически не изменила формы нахождения железа. В результате фото- и биодеградации почти все железо перешло в форму >0,22 мкм.
Рис. 4 – Распределение железа по фракциям в исследуемых водах до проведения эксперимента (а), после биодеградации (б), после фото- и биодеградации (в)
Расчет форм нахождения растворенных металлов проводился в программе Visual MINTEQ версии 3.1 для Windows [11] совместно с базой данных и Стокгольмской гуминовой моделью (SHM). Входными параметрами модели были pH, концентрации РОУ, анионов, катионов и микроэлементов.
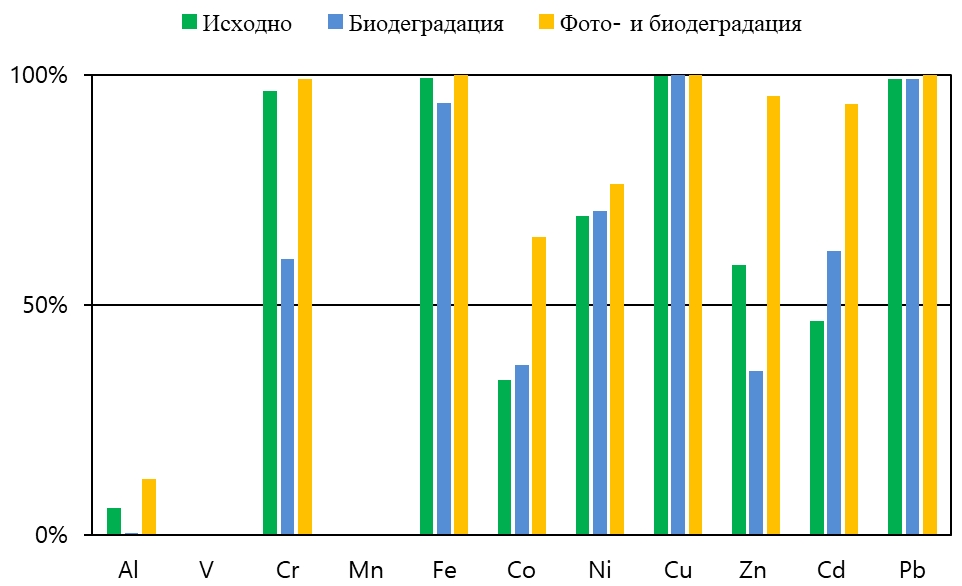
Полученные результаты показали, что в исследуемых водах реки в наибольшей степени с органическим веществом связаны такие металлы как Cr, Fe, Ni, Cu, Cd, Zn, Pb (рис. 5). В результате биодеградации на 25% уменьшилась доля Zn и на 15% увеличилась доля Cd, связанных с ОВ. В результате фото- и биодеградации доля металлов, связанных с ОВ, либо увеличилась, либо осталась примерно на том же уровне.
Рис. 5 – Доля металлов, связанных с органическим веществом, в исследуемых водах до (исходно) и после эксперимента во фракции <0,22 мкм по данным моделирования в программе vMinteq
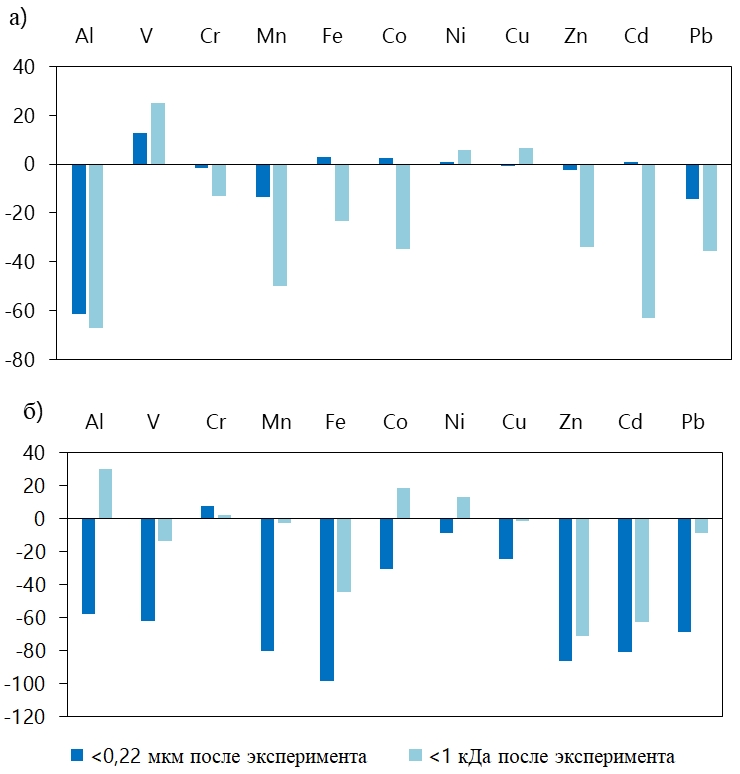
В ходе эксперимента были определены содержания таких металлов, как Al, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Cd, Pb во фракциях <0,22 мкм и <1 кДа (рис. 6). При биодеградации основные изменения произошли в низкомолекулярной фракции <1 кДа: в среднем на 40% уменьшились концентрации Al, Cr, Mn, Fe, Co, Zn, Cd, Pb и на 25%, 6% и 7% увеличились концентрации V, Ni, Cu соответственно, вероятно вследствие высвобождения их из высокомолекулярных органо-минеральных комплексов в результате деструкции. Значительно уменьшились содержания Al, Mn, Pb также во фракции <0,22 мкм.
Рис. 6 – Изменение концентраций металлов в пробах после эксперимента (а) по биодеградации и (б) фото- и биодеградации; исходное содержание металлов принято за 0, на графике показано изменение концентраций в % относительно исходных концентраций
В результате фото- и биодеградации содержания Al, Co, Ni увеличились во фракции <1 кДа на 30%, 19% и 14% соответственно. В среднем на 65% уменьшились содержания Al, V, Mn, Fe, Co, Cu, Zn, Cd, Pb во фракции <0,22 мкм.
До облучения высокая концентрация гуминовых веществ обеспечивала стабильность комплексов Fe(III) с органическими лигандами (до 99% железа связано с ОВ, рис. 5). В результате переноса заряда от лиганда к металлу происходит восстановление Fe(III) и одновременное окисление РОВ в первые дни эксперимента [12]. В насыщенных кислородом водах при нейтральном рН Fe(II) окисляется и подвергается гидролизу с последующей полимеризацией [13]. Полимеризация Fe(III) приводит к образованию малорастворимых частиц гидроксида (>0,22 мкм), которые приводят к снижению общей концентрации Fe во фракции менее 0,22 мкм на протяжении всего эксперимента. Учитывая, что при рН 4,5-6,5 поверхность осажденных гидроксидов железа положительно заряжена [14], наиболее вероятным механизмом удаления металлов в условиях эксперимента было бы связывание их отрицательно заряженных высокомолекулярных органических комплексов с гидроксидами Fe.
Заключение
Проведенные эксперименты показали, что инсоляция увеличивает степень деструкции и минерализации РОУ на 15% и одновременно способствует образованию более высокомолекулярных соединений. В результате фото- и биодеградации наблюдалось изменение форм нахождения металлов во всей растворенной фракции <0,22 мкм как следствие образования гидроксидов железа, стабилизированных органическими лигандами, совместно с которыми осаждаются и некоторые другие металлы. Процесс биодеградации оказался направлен, в основном, на низкомолекулярные формы соединений РОВ и металлов.
Таким образом, инсоляция может привести к снижению концентрации металлов (Al, V, Mn, Fe, Co, Cu, Zn, Cd, Pb) в водных системах ниже по течению и их прогрессивному накоплению в донных отложениях. В то же время, увеличение низкомолекулярных соединений Co и Ni может сделать последние потенциально более доступными для биодеградации.
| Финансирование Данное исследование выполнено при поддержке гранта РФФИ № 20-35-90017. | Funding This work was supported by the RFBR (grant № 20-35-90017). |
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Bowen J.C. Photodegradation disproportionately impacts biodegradation of semi-labile DOM in streams / J.C. Bowen, L.A. Kaplan, R.M. Cory // Limnol. Oceanogr. 9999, 2019. 1-14.
- Riedel T. Molecular signatures of biogeochemical transformations in dissolved organic matter from ten world rivers / T. Riedel, M. Zark, A. V. Vähätalo et al. // Front. Earth Sci., 2016. 4, 85.
- Vione D. Indirect photochemistry in sunlit surface waters: photoinduced production of reactive transient species / Vione, M. Minella, V. Maurino et al. // Chem. Eur J., 2014. 20, 10590-10606.
- Cory R.M. Interactions between sunlight and microorganisms influence dissolved organic matter degradation along the aquatic continuum / R.M. Cory, G.W. Kling // Limnol. Oceanogr., 2018. 3 (3), 102-116.
- Chupakova A.A. Photodegradation of river dissolved organic matter and trace metals in the largest European Arctic estuary / A.A. Chupakova, A.V. Chupakov, N.V. Neverova et al // Sci. Total Environ., 2018. 622-623, 1343-1352.
- Oleinikova O.V. Dissolved organic matter degradation by sunlight coagulates organo-mineral colloids and produces low-molecular weight fraction of metals in boreal humic waters / O.V. Oleinikova, O.Yu. Drozdova, S.A. Lapitskiy et al. // Geochem. Cosmochim. Acta, 2017. 211, 97-114.
- Дроздова О. Ю. Экспериментальное исследование процесса фотодеструкции органических соединений природных вод / О. Ю. Дроздова, Н. А. Анохина, В. В. Демин и др. // Вестник Московского университета. Серия 4: Геология., 2018. 4, 75–79.
- Kitidis, V. CDOM Dynamics and Photoammonification in the Marine Environment / V. Kitidis. Ph.D. Thesis, University of Newcastle., 2002. 182.
- Аринушкина Е.В. Руководство по химическому анализу почв / Е.В. Аринушкина. М.: МГУ, 1970. 488 с.
- Sheng, G.-P. A rapid quantitative method for humic substances determination in natural waters / G.-P. Sheng, M.-L. Zhang, H.-Q. Yu, // Anal. Chim. Acta, 2007. 592 (2), 162-167.
- Gustafsson, J.P. Visual MINTEQ / J.P. Gustafsson, Ver, 3.1., 2013. [Electronic resource]. URL: http://vminteq.lwr.kth.se. (accessed 8.03.2019).
- Drozdova O. Y. Coagulation of organo-mineral colloids and formation of low molecular weight organic and metal complexes in boreal humic river water under UV-irradiation / O. Y. Drozdova, A. R. Aleshina, V. V. Tikhonov et al. // Chemosphere, 2020. 250, 1–10.
- Zhu M. Precipitation pathways for ferrihydrite formation in acidic solutions / M. Zhu, C. Frandsen, A.F. Wallace et al. // Geochem. Cosmochim. Acta, 2016. 172, 247-264.
- Stumm, W. Chemistry of the Solid-Water Interface / W. Stumm // JohnWiley & Sons, New York, 1992. P. 448.
Список литературы на английском языке / References in English
- Bowen J.C. Photodegradation disproportionately impacts biodegradation of semi-labile DOM in streams / J.C. Bowen, L.A. Kaplan, R.M. Cory // Limnol. Oceanogr. 9999, 2019. 1-14.
- Riedel T. Molecular signatures of biogeochemical transformations in dissolved organic matter from ten world rivers / T. Riedel, M. Zark, A. V. Vähätalo et al. // Front. Earth Sci., 2016. 4, 85.
- Vione D. Indirect photochemistry in sunlit surface waters: photoinduced production of reactive transient species / Vione, M. Minella, V. Maurino et al. // Chem. Eur J., 2014. 20, 10590-10606.
- Cory R.M. Interactions between sunlight and microorganisms influence dissolved organic matter degradation along the aquatic continuum / R.M. Cory, G.W. Kling // Limnol. Oceanogr., 2018. 3 (3), 102-116.
- Chupakova A.A. Photodegradation of river dissolved organic matter and trace metals in the largest European Arctic estuary / A.A. Chupakova, A.V. Chupakov, N.V. Neverova et al // Sci. Total Environ., 2018. 622-623, 1343-1352.
- Oleinikova O.V. Dissolved organic matter degradation by sunlight coagulates organo-mineral colloids and produces low-molecular weight fraction of metals in boreal humic waters / O.V. Oleinikova, O.Yu. Drozdova, S.A. Lapitskiy et al. // Geochem. Cosmochim. Acta, 2017. 211, 97-114.
- Drozdova O. Yu. Jeksperimental'noe issledovanie processa fotodestrukcii organicheskih soedinenij prirodnyh vod [Experimental study of the process of photodestruction of organic compounds of natural waters] / O. Yu. Drozdova, N. A. Anokhina, V. V. Demin, etc. // Vestnik Moskovskogo universiteta [Bulletin of the Moscow University]. Series 4: Geology., 2018. 4, 75-79. [in Russian]
- Kitidis, V. CDOM Dynamics and Photoammonification in the Marine Environment / V. Kitidis. Ph.D. Thesis, University of Newcastle., 2002. 182.
- Arinushkina E. V. Rukovodstvo po himicheskomu analizu pochv [Manual on chemical analysis of soils] / E. V. Arinushkina. Moscow: MSU, 1970. 488 p. [in Russian]
- Sheng, G.-P. A rapid quantitative method for humic substances determination in natural waters / G.-P. Sheng, M.-L. Zhang, H.-Q. Yu, // Anal. Chim. Acta, 2007. 592 (2), 162-167.
- Gustafsson, J.P. Visual MINTEQ / J.P. Gustafsson, Ver, 3.1., 2013. [Electronic resource]. URL: http://vminteq.lwr.kth.se. (accessed 8.03.2019).
- Drozdova O. Y. Coagulation of organo-mineral colloids and formation of low molecular weight organic and metal complexes in boreal humic river water under UV-irradiation / O. Y. Drozdova, A. R. Aleshina, V. V. Tikhonov et al. // Chemosphere, 2020. 250, 1–10.
- Zhu M. Precipitation pathways for ferrihydrite formation in acidic solutions / M. Zhu, C. Frandsen, A.F. Wallace et al. // Geochem. Cosmochim. Acta, 2016. 172, 247-264.
- Stumm, W. Chemistry of the Solid-Water Interface / W. Stumm // JohnWiley & Sons, New York, 1992. P. 448.