IMPROVING SANITARY AND ENVIRONMENTAL SAFETY OF WASTEWATER
Дрововозова Т.И.1, Паненко Н.Н.2, Кулакова Е.С.3
1ORCID: 0000-0002-8724-7799, Доцент, Доктор технических наук, 2ORCID: 0000-0003-4426-7762, Ассистент, 3ORCID: 0000-0001-6778-1401, Кандидат технических наук, Новочеркасский инженерно-мелиоративный институт имени А.К. Кортунова Донского государственного аграрного университета.
ПОВЫШЕНИЕ САНИТАРНО-ЭКОЛОГИЧЕСКОЙ БЕЗОПАСНОСТИ СТОЧНЫХ ВОД
Аннотация
Определена проблема очистных сооружений канализации, обусловленная сбросом либо недоочищенных, либо полностью неочищенных сточных вод в водоём. С целью повышения экологической безопасности очистных сооружений канализации предложено путём усовершенствования схемы очистки сточных вод, заменить на стадии обеззараживания молекулярный хлор на комбинированное обезвреживание пероксидом водорода с последующей доочисткой на модифицированной фильтрующей загрузке и обеззараживание низкоконцентрированным гипохлоритом натрия.
Ключевые слова: доочистка, фильтрование, сточная вода, пероксид водорода, гипохлорит натрия.
Drovovozova T.I.1, Panenko N.N.2, Kulakova E.S.3
1ORCID: 0000-0002-8724-7799, Associate professor, PhD in Engineering, 2ORCID: 0000-0003-4426-7762, Assistant, 3ORCID: 0000-0001-6778-1401, PhD in Engineering, Novocherkassk Engineering and Land Reclamation Institute of Don State Agrarian University.
IMPROVING SANITARY AND ENVIRONMENTAL SAFETY OF WASTEWATER
Abstract
The problem of wastewater treatment facilities caused by the discharge of either under-treated or completely untreated wastewater into the reservoir is determined. In order to improve the environmental safety of wastewater treatment facilities, it was proposed to improve wastewater treatment scheme, to replace the molecular chlorine for the decontamination with hydrogen peroxide at the disinfection stage, followed by post-treatment with a modified filtering load and disinfection with low-concentration sodium hypochlorite.
Keywords: post-treatment, filtration, wastewater, hydrogen peroxide, sodium hypochlorite.
В последние десятилетия природные водные объекты, прилегающие к городам и сельским поселениям, испытывают интенсивную антропогенную нагрузку, обусловленную сбросом либо недоочищенных, либо полностью неочищенных сточных вод. Это, в свою очередь, приводит к тому, что водные объекты становятся не пригодными для использования их в качестве источников питьевого водоснабжения. Создавшаяся ситуация свидетельствует о недостаточно эффективной работе очистных сооружений канализации и, как следствие, о необходимости их реконструкции. Кроме того, большинство очистных сооружений канализации в России по-прежнему использует в качестве обеззараживающего реагента газообразный хлор, являющийся одним из наиболее опасных веществ с точки зрения возникновения чрезвычайной ситуации.
В связи с вышеизложенным, целью работы является повышение экологической безопасности очистных сооружений канализации путем усовершенствования схемы очистки сточных вод, замены на стадии обеззараживания молекулярного хлора на комбинированное обезвреживание пероксидом водорода с последующей доочисткой на модифицированной фильтрующей загрузке и обеззараживание низкоконцентрированным гипохлоритом натрия.
В качестве объекта исследования были выбраны типовые очистные сооружения канализации (КОС), включающие механическую, биологическую очистку и обеззараживание жидким хлором.
Физико-химический состав очищенных сточных вод (ОСВ) КОС показал, что вода не соответствует требованиям при выпуске в природный водоём по содержанию взвешенных веществ, нитритов, нитратов, фосфору, по показателю ХПК. При сбросе ОСВ в рыбохозяйственный водоём установлены следующие нормы, мг/дм3: ВВ – 3,0; ХПК – 15,0; БПК5 – 2,0; NH4+ - 0,4; NO3¯ - 9,0; NO2¯ - 0,02; фосфаты (по фосфору) – 0,05 [1, с. 11].
Данные лабораторных исследований показали, что содержание азота нитратов в очищенных сточных водах превышает нормативный в 6 раз, азота нитритов в 5 раз, фосфата (по фосфору) в 52 раза, взвешенных веществ – в 3 раза, по показателю ХПК – в 2 раза (табл. 1).
Таблица 1 – Результаты химических анализов сточных вод, поступающих и очищенных на очистных сооружениях (на примере реального объекта)
| Определяемые компоненты, мг/дм3 | Место отбора | ||
| Приемная камера промышленных стоков | Приемная камера бытовых стоков | Биологические пруды | |
| Взвешенные вещества (ВВ) | 124 | 176,4 | 9,6 |
| Сухой остаток | 1188 | 896 | 1004 |
| Хлориды | 138 | 179 | 167 |
| SO42- | 422 | 269 | 317 |
| NH4+ (N2) | 2,5 | 24,5 | 0,28 |
| NO2¯ | 0,08 | 0,2 | 0,096 |
| NO3¯ | 1,42 | 1,24 | 55,8 |
| PO43- (P) | 0,4 | 2,6 | 2,6 |
| O2 | - | - | 4,0 |
| ХПК | 172 | 192 | 28 |
| БПК5 | 86,3 | 97,5 | 3,15 |
| АПАВ | 0,84 | 0,53 | 0,051 |
Высокое значение ХПК свидетельствует о наличии в сточной воде большого количества трудноокисляемых органических соединений, поэтому дальнейшее хлорирование такой воды неизбежно приведёт к образованию в ней хлорорганических производных, которые в последующем беспрепятственно поступают в природный водоём. Выше указанные обстоятельства указывают на необходимость использование экологически безопасного сильного окислителя, каким, на наш взгляд, является пероксид водорода (Н2О2), и последующего фильтрования с целью удаления взвешенных веществ и нежелательных компонентов.
Учитывая химический состав сточных вод и удельные дозы пероксида водорода, определена максимальная концентрация Н2О2, необходимая для обезвреживания сточных вод КОС, которая составляет 10 мг/дм3.
Сточная вода, отобранная во вторичном отстойнике КОС и обработанная раствором пероксида водорода в концентрации 10 мг Н2О2/дм3, профильтрована через модельный фильтр, высотой 400 мм, диаметром 50 мм, содержащий модифицированную фильтрующую загрузку.
Модифицированная загрузка, состоит из следующих материалов (послойно): антрацита, перлита с размерами зерен 2-3 мм, анионита. Перлит – это природный материал, который состоит из вулканического стекла, в составе которого 70-75% SiO2; 12-14% AI2O3; 3-5% Na2O; примерно столько же К2О; до 1% Fe2O3, CaO, МgО. Одной из особенностей перлита, как природного материала, является достаточно высокая абсорбционная способность. Природный материал – антрацит – обладает высокой адсорбционной способностью в отношении органических соединений, а также механических примесей в очищаемой воде. Сильнокислотный анионит рекомендуется использовать для удаления из воды ионов биогенов.
В отфильтрованной воде были определены следующие показатели: взвешенные вещества, азот нитратов, азот нитритов, фосфаты (по фосфору), ХПК. Все анализы выполнялись в аккредитованной лаборатории очистных сооружений канализации по гостированным методикам [2-6]. В табл. 2 представлены результаты физико-химических исследований сточной воды до выше указанной доочистки и после неё.
Таблица 2 – Концентрации загрязняющих веществ в сточной воде до и после рекомендуемой доочистки.
| Определяемый компонент | Содержание до доочистки, мг/дм3 | Содержание после доочистки, мг/дм3 | ПДК, мг/дм3 | Нормативно-допустимые сбросы, мг/дм3 |
| Взвешенные вещества | 9,6 | отсутствуют | 3,0 | 10,11 |
| Азот нитритов | 0,096 | отсутствует | 0,02 | 0,008 |
| Азот нитратов | 55,8 | 2,31 | 9,0 | 14,48 |
| Фосфаты (по фосфору) | 2,6 | отсутствует | 0,05 | 0,2 |
| ХПК | 28 | 15 | 15 | - |
Полученные результаты показали, что после прохождения воды через модифицированную загрузку, состоящую из антрацита, перлита и анионита послойно, степень очистки сточной воды значительно повышается: по содержанию взвешенных веществ на 100%, по азоту нитритов и фосфату – на 100%, по азоту нитратов – на 95,7 %.
Таким образом, для эффективной очистки сточных вод, характеризующихся содержанием взвешенных веществ и биогенов в концентрациях, превышающих ПДК, рекомендуется применять модифицированную загрузку из искусственного материала (анионита) и материалов естественного происхождения – антрацита и перлита, сочетание которых позволяет увеличить эффект очистки каждого из них, с одной стороны, а, с другой – уменьшить объёмы загрузок, что позволит снизить экономические затраты на очистку.
Поскольку пероксид водорода относится к веществам 2 класса опасности, содержание которого в природных водах выше предельно допустимой концентрации является недопустимым и опасным как для здоровья человека, так и для жизнедеятельности всех гидробионтов, с другой стороны, пероксид водорода является наиболее экологически безопасным реагентом, позволяющим удалять из сточной воды, окисляемые органические и неорганические соединения, возникает необходимость определения степени разложения пероксида водорода в сточной воде после фильтрования ее через фильтрующую загрузку.
Количество Н2О2 в доочищенной сточной воде определяли перманганатометрическим титрованием. В сточную воду вносили раствор пероксида водорода в концентрации 10 мг/дм3 в пересчёте на чистый Н2О2. Воду отфильтровывали через рекомендуемую фильтрующую загрузку определяли остаточную концентрацию пероксида в очищенной сточной воде. Результаты экспериментов представлены в табл. 3
Таблица 3 –Остаточные концентрации пероксида водорода в СВ
| Объект исследования | Остаточная концентрация пероксида водорода, мг/дм3 | ||
| сразу после фильтрации | через 1 час | через 10 часов | |
| Отфильтрованная сточная вода | 0,12 | 0,12 | отсутствует |
Результаты экспериментов показали, что после фильтрования сточных вод, содержащих 10 мгН2О2/дм3, через фильтрующую загрузку содержание пероксида снижается на 98,8%. Высокий эффект разложения объясняется, на наш взгляд, входящими в состав антрацита и перлита катализаторов разложения Н2О2 (антрацит содержит FeS2, перлит содержит в своем составе до 1% Fe2O3, МgО, 12-14% AI2O3). Тем не менее, сразу после фильтрования и через час, в сточной воде ПДК пероксида водорода для рыбохозяйственных водоемов не достигается. Однако, через 10 часов в очищенной сточной воде пероксид водорода не обнаруживается.
Проведенные исследования показали, что концентрация пероксида водорода 10 мг/дм3 в пересчёте на чистый Н2О2 при последующем фильтровании СВ через модифицированную загрузку, является безопасной и с экологической и с санитарно-гигиенической точек зрения.
Исходя из выше изложенного, рекомендуемый способ очистки сточных вод включает следующие этапы:
- Механическая очистка сточных вод, позволяющая задерживать нерастворимые и минеральные вещества.
- Биологическая очистка сточных вод, способствующая окислению и минерализации органических веществ.
- Введение пероксида водорода в концентрации 10 мг/дм3 в пересчёте на чистый Н2О2 и выдерживание 2 часа с целью достижения требуемого эффекта обезвреживания и обесцвечивания.
- На заключительном этапе доочистки сточные воды пропустить через комбинированную фильтрующую загрузку, позволяющую одновременно удалить из воды остаточные количества взвешенных веществ, биогенов и разложить остаточные концентрации пероксида, обеспечивая, тем самым и санитарно-гигиеническую и экологическую безопасность очищенных сточных вод.
- С целью обеспечения пролонгированного бактерицидного действия сточные воды обрабатывают гипохлоритом натрия в концентрации 1,5 мг/дм3 в пересчёте на активный хлор (рис.1).
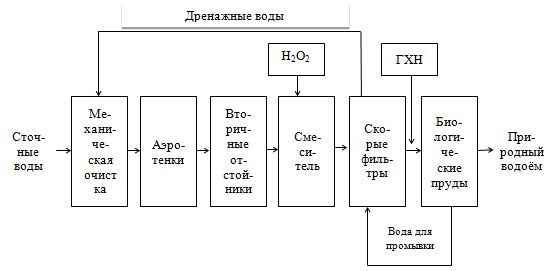
Рис. 1 – Усовершенствованная схема очистки сточных вод: Н2О2 – пероксид водорода; ГХН – гипохлорит натрия
Комбинированная доочистка сточной воды пероксидом водорода и фильтрование её через рекомендуемую модифицированную загрузку позволит решить ряд экологических проблем:
1) предотвратить сброс недостаточно очищенных сточных вод в природный водоём, и, тем самым, предотвратить экологический ущерб, наносимый окружающей среде;
2) снизить дозу гипохлорита натрия на финишном этапе обеззараживания до 1,5 мг/дм3, тем самым в обрабатываемой воде снижается концентрация остаточного активного хлора, снижаются риски образования хлорпроизводных, что делает сточные воды безопасными для водоёмов с экологической и санитарно-гигиенической точек зрения;
3) замена молекулярного хлора на стадии обеззараживания на низкоконцентрированный гипохлорит натрия позволит снизить техногенную опасность объекта.
Список литературы / References
- Гигиенические требования к охране поверхностных вод [Текст]: СанПиН 2.1.5.980-2000. – изд. офиц. - М., 2001. - 18 стр.
- Количественный химический анализ вод. Методика измерений массовых концентраций взвешенных веществ и прокаленных взвешенных веществ в пробах питьевых, природных и сточных вод гравиметрическим методом ПНДФ 14.1:2:4.254-2009 - М., 2012. - 12 с.
- РД 52.24.421-2012 "Химическое потребление кислорода в водах. Методика измерений титриметрическим методом" (утв. Федеральной службой по гидрометеорологии и мониторингу окружающей среды 26 декабря 2011 г. – 23 с.
- Количественный химический анализ вод. Методика измерений массовой концентрации нитрит-ионов в питьевых, поверхностных и сточных водах фотометрическим методом с реактивом Грисса ПНД Ф 14.1:2:43-95.- М., 2011. - 20 с.
- Количественный химический анализ вод. Методика измерений массовой концентрации нитрат-ионов в питьевых, поверхностных и сточных водах фотометрическим методом с салициловой кислотой ПНД Ф 14.1:2:4.4-95.- М., 2011. – 16 с.
- Количественный химический анализ вод. Методика измерений массовой концентрации фосфат-ионов в питьевых, поверхностных и сточных водах фотометрическим методом с молибдатом аммония ПНД Ф 14.1:2:4.112-97.- М., 2011. – 18 с.
Список литературы на английском языке / References in English
- Gigienicheskie trebovanija k ohrane poverhnostnyh vod: SanPiN 2.1.5.980-2000 [Hygienic requirements to surface water protection: Sanitary rules and norms 2.1.5.980-2000. – M., 2001. - 18 p. [in Russian]
- Kolichestvennyj himicheskij analiz vod. Metodika izmerenij massovyh koncentracij vzveshennyh veshhestv i prokalennyh vzveshennyh veshhestv v probah pit'evyh, prirodnyh i stochnyh vod gravimetricheskim metodom PNDF 14.1:2:4.254-2009 [Quantitative chemical analysis of waters. The technique of measurement of mass concentration of suspended substances and calcinated substances in samples of drinking, natural and waste water by gravimetric method – Environmental normative document of the Federal level 14.1:2:4.254-2009]. – M., 2012. – 12 p. [in Russian]
- RD 52.24.421-2012 "Himicheskoe potreblenie kisloroda v vodah. Metodika izmerenij titrimetricheskim metodom" (utv. Federal'noj sluzhboj po gidrometeorologii i monitoringu okruzhajushhej sredy 26 dekabrja 2011 g.) [Guidance document 52.24.421-2012 "Chemical demand of oxygen in waters. The technique of measurement of the titrimetric method" (app. The Federal service for Hydrometeorology and environmental monitoring, December 26, 2011)] – 23 p. [in Russian]
- Kolichestvennyj himicheskij analiz vod. Metodika izmerenij massovoj koncentracii nitrit-ionov v pit'evyh, poverhnostnyh i stochnyh vodah fotometricheskim metodom s reaktivom Grissa PND F 14.1:2:43-95 [Quantitative chemical analysis of waters. The technique of measurement of mass concentration of nitrite ions in drinking, surface and waste waters by photometric method with Griess reagent – environmental normative document of the Federal level 14.1:2:43-95]. – M., 2011. – 20 p. [in Russian]
- Kolichestvennyj himicheskij analiz vod. Metodika izmerenij massovoj koncentracii nitrat-ionov v pit'evyh, poverhnostnyh i stochnyh vodah fotometricheskim metodom s salicilovoj kislotoj PND F 14.1:2:4.4-95 [Quantitative chemical analysis of waters. The technique of measurement of mass concentration of nitrate ions in drinking, surface and waste waters by photometric method with salicylic acid – environmental normative document of the Federal level 14.1:2:4.4-95]. – M., 2011. – 16 p. [in Russian]
- Kolichestvennyj himicheskij analiz vod. Metodika izmerenij massovoj koncentracii fosfat-ionov v pit'evyh, poverhnostnyh i stochnyh vodah fotometricheskim metodom s molibdatom ammonija PND F 14.1:2:4.112-97 [Quantitative chemical analysis of waters. The technique of measurement of mass concentration of phosphate ions in drinking, surface and waste waters by photometric method with ammonium molybdate – environmental normative document of the Federal level 14.1:2:4.112-97]. – M., 2011. – 18 p. [in Russian]
