THE ROLE OF SALINITY AND ION COMPOSITION OF WATER IN THE FORMATION OF METHANE CONCENTRATIONS IN AQUATIC ECOSYSTEMS
РОЛЬ МИНЕРАЛИЗАЦИИ (СОЛЕНОСТИ) И ИОННОГО СОСТАВА ВОД В ФОРМИРОВАНИИ КОНЦЕНТРАЦИЙ МЕТАНА В ВОДНЫХ ЭКОСИСТЕМАХ
Научная статья
Гарькуша Д.Н.1, *, Фёдоров Ю.А.2
1 ORCID: 0000-0001-5026-2103;
1, 2 Южный федеральный университет, Ростов-на-Дону, Россия
* Корреспондирующий автор (gardim1[at]yandex.ru)
АннотацияРассмотрено влияние ионного состава и солености (минерализации) вод на формирование концентраций метана в водных объектах. Показано, что влияние этих факторов на концентрации метана не является определяющим. Основными факторами выступают интенсивность продукционно-деструкционных процессов, контролирующих содержание органического вещества и окислительно-восстановительные условия, а также гидрологические и морфометрические параметры водных объектов, обуславливающие распределение литологических типов донных отложений. Наличие в большом количестве солей, в том числе сульфатов в высокоминерализованных водоемах, при повышенных концентрациях лабильного органического вещества в их водной толще и грязевых отложениях не препятствует одновременному активному протеканию процессов метаногенеза и сульфатредукции, вследствие снижения конкуренции за питательные субстраты между сульфатредукторами и метаногенами.
Ключевые слова: парниковые газы, метан, водные экосистемы, катион-анионный состав, соленость, минерализация.
THE ROLE OF SALINITY AND ION COMPOSITION OF WATER IN THE FORMATION OF METHANE CONCENTRATIONS IN AQUATIC ECOSYSTEMS
Research article
Garkusha D.N.1, Fedorov Yu.A.2
1 ORCID: 0000-0001-5026-2103;
1, 2 Southern Federal University (SFedU), Rostov-on-Don, Russia
* Корреспондирующий автор (gardim1[at]yandex.ru)
AbstractThe present study examines the influence of ion composition and salinity of water on the formation of methane concentrations in water bodies. The research demonstrates that the influence of these factors on methane concentrations is not definitive. The main factors are the intensity of production and destruction processes that control the content of organic matter and redox conditions as well as the hydrological and morphometric parameters of water bodies that determine the distribution of lithological types of bottom deposits. The presence of a large number of salts, including sulfates in highly mineralized water bodies with increased concentrations of labile organic matter in their water column and mud deposits, does not prevent the simultaneous active flow of methanogenesis and sulfate reduction process due to reduced competition for nutrient substrates between sulfate-reducing microorganisms and methanogens.
Keywords: greenhouse gases, methane, aquatic ecosystems, cation-anion composition, salinity, mineralization.
Исследования показывают [13], [17], [18], что для таких водных объектов как озера, водохранилища, реки, эстуарии, моря и океаны характерны определенные величины содержания метана (СН4) в воде. В этом ряду в среднем наиболее высокие его концентрации фиксируются в реках, минимальные характерны для вод морей и океанов [18]. Наблюдаемое снижение концентраций СН4 при увеличении солености в зонах смешения «река – эстуарий → море» и «река – море (океан)» [18] требует обсуждения и установления, влияет ли непосредственно соленость (минерализация) и ионный состав вод на концентрации СН4 в воде и донных отложениях водных объектов. И, если влияет, то каким образом – прямо или опосредованно, то есть через влияние на другие факторы? Для этого рассмотрим имеющиеся сведения о поведении СН4 в реках и зонах смешения речных и морских вод, и связи концентраций этого газа с соленостью.
На настоящий момент известно [2], [18], что в естественных условиях основным фактором, контролирующим распределение СН4 в реках, является скорость течения, определяющая характер механической миграции органического вещества (вынос, транспортировка, аккумуляция), и, как следствие, тип донных отложений. Наибольшей способностью концентрировать органические вещества, взвеси и химические элементы обладают мелкоалевритовые и глинистые илы, отлагающиеся на участках со спокойным гидродинамическим режимом. Седиментация значительного количества взвешенных веществ на дно, а вместе с этим и повышенное накопление органического вещества на таких участках ведет к снижению содержания кислорода в воде, к ухудшению условий аэрации осадков и образованию в них восстановительной обстановки. Всё это оказывает благоприятное воздействие на активизацию роста и дальнейшее развитие анаэробных микроорганизмов, в том числе, и метаногенного сообщества.
В воде рек содержание СН4 обычно возрастает по направлению к устью. При этом данную тенденцию ослабляет или полностью нивелирует влияние крупных поставщиков органических веществ, каковыми являются города, промышленные объекты или (и) загрязнённые притоки, в зоне воздействия которых четко фиксируется резкое повышение содержания СН4 в воде и донных осадках. Как показано в работе [2], из-за быстрого окисления и миграции в атмосферу СН4, поступившего в водную толщу, распространение его на заметные расстояния от источников поступления (генерации) не происходит. Это свойство СН4 благоприятствует его использованию как индикатора антропогенного загрязнения и оконтуривания зон загрязнения органическими веществами [3], [18].
Максимальные концентрации СН4 в воде устьев рек обусловлены выносом рекой органических веществ и накоплением их в дельте, где обычно отлагаются донные отложения, сложенные более тонкозернистым материалом, по сравнению с вышерасположенными участками. Немаловажным фактором повышенных содержаний СН4 в устьях рек является и то, что, как правило, устьевые участки рек издавна наиболее плотно заселены, в связи с чем испытывают хроническое антропогенное воздействие.
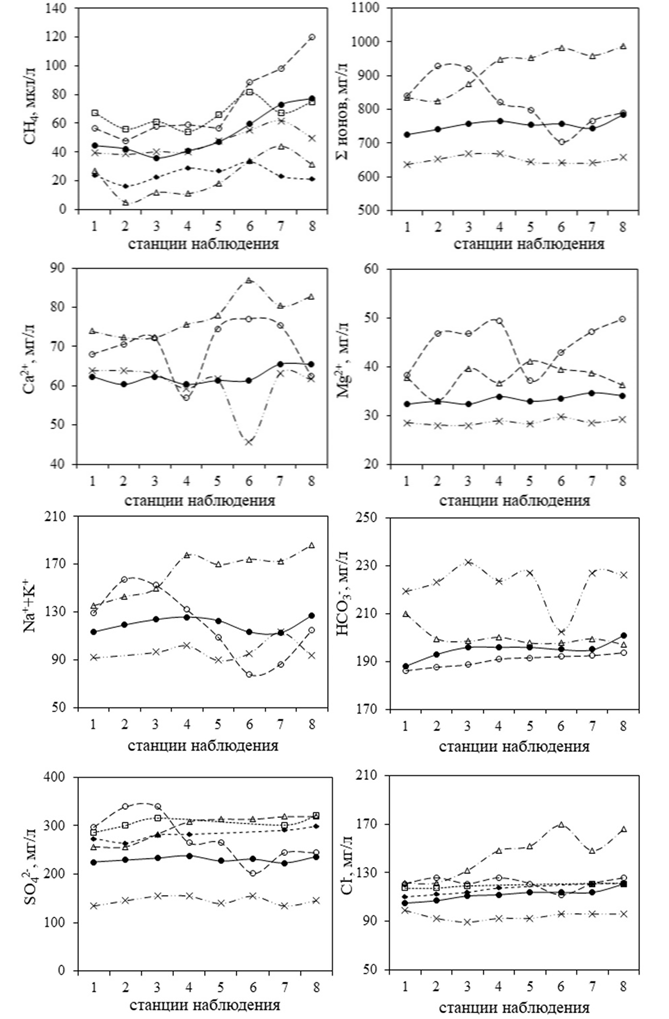
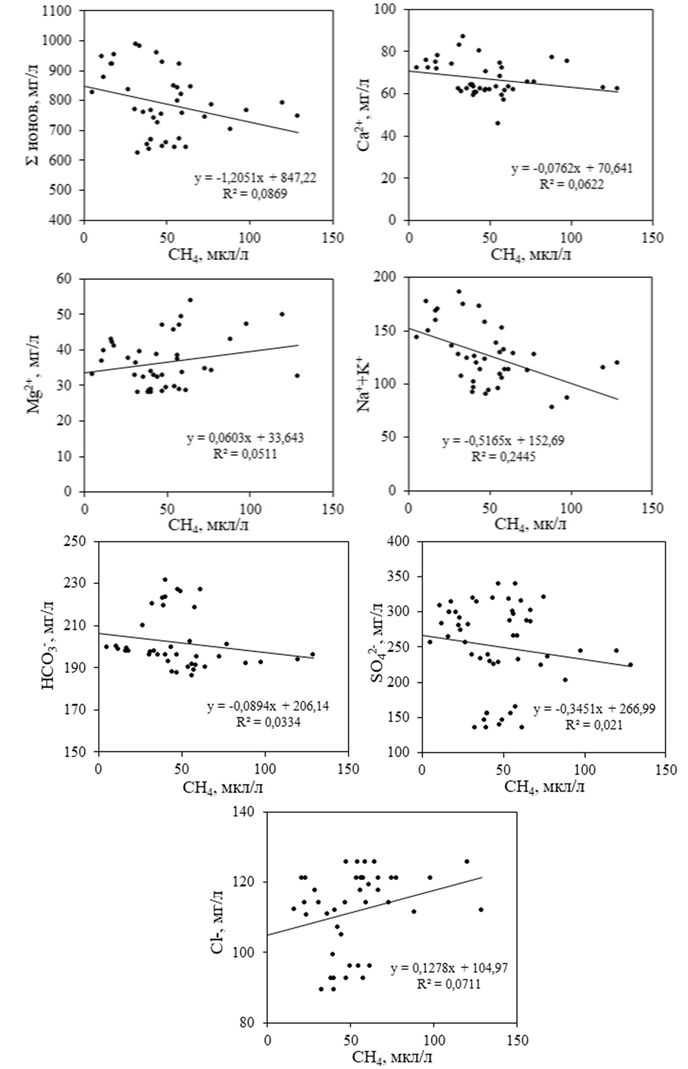
Синхронное изучение сезонных изменений (июль, август, сентябрь и октябрь 2002 г., май и июль 2003 г.) катион-анионного состава вод нижнего течения реки Дон, концентраций СН4 и взвешенного вещества на восьми станциях, относительно равномерно распределенных по продольному профилю р. Дон «выше г. Аксай – ниже г. Азов», помимо отчетливого увеличения концентраций СН4 в дельте Дона (рис. 1), показало наличие относительно слабых отрицательных связей концентраций ионов Са2+, Na++K+, HCО3-, SO42- и в целом суммы ионов с концентрациями СН4 (r – коэффициент корреляции – составляет -0.25, -0.49, -0.18, -0.15 и -0.29, соответственно), а также слабых положительных связей концентраций ионов Mg2+ и Cl- с концентрациями СН4 (r – +0.23 и +0.27, соответственно) (рис. 2). Наличие слабой положительной корреляции между СН4 и Mg2+, СН4 и Cl- может носить как случайный (вероятно, это больше относится к связи СН4 и Mg2+), так и опосредованный характер, через наложение непараллельных процессов, контролирующих концентрации данных ионов и метана. Например, на фоне увеличения концентраций СН4 по направлению к устью реки Дон, связанного с выше обозначенными факторами, концентрация хлора как элемента, обладающего высокой растворимостью и слабо выраженной способностью к сорбции и потреблению живыми организмами, под влиянием естественных (выщелачивание из горных пород и почв) и антропогенных факторов (поступление в реку в составе свалочных, коммунальных и промышленных сточных вод, в результате смыва удобрений и соли, применяемой для растворения льда на дорогах и др.), также в целом увеличивается (см. рис. 1), что и обуславливает наличие положительной связи между метаном и хлоридными ионами.
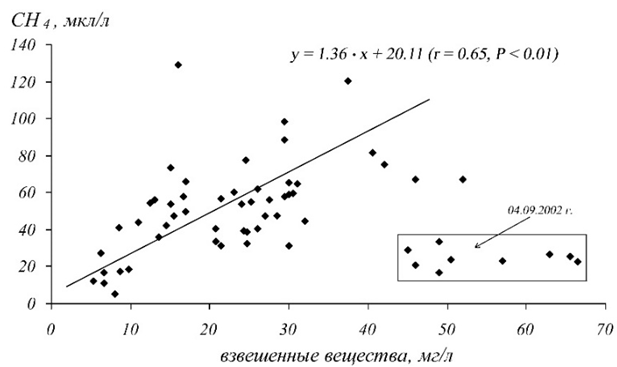
Более значимая положительная связь при проведении данных исследований (r = +0.65) отмечалась между концентрациями в воде метана и взвешенных веществ (рис. 3). Эта связь, вероятно, обусловлена тем, что внутри взвешенных веществ создаются анаэробные микрозоны [29] вокруг, так называемых «hot spots» или "горячих точек" [26], в которых идут процессы метаногенеза. По нашим данным [4], полученным при проведении мезокосменного эксперимента на эвтрофном рыбоводном пруду, вклад метаногенеза, протекающего во взвешенных в воде частицах, в том числе включая фекальные пеллеты зоопланктона, в формирование уровня содержания метана в воде составляет 25–30%. Остальная доля приходится на образование газа в донных отложениях, откуда он затем мигрирует в воду.
Рис. 1 – Сезонные изменения концентраций метана и основных ионов в нижнем течении реки Дон по продольному профилю «выше г. Аксай – ниже г. Азов»: станция 1 – р. Дон, выше г. Аксай; ст. 2 – р. Дон, водозабор г. Ростова-на-Дону; ст. 3 – р. Дон, 0.5 км ниже впадения р. Темерник; ст. 4 – р. Дон, 0.5 км ниже сброса ПУ "Водоканал"; 5 – р. Дон, 0.5 км ниже х. Колузаево; 6 – рук. Большая Каланча, х. Дугино; 7 – р. Дон, выше г. Азов, водозабор; 8 – р. Дон, ниже г. Азов, водосброс
Рис. 2 – Зависимости, построенные по результатам сезонных наблюдений за изменениями концентраций метана и основных ионов в нижнем течении реки Дон по продольному профилю «выше г. Аксай – ниже г. Азов»
Анализ расположения точек на графике (см. рис. 3) показывает, что ряд точек, значительно отклоняющихся от аппроксимирующей эту зависимость прямой, характеризует содержания взвеси и метана в воде в начале сентября 2002 года. Относительно резкое снижение в воде в данный период концентраций метана при максимальных содержаниях взвешенного вещества могло быть обусловлено как изменением качественного состава взвешенного вещества (например, вследствие цветения «токсичных» сине-зеленных водорослей или роста доли минеральной компоненты взвеси), так и изменением физико-химических условий (например, снижением температуры воды с 22.5–23.5°С до 20.8–21.0°С в период с 20.08.02 г. по 04.09.02 г.
Рис. 3 – Зависимость между концентрациями в воде взвешенных веществ и метана, построенная по результатам сезонных наблюдений в нижнем течении реки Дон по продольному профилю «выше г. Аксай – ниже г. Азов»
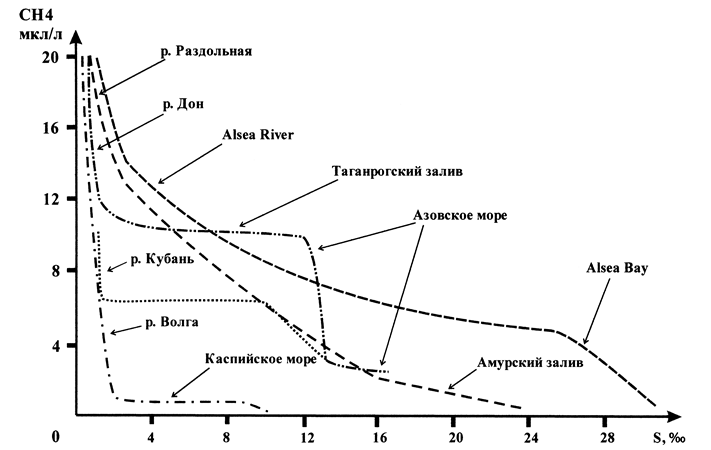
В зонах смешения «река – эстуарий → море» и «река – море (океан)» отмечается достаточно резкое падение концентрации СН4 [18]. Среди исследованных авторами зон смешения речных и морских вод можно выделить эстуарии рек Дон (Таганрогский залив Азовского моря), Кубань (Темрюкский залив Азовского моря), Раздольная (Амурский залив Японского моря), Северная Двина (Двинская губа Белого моря), район впадения реки Волга в Каспийское море [3], [5], [23]. Согласно результатам проведенных исследований, в Азовском море в зоне смешения пресных вод реки Дон с солоноватыми водами Таганрогского залива в интервале солёности 1–2‰ наблюдается так называемый «метановый барьер» [18], [20], характеризующийся достаточно резким снижением концентрации СН4 (с 78.0 до 12.0 мкл/л, в среднем в 2.5 раза), после чего по направлению к устью залива его концентрации уменьшаются более плавно (в 1.1–1.3 раза) (рис. 4). На выходе из устья Таганрогского залива в открытую акваторию Азовского моря, обычно при солености около 12‰, отмечается второй «метановый барьер», на котором концентрации СН4 в водной толще снова резко снижаются (с 12.0 до 3.0–4.0 мкл/л, в среднем в 2.8 раза).
Рис. 4 – Изменение содержания метана в воде зон смешения “река – эстуарий – море” при увеличении солености Примечание: составлено по [18]
В Темрюкском заливе, который является зоной смешения вод р. Кубань с водами Азовского моря, первое резкое снижение содержания СН4 (с 17.1–21.0 до 7.2–7.9 мкл/л) зафиксировано при значении солености 2‰. Второе резкое снижение концентраций СН4 наблюдалось при солености 9‰. Для зоны смешения вод р. Волга (рукав Бахтемир) и Каспийского моря в интервале величины солености 1–2‰ фиксируется первый «метановый барьер», выражающийся в уменьшении содержания СН4 с 17.6 мкл/л до 1.8 мкл/л. Второй менее выраженный спад (более чем в 2 раза) обнаруживается при солености 9‰.
Зона смешения вод р. Раздольная с водами Амурского залива Японского моря характеризуется более плавным снижением концентрации СН4 с 20.0–22.5 мкл/л до 2.0–0.2 мкл/л по мере увеличения солености [8]. При этом первый «метановый барьер» прослеживался при солёности 1–2‰, второй – 16‰. Аналогичная закономерность выявлена американскими исследователями для рек Потомак и Элси [25], [30]. В этих эстуариях в воде выявлено резкое падение концентрации СН4 в зоне смешения при солёности 1–4‰. В зонах переходных от эстуарных к морским водам, при солёности характерной для каждого водного объекта (см. рис. 4), выявлен второй, менее выраженный метановый барьер.
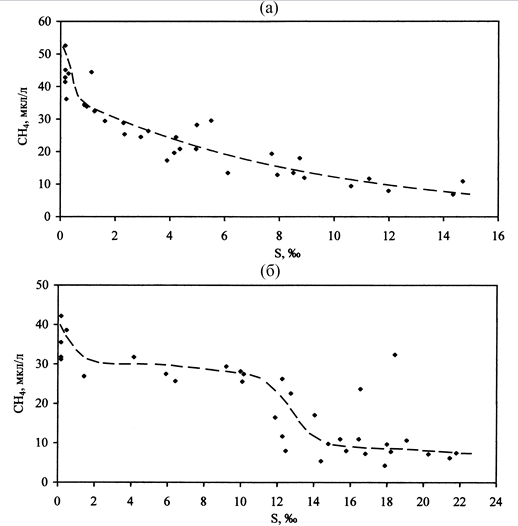
В зоне смешения пресных речных вод р. Северная Двина и солоноватых вод Двинской губы Белого моря, верхняя граница которой проходит глубоко в дельте и смещается в зависимости от фазы приливно-отливного цикла, нагонных явлений, уровня моря и расхода воды в реке [5], также наблюдается снижение содержания СН4 по мере возрастания солености (рис. 5). При этом, как показано на примере протоки Маймакса, первый спад содержания СН4 как в поверхностном, так и в придонном слое фиксируется в интервале солености 1–2‰, второй – при солености 12–14‰ – отмечен только в придонном горизонте, в то время как в поверхностном слое снижение концентраций СН4 в этом интервале солености происходит более плавно. В отличие от рассмотренных выше бесприливных зон смешения (р. Дон – Азовское море, р. Кубань – Азовское море, р. Волга – Каспийское море) в р. Северная Двина первый спад выражен слабее, а второй намного сильнее (для придонного слоя). Это может быть объяснено тем, что в Северной Двине в результате мощного влияния приливно-отливных явлений взаимодействие речных и морских вод начинается не в пределах устьевого взморья, а глубоко в дельте реки в узких пространствах русел рукавов и проток. И, как следствие, в интервале солености 1–2‰ не происходит такого резкого снижения концентрации СН4 в результате разбавления морскими водами, как в условиях широких пространств устьевого взморья рек Дон, Кубань и Волга. Более выраженный второй спад при солености 12–14‰ и обусловлен поступлением вод из протоки Маймакса в широкое русло Корабельного устья.
Рис. 5 – Распределение содержания метана в поверхностном (а) и придонном (б) слоях воды в зависимости от солености в зоне смешения «р. Северная Двина – Двинская губа Белого моря» [5].
В целом характер изменения содержания СН4 при возрастании солености в зонах смешения «река – море» (уменьшение по экспоненте) указывает на то, что данное явление обусловлено не только разбавлением речного стока морскими водами, но и снижением интенсивности продуцирования СН4 в верхнем горизонте донных отложений морей и зон смешения, что выражается в уменьшении концентраций СН4 в этом слое [2], [6], [18]. Последнее может быть обусловлено рядом причин.
Во-первых, в зонах смешения река – море происходит переход от пресноводной структуры зональности микробиологических процессов в донных осадках к морской, характеризующейся более мощной зоной сульфатредукции, отделяющей ниже расположенную зону метангенерации от поверхности дна. То есть увеличение солености и, как следствие, содержания сульфатных ионов в водах зон смешения, приводит к расширению зоны сульфатредукции, вследствие проникновения сульфатов на большую глубину донных отложений. В таких условиях преимущество в конкурентной борьбе за обладание питательными субстратами (ацетат, формиат и молекулярный водород) имеют сульфатредукторы, поскольку осуществляют термодинамически более выгодный процесс, чем метаногены [18], [28], [31]. При исчерпании сульфатов на некоторой глубине, процесс сульфатредукции замедляется и активизируется процесс метаногенеза. При этом диффундируя через мощную зону сульфатредукции, значительная часть СН4 сначала анаэробно окисляется, а затем аэробно – в верхнем слое донных отложений [7], [9], [18], что может существенно снижать объемы его поступления в водную толщу, и, как следствие, уменьшать его концентрации в ней.
Во-вторых, эстуарные участки (зоны смешения река – море) являются мощными геохимическими барьерами. При превращении речной воды в морскую основной качественный скачок осуществляется в диапазоне солёности от 1 до 2‰ [1], при этом, помимо изменения соотношения между компонентами основного солевого состава и ионной силы раствора, наблюдаются изменения температурного и кислородного режима воды, кислотно-щелочных условий, количество пелитовых частиц во взвеси уменьшается втрое, происходит осаждение значительных количеств металлов [11], [21], [24], уменьшается количество питательных биогенных солей, происходит снижение численности бактериопланктона, количества сапрофитных бактерий и интенсивности фотосинтеза, отмечается резкое уменьшение РОВ и ВОВ [1]. Важную роль играют увеличение глубин и удалённость от берегов, в результате чего в донные отложения участков, удаленных от зон смешения и прибрежной зоны (основная зона развития фитопланктона), поступает более минерализованное органическое вещество, что делает его менее доступным для микроорганизмов, в том числе, метанобразующих архей.
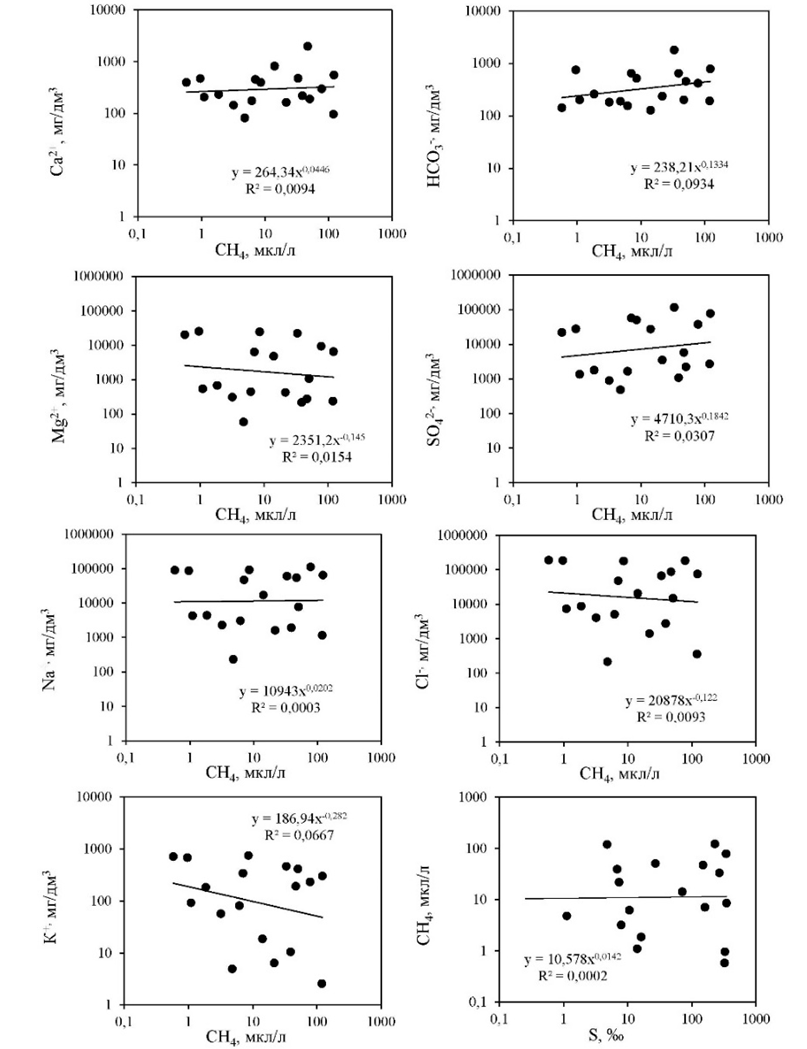
По данным экспедиционных исследований, проведенных на водных объектах юга ЕТР [14], [16], [27], характеризующихся различной минерализацией (от менее 0.3 до 347.1 г/дм3) и степенью антропогенной нагрузки (Азовское море, его лиманы и заливы (5 станций), высокоминерализованные озера (11 станций), водотоки (2 станции)), построены зависимости (рис. 6), показывающие отсутствие достоверных связей между концентрациями метана и основными ионами в воде (для концентраций СН4 и ионов Са2+, Mg2+, Na+, Cl-, SO42-и солености – r варьирует от -0.18 до +0.1, при P > 0.05) или наличие слабых достоверных связей (для концентраций СН4 и ионов K+ и HCО3- – r составляет -0.26 и +0.31, соответственно, при P < 0.05). При этом, наличие достоверной положительной связи между концентрациями СН4 и гидрокарбонат-иона (HCО3-) может быть теоретически объяснено взаимосвязью процессов формирования этих компонентов химического состава вод в ходе интенсивного разложения остатков органических веществ. Так, накопление гидрокарбонат-иона в воде часто обязано растворению СО2 – продукта минерализации растительных остатков в почвах, воде и донных отложениях. В свою очередь СН4 также является продуктом разложения органического вещества в анаэробных условиях донных отложений и водной толщи, причем для метаногенов СО2 является одним из основных (универсальных) питательных субстратов [18].
На основе рассмотренного материала можно сделать вывод, что влияние ионного состава и солености (минерализации) вод на концентрации метана не является определяющим фактором. Основным фактором выступает интенсивность продукционно-деструкционных процессов, контролирующих содержание органического вещества и окислительно-восстановительные условия в водных объектах, а также гидрологические и морфометрические параметры водного объекта, определяющие распределение литологических типов донных отложений. Наличие в большом количестве солей, в том числе сульфатов в высокоминерализованных водоемах, при повышенных концентрациях лабильного органического вещества в их водной толще и грязевых отложениях не препятствует одновременному активному протеканию процессов метаногенеза и сульфатредукции, вследствие снижения конкуренции за питательные субстраты между сульфатредукторами и метаногенами [14], [16], [27].
Рис. 6 – Зависимости между соленостью, концентрациями ионов и метаном в водной толще водных объектов юга ЕТР
| Финансирование Работа выполнена при финансовой поддержке проектов РФФИ № 19-05-00770 (разработка концепции, построение и анализ регрессионных моделей) и № 19-05-50097 (изучение влияния солености и ионного состава на тесноту связи содержания метана с физико-химическими параметрами). | Funding The work was carried out with the financial support of RFBR projects No. 19-05-00770 (concept development, construction and analysis of regression models) and No. 19-05-50097 (study of the effect of salinity and ionic composition on the close relationship of methane content with physical and chemical parameters). |
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Артемьев В.Е. Геохимия органического вещества в системе «река – море» / В.Е. Артемьев. – Москва: Наука, 1993. – 204 с.
- Гарькуша Д.Н. Метан в устьевой области реки Дон / Д.Н. Гарькуша, Ю.А. Федоров. – Ростов-на-Дону – Москва: ЗАО «Ростиздат», 2010. – 181 с.
- Гарькуша Д.Н. Метан как индикатор условий раннего диагенеза и экологического состояния водных экосистем / Д.Н. Гарькуша, Ю.А. Фёдоров, Н.С. Тамбиева // Изв. Вузов. Сев.-Кав. регион. Серия Естеств. науки. – 2013. – № 6. – С. 78–82.
- Гарькуша Д.Н. Натурное моделирование загрязнения пресного водоема кадмием / Д.Н. Гарькуша, Ю.А. Федоров, Н.С. Тамбиева, Т.В. Князева // Водные ресурсы. – 2018. – Т. 45.– № 5. – С. 514–525.
- Гарькуша Д.Н. Метан в воде и донных отложениях устьевой области Северной Двины (Белое море) / Д.Н. Гарькуша, Ю.А. Федоров, М.И. Хромов // Океанология. – – Т. 50. – № 4. – С. 534–547.
- Дзюбан А.Н. Численность бактерий и микробиологические процессы в воде Тугурского залива Охотского моря / А.Н. Дзюбан // Микробиология. – 2003. – Т. 72. № 3. – С. 419–426.
- Егоров А.В. Биогеохимия метана в осадках Балтийского и Черного морей: кинетические модели диагенеза / А.В. Егоров // Океанология. – 2000. – Т. 40. – № 5. – С. 690–696.
- Лапин И.А. Биогеохимические аспекты поведения растворенного органического вещества в эстуарии реки Раздольная – Амурский залив Японского моря / И.А. Лапин, В.В. Аникеев, Ю.Я. Винников и др. // Океанология. – 1990. – Т. 30. – Вып. 2. – С. 234–240.
- Леин А.Ю. Биогеохимический цикл метана в океане / А.Ю. Леин, М.В. Иванов / Отв. ред. А.П. Лисицын. – Москва: Наука, 2009. – 576 с.
- Леин А.Ю. Биогеохимические процессы циклов серы и углерода в Карском море / А.Ю. Леин, И.И. Русанов, А.С. Саввичев и др. // Геохимия. – 1996. – № 11. – С. 1027–1044.
- Лисицын А.П. Новые возможности четырехмерной океанологии и мониторинга второго поколения – опыт двухлетних исследований на Белом море // Актуальные проблемы океанологии / А.П. Лисицын / Под. ред. Н.П. Лаверова. – Москва: Наука, 2003. – С. 503–556.
- Намсараев Б.Б. Бактериальное окисление метана в эстуарии реки Енисей и Карском море / Б.Б. Намсараев, И.И. Русанов, И.Н. Мицкевич и др. // Океанология. – 1995. – Т. 35. – № 1. – С. 88–93.
- Федоров Ю.А. Закономерности распределения и образования метана в водных экосистемах / Ю.А. Федоров, Д.Н. Гарькуша // Метеоспектр. – 2007. – № 4. – С. 249–251.
- Федоров Ю.А. Метан и сероводород в лечебных сульфидных грязях (на примере озера Большой Тамбукан) / Ю.А. Федоров, Д.Н. Гарькуша, И.В. Доценко, К.А. Афанасьев // Изв. Вузов. Сев.-Кав. регион. Серия Естеств. науки. – 2014. – №3. – С. 102–109.
- Федоров Ю.А. Газовый состав пелоидов Таманского полуострова / Ю.А. Федоров, Д.Н. Гарькуша, Е.Г. Потапов, Р.Г. Трубник // Курортная медицина. – – № 3. – С. 26–33.
- Фёдоров Ю.А. Сопряженные циклы метана и сероводорода в лечебных грязях водоемов бассейнов Азовского и Каспийского морей / Ю.А. Фёдоров, Д.Н. Гарькуша, Р.Г. Трубник // Международный научно-исследовательский журнал. – 2017. – №09(63). – Часть 2. – Сентябрь. – С. 17–21.
- Фёдоров Ю.А. Глобальные вариации концентраций метана в водных экосистемах / Ю.А. Фёдоров, Н.С. Тамбиева, Д.Н. Гарькуша // Тез. докл. XV Межд. шк. морской геологии. Т.I. – Москва, 2003. – С. 344–345.
- Федоров Ю.А. Метан в водных экосистемах / Ю.А. Фёдоров, Н.С. Тамбиева, Д.Н. Гарькуша, В.О. Хорошевская. – 2-е изд., перераб. и доп. – Ростов-на-Дону – Москва: ЗАО «Ростиздат», 2007. – 330 с.
- Федоров Ю.А. Распределение содержания метана в воде по профилю "р. Дон – Азовское море – Чёрное море – пролив Босфор – бухта Золотой Рог – Мраморное море – Средиземное море" / / Ю.А. Фёдоров, Н.С. Тамбиева, В.О. Хорошевская // Межвуз. сб. науч. тр.: «Безопасность жизнедеятельности. Охрана окружающей среды». – Ростов-на-Дону: РГАСМ, 1999. – В. 2. – С. 29–34.
- Федоров Ю.А. Теоретические аспекты формирования метанового барьера в зоне смешения «река – эстуарий – море» / / Ю.А. Фёдоров, Н.С. Тамбиева, В.О. Хорошевская // Межвуз. сб. науч. тр.: «Безопасность жизнедеятельности. Охрана окружающей среды». – Ростов-на-Дону: РГАСМ, 1998. – В. 2. – С. 82–84.
- Хованский А.Д. Особенности формирования барьеров в аквальных системах / А.Д. Хованский, А.Ю. Митропольский, В.П. Усенко. – Киев, 1988. – 51 с.
- Хованский А.Д. Ландшафтно-геохимическое районирование водных объектов системы “река – море” / А.Д. Хованский, В.П. Усенко, А.Ю. Митропольский. – Киев, 1986. – 58 с.
- Хорошевская В.О. Поведение содержания метана в зонах смешения «река-море» / В.О. Хорошевская, Ю.А. Федоров // Тез. Докл. XV Межд. шк. морской геологии. Т.II. – Москва, 2003. – С. 211–212.
- Хрусталев Ю.П. Закономерности осадконакопления во внутриконтинентальных морях аридной зоны / Ю.П. Хрусталев. – Ленинград: Наука, 1989. – 261 с.
- Angelis M.A. Methane in surface waters of Oregon estuaries and rivers / M.A. Angelis, M.D. Lilley // Limnol. Oceanogr. – 1987. – Vol. 32. – № 3. – P. 716-722.
- Darling W.G. The hydrogeochemistry of methane: Evidence from English groundwaters / W.G. Darling, D.C. Gooddy // Chemical Geology. – 2006. – Vol. 229. – Issue 4. – P. 293–312.
- Fedorov Y.A. Sulfite-Reducing Clostridia and their Participation in Methane and Hydrogen Sulfide Formation in the Bottom Sediments of Water Objects and Streams of the ETR South / Y.A. Fedorov, D.N. Gar’kusha, R.G. Trubnik, M.A. Morozova // Water Resources. – – Vol. 46. – № 1. – P. S85–S93.
- McCarty P.L. Energetics of organic matter degradation // Water Pollution Microbiology / P.L. McCarty / Ed. Mitchell R. Wiley Interscience, 1972. – P. 91.
- Murphy E.M. The influence of microbial activity and sedimentary organic carbon on the isotope geochemistry of the Middendorf aquifer / E.M. Murphy, J.A. Schramke, J.K. Fredrickson, H.W. Bledsoe, A.J. Francis, D.S. Sklarew, J.C. Linehan // Water Resources Research. – 1992. – Vol. 28. –Р. 723–740.
- Swinnerton J.R. Distribution of methane and carbon monooxide between the atmosphere and natural water / J.R. Swinnerton, K.J. Linnenbom, C.H. Cheek // Environ. Sci. Technol. – 1969. – Vol. 3. – P. 836–838.
- Winfrey M.R. Effect of sulphate on carbon and electron flow during microbial methanogenesis in freshwater sediments / M.R. Winfrey, I.G. Zeikus // Appl. Environ. Microbiol. – 1977. Vol. 22, № 2. P. 275–281.
Список литературы на английском языке / References in English
- Artem'yev V.E. Geohimiya organicheskogo veshchestva v sisteme «reka – more» [Geochemistry of organic matter in the "river – sea" system]. – Moscow: Nauka, 1993. – 204 p. [in Russian]
- Gar'kusha D.N. Metan v ust'evoj oblasti reki Don [Methane in the estuary region of the Don river] / Gar'kusha D.N., Fedorov Yu.A.. -Rostov-on-Don – Moscow: ZAO «Rostizdat», 2010. – 181 p. [in Russian]
- Gar'kusha D.N. Metan kak indikator uslovij rannego diageneza i ekologicheskogo sostoyaniya vodnyh ekosistem [Methane as an indicator of conditions of early diagenesis and ecological state of water ecosystems] / Gar'kusha D.N., Fedorov Yu.A., Tambieva N.S. // Izvestiya Vuzov. Severo-Kavkazskij region. Seriya Estestvennye nauki [Izvestiya Vuzov. North Caucasus region. Natural Sciences series]. – 2013. – № 6. – P. 78–82. [in Russian]
- Gar'kusha D.N. Naturnoe modelirovanie zagryazneniya presnogo vodoema kadmiem [Full-Scale modeling of fresh water pollution with cadmium] / Gar'kusha D.N., Fedorov Yu.A., Tambieva N.S., Knyazeva T.V. // Vodnye resursy [Water resources]. – 2018. – Vol. 45. – № 5. – P. 514–525. [in Russian]
- Gar'kusha D.N. Metan v vode i donnyh otlozheniyah ust'evoj oblasti Severnoj Dviny (Beloe more) [Methane in water and bottom sediments of the estuarine region of the Northern Dvina (White sea)] / Gar'kusha D.N., Fedorov Yu.A., Khromov M.I. // Okeanologiya [Oceanology]. – 2010. – Vol. 50. – № 4. – P. 534–547. [in Russian]
- Dzyuban A.N. Chislennost' bakterij i mikrobiologicheskie processy v vode Tugurskogo zaliva Ohotskogo morya [The number of bacteria and microbiological processes in the water of the Tugur Bay of the sea of Okhotsk] / Dzyuban A.N. // Mikrobiologiya [Microbiology]. – 2003. – Vol. 72. – № 3. – P. 419–426. [in Russian]
- Egorov A.V. Biogeohimiya metana v osadkah Baltijskogo i CHernogo morej: kineticheskie modeli diageneza [Biogeochemistry of methane in the sediments of the Baltic and Black seas: kinetic models of diagenesis] / Egorov A.V. // Okeanologiya [Oceanology]. – 2000. – Vol. 40. № 5. – P. 690–696. [in Russian]
- Lapin I.A. Biogeohimicheskie aspekty povedeniya rastvorennogo organicheskogo veshchestva v estuarii reki Razdol'naya – Amurskij zaliv YAponskogo morya [Biogeochemical aspects of the behavior of dissolved organic matter in the Razdolnaya river estuary – Amur Bay of the sea of Japan] / Lapin I.A., Anikeev V.V., Vinnikov Yu.Ya., etc. // Okeanologiya [Oceanology]. – 1990. – Vol. 30. – № 2. – P. 234–240. [in Russian]
- Lein A.Yu. Biogeohimicheskij cikl metana v okeane [Biogeochemical cycle of methane in the ocean] / Lein A.Yu., Ivanov M.V. Ed. A.P. Lisicyn. – Moscow: Nauka, 2009. – 576 p. [in Russian]
- Lein A.Yu. Biogeohimicheskie processy ciklov sery i ugleroda v Karskom more [Biogeochemical processes of sulfur and carbon cycles in the Kara sea] / Lein A.Yu., Rusanov I.I., Savvichev A.S., etc. // Geohimiya [Geochemistry]. – 1996. – № 11. – P. 1027–1044. [in Russian]
- Lisitsyn A.P. Novye vozmozhnosti chetyrekhmernoj okeanologii i monitoringa vtorogo pokoleniya – opyt dvuhletnih issledovanij na Belom more [New opportunities of four-dimensional Oceanology and monitoring of the second generation-experience of two-year research on the White sea] / Lisitsyn A.P. // Aktual'nye problemy okeanologii [Actual problems of Oceanology] / Ed. N.P. Laverova. – Moscow: Nauka, 2003. – P. 503–556. [in Russian]
- Namsaraev B.B. Bakterial'noe okislenie metana v estuarii reki Enisej i Karskom more [Bacterial methane oxidation in the Yenisei river estuary and the Kara sea] / Namsaraev B.B., Rusanov I.I., Mitskevich I.N., etc. // Okeanologiya [Oceanology]. – 1995. – Vol. 35. – № 1. – P. 88–93. [in Russian]
- Fedorov A.Yu. Zakonomernosti raspredeleniya i obrazovaniya metana v vodnyh ekosistemah [Regularities of distribution and formation of methane in aquatic ecosystems] / Fedorov A.Yu., Gar'kusha D.N. // Meteospectr. – 2007. – № 4. – P. 249–251. [in Russian]
- Fedorov Yu.A. Metan i serovodorod v lechebnyh sul'fidnyh gryazyah (na primere ozera Bol'shoj Tambukan) [Methane and hydrogen sulfide in therapeutic sulfide mud (on the example of lake Bolshoy Tambukan)] / Fedorov Yu.A., Gar'kusha D.N., Dotsenko I.V., Afanasyev K.A. // Izvestiya Vuzov. Severo-Kavkazskij region. Seriya Estestvennye nauki [Izvestiya Vuzov. North Caucasus region. Natural Sciences series]. – 2014. № 3. – P. 102–109. [in Russian]
- Fedorov Yu.A. Gazovyj sostav peloidov Tamanskogo poluostrova [Gas composition of peloids of the Taman Peninsula] / Fedorov Yu.A., Gar'kusha D.N., Potapov E.G., Trubnik R.G. // Kurortnaya medicina [Resort medicine]. – 2017. – № 3. – P. 26–33. [in Russian]
- Fedorov Yu.A. Sopryazhennye cikly metana i serovodoroda v lechebnyh gryazyah vodoemov bassejnov Azovskogo i Kaspijskogo morej [Conjugated cycles of methane and hydrogen sulfide in therapeutic mud reservoirs of the Azov and Caspian seas] / Fedorov Yu.A., Gar'kusha D.N., Trubnik R.G. // Mezhdunarodnyj nauchno-issledovatel'skij zhurnal [International research journal]. 2017. №09(63). – Part 2, September. –P. 17–21. [in Russian]
- Fedorov Yu.A. Global'nye variacii koncentracij metana v vodnyh ekosistemah [Global variations of methane concentrations in aquatic ecosystems / Fedorov Yu.A., Tambieva N.S., Gar'kusha D.N. // Tez. dokl. XV Mezhd. shk. morskoj geologii [Thesis of reports XV International school of marine Geology]. Vol. I. – Moscow, 2003. – P. 344–345. [in Russian]
- Fedorov Yu.A. Metan v vodnyh ekosistemah [Methane in water ecosystems] / Fedorov Yu.A., Tambieva N.S., Gar'kusha D.N., V.O. Khoroshevskaya. – 2nd ed., reprint. – Rostov-on-Don-Moscow: ZAO «Rostizdat», 2007. – 330 p. [in Russian]
- Fedorov Yu.A. Raspredelenie soderzhaniya metana v vode po profilyu "r. Don – Azovskoe more – Chyornoe more – proliv Bosfor – buhta Zolotoj Rog – Mramornoe more – Sredizemnoe more" [Distribution of methane content in water according to the profile. "R. Don – Azov sea – Black sea – Bosphorus Strait – Golden horn Bay – Marmara sea – Mediterranean sea"] / Fedorov Yu.A., Tambieva N.S., Khoroshevskaya V.O. // Mezhvuzovskij sbornik nauchnyh trudov «Bezopasnost' zhiznedeyatel'nosti. Ohrana okruzhayushchej sredy» [Interuniversity collection of scientific papers "Safety of life. Environmental protection»]. – Rostov-on-Don: RGASM, 1999. – Vol. 2. –P. 29–34. [in Russian]
- Fedorov Yu.A. Teoreticheskie aspekty formirovaniya metanovogo bar'era v zone smesheniya «reka – estuarij – more» [Theoretical aspects of the formation of the methane barrier in the mixing zone "river – estuary – sea"] / Fedorov Yu.A., Tambieva N.S., Khoroshevskaya V.O. // Mezhvuzovskij sbornik nauchnyh trudov «Bezopasnost' zhiznedeyatel'nosti. Ohrana okruzhayushchej sredy» [Interuniversity collection of scientific papers "Safety of life. Environmental protection»]. – Rostov-on-Don: RGASM, 1998. –Vol. 2. – P. 82–84. [in Russian]
- Khovansky A.D. Osobennosti formirovaniya bar'erov v akval'nyh sistemah [Features of barrier formation in aquatic systems] / Khovansky A.D., Mitropolsky A.Yu., Usenko V.P. – Kiev, 1988. 51 p. [in Russian]
- Khovansky A.D. Landshaftno-geohimicheskoe rajonirovanie vodnyh ob"ektov sistemy “reka – more” [Landscape and geochemical zoning of water objects of the “river – sea " system] / Khovansky A.D., Usenko V.P., Mitropolsky A.Yu.. – Kiev, 1986. – 58 p. [in Russian]
- Khoroshevskaya V.O. Povedenie soderzhaniya metana v zonah smesheniya «reka-more» [Behavior of methane content in the "river – sea" mixing zones] / Khoroshevskaya V.O., Fedorov Yu.A. // Tez. dokl. XV Mezhd. shk. morskoj geologii [Thesis of reports XV International school of marine Geology]. Vol. II. – Moscow, 2003. – P. 211–212. [in Russian]
- Khrustalev Yu.P. Zakonomernosti osadkonakopleniya vo vnutrikontinental'nyh moryah aridnoj zony [Regularities of sedimentation in the intracontinental seas of the arid zone] / Khrustalev Yu.P. – Leningrad: Nauka, 1989. – 261 p. [in Russian]
- Angelis M.A. Methane in surface waters of Oregon estuaries and rivers / M.A. Angelis, M.D. Lilley // Limnol. Oceanogr. – 1987. – Vol. 32. – № 3. – P. 716-722.
- Darling W.G. The hydrogeochemistry of methane: Evidence from English groundwaters / W.G. Darling, D.C. Gooddy // Chemical Geology. – 2006. – Vol. 229. – Issue 4. – P. 293–312.
- Fedorov Y.A. Sulfite-Reducing Clostridia and their Participation in Methane and Hydrogen Sulfide Formation in the Bottom Sediments of Water Objects and Streams of the ETR South / Y.A. Fedorov, D.N. Gar’kusha, R.G. Trubnik, M.A. Morozova // Water Resources. – 2019. – Vol. 46. – № 1. – P. S85–S93.
- McCarty P.L. Energetics of organic matter degradation // Water Pollution Microbiology / P.L. McCarty / Ed. Mitchell R. Wiley Interscience, 1972. – P. 91.
- Murphy E.M. The influence of microbial activity and sedimentary organic carbon on the isotope geochemistry of the Middendorf aquifer / E.M. Murphy, J.A. Schramke, J.K. Fredrickson, H.W. Bledsoe, A.J. Francis, D.S. Sklarew, J.C. Linehan // Water Resources Research. – 1992. – Vol. 28. –Р. 723–740.
- Swinnerton J.R. Distribution of methane and carbon monooxide between the atmosphere and natural water / J.R. Swinnerton, K.J. Linnenbom, C.H. Cheek // Environ. Sci. Technol. – 1969. – Vol. 3. – P. 836–838.
- Winfrey M.R. Effect of sulphate on carbon and electron flow during microbial methanogenesis in freshwater sediments / M.R. Winfrey, I.G. Zeikus // Appl. Environ. Microbiol. – 1977. Vol. 22, № 2. P. 275–281.