ПРЯМОЕ И КОМПЛЕМЕНТ-ОПОСРЕДОВАННОЕ ДЕЙСТВИЕ АНТИМИКОБАКТЕРИАЛЬНЫХ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ НА РОСТ MYCOBACTERIUM TUBERCULOSIS IN VITRO.
Авдиенко В.Г.1, Майоров К.Б.2, Бабаян С.С.2, Онян А.В.3
1Кандидат медицинских наук, 2Кандидат биологических наук, 3младший научный сотрудник, ФГБНУ "Центральный научно-исследовательский институт туберкулеза", г. Москва
Работа выполнена при поддержке гранта РФФИ №14-04-01043
ПРЯМОЕ И КОМПЛЕМЕНТ-ОПОСРЕДОВАННОЕ ДЕЙСТВИЕ АНТИМИКОБАКТЕРИАЛЬНЫХ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ НА РОСТ MYCOBACTERIUM TUBERCULOSIS IN VITRO
Аннотация
Впервые представлены экспериментальные данные по поиску противотуберкулезных моноклональных антител (МАТ), действующих на рост живых вирулентных микобактерий в присутствие комплемента и без него in vitro. В цитотоксических тестах исследована панель из 32 МАТ. Среди них не выявлены антитела, которые бы ингибировали репликацию возбудителя in vitro. Добавление комплемента к МАТ также не приводило к статистически значимым результатам воздействия на микобактерии. Авторы предполагают, что специфичности антител, способные ингибировать рост микобактерий in vitro редки или вовсе отсутствуют в организме хозяина.
Ключевые слова: туберкулез, моноклональные антитела, микобактерии, цитотоксичность.
Avdienko V.G.1, Majorov K.B.2, Babayan S.S.2, Onyan A.V.3
1Candidate of Medical Sciences, 2Candidate of Biological Sciences, 3Staff scientist, Federal State Budgetary Scientific Institution «Central Tuberculosis Research Institute», Moscow
DIRECT AND COMPLEMENT-MEDIATED EFFECTS OF ANTIMYCOBACTERIAL MONOCLONAL ANTIBODIES ON MYCOBACTERIUM TUBERCULOSIS GROWTH IN VITRO
Abstract
Firstly experimental data on the searching of TB monoclonal antibodies are present, which has an effect on the growth of live virulent mycobacteria in the presence of the complement and also without one in vitro. The panel from 32 monoclonal antibodies was researched in cytotoxicity tests. Among the antibodies there was no one, which was able to inhibit a replication of the pathogen in vitro. Adding of the complement also none resulted to statistically significant data of the influence on mycobacteria. The authors suppose that there are a little or absence at all of the specifities of antibodies which are able to inhibit a replication of mycobacterial growth in vitro.
Keywords: tuberculosis, monoclonal antibodies, mycobacteria, cytotoxity.
Туберкулезные бациллы являются факультативным внутриклеточным паразитом и для их непосредственного связывания с антителами необходима экстрацеллюлярная фаза, во время которой происходит диссеминация возбудителя и заражение макрофагов [3].
Именно во время этой фазы многими авторами описано действие МАТ на течение экспериментального туберкулеза. Так, предварительная обработка культуры Mycobacterium tuberculosis МАТ против поверхностного антигена липоарабиноманнана B (LAM) более чем двукратно увеличивала время выживания животных при сублетальном заражении мышей [12]. Опсонизирующее действие МАТ 4057D2 против гепарин-связывающего гемагглютинина HBHA и ламинин-связывающего белка, необходимых для внелегочной диссеминации вирулентных микобактерий, ослабляло диссеминацию после внутриназальной инфекции у мышей [11]. МАТ против антигена MPT/MPB-83 (липогликопротеина M. tuberculosis и M. bovis), связывались с поверхностью M. bovis и повышали время выживания мышей зараженных высокими дозами M.bovis, при этом изменялась морфология гранулем и распространение бацилл в легких, явно модулируя вирулентность in vivo [2]. Аналогичный феномен наблюдали для МАТ TBA61 (IgA) против альфа-кристаллина, при этом МАТ IgG1 против этого же эпитопа не имели протективной эффективности [14]. Добавление же к TBA61 МАТ TBA84 (IgA) против 38-kDa PstS-1 не давало желаемого эффекта, указывая на анергистические эффекты действия антител [6].
Для человека описаны потенциально синергистические функции гуморального и клеточно-опосредованного иммунитета против туберкулеза, когда, например, антитела против микобактериальных антигенов у BCG-вакцинированных людей повышают клеточно-опосредованный ответ на микобактерии [13], но при этом сыворотка от людей, бывших в контакте с туберкулезными больными с высокими IgG титрами может блокировать пролиферацию на туберкулин [4].
Имеется косвенное упоминание об антителах непосредственно оказывающих ингибирующие действие на микобактерии, эти антитела должны были бы мимикрировать действие грибных киллерных токсинов и являться бактерицидными для микобактерий. Хотя подобных антител и не обнаружено при туберкулезе, факт, что микобактерия может быть убита напрямую антителами, вполне возможен из самого антитело-опосредованного механизма протекции. Кроме того, нет работ, где бы был проведен поиск таких антител, способных влиять на рост живых микобактерий в эксперименте, на широкой панели антимикобактериальных МАТ против различных антигенов.
C целью изучить возможность непосредственного воздействия МАТ на микобактерии, авторы создали панель антимикобактериальных МАТ, реагирующих с поверхностными антигенами Mycobacterium tuberculosis. Они были получены методом гибридомной технологии на протяжении длительного времени против различных антигенных препаратов: цельных клеток, липидных фракций, рекомбинантных белков и из B-клеток легкого зараженных мышей. Для проведения цитотоксических экспериментов требовалась максимальная чистота изучаемых МАТ, чтобы исключить любые побочные эффекты действия других антител МАТ, гибридомы были выращены in vitro в культуральной среде, содержащей аффинноочищенную на белкaх A и G фетальную сыворотку, не содержащую иных иммуноглобулинов.
Специфичность и изотип МАТ изучали в непрямом твердофазном иммуноферментном анализе с микобактериальными антигенами, в качестве вторых меченых антител использовали иммунопероксидазные конъюгаты против подклассов IgG и IgM (Jackson, Великобритания).
Спектр распознаваемых МАТ антигенов исследовали методом иммуноблоттинга (Western blotting) по стандартной методике c расфракционированными в диск-электрофорезе в 15% полиакриламидном геле в присутствии додецилсульфата натрия в редуцирующих условиях антигенами цельных клеток M.tuberculosis H37Rv.
Для очистки фетальной сыворотки и МАТ из супернатантов культуральных жидкостей использовали иммуноаффинную хроматографию на колонках с сефарозой, ковалентно-сшитой с белком A, G или L в FPLC (Pharmacia, Швеция). Эффлюаты МАТ диализовали против физраствора забуференного фосфатами (PBS), концентрировали ультрафильтрацией, а после диализа стерилизовали через фильтры 0,2mm и аликвотировали, без добавления каких-либо консервантов. Очищенную фетальную сыворотку также стерилизовали и замораживали при -20оС до использования.
В цитотоксических экспериментах применяли M.tuberculosis H37Rv из коллекции ФГБНУ «ЦНИИ туберкулеза», Москва. Микобактерии в аликвотах хранили при температуре -80оС. Для получения бактерий в log-фазе, культуру выращивали в бульоне Дюбо в течение 14 дней при 37оС. Отмывали в PBS c 0,05% Tween80 и ресуспендировали в среде, применяемой в конкретном эксперименте, и фильтровали через стерильный фильтр с размером пор 4 мкм для удаления агломератов. Далее определяли концентрацию M.tuberculosis в полученном фильтрате по КОЕ.
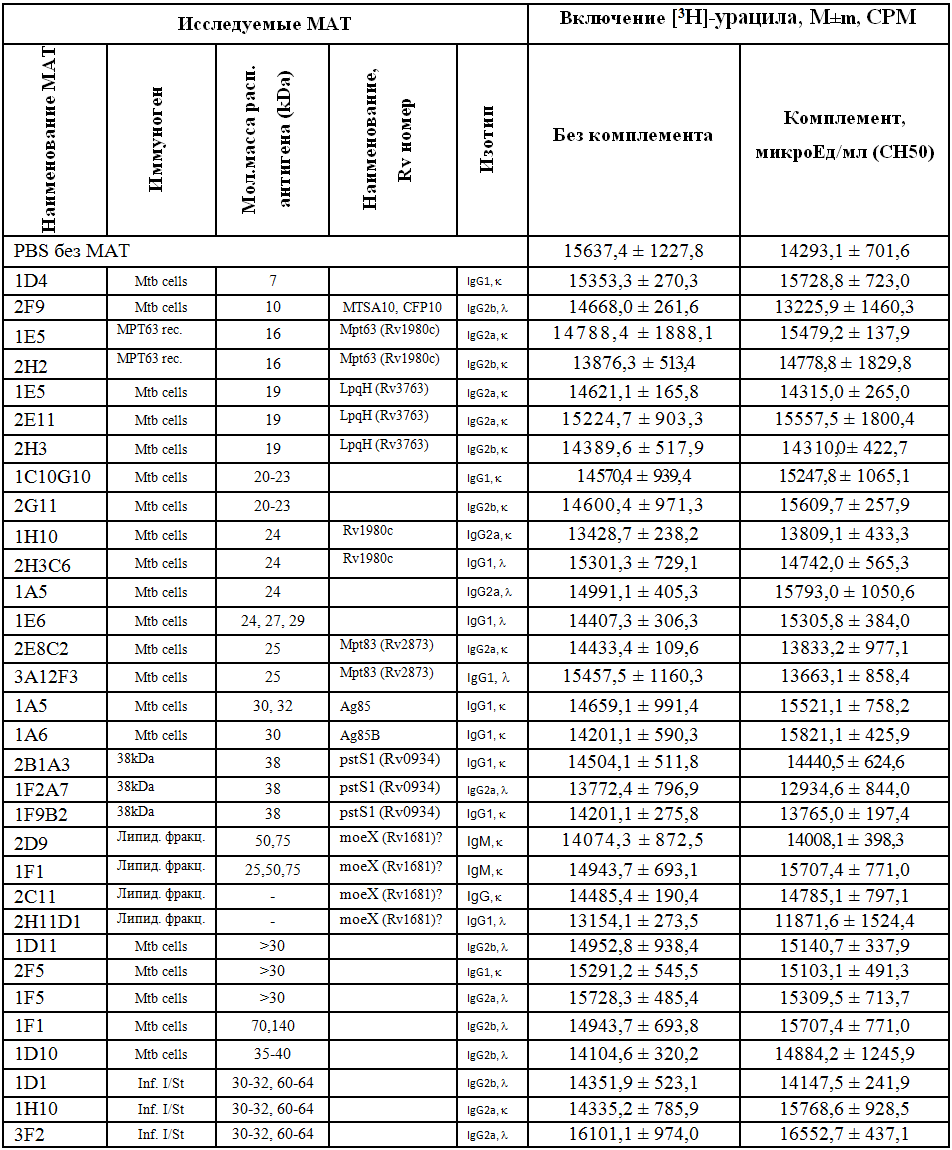
Цитотоксический тест проводили по методике [9]. Для этого в плоскодонный планшет помещали живые микобактерии M. tuberculosis H37Rv в количестве 4-40*104 КОЕ и МАТ или МАТ и комплемент кролика в дозе CH50 1 микроЕд/мл (Sigma, США). Через 6 часов в каждую лунку добавляли 1 микроCi [3H]-урацила, в качестве контроля использовали лунки с микобактериями, но без МАТ или без МАТ и комплемента. После 24 часовой инкубации рост культуры останавливали замораживанием при минус 30оС и харвестировали содержимое лунок на стеклянные фильтры (Scatron, Норвегия). После высушивания радиоактивность подсчитывали методом жидкостной сцинтилляции на бета-счетчике (Wallac, Финляндия). Результаты представляли как средний счет импульсов в минуту по каждому трипликату лунок (CPM) (Таблица №1).
Таблица 1 - Противотуберкулезная активность моноклональных антител в цитотоксическом тесте по включению [3H]-урацила M.tuberculosis H37Rv.
Заключение.
Из полученных данных видно, что различия между контрольными значениями и опытными данными в присутствии МАТ отсутствуют. Это указывает на то, что исследуемые МАТ не обладают прямым или опосредованным ингибирующим эффектом на микобактерии. Авторы предполагают, что вероятность обнаружения ингибирующих специфичностей антител низка. Кроме того, действие МАТ in vivo может сильно отличаться от прямого действия антител in vitro. Это может быть не только антимикобактериальная активность и активация комплемента, но и опсонизация [1], повышение Ca2+-сигналлинга макрофагов[7], выработка оксидантов, повышающих внутриклеточный киллинг [10], усиление выведения иммуномодуляторных микобактериальных антигенов типа LAM B [5] и активации комплемента [12].
По-видимому, действие антител на микобактерии при туберкулезе становится актуальным внутри организма, при непосредственном контакте с возбудителем или его антигенами in vivo.
Литература
- Armstrong JA, Hart PD. Phagosome-lysosome interactions incultured macrophages infected with virulent tubercle bacilli. Reversal of the usual non fusion pattern and observations on bacterial survival.// J ExpMed. 1975;142: 1–16.
- Chambers MA, Gavier-Widen D, Hewinson RG. Antibody bound to the surface antigen MPB83 of Mycobacterium bovis enhances survival against high dose and low dose challenge.//FEMS Immunol Med Microbiol. 2004; 41:93-100.
- Driver ER, Ryan GJ,Hoff DR, Irwin SM, Basaraba RJ, Kramnik I, Lenaerts AJ. Evaluation of a mouse model of necrotic granuloma formation using C3HeB/FeJ mice for testing of drugs against Mycobacterium tuberculosis. //Antimicrob Agents Chemother. 2012; 56: 3181–3195.
- Encinales L, Zuniga J, Granados-Montiel J, Yunis M, Granados J, Almeciga I, Clavijo O, Awad C, Collazos V, Vargas-Rojas MI, et al. Humoral immunity in tuberculin skin test anergy and its role in high-risk persons exposed to active tuberculosis.//Mol Immunol. 2010; 47: 1066–1073.
- Glatman-Freedman A., Mednik A.J., Lendval N. AND Casadevall A. Clearance and Organ Distribution of Mycobacterium tuberculosis Lipoarabinomannan (LAM) in the Presence and Absence of LAM-Binding Immunoglobulin M.//Inf. Immun., 2000 Jan.; 68(1): 335–341.
- Lopez Y, Yero D, Falero-Diaz G, Olivares N, Sarmiento ME, Sifontes S, Solis RL, Barrios JA, Aguilar D, Hernandez- Pando R. Induction of a protective response with an IgA monoclonal antibody against Mycobacterium tuberculosis 16 kDa protein in a model of progressive pulmonary infection.//Int J Med Microbiol. 2009; 299: 447–452.
- Malik ZA, Denning GM, Kusner DJ. Inhibition of Ca2+signaling by M. tuberculosis is associated with reduced phagosome–lysosome fusion and increased survival within human macrophages.//J Exp Med. 2000; 191: 287–302.
- Manivannan S, Rao NV, Ramanathan VD. Role of complement activation and antibody in the interaction between Mycobacterium tuberculosis and human macrophages.//Indian J Exp Biol. 2012; 50: 542–550.
- Majorov K. B., Lyadova I.V., Kondratieva T.K., Eruslanov E.B., Rubakova E.I., Orlova M.O., Mischenko V.V., and Apt A.S. Different Innate Ability of I/St and A/Sn Mice To Combat Virulent Mycobacterium tuberculosis: Phenotypes Expressed in Lung and Extrapulmonary Macrophages.//InfImmun., 2003; 71(2): 697-707.
- Mossalayi M.D., Vouldoukis I, Mamani-Matsuda M, Kauss T, Guillon J, Maugein J, Moynet D, Rambert J, Desplat V. CD23 mediates antimycobacterial activity of human macrophages.//Infect Immun. 2009; 77: 5537–5542.
- Pethe K., P. Bifani, H. Drobecq, C. Sergheraert, A.-S. Debrie, C. Locht, and Menozzi F.D. Mycobacterial heparin-binding hemagglutinin and laminin-binding protein share antigenic methyllysines that confer resistance to proteolysis.// 2002; 99(16): 10759–10764.
- Teitelbaum R., Glatman-Freedman A., Chen B., Robbins J. B., Unanue E., Casadevall A., AND Bloom B.R. A mAb recognizing a surface antigen of Mycobacterium tuberculosis enhances host survival.//Proc.Natl. Acad. Sci. USA. 1998; 95: 15688–15693.
- de Valliere S, Abate G, Blazevic A, Heuertz RM, Hoft DF. Enhancement of innate and cell-mediated immunity by antimycobacterial antibodies.//Infect Immun. 2005; 73: 6711–6720.
- Williams A, Reljic R, Naylor I, Clark SO, Falero-Diaz G,Singh M, Challacombe S, Marsh PD, Ivanyi J. Passive protection with immunoglobulin A antibodies against tuberculous early infection of the lungs.//Immunology. 2004; 111: 328–333.
References
- Armstrong JA, Hart PD. Phagosome-lysosome interactions incultured macrophages infected with virulent tubercle bacilli. Reversal of the usual non fusion pattern and observations on bacterial survival.// J ExpMed. 1975;142: 1–16.
- Chambers MA, Gavier-Widen D, Hewinson RG. Antibody bound to the surface antigen MPB83 of Mycobacterium bovis enhances survival against high dose and low dose challenge.//FEMS Immunol Med Microbiol. 2004; 41:93-100.
- Driver ER, Ryan GJ,Hoff DR, Irwin SM, Basaraba RJ, Kramnik I, Lenaerts AJ. Evaluation of a mouse model of necrotic granuloma formation using C3HeB/FeJ mice for testing of drugs against Mycobacterium tuberculosis. //Antimicrob Agents Chemother. 2012; 56: 3181–3195.
- Encinales L, Zuniga J, Granados-Montiel J, Yunis M, Granados J, Almeciga I, Clavijo O, Awad C, Collazos V, Vargas-Rojas MI, et al. Humoral immunity in tuberculin skin test anergy and its role in high-risk persons exposed to active tuberculosis.//Mol Immunol. 2010; 47: 1066–1073.
- Glatman-Freedman A., Mednik A.J., Lendval N. AND Casadevall A. Clearance and Organ Distribution of Mycobacterium tuberculosis Lipoarabinomannan (LAM) in the Presence and Absence of LAM-Binding Immunoglobulin M.//Inf. Immun., 2000 Jan.; 68(1): 335–341.
- Lopez Y, Yero D, Falero-Diaz G, Olivares N, Sarmiento ME, Sifontes S, Solis RL, Barrios JA, Aguilar D, Hernandez- Pando R. Induction of a protective response with an IgA monoclonal antibody against Mycobacterium tuberculosis 16 kDa protein in a model of progressive pulmonary infection.//Int J Med Microbiol. 2009; 299: 447–452.
- Malik ZA, Denning GM, Kusner DJ. Inhibition of Ca2+signaling by M. tuberculosis is associated with reduced phagosome–lysosome fusion and increased survival within human macrophages.//J Exp Med. 2000; 191: 287–302.
- Manivannan S, Rao NV, Ramanathan VD. Role of complement activation and antibody in the interaction between Mycobacterium tuberculosis and human macrophages.//Indian J Exp Biol. 2012; 50: 542–550.
- Majorov K. B., Lyadova I.V., Kondratieva T.K., Eruslanov E., Rubakova E.I., Orlova M.O., Mischenko V.V., and Apt A.S. Different Innate Ability of I/St and A/Sn Mice To Combat Virulent Mycobacterium tuberculosis: Phenotypes Expressed in Lung and Extrapulmonary Macrophages.//Inf Immun., 2003; 71(2): 697-707.
- Mossalayi M.D., Vouldoukis I, Mamani-Matsuda M, Kauss T, Guillon J, Maugein J, Moynet D, Rambert J, Desplat V. CD23 mediates antimycobacterial activity of human macrophages.//Infect Immun. 2009; 77: 5537–5542.
- Pethe K., P. Bifani, H. Drobecq, C. Sergheraert, A.-S. Debrie, C. Locht, and Menozzi F.D. Mycobacterial heparin-binding hemagglutinin and laminin-binding protein share antigenic methyllysines that confer resistance to proteolysis.// 2002; 99(16): 10759–10764.
- Teitelbaum R., Glatman-Freedman A., Chen B., Robbins J. B., Unanue E., Casadevall A., AND Bloom B.R. A mAb recognizing a surface antigen of Mycobacterium tuberculosis enhances host survival.//Proc.Natl. Acad. Sci. USA. 1998; 95: 15688–15693.
- de Valliere S, Abate G, Blazevic A, Heuertz RM, Hoft DF. Enhancement of innate and cell-mediated immunity by antimycobacterial antibodies.//Infect Immun. 2005; 73: 6711–6720.
- Williams A, Reljic R, Naylor I, Clark SO, Falero-Diaz G,Singh M, Challacombe S, Marsh PD, Ivanyi J. Passive protection with immunoglobulin A antibodies against tuberculous early infection of the lungs.//Immunology. 2004; 111: 328–333.