Системный подход к этиологии, патогенезу патологических процессов бассейна левой почечной вены и развитию первичной катехоламиновой гипертензии
Системный подход к этиологии, патогенезу патологических процессов бассейна левой почечной вены и развитию первичной катехоламиновой гипертензии
Аннотация
В бассейне левой почечной вены имеется группа патологических состояний, связанных с определенными анатомическими структурами, а также гемодинамическими нарушениями, обусловленными синтопией вен артериального и венозного бассейнов. Актуальность проблемы — это широкая распространенность, определяющая роль в структуре сердечно-сосудистой и общей летальности. Ситуация усугубляется у больных с рефрактерной артериальной гипертензией, а также кризовой артериальной гипертензией, где риск развития сердечно-сосудистых осложнений в ближайшие 30 лет составляет свыше 20–30%. Устранение причины приводит к полному излечению или значительному улучшению, позволяющему снизить летальность и улучшить качество жизни. Цель исследования — изучить этиологию, патогенез патологических процессов бассейна левой почечной вены и развития первичной катехоламиновой гипертензии.
В ходе нашего исследования были изучены 2 направления. Анатомический материал, который позволил изучить бассейн левой почечной вены, наличие либо отсутствие клапанных структур и их влияние на патологические процессы, а также гемодинамическое воздействие артерий, аорты, верхней брыжеечной вены на бассейн левой почечной вены. Изучение клапанных структур проводилось на 60 органокомплексах, с использованием классических методик. Система ЛПВ заполнялась водной взвесью сульфата бария с последующим проведением рентгенографии. Изучение синтопии аорты и верхней брыжеечной вены с ЛПВ проведено путем исследования на 100 трупах. В дальнейшем изучалось гемодинамическое воздействие артериальных стволов на ЛПВ. Клинический материал предоставлен результатами хирургического лечения 59 больным, которым на основании клинических обследований и изучения гистологического материала (надпочечников), выставлен диагноз первичной катехоламиновой гипертензии.
Системный подход к этиологии, патогенезу патологических процессов бассейна ЛПВ позволил доказать группу причин, вызывающих повышенное давление бассейна ЛПВ (синтопия почечной вены и артериальных структур, а также гидродинамическое воздействие аорты и ВБА). Повышенное давление бассейна ЛПВ приводит в 61% к недостаточности клапанных структур и развитию варикозного расширения вен таза и варикоцеле. Отсутствие клапанов в надпочечной вене и почке приводит к прямому воздействию венной гипертензии на ткани данных органов, вызывая гипоксию и развитие их гиперфункции. В результате венной гипертензии бассейна левого надпочечника развивается первичная катехоламиновая гипертония. В результате венной гипертензии и гипоксии развивается повышенный выброс ренина и включение РААС в патогенезе артериальной гипертензии.
1. Введение
В бассейне левой почечной вены имеется целая группа патологических состояний, связанных с определенными анатомическими структурами, а также гемодинамическими нарушениями, обусловленными синтопией вен артериального и венозного бассейнов , . В отношении варикоцеле, варикозного расширения вен таз имеются многочисленные исследования. Что касается левого надпочечника, то воздействия гемодинамики на структуру и функцию надпочечника работы носят единичный характер. Особое значение имеет как артериальная гипертензия, которая развивается при поражении левого надпочечника.
Актуальность проблемы артериальной гипертензии очевидна. Это широкая распространенность, определяющая роль в структуре сердечно-сосудистой и общей летальности. Ситуация усугубляется у больных с рефрактерной артериальной гипертензией, а также кризовой артериальной гипертензией, где риск развития сердечно-сосудистых осложнений ближайшие 30 лет составляет свыше 20–30 процентов , . В особую группу следует выделить больных с симптоматической артериальной гипертензией, где, как правило, отмечается как тяжелое течение заболевания, так и высокий процент осложнений. Устранение причины приводит к полному излечению или значительному улучшению, позволяющему снизить летальность и улучшить качество жизни. Процент таких симптоматических гипертензий по данным разных авторов от 4 до 20 процентов. Имея значительный опыт лечения артериальной гипертензии с различной этиологией, мы на основании изучения трупного материала (160) и клинического исследования (56 больных), пришли к выводу о первичной катехоламиновой артериальной гипертензии, как самостоятельного заболевания, имеющего свою анатомическую предуготовленность и клиническое течение . Оперативное лечение полностью устраняет клиническую картину, или переводит заболевание в более легкую форму, что позволяет снизить осложнение и летальность.
Цель исследования — изучить этиологию, патогенез патологических процессов бассейна левой почечной вены и развития первичной катехоламиновой гипертензии.
2. Материалы и методы
В ходе нашего исследования были изучены 2 направления. Анатомический материал, который позволил изучить бассейн левой почечной вены, наличие либо отсутствие клапанных структур и их влияние на патологические процессы, а также гемодинамическое воздействие артерий, аорты, верхней брыжеечной вены на бассейн левой почечной вены. Изучение клапанных структур проводилось на 60 органокомплексах, с использованием классических методик. Система ЛПВ заполнялась водной взвесью сульфата бария с последующим проведением рентгенографии.
Изучение синтопии аорты и верхней брыжеечной вены с ЛПВ проведено путем исследования на 100 трупах. В дальнейшем изучалось гемодинамическое воздействие артериальных стволов на ЛПВ с последующим использованием математических методик, связанных с законами гидродинамики. Клинический материал представлен результатами хирургического лечения 59 больным, которым на основании клинических обследований и изучения гистологического материала (надпочечников), выставлен диагноз первичной катехоламиновой гипертензии .
Также в данном исследовании проведен анализ 59 больных с первичной катехоламиновой артериальной гипертонией. Возраст больных от 15 до 65 лет (средний возраст 44±11 лет). Чаще болели женщины 40 случаев (67,8%), мужчины 19 случаев (32,2%). Длительность заболевания от года до 10 лет. Все больные прооперированы, выполнено 56 адреналэктомий (слева 52 (92,9%), справа 4 (7,1%)). Троим больным выполнена рентгенэндоваскулярная окклюзия центральной надпочечниковой вены по разработанной нами методике. Отдаленные результаты прослежены свыше 10 лет у 30 больных (50,9%). Кроме обычных методов исследования, изучался гормональный профиль (определение ренина, альдостерона и т.д.), радиоиммунные методы. Проводилась селективная флебография надпочечниковой вены, забор крови из почечных и надпочечных вен. УЗИ проводили на аппаратах «Aloka-SSD-1700». «Aloka-SSD-680» (Япония) с конвексными датчиками с частотой 3,5 МГц; КТ — на томографе «СТ МАХ», МРТ — на томографе «Signa Contur», обе фирмы «General Electric». Ангиографическое исследование осуществляли на аппарате «Angioskop D 33» фирмы «Siemens».
Статистический анализ проводился с помощью программы Microsoft Office Excel: вычисление средних величин; расчета интенсивных и экстенсивных показателей, динамика вариационных рядов; ранговой корреляции Пирсона.
3. Результаты и их обсуждение
Выполнено комплексное изучение анатомии клапанных структур, синтопии аорты, левой брыжеечной вены, синтопии левой почечной вены, а также изучение гемодинамики с использованием гидродинамических математических методик, позволивших доказать наличие предрасполагающих и производящих факторов в развитии целого ряда патологических состояний. Если с варикозным расширением вен таза, варикоцеле достаточно исследований, то процессы, происходящие в надпочечнике и почке, требуют дальнейшего изучения. Доказана целая группа различных заболеваний в левом надпочечнике, на порядок чаще, чем в правом. Исследование с использованием классических методик на трупном материале показал высокую частоту несостоятельности клапанов гонадной вены (55%), с развитием нисходящего рефлюкса, а также относительную несостоятельность диафрагмального клапана (23,3%), что является проявлением восходящего рефлюкса. Данный рефлюкс в 100% оказывает воздействие на левый надпочечник, где клапанные защиты на структуру отсутствуют. В 100% надпочечниковая вена сливается под острым углом с диафрагмальной и несостоятельность клапана диафрагмальной вены можно переформатировать на надпочечниковую вену. Открытым стоит вопрос в отношении левой почки. В настоящее время многочисленные работы, показывающие морфологию почек, указывают на больший размер левой почки, не отражая функциональной разницы. Есть все основания предположить, что такая разница есть и она носит существенное значение.
Несостоятельность клапанных структур — это следствие различных воздействий, где основная причина — это гипертензия в том или другом венозном бассейне. Наиболее распространенная патология — это варикозная болезнь, где несостоятельность клапанных структур объясняется прежде всего венозной гипертензией , .
В своих исследованиях на 100 трупах, показывая синтопию аорты, верхней брыжеечной по отношению к левой почечной вене с последующим изучением гидродинамики, как селективного воздействия, так и сочетанного, мы показали, с использованием математических методик, четкое влияние вышеперечисленных структур на левую почечную вену в плане развития венозной гипертензии.
В норме ЛПВ проходит от почки по направлению к позвоночнику почти горизонтально, пересекая аорту спереди и впадая в нижнюю полую вену (НПВ) на уровне первых двух поясничных позвонков. В ходе исследования было установлено, что длина левой почечной вены: 5,8 +/- 1,5 см. Диаметр левой почечной вены равен: 1,2 +/- 1,2 см. В норме пиковая систолическая скорость кровотока (ПССК) колеблется от 18 до 33 см/с, при отклонении наблюдается увеличение динамики ПССК. В левую почечную вену впадают: левая надпочечниковая вена сверху и левая яичковая (яичниковая) вена снизу.
Синтопия артериальных структур и бассейна ЛПВ не являются основной причиной венозной гипертензии. Только в ряде случаев можно с уверенностью говорить о значении синтопии в развитии венозной гипертензии.
Удвоение почечной вены. Мы наблюдали один клинический случай, где почечная вена была представлена двумя стволами — один диаметром 1 см, проходящий впереди аорты и второй меньшего диаметра 0,5 см, проходил позади аорты. Частота встречаемости в проводимом исследовании составила 1% (1 случай) (рис. 1).
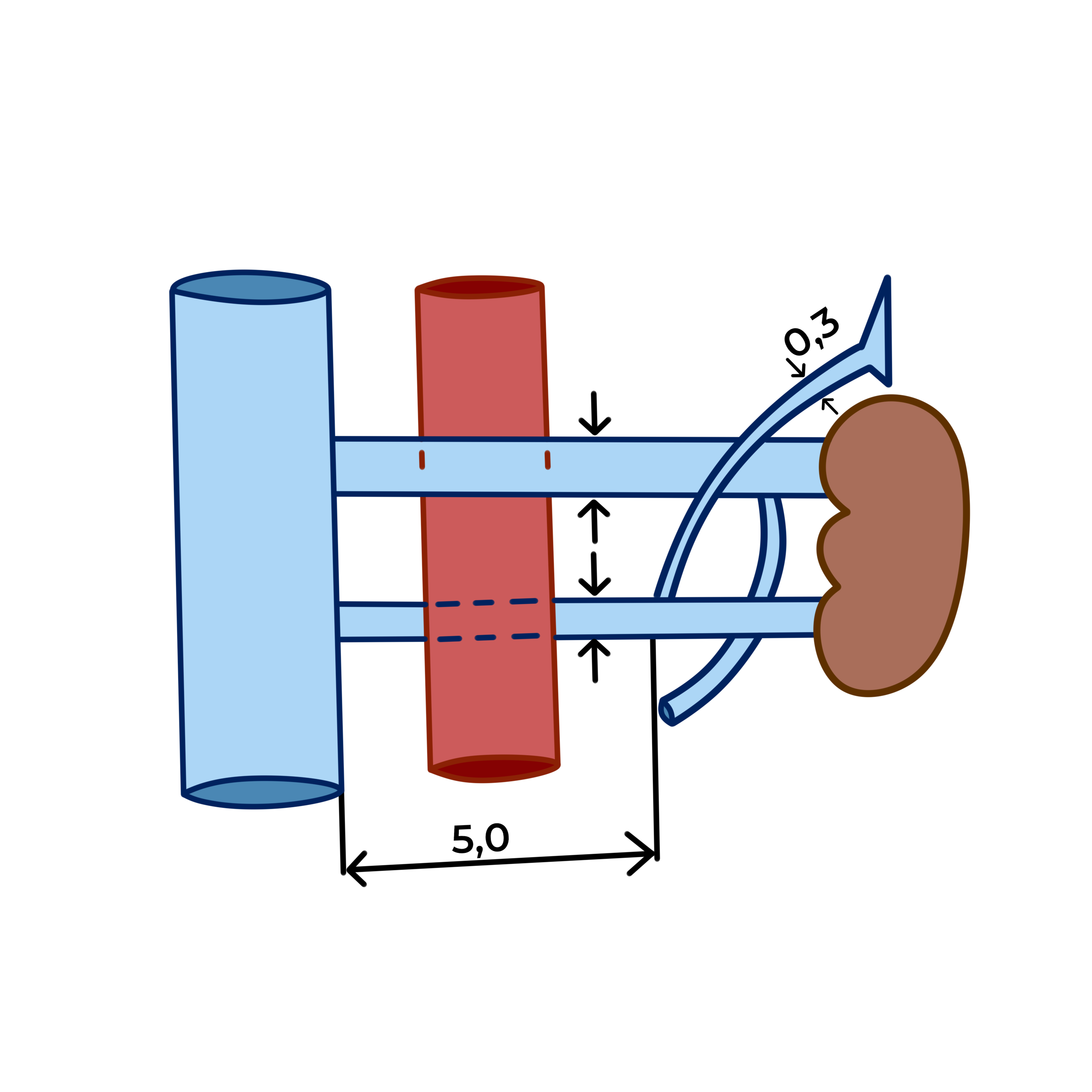
Рисунок 1 - Удвоение почечной вены
Проксимальное раздвоение почечной вены — при этом виде аномалии левая почечная вена выходит из ворот почки одним стволом, а затем разделяется на 2 ствола. Верхний ствол проходит типично, впереди аорты, и впадает в НПВ на уровне второго поясничного позвонка . Второй ствол проходит косо вниз позади аорты и впадает в полую вену на уровне третьего поясничного позвонка (рис.2).
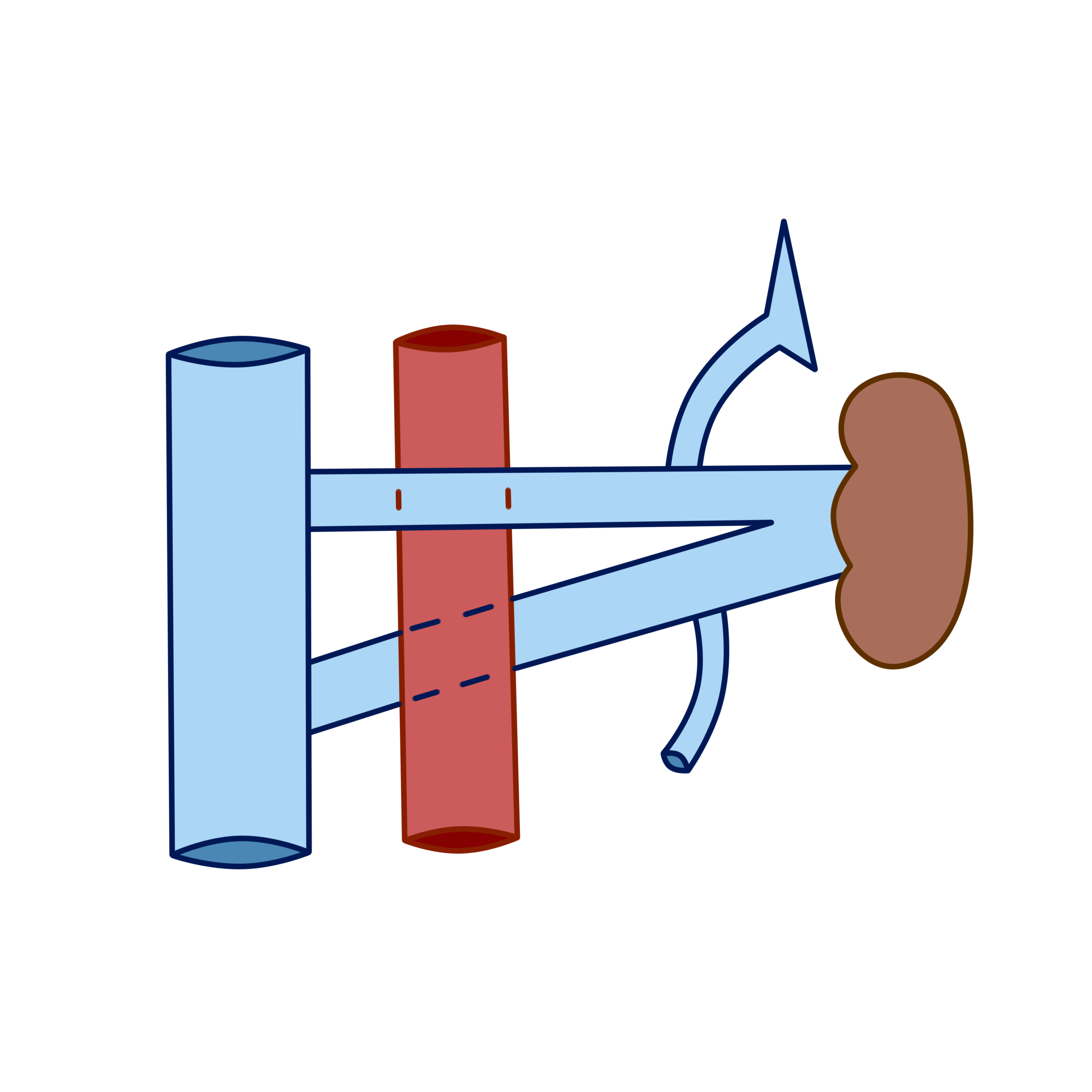
Рисунок 2 - Проксимальное раздвоение почечной вены
В данном варианте, аорта оказывает давление на нижний ствол левой почечной вены, который проходит позади аорты, давление в этом сосуде повышено, возникает венозная гипертензия и нарушение венозного оттока от почки.
В норме ЛПВ выходит из почки горизонтально, пересекая аорту спереди и впадая в НПВ на уровне первых двух поясничных позвонков (рис.3).
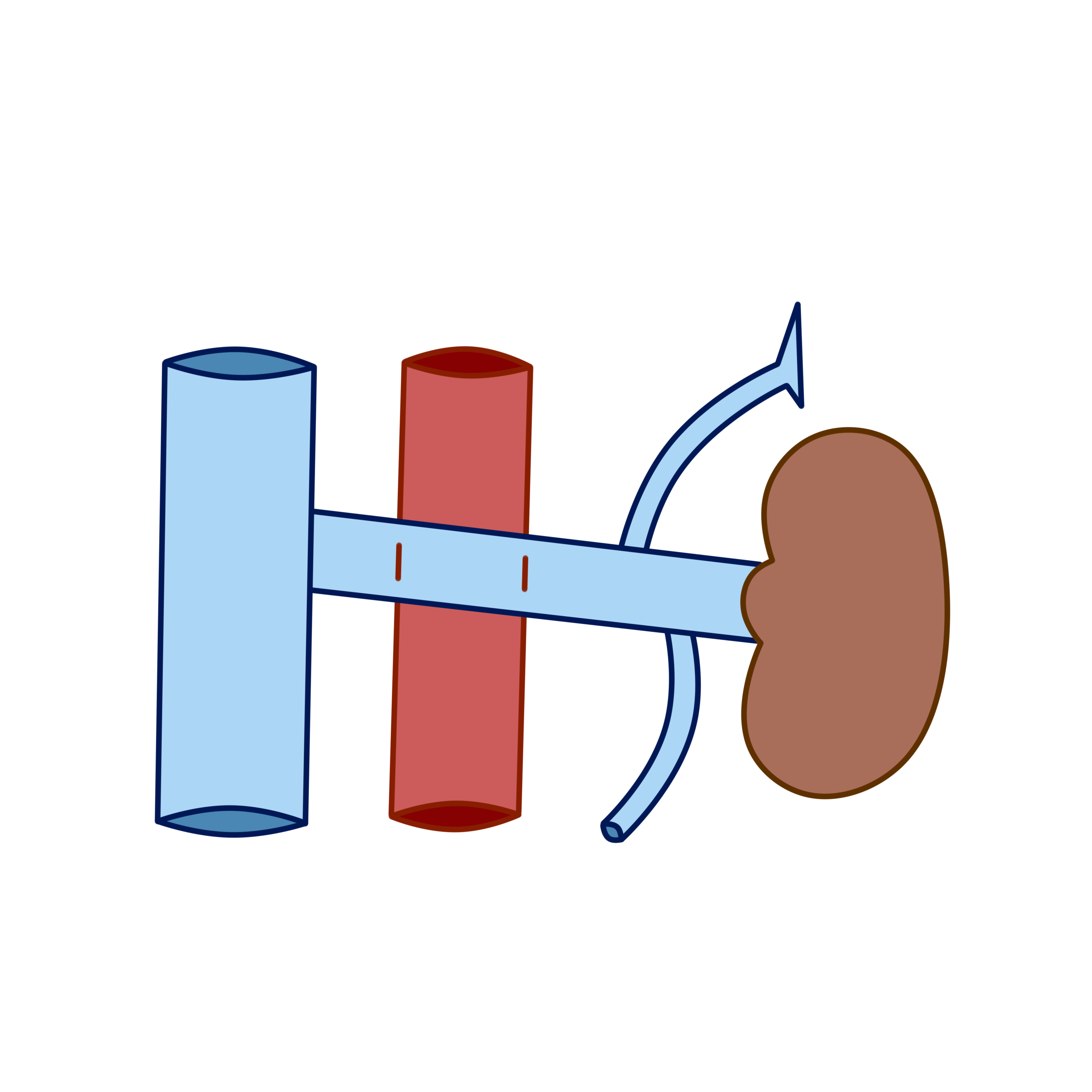
Рисунок 3 - Нормальное расположение почечной вены по отношению к аорте
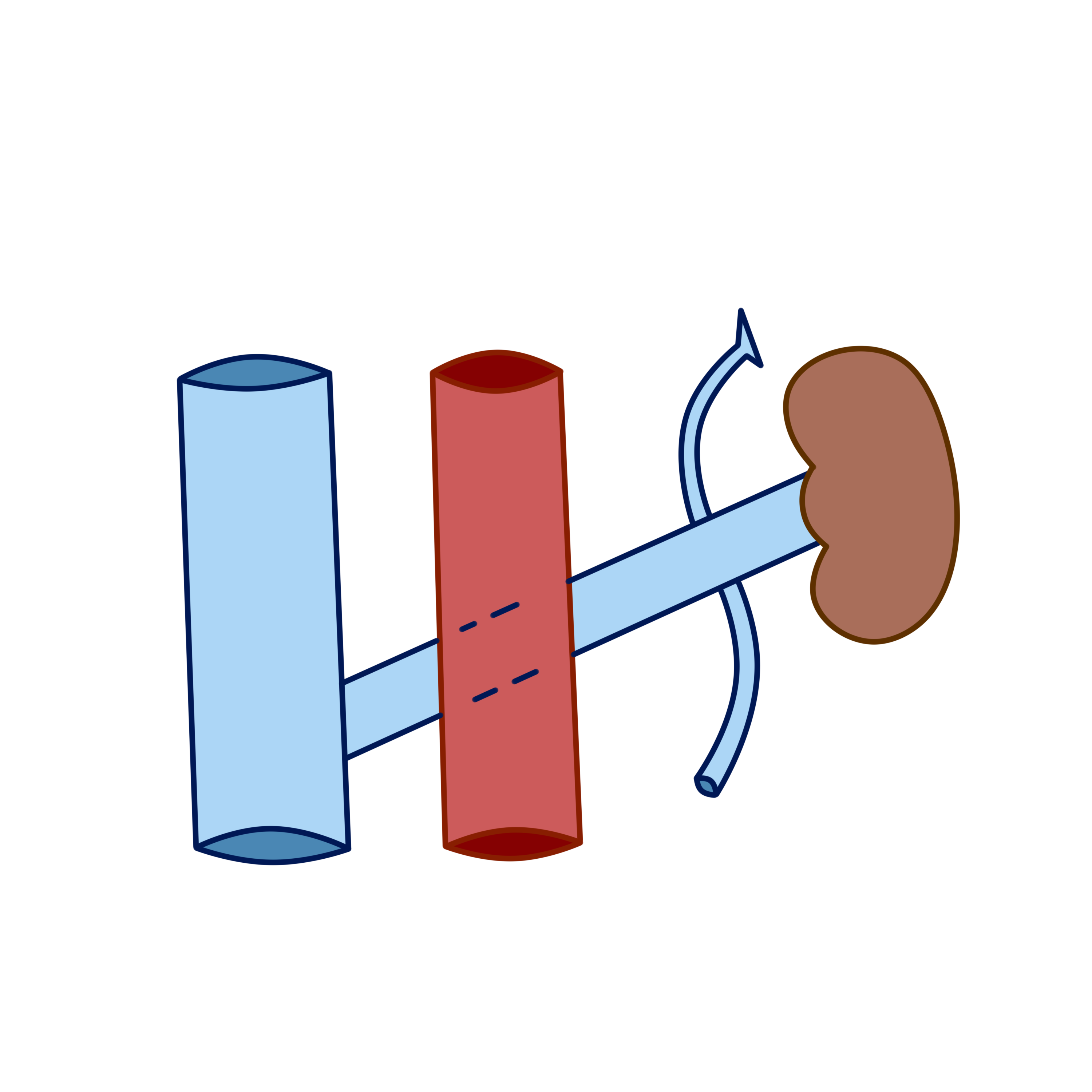
Рисунок 4 - Патологическое расположение почечной вены по отношению к аорте
Как говорилось ранее, в норме ЛПВ выходит из почки горизонтально, пересекает аорту спереди и впадая в НПВ на уровне первых двух поясничных позвонков. При данном варианте площадь наложения ЛПВ на аорту принимаем за единицу (S наложения = 1 см2).
Левая почечная вена может направляться от почки горизонтально или иметь косое направление и впадает в НПВ. В таком случае площадь наложения ЛПВ относительно больше, чем при горизонтальном направлении (площадь наложения ЛПВ на аорту составляет приблизительно 1,3 см2). При большей площади наложения ЛПВ на аорту — большее давление оказывает аорта на ЛПВ.
Также были зафиксированы иные варианты расположения:
1) Высокое расположение вены. В таком варианте ЛПВ проходит на уровне двенадцатого грудного позвонка. Данная позиция была обнаружена в 4% случаев (4 случая). В связи с особенностями направления левой почечной вены мы видим, что площадь наложения левой почечной вены на аорту относительно больше, чем при горизонтальном направлении (площадь наложения составляет приблизительно 1,3 см2) (рис.5).

Рисунок 5 - Высокое расположение левой почечной вены
2) Низкое расположение вены. При данном варианте ЛПВ проходит на уровне третьего поясничного позвонка. По встречаемости такая позиция составила 1% (1 случай). Аналогичная ситуация, что и при высоком расположении левой почечной вены (увеличение площади наложения левой почечной вены на аорту) (рис.6).
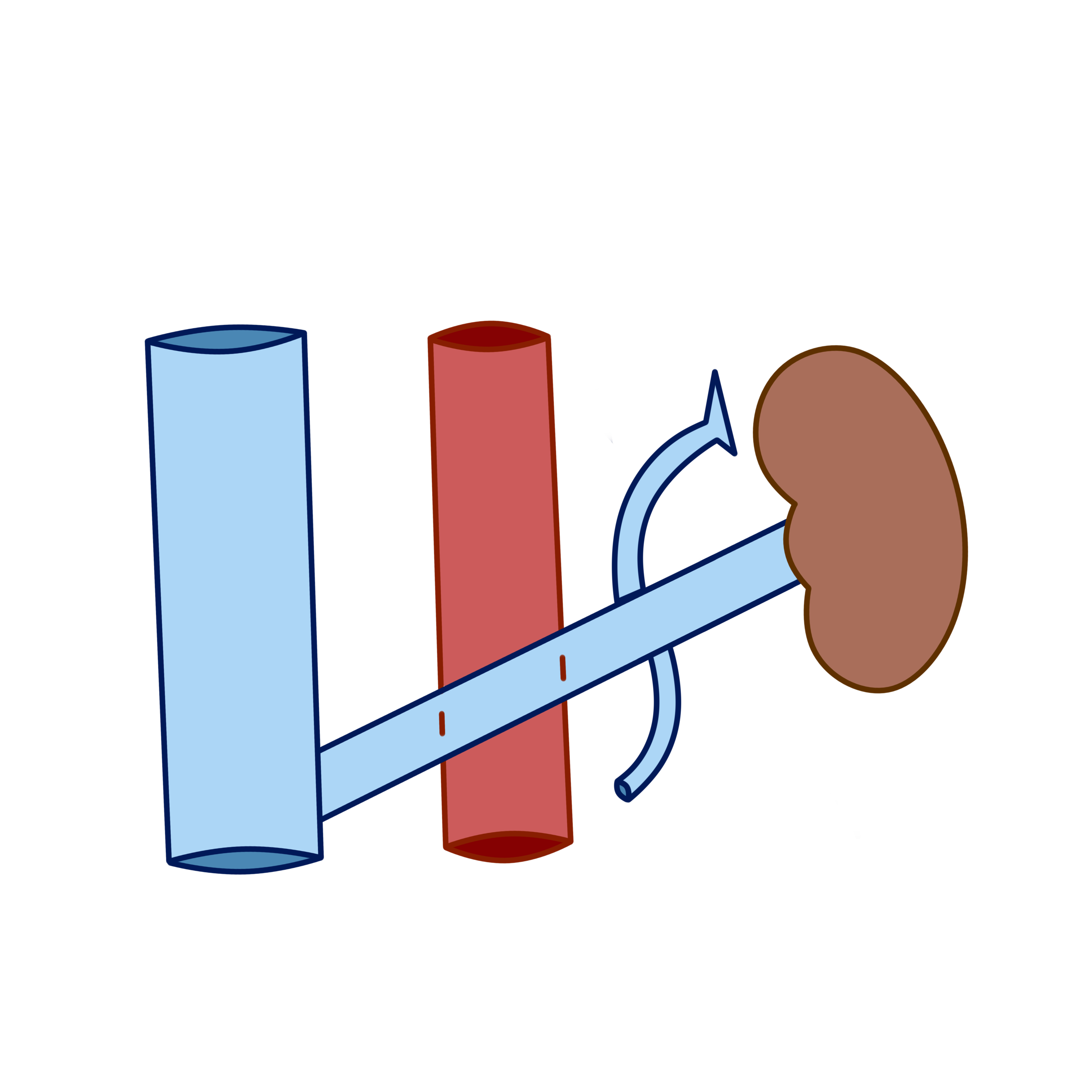
Рисунок 6 - Низкое расположение почечной вены
Меньшее влияние на ЛПВ оказывает давление верхней брыжеечной артерии.
Синдром Щелкунчика — доброкачественное заболевание почек, в основе которого лежит сдавливание ЛПВ между брюшной аортой и ВБА, вследствие чего повышается давление в системе ЛПВ. С учетом клинических данных, частота встречаемости данного патологического состояния состовляет 0,5% (рис. 7).
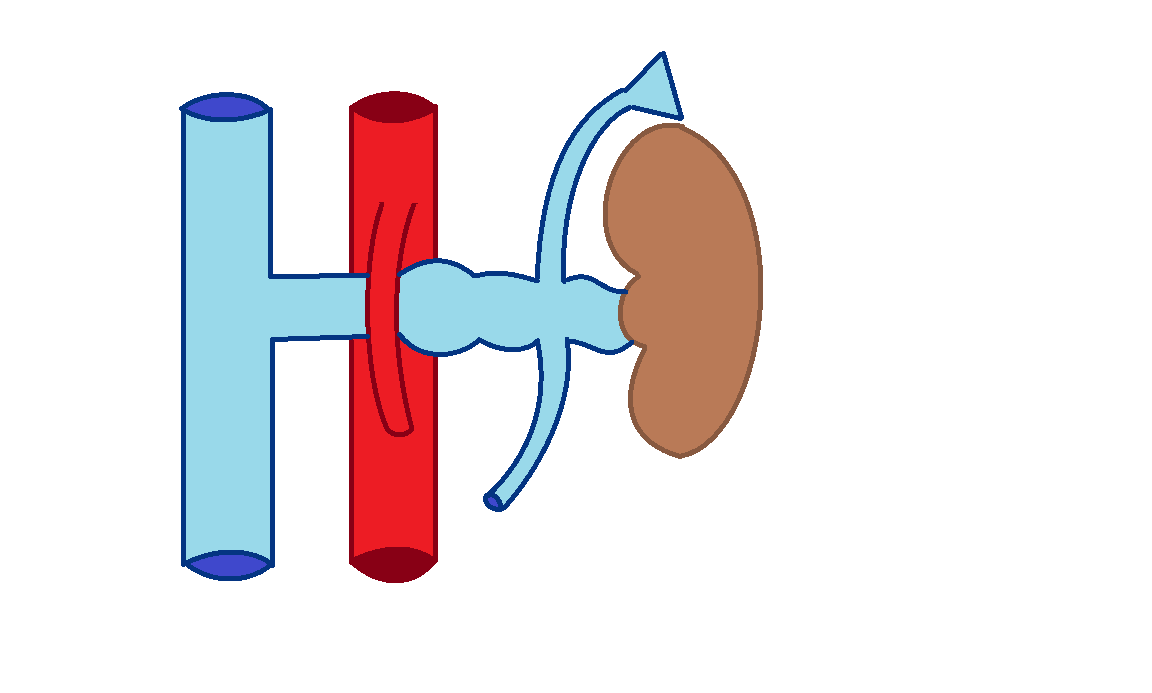
Рисунок 7 - Синдром Щелкунчика
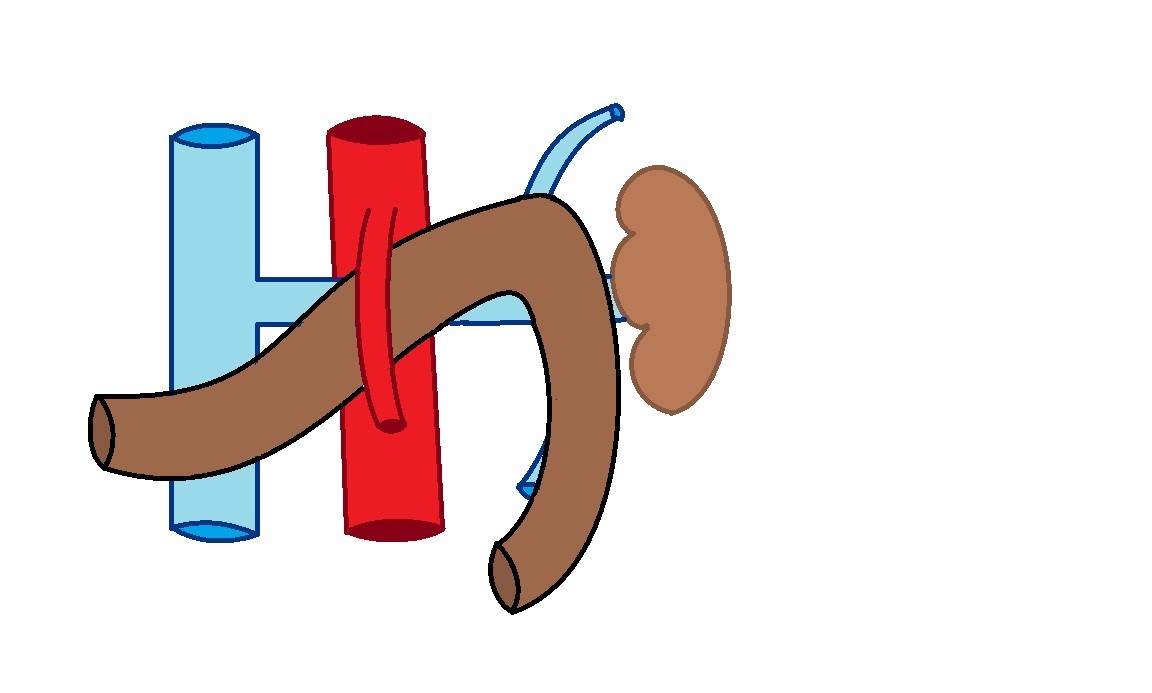
Рисунок 8 - Синдром верхней брыжеечной артерии
Только 10% (6 случаев) наблюдений объясняют венную гипертензию синтопией ЛПВ с артериальными структурами. Как же объяснить остальные 50% (30 случаев). Изучение пульсионного воздействия аорты, ВБА, а также их суммарное воздействие на ЛПВ с использованием математических методов показало их четкое воздействие на венозную гипертензию.
Несмотря на невысокие цифры пульсионного воздействия 1,15 Па и 0,6 Па, данное воздействие продолжается в течение многих десятилетий. Это воздействие в совокупности с другими факторами синтопии с артериальными структурами, приводит к венной гипертензии, как в венозных стволах, так и во внутриорганных, приводящих к гипоксии и выбросу вазоактивных субстанций в системный кровоток в большем объеме. Таким образом, избыточная продукция гормонов надпочечника и левой почки создают в бассейне ЛПВ «резервуар» вазопрессорных субстанций.
В итоге имеет место развитие гипертензии различного генеза. В надпочечнике формируется первичная катехотаминовая гипертензия. Ишемия ЮГА запускает механизм РААС.
Ретроспективный анализ у 59 больных с первичной катехоламиновой артериальной гипертонией показал, что только у 3 больных (5,1%) на амбулаторном этапе при сочетанном поражении было выявлено подозрение на поражение надпочечников. На УЗИ была выявлена киста почки у 2-х больных и у одного однокамерный эхинококк. Клинически это проявлялась повышенным артериальным давлением с периодическими симпатоадреналовыми кризами. Диагноз у остальных больных ставился в условиях стационаров различного профиля. Следует отметить высокую частоту данного заболевания. Группа больных с первичной катехоламиновой артериальной гипертонией составила 25,3% и по частоте встречаемости уступает только больным с реноваскулярной артериальной гипертензией. У женщин данная патология встречается в два раза чаще, чем у мужчин. Заболевание клинически развивается преимущественно в трудоспособном возрасте 39–55 лет. Длительность заболевания составляет от 1 до 10 лет. Больные получали постоянное лечение в поликлиниках и стационарах по поводу гипертонической болезни, вегетососудистой гипертонии и различных психических заболеваний. Отдельные больные получали лечение у психиатра. Следует отметить прогрессирующий характер заболевания у всех больных. По течению артериальной гипертензии у 19 больных (32,2%) на фоне повышенного давления от 140/90 и выше отмечались симпатоадреналовые кризы. В зависимости от уровня артериального давления мы выделили три формы заболевания:
1. Тяжелая — АД выше 200/120 (феохромоцитома).
2. Средняя — АД от 160/100 до 200/120.
3. Легкая — АД от 160/100 и ниже.
Мы не брали в анализ больных с феохромацитомами. 50 больных (84,8%) относились к средней форме заболевания и 9 больных (15,25%) относились к легкой форме. Нам пришлось отказаться от больных контрольной группы (10 человек), их пришлось оперировать, в связи с неэффективностью консервативной терапии и прогрессированием заболевания , . Клинические проявления заболевания, связанные с гиперфункцией мозгового слоя надпочечника, обусловлены самыми различными этиологическими причинами. Наиболее яркие проявления во время кризов. Основные клинические проявления по мере их частоты: повышение АД, сердцебиение, онемение, судороги рук и ног, дрожание тела, озноб, чувство жара, учащенный диурез до приступа, во время и чаще после приступа. Общие проявления: боли в голове, слабость, недомогание, потливость, лихорадка. Клинические проявления очень разнообразны. При изучении анамнеза почти у всех удается выявить психоэмоциональные или физические факторы, провоцирующие начало приступов. Из поступивших больных — 7 человек (11,9%) перенесли нарушение мозгового кровообращения, без выраженного неврологического дефицита, 2 больных (3,4%) перенсли инфаркт миокарда, у всех больных были изменения на глазном дне в виде ангиопатии, ангиоретинопатии, нейроретинопатии. Все больные отмечали снижение качества жизни, 3 (5,1%) из них были инвалидами 3 группы.
Уточнение диагноза, первичная катехоламиновая артериальная гипертония, имеет определенные трудности в связи с относительным характером информации, которые дают дополнительные методы исследования. Определение уровня катехоламинов показало верхнюю границу нормы или ее незначительное увеличение , . Аналогичные результаты дало изучение уровня экскреции с мочой ванинилминдальной кислоты. Пневмоперитонеум и радиоизотопные методы в настоящее время представляют исторический интерес. Аортография для выявления ПКГ малоинформативна, но мы ее применяем всегда с целью дифференциальной диагностики. Результаты УЗИ хороши для диагностики кист. Широкое внедрение КТГ, МЯР позволило значительно улучшить диагностику, однако выявление гиперплазии мозгового слоя, небольших менее 1 см или плоскостных гематом, кист, по-прежнему проблематично. Опыт применения у больных с первичной катехоламиновой артериальной гипертонии показал низкую информативность данных методик. Между тем, выявление более плотных структур, феохромоцитомы, альдостеромы, кортикостеромы, рака надпочечника и т.д. достаточно надежно. Последние годы для диагностики поражения надпочечников мы широко используем селективную венографию. Метод позволяет подтвердить диагноз феохромацитомы, первичного альдостеронизма, предположить поражение мозгового и корковых слоев надпочечников , . Однако имеются существенные проблемы с катетеризацией правой надпочечниковой вены. У 3 (5,1%) больных мы получили ложную информацию из-за разрыва вен мозгового слоев надпочечников. У 2 (3,4%) больных венография осложнилась разрывом надпочечника. Наблюдение за больными в течении года показало регресс клинических проявлений. За больными ведется дальнейшее наблюдение. Результаты последнего определят место данного способа в лечении первичной катехоламиновой артериальной гипертонии. На основании клиники и данных дополнительных методов исследования удается с достаточно высокой степенью достоверности поставить диагноз. Однако, иногда только данные интраоперационной диагностики позволяют уточнить диагноз. Учитывая прогрессирующий характер заболевания, трудность выбора и ограниченную эффективность консервативного лечения, мы придерживаемся активной тактики в лечении первичной катехоламиновой артериальной гипертонии. Противопоказанием являются мозговые инсульты и инфаркты миокарда, перенесенные в ближайшие 3–4 месяца, сопутствующие инкурабенные заболевания, активные воспалительные процессы, сердечная декомпенсация.
Глубокое расположение надпочечников, сложная синтопия с окружающими органами и тканями затрудняет ревизию, и оперативные вмешательства на надпочечниках. При известной локализации мы используем боковой поддиафрагмальный доступ в Х межреберье от средне-подмышечной линии до наружного края прямой мышцы. При появлении технических трудностей можно легко перейти на торакофренолюмботомию, продолжив доступ вверх. В настоящее время широко используется эндоскопические методики (табл.1).
Таблица 1 - Характер выполненных операций на надпочечниках при первичной катехоламиновой артериальной гипертензии
№ | Вид операции | Кол-во больных | ||
n | % | |||
1 | Односторонняя адреналэктомия | Справа | 4 | 6,6 |
Слева | 52 | 85,2 | ||
2 | Эндоваскулярная окклюзия внутриорганной венозной системы 3% этоксисклеролом | 3 | 4,9 | |
3 | Эндоваскулярный разрыв надпочечника (вынужденный) | 2 | 3,3 | |
Всего: | 61 | 100 | ||
В результате ретроспективного анализа 56 случаев удаленных надпочечников условно было выделено пять групп поражений:
1) сочетание поражения надпочечников с другими поражениями — 8,9%;
2) осумковатая гематома, склерозы — 5,4%;
3) сочетание поражений коркового и мозгового слоя — 39,3%;
4) локальное поражение мозгового слоя — 37,5%;
5) мозговой слой не изменен — 8,9%, корковый аденоматозный изменен.
При исследовании каждой группы, были рассмотрены все случаи и дано патогистологическое заключение.
В первую группу поражений надпочечников входят 5 (8,9%) случаев от общего количества исследуемых:
1) киста правой почки с очагами хронического воспаления, гипертрофия мозгового слоя надпочечников — 1 (правый надпочечник);
2) однокамерный эхинококк в стадии заживления и организации и склероз — 1 (правый надпочечник);
3) киста левой почки, ткань селезенки с выраженным фиброзом по периферии — 1 (левый надпочечник) ;
4) гипертрофия мозгового слоя почек с отдельно располагающимися кусочками надпочечника с мелкозернистой розовой цитоплазмой — 1 (левый надпочечник);
5) нейробластома левого надпоченика — 1 (левый надпочечник).
Во вторую группу поражений надпочечников входят 3 (5,4%) случая от общего количества исследуемых:
1) геморрагический некроз надпочечника, с исходом в полость — 2 (левые надпочечники);
2) осумковатая гематома со склерозом и очаговым кальцинозом стенки — 1 (левый надпочечник).
В третью группу поражений надпочечников входят 22 (39,3%) случая от общего количества исследуемых:
1) очаговая гиперплазия коркового слоя; кровоизлияние по типу гематомы в мозговом слое — 14 (правые надпочечники);
2) в корковом слое светлые клетки с прозрачной цитоплазмой; в мозговом слое сосуды с утолщенными стенками, очаговые кровоизлияния — 3 (правые надпочечники);
3) в пучковой и сетчатой зонах коркового слоя и в мозговом слое множественные инфильтраты из клеток лимфоидного типа — 1 (левый надпочечник);
4) в мозговом слое надпочечников гематомы; в корковом слое дистрофия клеток — 4 (левые надпочечники).
В четвертую группу поражений надпочечников входит 21 (37,5%) случай от общего количества исследуемых:
1) кровоизлияние в мозговой слой по типу гематомы — 6 (левые надпочечники);
2) гиперплазия мозгового слоя надпочечников — 5 (левые надпочечники);
3) гиперплазия мозгового слоя; мозговой слой значительно расширен с пролиферацией клеток с наличием митозов — 7 (левые надпочечники);
4) мозговой слой местами расширен с мелкоочаговыми кровоизлияниями — 3 (левые надпочечники).
В пятую группу поражений надпочечников входят 5 (8,9%) случаев от общего количества исследуемых:
1) очаговая гиперплазия коры правого надпочечника — 1 (правый надпочечник);
2) ткань надпочечника с сохраненным делением клеточных слоев — 2 (левые надпочечники);
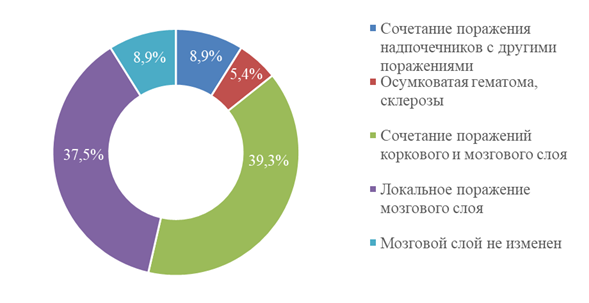
Рисунок 9 - Результаты патогистологических исследований удаленных надпочечников
1) первичная (на первом плане поражения различного характера мозгового слоя и в сочетании с поражением коры, 43 (72,9%) больных);
2) вторичная (надпочечник поражен вследствие сдавления кистой или другими структурами, 5 (8,5%) больных);
3) в сочетании с гипертонической болезнью, 11 (18,6%) больных;
В 12 (20,3%) случаях наблюдений отмечено течение заболевания на фоне стабильно повышенного давления. При удалении надпочечника клиника менялась . Уходили симпатоадреналовые кризы, но повышенное АД сохранялось, приобретало более мягкое течение и лучше поддавалось медикаментозной терапии. Симпатоадреналовые кризы не возобновлялись.
Анализ результатов хирургического лечения первичной катехоламиновой гипертонии, показал высокую эффективность оперативных методов лечения, хорошие удовлетворительные результаты у 55 больных (96,6%). Летальных исходов не было. Только у 1 (1,7%) больного отмечена надпочечниковая недостаточность легкой степени, купировшаяся через 6 месяцев.
4. Заключение
1. Системный подход к этиологии, патогенезу патологических процессов бассейна ЛПВ позволил доказать группу причин, вызывающих повышенное давление бассейна ЛПВ (синтопия почечной вены и артериальных структур, а также гидродинамическое воздействие аорты и ВБА).
2. Повышенное давление бассейна ЛПВ приводит в 61% к недостаточности клапанных структур и развитию варикозного расширения вен таза и варикоцеле.
3. Отсутствие клапанов в надпочечной вене и почке приводит к прямому воздействию на ткани данных органов, вызывая гипоксию и развитие их гиперфункции.
4. В результате венной гипертензии бассейна левого надпочечника развивается первичная катехоламиновая гипертония.
5. В результате венной гипертензии и гипоксии развивается повышенный выброс ренина и включение РААС в патогенезе артериальной гипертензии.
