ПАТОГЕНЕТИЧЕСКАЯ РОЛЬ ПРО- И АНТИОКСИДАНТНОЙ СИСТЕМ КРОВИ В МЕХАНИЗМАХ РАЗВИТИЯ ВОСПАЛИТЕЛЬНОЙ ПАТОЛОГИИ ТКАНЕЙ ПОЛОСТИ РТА У ПАЦИЕНТОВ
ПАТОГЕНЕТИЧЕСКАЯ РОЛЬ ПРО- И АНТИОКСИДАНТНОЙ СИСТЕМ КРОВИ В МЕХАНИЗМАХ РАЗВИТИЯ ВОСПАЛИТЕЛЬНОЙ ПАТОЛОГИИ ТКАНЕЙ ПОЛОСТИ РТА У ПАЦИЕНТОВ
Аннотация
В последние годы в литературе представлены данные об участии активных форм кислорода (АФК) и процесса перекисного окисления липидов (ПОЛ) в аспекте их патогенетической роли в развитии ряда воспалительных заболеваний тканей полости рта, несмотря на их участие в СРО при физиологических условиях. Изучение механизмов развития процесса перекисного окисления липидов и активности антиокислительной системы в крови и их участие в генезе воспалительной патологии тканей пародонта в клинике у больных. В исследование включено 25 пациентов, разделённых на две группы: контрольная (здоровые субъекты, n=10) и больные с воспалительной патологией тканей полости рта (n=15). Проведен пародонтологический, клинический, рентгенологический анализ показателей тканей полости рта и биохимические исследования крови. Выявлено повышение уровней индексов OHI-s, PMA и SBI, свидетельствующих о наличии воспалительного процесса. Отмечено повышение содержания малонового диальдегида (МДА) и снижение активности супероксиддисмутазы (СОД) в эритроцитах, что указывает на развитие окислительного стресса. Выявлено снижение уровня NOx и повышение содержания общего холестерина (ХС) и ХС ЛПНП в плазме крови, являющиеся маркерами дисфункции эндотелия сосудов. Активация оксидативных процессов на системном уровне может рассматриваться как компонент ответа острой фазы развития воспалительного процесса в тканях полости рта.
1. Введение
На современном этапе развития медико-стоматологической науки воспалительные заболевания пародонта являются одной из актуальных проблем, обусловленной их распространенностью, а также неблагоприятным влиянием на состояние организма. В многочисленных исследованиях установлено сочетание различных соматических заболеваний с существенными функциональными и морфологическими изменениями в зубочелюстной системе. Представителем патологии тканей полости рта является пародонтит — иммунноопосредованный воспалительный процесс, приводящий к утрате прикрепления периодонта к поверхности корня зуба и разрушению прилежащей альвеолярной кости. Рассматривая патогенетические механизмы, определяется важная роль взаимосвязи между патологическим изменением тканей пародонта и системными заболеваниями: сердечно-сосудистой патологией и сахарным диабетом , , . Сочетание соматических патологических процессов с пародонтитом может быть обусловлено нарушением микробиоценоза, изменениями метаболизма, гемодинамики, иммунологическими и нейрорегуляторными расстройствами.
В последние годы, данные литературы представляют информацию об участии активных форм кислорода (АФК) и процесса перекисного окисления липидов (ПОЛ) в аспекте их патогенетической роли в развитии и прогрессировании воспалительных заболеваний тканей полости рта . Вместе с тем следует отметить участие свободно-радикального окисления в нормальном клеточном метаболизме. В условиях эндогенной интоксикации, вызванной нарушением микробиоциноза, происходит повышенная выработка АФК клетками врожденной иммунной системы — нейтрофилами и макрофагами в процессе фагоцитоза как «дыхательный взрыв». В развитии окислительного стресса наряду с АФК участвует недостаточная активность ферментов антиоксидантной системы (АОС). Таким образом, отсутствие сбалансированности между про- и антиоксидантной системами является условием для повреждения клеток тканей, молекул ДНК, белков и метаболически важных ферментов . За последние годы многочисленные кинические и фундаментальные экспериментальные исследования свидетельствуют о взаимосвязи окислительного стресса и с патологией тканей полости рта , , , . Изучение механизмов развития ПОЛ при пародонтите у больных позволит установить его патогенетическую роль в развитии воспалительного процесса.
Целью данного исследования является изучение механизмов развития процесса перекисного окисления липидов и активности антиокислительной системы в крови как патогенетического звена, воспалительной патологии тканей пародонта у больных.
2. Методы и принципы исследования
Отбор больных с воспалительной патологией тканей полости рта производили в условиях стоматологической поликлиники АО «Стоматология», а все биохимические и функциональные исследования проводили на базе лаборатории патобиохимии ИБМИ ВНЦ РАН в соответствии с договором и планом НИР. В исследование включено 25 пациентов в возрасте от 22 до 65 лет и длительностью заболевания от 1 до 5 лет, которые были разделены на две группы: 1-ая группа — контрольная — исследуемые здоровые субъекты, без отсутствия манифестации других патологий (n=10). 2-ая группа — больные с воспалением тканей пародонта (n=15). Участники всех обследуемых групп прошли пародонтологический анализ показателей клинических и биохимических исследований. Обследование тканей полости рта включало измерение глубины пародонтального кармана с использованием зонда UNC-PCP15 (Hu Friedy) в шести местах (мезиобуккальном, средне-буккальном, дистобуккальном, мезиолингвальном, среднеязычном и дистолингвальном) для каждого зуба, исключая третьи коренные зубы. Данные измерения были выражены в миллиметрах и рассчитаны средние значения данных на исследуемых участках пародонта у каждого пациента. Состояние тканей пародонта также оценивали по следующим показателям: упрощенный индекс гигиены — OHI-s, РМА — папиллярно-маргинально-альвеолярный индекс, SBI — индекс кровоточивости. Рентгенологическая оценка для определения степени резорбции костной массы зубо-челюстной системы проводилась с использованием прикусных и периапикальных рентгенограмм, а также панорамных снимков. Биохимические исследования в крови включали: определение интенсивности ПОЛ по данным концентрации малонового диальдегида (МДА) в гемолизате эритроцитов по реакции с тиобарбитуровой кислотой ; активности ферментов антиокислительной системы (АОС): каталазы ; СОД , концентрации церулоплазмина (ЦП) методом Равина и суммарных метаболитов оксида азота – NOx в плазме крови модифицированным методом Метельской В.А. .
Принимая во внимание участие нарушенного обмена холестерина в снижении биодоступности L-аргинина к ферменту эндотелиальной NO-синтазе (eNOS), а также возрастной аспект больных, определяли показатели обмена холестерина общепринятыми методиками: содержание общего холестерина, холестерина липопротеинов низкой плотности, (ХС ЛПНП), холестерина липопротеинов высокой плотности (ХС ЛПВП). Проводили сравнительный анализ данных у больных с пародонтитом с результатами контрольной группы. Исследование проводили в соответствии с Надлежащей клинической практикой и принципами Хельсинкской декларации 1975 г. и ее пересмотренному варианту 2000 г. и этическими стандартами Этического комитета ИБМИ ВНЦ РАН (протокол № 6 от 26.12.2018 г.). Все больные подписали добровольное информированное согласие до включения в исследование.
С помощью программы MicrosoftExcel проводили статистическую обработку полученных данных и представили в виде среднего значения (Mean) и среднеквадратичной ошибки (SξM). Принимая во внимание равномерность распределения данных, достоверность различий определяли по t-критерию Стьюдента и считали различия достоверными при p<0,05.
3. Основные результаты
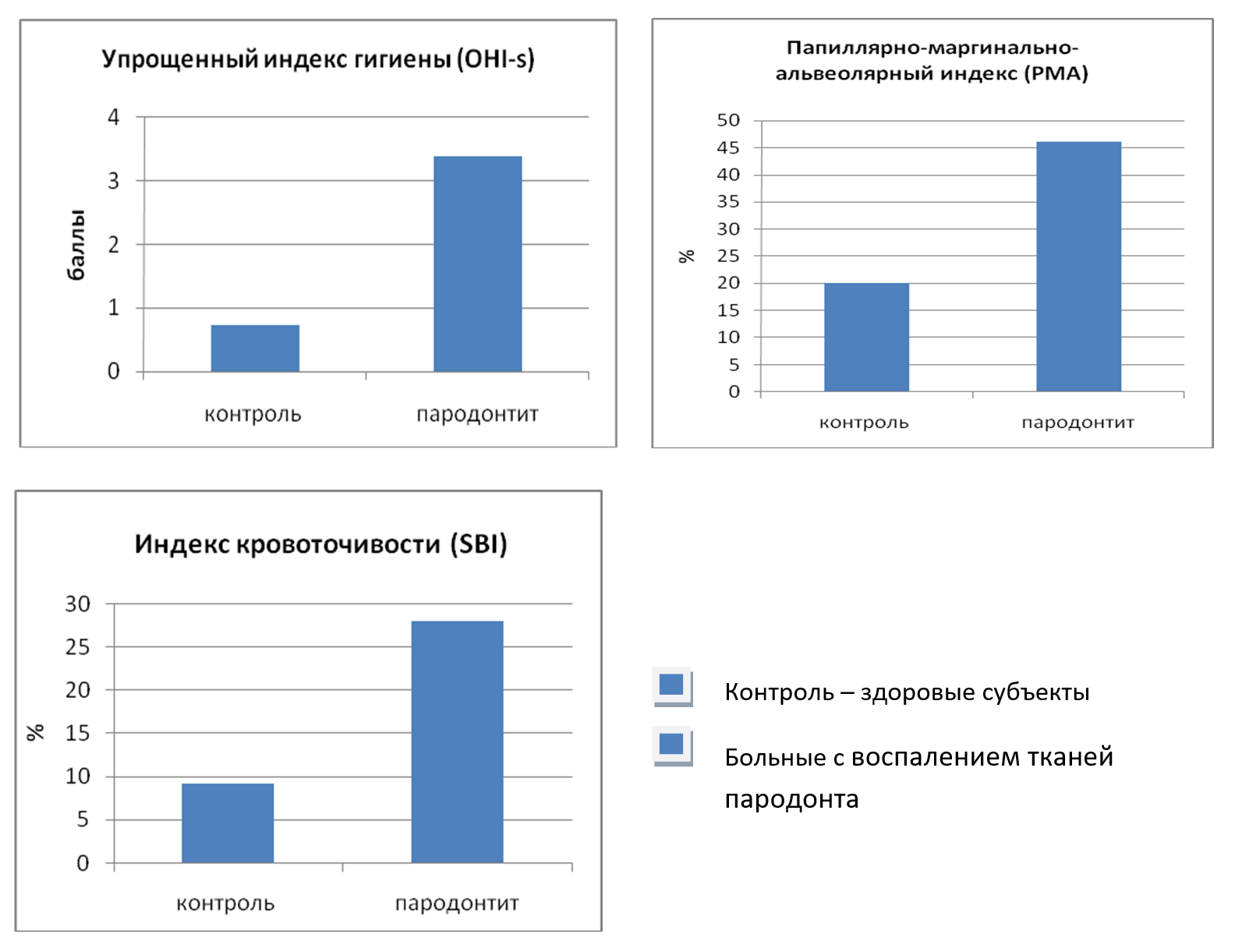
Рисунок 1 - Динамика индексных показателей, характеризующих состояние тканей пародонта, у больных с пародонтитом
Примечание: M±m
Таблица 1 - Данные показателей окислительно-восстановительных процессов, обмена оксида азота и холестерина у больных с воспалительной патологией тканей пародонта
Показатели | Контроль – здоровые субъекты | Пациенты с пародонтитом |
МДА нмоль/мл. | 18,45±0,245 | 28,7±0,561111) |
СОД усл.ед. | 69,24±0,38 | 35,5±0,951111) |
Каталаза мкат/л. | 235,8±2,63 | 381,34±14,71111) |
ЦП мг/дл | 330,1±15,6 | 498,2±2,861111) |
NOxммоль | 69,15±0,4165 | 39,12±0,431111) |
ОХС ммоль/л | 4,9±0,23 | 5,62±0,181111) |
ХС ЛПНП ммоль/л | 2,98±0,281 | 3,99±0,261111) |
ХС ЛПВП ммоль/л | 1,36±0,058 | 0,98±0,611111) |
Примечание: M±m; МДА – малоновый диальдегид; СОД – супероксиддисмутаза, ЦП – церулоплазмин; NOx – суммарные метаболиты оксида азота; ОХС – общий холестерин; ХС ЛПНП - липопротеины низкой плотности; ХС ЛПВП – липопротеины высокой плотности; 1111) p<0,001 достоверность данных показателей при пародонтите по сравнению с уровнем контроля
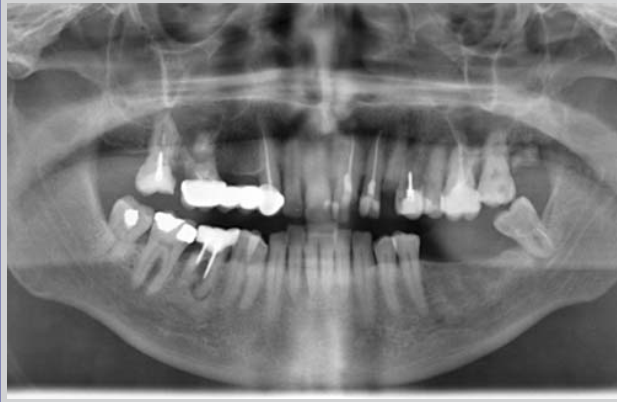
Рисунок 2 - Рентгенограмма, характеризующая у больных воспалительный процесс в тканях пародонта
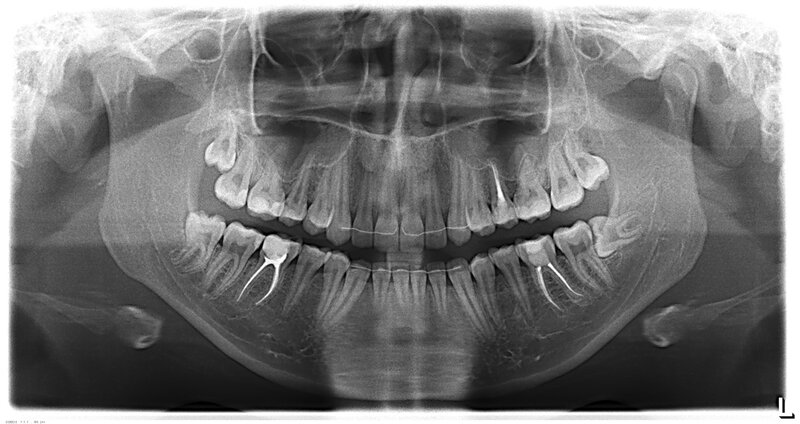
Рисунок 3 - Рентгенография зубо-челюстной системы пациента без отклонений от нормы
4. Заключение
Анализ полученных данных у пациентов с воспалительной патологией тканей полости рта показал наличие существенных изменений в измеряемых и расчетных характеристиках состояния тканей полости рта по сравнению с контролем. Результаты повышения уровней индексов OHI-s и SBI свидетельствуют о наличии активного воспалительного процесса в тканях полости рта. Присутствие атерогенных липопротеидов низкой плотности (ХС ЛПНП), изменяющих молекулярную структуру эндотелия сосудистой стенки, способствует расстройствам микроциркуляции, что приводит к нарушению транспорта кислорода и соответственно к циркуляторной и тканевой гипоксии. Образующиеся активные формы кислорода (АФК) индуцируют активацию процесса ПОЛ и развитие оксидативного стресса, что является патогенетическим звеном развития воспалительного процесса. АФК изменяют молекулярную структуру эндотелиальной NO-синтазы (eNOS) и продукцию NOx, являющиеся маркером эндотелиальной дисфункции сосудов и микроциркуляторных гемодинамических нарушений в тканях полости рта . Более того, активация фосфолипазной системы в условиях окислительного стресса, способствует образованию медиаторов воспаления, что подтверждается данными литературы , , . Проведенный анализ показателей окислительного стресса и индексной оценки воспалительного процесса в тканях полости рта позволил утверждать, что нарушение системных окислительно-восстановительных процессов, недостаток NOx, повышение уровня атерогенных липопротеинов, и возможное образование медиаторов воспалительного процесса, явились патогенетическими звеньями развития воспалительного процесса у пациентов.
