АНАЛИЗ ПРОЦЕССА СТЕРИЛИЗАЦИИ ОБОРУДОВАНИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ В АСЕПТИЧЕСКОМ ПРОИЗВОДСТВЕ
АНАЛИЗ ПРОЦЕССА СТЕРИЛИЗАЦИИ ОБОРУДОВАНИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ В АСЕПТИЧЕСКОМ ПРОИЗВОДСТВЕ
Обзор
Словеснов Н.А.1, *, Мирсаитов С.Ф.2, Светличный В.В.3, Словеснов Е.А.4
1 ORCID: 0000-0003-4624-1937;
1, 2 Федеральное государственное бюджетное образовательное учреждение высшего образования "МИРЭА - Российский технологический университет", ФГБОУ ВПО РТУ МИРЭА, Москва, Россия;
3 ЗАО «ФармФирма «Сотекс», Сергиев Посад, Россия;
4 Федеральное государственное образовательное бюджетное учреждение высшего образования «Финансовый университет при Правительстве Российской Федерации», ФГБОУ ВПО «Финансовый университет при Правительстве Российской Федерации», Москва, Россия
* Корреспондирующий автор (slovesnnik[at]gmail.com)
АннотацияТехнология изготовления стерильных (асептических) лекарственных средств, обеспечивающих высокую степень чистоты препарата, его стерильность, в соответствии с правилами GMP, постоянно совершенствуется на основе последних достижений науки и практики. Для реализации этой технологии, в фармацевтической отрасли особое внимание уделяется подготовке оборудования, а именно этапу стерилизации оборудования.
В данной статье рассмотрены методы проведения стерилизации и методы подтверждения стерильности. Рассмотрена безразборная стерилизация (стерилизация на месте «SIP») технологического оборудования асептического производства, а также представлена структурная схема ИИС, разработанная по требованиям нормативной документации.
Ключевые слова: стерилизация, стерилизация паром на месте, подтверждение стерильности.
ANALYSIS OF EQUIPMENT STERILIZATION PROCESS FOR APPLICATION IN ASEPTIC PRODUCTION
Review
Slovesnov N.A.1, *, Mirsaitov S.F.2, Svetlichny V.V.3, Slovesnov E.A.4
1 ORCID: 0000-0003-4624-1937;
1, 2 Federal State Budgetary Educational Institution of Higher Education, MIREA – Russian Technological University, FSBEI of HPE, MIREA RTU, Moscow, Russia;
3 Sotex FarmFirma CJSC, Sergiev Posad, Russia;
4 Federal State Educational Budgetary Institution of Higher Education, Financial University under the Government of the Russian Federation, FSBEI of HPE, Financial University under the Government of the Russian Federation, Moscow, Russia
* Corresponding author (slovesnnik[at]gmail.com)
AbstractThe production technology of sterile (aseptic) drugs providing a high degree of purity, and sterility, following the rules of GMP, is continuously improved based on the latest achievements of science and practice. Special attention is paid to the preparation of equipment, namely the stage of equipment sterilization, to implement this technology in the pharmaceutical industry.
This article discusses sterilization methods and methods for confirming sterility. The authors have considered sterilization in place (sterilization at the SIP place) of aseptic production equipment, and a block diagram of the IMS developed according to the requirements of regulatory documentation was also presented.
Keywords: sterilization, steam sterilization in place, confirmation of sterility.
ВведениеФармацевтическая промышленность является одной из наиболее важных отраслей экономики государства. В современном мире фармацевтическая промышленность — это наукоемкое и высокотехнологичное производство, работающее в условиях рыночных отношений.
Высокое качество любого препарата (как и его цена) зачастую определяет его конкурентное преимущество на рынке в сравнении с его аналогами других производителей. Поэтому, для обеспечения заданных критериев качества необходимо иметь устойчивую систему контроля качества на предприятии, основанной на анализе многочисленных данных, полученных из разных источников (производственных, технологических, и т.д.). Все это в совокупности делает процесс производства лекарственных препаратов сложным и основанным на высокой степени автоматизации производства.
Одним из важнейших этапов производства лекарственных препаратов (и частью системы контроля качества) является подготовка оборудования, имеющего непосредственный контакт с ЛП в процессе его приготовления, в частности процедуры его стерилизации.
Стерильное оборудование — это первый шаг к асептическому производству. Если оборудование не стерильно или невозможно доказать его стерильность, то речи об асептическом производстве лекарственных средств быть не может.
Стерилизация— валидируемый процесс освобождения какого-либо предмета или материала от всех видов микроорганизмов, либо их уничтожение [1, С. 52].
Процесс отмирания микроорганизмов, во время стерилизации, описывается экспоненциальным законом. Исходя из этого, вероятность наличие жизнеспособных микроорганизмов на каждом отдельном изделии может быть снижена до очень малых чисел, но никогда не может быть доведена до нуля [2, С. 76].
Стерилизация оборудования осуществляется термическим и химическим путями.
- Термическая стерилизация
Исходя из названия понятно, что эти методы стерилизации осуществляются при нагревании поверхностей до определенной температуры в течении определенного времени.
К термической стерилизации относятся следующие методы:
- Суховоздушная стерилизация – при данном методе стерилизации к материалу стерилизуемого оборудования подается горячий, сухой воздух заданной температуры. При достижении материалом заданной температуры начинается отсчет времени действия.
- Стерилизация текучим паром – при данном методе стерилизации, к материалу стерилизуемого оборудования подается водяной пар без давления в течении заданного времени. При таком методе стерилизации уничтожаются лишь вегетативные формы микроорганизмов. При наличии микроорганизмов споровых форм данный метод стерилизации неэффективен.
- Стерилизация паром под давлением – наиболее надежный и широко распространённый метод стерилизации. При данном методе стерилизации к материалу стерилизуемого оборудования подается водяной пар под давлением, благодаря чему достигается температура выше 100 °С [2, С. 83]. Процесс стерилизации паром под давлением представляет из себя подачу сухого, насыщенного и неперегретого пара, который используется в качестве стерилизующего средства, в оборудование таким образом, чтобы пар контактировал с рабочими поверхностями технологического оборудования, с которыми в последствии будет контактировать лекарственное средство.
- Химическая стерилизация
Методы химической стерилизации основаны на высокой специфической (избирательной) чувствительности микроорганизмов к различным химическим веществам, что обусловливается физико-химической структурой их клеточной оболочки и протоплазмы. Для многих веществ эффект антимикробного действия до конца не изучен, как и не изучены до конца возможные побочные влияния остатков данных средств. Основой любого варианта химической стерилизации является взаимодействие бактерицидного вещества с микроорганизмами [3, С. 557].
Для стерилизации оборудования, предназначенного для асептического производства, наиболее эффективным методом является стерилизация паром под давлением, в связи с простотой выполнения технологического процесса и отсутствием побочных последствий для продукта, который будет контактировать с данным оборудованием. При таком методе стерилизации емкости, трубопроводы, и все части оборудования, которые могут соприкасаться с продуктом во время асептического технологического процесса производства лекарственных средств нагреваются чистым паром под давлением до определенной температуры и выдерживаются под этой температурой определенное время [4, С. 435]. Такой метод стерилизации оборудования называют стерилизацией на месте (SIP - sterilization-in-place).
Стерилизация на месте (sterilization-in-place "SIP") – Метод стерилизации внутренних поверхностей оборудования или всей системы "на месте" без ее разборки с использованием стерилизующих средств [4, С. 437].
Стерилизация паром на месте становится все более широко используемой в фармацевтической и биотехнологической отраслях, поскольку производители стремятся повысить уровень обеспечения стерильности, произведенной асептической продукции [6, С. 3].
Стерильность оборудования, а значит, успешное прохождение процесса стерилизации подтверждается несколькими способами:
- Химическими индикаторами.
Химические индикаторы представляют собой вещества, которые при выдержке определенного температурного режима изменяют свой цвет или агрегатное состояние. Соответственно, если после процесса стерилизации индикатор поменял цвет на нужный, то цикл считается успешно завершенным и оборудование стерильно [11, С. 253].
- Биологическими индикаторами.
Биологические индикаторы представляет собой препарат из патогенных спорообразующих микроорганизмов с известной высокой устойчивостью к данному типу стерилизационного процесса. Задачей биологических индикаторов является подтверждение способности стерилизационного процесса убивать устойчивые микробные споры. Это наиболее критичный и достоверный тест стерилизационного процесса [8, С. 162].
- Физический метод.
Подтверждение стерилизации при таком методе заключается в измерении таких параметров, как температура, давление и время стерилизации. Периодически проводится повторная квалификация цикла стерилизации при заданных температуре, давлении и времени выдержки. При данной квалификации используются химические и биологически индикаторы. При успешном прохождении квалификации, разрешается использовать такой цикл стерилизации. В дальнейшем любое отклонение от стандартных режимов стерилизации является сигналом для оператора о вероятном сбое аппаратуры и не стерильности оборудования.
- Аналитический метод.
При данном методе подтверждения стерилизации рассчитывается критерий летальности F0. Величина F0 – мера способности тепловой стерилизационной обработки инактивировать микроорганизмы, рассчитанная при температуре 121,1°C, величине z, равной 10°C, и величине D, равной 1 минуте. Величина z – Изменение температуры, необходимое для изменения величины D в 10 раз. D величина – Время или доза облучения, необходимая для достижения инактивации 90% популяции тест-микроорганизмов при установленных условиях [5, С. 10].
В настоящее время критерий летальности рассчитывается благодаря данным полученным с помощью датчиков температуры, после проведения цикла стерилизации. Используют обычно для этого либо отчет в виде графика, на котором присутствую кривые показаний датчиков температуры или отчет, в котором значения температуры представлены в табличном виде.
После проведения цикла стерилизации необходимо подтвердить стерильность оборудования. При стерилизации паром на месте прямым путем (с использованием химических или биологических индикаторов) это выполнить невозможно, так как при извлечении индикаторов герметичность, а значит и стерильность оборудования будет нарушена. Исходя из этого, использование химических и биологических индикаторов возможно только при периодической валидации (аттестации) процесса стерилизации, так как оборудование до попадания в него продукта остается герметичным и посмотреть оценить состояние индикаторов невозможно. Поэтому в ходе производственного процесса для подтверждения стерильности используют физический метод.
Основными параметрами стерилизации при физическом методе подтверждения стерилизации является температура, которая должна быть не менее 121 °С и время, в течении которого эта температура выдерживается. Однако, если проводится стерилизация оборудования, которое имеет в своем составе фильтры (стерилизующие, дыхательные и т.д.), то в этом процессе появляется и предельное верхнее значение температуры. Это максимальная температура, при которой не происходит деформации пор фильтра, а соответственно его пропускной и фильтрующей способности. В большинстве случае верхнее значение температуры составляет 135 °С [9, С. 58] [10, С. 750].
При данном методе происходит запись значений технологических параметров (температур и давления), а также время, в течение которого проходит процесс.
Согласно ГОСТ Р ИСО 13408-5-2011 при стерилизации оборудования необходимо контролировать следующие параметры [5, С. 23]:
- Температуру стерилизуемой поверхности в критических точках оборудования;
- Температуру в нижней точке (на сливе конденсата в дренаж);
- Давление пара в оборудовании.
Во время процесса стерилизации необходимо обеспечить регулирование и контроль (запись) текущих параметров во время процесса стерилизации. При этом каналы измерения температуры и давления, предназначенные для регулирования процесса и контроля (регистрации) должны быть развязаны между собой. То есть, использовать один и тот же канал измерения для управления процессом и для регистрации данных недопустимо.
Для обеспечения этих требований необходимо реализовать информационно-измерительную систему со следующей структурной схемой (см. рисунок 1) [7, С. 97].
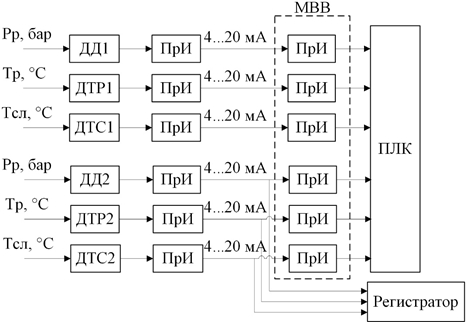
Рис. 1 – Структурная схема ИИС: (Рр, бар – давление среды при SIP; Тр, °С – температура поверхности оборудования; Тсл, °С – температура в нижней точке (на сливе в дренаж); ДД1 – датчик давления контура регулирования; ДТР1 – датчик температуры поверхности оборудования контура регулирования; ДТС1 – датчик температуры нижней точки контура регулирования; ДД2 – датчик давления контура регистрации; ДТР2 – датчик температуры поверхности оборудования контура регистрации; ДТС2 – датчик температуры нижней точки контура регистрации; ПрИ – преобразователь интерфейса; ПЛК – промышленный логический контроллер; МВВ – модуль ввода-вывода ПЛК)
Как видно из структурной схемы, разрабатываемая система имеет два контура в каждый из которых входит три канала измерения: контур регулирования (ДД1, ДТР1, ДТС1) и контур регистрации (ДД2, ДТР2, ДТС2). Каждый канал измерения имеет датчик и преобразователь интерфейса, с помощью которого сигнал от датчика преобразуется в сигнал токовой петли. Все каналы измерения контура регулирования подключены непосредственно к модулю ввода-вывода, который имеет АЦП для преобразования сигнала токовой петли в цифровой, удобный для дальнейшей обработки ПЛК. Каналы контура регистрации с помощью интерфейса токовой петли подключены к ПЛК и к Регистратору. На регистраторе ведется запись технологических параметров во время процесса стерилизации с периодом 1 секунда. Каналы контура регистрации подключены к ПЛК для обеспечения самодиагностики всех измерительных каналов ИИС посредством сравнения сигналов с датчиков, измеряющих один и тот же параметр. Если разница значений параметров с разных датчиков выходит за допустимые пределы, то процесс стерилизации останавливается.
С помощью датчиков температуры ведется регистрация значения температуры, как в критических точках стерилизуемого оборудования, так и на сливе конденсата в дренаж.
Регулировка температуры во время цикла стерилизации производится по показаниям датчика давления. По значению давления в оборудовании, рассчитывается теоретическое значение температуры, которое должна быть при данном давлении. Исходя из теоретической температуры, в оборудовании поддерживается заданное давление чистого пара.
Перед началом цикла стерилизации проверяется герметичность оборудования, для безопасности оборудования и персонала. Для этого в оборудование подается сжатый воздух, до определенного значения давления. С помощью датчика давления оценивают падение значения давления за определенное время и делают вывод о герметичности оборудования.
Регистратор необходим для предоставления отчета по циклу стерилизации. В данном отчете может фигурировать, как график, на котором имеются кривые температуры, так и таблица, в которой с определенной частотой записаны значения температуры. Если во время цикла стерилизации все параметры находились в допустимых пределах, время выдержке равно заданному, то цикл считается успешно завершенным и стерилизуемое оборудование считается стерильным. Если же, в какой-то момент один из параметров вышел за свои предельные значения или время стерилизации менее заданного, то стерилизуемое оборудования считается нестерильным.
Благодаря такой схеме ИИС возможно корректно проводить SIP технологического оборудования, а также дополнительно обеспечить самодиагностику измерительных каналов, и оповещение оператору о неисправности.
Заключение
В данной статье были кратко рассмотрены существующие методы стерилизации оборудования. Рассмотрены основные аспекты и требования к процессу SIP (стерилизация на месте). Были указаны методы подтверждения стерильности оборудования, их применение в процессе SIP. Разработана структурная схема информационно-измерительной системы, с помощью которой возможно подтверждение стерилизации физическим методом.
В дальнейшем предлагается рассмотреть возможность использования аналитического метода подтверждения стерильности оборудования и именно с помощью данного метода фиксировать окончание процесса стерилизации.
| Конфликт интересов Не указан | Conflict of Interest «None declared» |
Список литературы / References
- ГОСТ Р ИСО 17665-1-2016 (ISO/TS 17665-2:2016) Стерилизация медицинской продукции. Влажное тепло. Часть 1. Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий. – М.: Стандартинформ, 2016. – С. 52 – 58.
- Краснюк И.И. Технология лекарственных форм. / Краснюк И.И. М.: Академия – 2004. – С. 75 – 87.
- Чуешов В.И. Промышленная технология лекарств. В 2 ч. Ч. 2. / Чуешов В.И. Х.: МТК-Книга. С. 556 – 559.
- Paul R.S., Heldman D.R. Introduction to Food Engineering / Paul R.S., Heldman D.R.– Amsterdam: Elsevier, 2009. – P. 435-440.
- ГОСТ Р ИСО 13408-5-2011. Асептическое производство медицинской продукции. Часть 5. Стерилизация на месте. – М.: Стандартинформ, 2012. – С. 6 – 24.
- Dion M. Steam Sterilization Principles / Dion M., Parker W. // Pharmaceutical engineering. – 2013. – Vol. 33(6). – P. 3-5.
- Словеснов Н.А. Разработка автоматической системы очистки и стерилизации мобильных реакторов фармацевтического назначения / Словеснов Н.А., Мирсаитов С.Ф., Светличный В.В. // Материалы конференции «Приоритетные дискуссии XXI века: междисциплинарные исследования современности». – Ростов-на-Дону 2019. – С. 95 – 98.
- Абрамова И.М. Пути оптимизации способов и средств предстерилизационной очистки, стерилизации и методов их контроля / Абрамова И.М. // Материалы Всероссийской научной конференции, посвященной 100-летию со дня рождения В.И. Вашкова – Москва, 2002 – C. 158 – 165.
- Nordhauser F.M. Sterilization of Drugs and Devices Tehnologies for the 2000th. / Nordhauser F.M., Olson W.P. – London: Taylor & Francis group, 2000. – P. 55-59.
- Flickinger M.C. Downstream Industrial Biotechnology: Recovery and Purification. / Flickinger M.C. – North Carolina: Wiley, 2013. – P. 750.
- Галынкин В.А. Основы фармацевтической микробиологии: учеб. Пособие / Галынкин В.А., Заикина Н.А., Кочеровец В.И. – СПб.: Проспект Науки, 2008. – С. 249 – 260.
Список литературы на английском языке / References in English
- GOST R ISO 17665-1:2006 Sterilizacija medicinskoj produkcii. Vlazhnoe teplo. Chast' 1. Trebovanija k razrabotke, validacii i tekushhemu kontrolju processa sterilizacii medicinskih izdelij [Sterilization of health care products - Moist heat - Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices] – М.: Standartinform, 2016. – P. 52 – 58. [in Russian]
- Krasnjuk I.I. Tehnologija lekarstvennyh form [Technology of dosage forms]. / Krasnjuk I.I. M.: Akademija – 2004. – P. 75 – 87. [in Russian]
- Chueshov V.I. Promyshlennaja tehnologija lekarstv. V 2 ch. Ch. 2 [Industrial technology of drugs. In 3 h the P. 2]. / Krasnjuk I.I. H.: MTK-Kniga. P. 556 – 559. [in Russian]
- Paul R.S. Introduction to Food Engineering / Paul R.S., Heldman D.R.– Amsterdam: Elsevier, 2009. – P. 435-440. [in Russian]
- GOST ISO 13408-5:2006 Asepticheskoe proizvodstvo medicinskoj produkcii. Chast' 5. Sterilizacija na meste [Aseptic processing of health care products - Part 5: Sterilization in place] – М.: Standartinform, 2012. – P. 6 – 24. [in Russian]
- Dion M.Steam Sterilization Principles/ Dion M., Parker W. // Pharmaceutical engineering. – 2013. Vol. 33(6). – P. 3-5. [in Russian]
- Slovesnov N.A. Razrabotka avtomaticheskoj sistemy ochistki i sterilizacii mobil'nyh reaktorov farmacevticheskogo naznachenija [Development of an automatic system for cleaning and sterilization of pharmaceutical mobile reactors]/ Slovesnov N.A., Mirsaitov S.F., Svetlichnyj V.V. // Materialy konferencii «Prioritetnye diskussii XXI veka: mezhdisciplinarnye issledovanija sovremennosti» [Materials of the conference “Priority Discussions of the 21st Century: Interdisciplinary Studies of the Present]. – Rostov-na-Donu 2019. – P. 95 – 98. [in Russian]
- Abramova I.M. Puti optimizacii sposobov i sredstv predsterilizacionnoj ochistki, sterilizacii i metodov ih kontrolja [Ways to optimize methods and means of pre-sterilization cleaning, sterilization and methods for their control] / Abramova I.M. // Materialy Vserossijskoj nauchnoj konferencii, posvjashhennoj 100-letiju so dnja rozhdenija V.I. Vashkova [Materials of the All-Russian Scientific Conference dedicated to the centenary of the birth of V.I. Vashkova]. – Moscow, 2002 – P. 158 – 165. [in Russian]
- Nordhauser F.M. Sterilization of Drugs and Devices Tehnologies for the 2000th. / Nordhauser F.M., Olson W.P. – London: Taylor & Francis group, 2000. – P. 55-59. [in Russian]
- Flickinger M.C. Downstream Industrial Biotechnology: Recovery and Purification. / Flickinger M.C. – North Carolina: Wiley, 2013. – P. 750. [in Russian]
- Galynkin V.A. Osnovy farmacevticheskoj mikrobiologii: ucheb. Posobie [Fundamentals of pharmaceutical microbiology: textbook. Allowance] / Galynkin V.A., Zaikina N.A., Kocherovec V.I. – SPb.: Prospekt Nauki, 2008. – P. 249 – 260. [in Russian]
