ПЕРИОПЕРАЦИОННЫЕ ОСЛОЖНЕНИЯ АОРТОКОРОНАРНОГО ШУНТИРОВАНИЯ В ЗАВИСИМОСТИ ОТ ДЛИТЕЛЬНОСТИ ПЕРИОДА ОТ НАЧАЛА ОСТРОГО ИНФАРКТА МИОКАРДА
Дембеле А.1, Пастухова Н.К. 2
1Аспирант, 2Доктор медицинских наук, Санкт-Петербургский государственный педиатрический медицинский университет, Россия.
ПЕРИОПЕРАЦИОННЫЕ ОСЛОЖНЕНИЯ АОРТОКОРОНАРНОГО ШУНТИРОВАНИЯ В ЗАВИСИМОСТИ ОТ ДЛИТЕЛЬНОСТИ ПЕРИОДА ОТ НАЧАЛА ОСТРОГО ИНФАРКТА МИОКАРДА
Аннотация
В статье рассматриваются – периоперационные осложнения аортокоронарного шунтирования (АКШ), выполненного в разные периоды от начала инфаркта миокарда.
Ключевые слова: Аортокоронарное шунтирование (АКШ), осложнения.
Dembele A.1, Pastukhova N. C .2
1Postgraduate student, 2Doctor of Medical Sciences, Saint-Petersburg State Pediatric-Medical University.
STUDYING OF PERIOPERATIVE COMPLICATIONS OF CORONARY ARTERY BYPASS GRAFTING (CABG) DEPENDING ON THE LENGTH OF TIME BETWEEN THE ONSET OF AN ACUTE MIOCARDIAL INFARCTION (AMI) AND THE SURGICAL INTERVENTION
Abstract
This article analyses the perioperative complications of coronary artery bypass grafting (CABG), depending on the length of time between the onset of an acute myocardial infarction and the surgical intervention.
Keywords: Coronary artery bypass grafting (CABG), Complications.
Введение
В настоящее время аортокоронарное коронарное шунтирование (АКШ) остается самым распространенным видом кардиохирургического вмешательства во всем мире. АКШ может выполняться в различные сроки от начала инфаркта миокарда. К сожалению, частота осложнений, возникающих в периоперационном периоде, не уменьшается. Факторами риска являются пожилой возраст, инсульт в анамнезе, сахарный диабет, гипертоническая болезнь и женский пол и др.
Послеоперационная фибрилляция предсердий является самым распространённым осложнением после АКШ. Она наблюдается у 20% - 50% пациентов и четырехкратно увеличивает риск развития инсульта и трехкратно риск наступления кардиогенной смерти. Не исключена вероятность развития острого нарушения мозгового кровообращения от 1,4% до 3,8% [5]. Изолированная фибрилляция предсердий обычно прекращается спонтанно в течение 6 недели после операции [4].
Системная воспалительная реакция может быть не значительной, но может прогрессировать до полиорганной дисфункции. Факторами ее развития чаще всего являются контакт крови с экстракорпоральным кругом кровообращения, эндотоксемия, ишемия и реперфузионное повреждение после снятия аортального кросс-зажима. Случаи острой почечной недостаточности (ОПН) после АКШ встречаются в 2- 3%, из них около 1% пациентов нуждаются в диализе. Причинами ОПН являются: уже имеющаяся почечная патология, низкий сердечный выброс при хронической сердечной недостаточности (ХСН) или шоке, сахарный диабет (СД), пожилой возраст, чернокожая раса, женский пол [3]. Кратковременные когнитивные изменения наблюдаются у 30% пациентов после АКШ с применением аппарата искусственного кровообращения (АИК). Послеоперационный делирий встречается у 10% пациентов. Факторами риска являются уже имеющиеся цереброваскулярные заболевания, патология центральной нервной системы и др. [5]. Кроме того, у 10%-20% пациентов страдающих хроническим обструктивным бронхитом (ХОБЛ), СД, ожирением после АИК описаны нозокомиальные инфекции [1].
Для уменьшения частоты периоперационных осложнений необходимо тщательно планировать не только тактику оперативного вмешательства, но и обеспечить эффективную предоперационную подготовку и лечебные мероприятия в раннем послеоперационном периоде.
Цель исследования. Изучить осложнения периоперационного периода и их частоту при выполнении АКШ в разные сроки от момента развития острого инфаркта миокарда.
Материалы и методы исследования
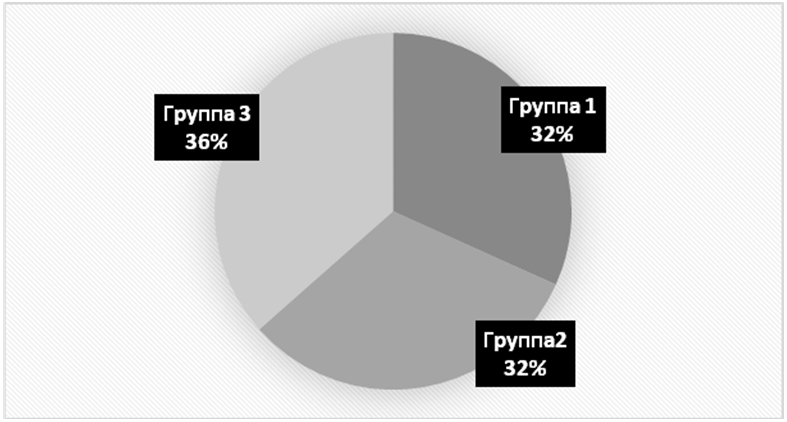
Изучено 63 пациента. Их них 41 мужчин, 22 женщин, в возрасте 61,3±1,62 лет. В зависимости от длительности периода от дня дебюта ОИМ пациенты разделены на три группы (рис.1).
- 1 группа: АКШ проведено в первые 10 дней от момента развития ОИМ - 20 пациентов.
- 2 группа: АКШ проведено от 10-ого до 30-го дня от начала ОИМ − 20 пациентов.
- 3 группа: АКШ проведено в интервале от одного до пяти месяцев от начала ОИМ – 23 пациента.
Рис.1 Структура исследования
Причинами выполнения АКШ в эти сроки явились:
- Признаки критического стеноза или окклюзии магистральных коронарных артерий на коронарографии.
- Диффузное поражение сосудов коронарного русла.
- Кальциноз коронарных артерии, в сочетании с сердечной недостаточностью.
- Ранняя постинфарктная стенокардия.
- Нестабильная стенокардия.
Чем раньше возникали эти проблемы, тем ранее выполнялось АКШ.
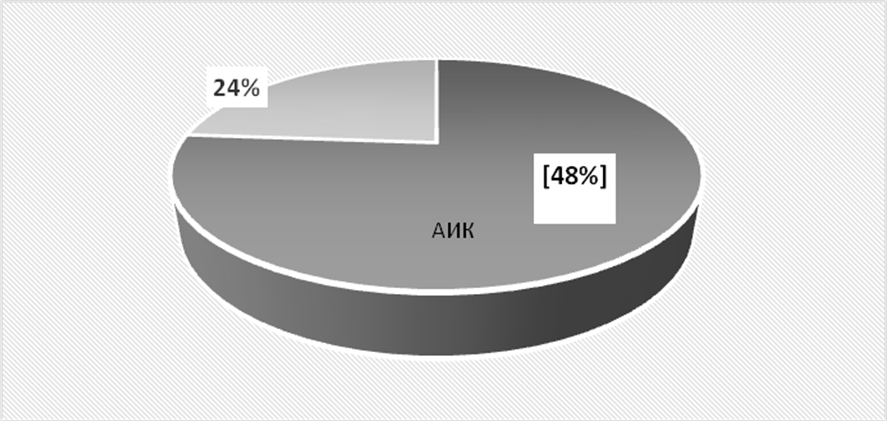
У 48 (76%) больных АКШ осуществлялось с помощь аппарата искусственного кровообращения (АИК), у 15 (24%)–без АИК (рис.2).
Рис.2 Применение АИК
В 1 группе АИК у 19 пациентов (95%), без АИК - 1 пациент (5%), во 2 группе АИК у 11 пациентов (55%), без АИК - 9 пациентов (45%), в 3 группе АИК у 18 пациентов (78%), без АИК - 5 пациентов (22%).
Результаты и обсуждение
Мы определили длительность АИК и пережатия аорты и сравнили эти параметры в группах (таб.1).
Таблица 1 - Длительность АИК и пережатия аорты по группам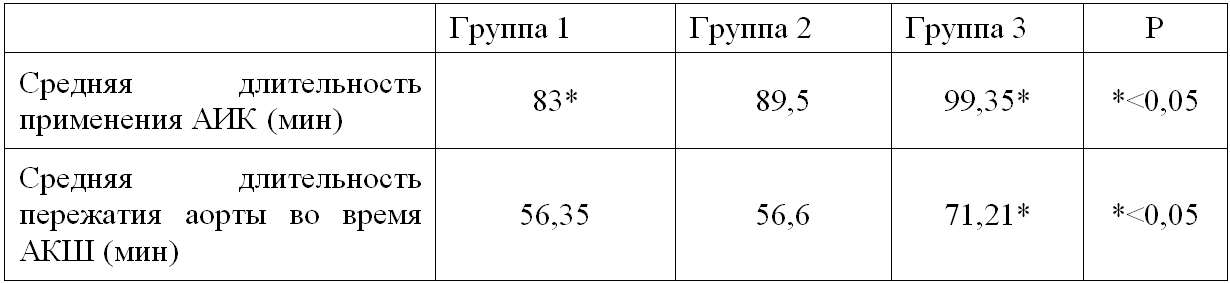
В 1 группе длительность АКШ, как и длительность пережатия аорты были наименьшими по сравнению с другими группами. В 3 группе искусственное кровообращение продолжалось дольше всех - 99,35 мин, как и пережатие аорты 71,2 мин.
У пациентов всех групп на 2-е сутки послеоперационного периода отмечено нарастание количества лейкоцитов, которое по группам достоверно не отличалось, однако у пациентов первой группы количество лейкоцитов увеличилось на 29%, у второй группы на 46%, а у третьей на 40% (таб. 2).
Таблица 2 - Сравнение уровня лейкоцитов в послеоперационном периоде по группам
Увеличение лейкоцитов вероятнее всего связано с кардиотомным синдромом.
Зарегистрированы следующие периоперационные осложнения, кроме того, наблюдалось сочетание нескольких осложнений (таб.3).
Таблица 3 - Распределение осложнений при АКШ по группам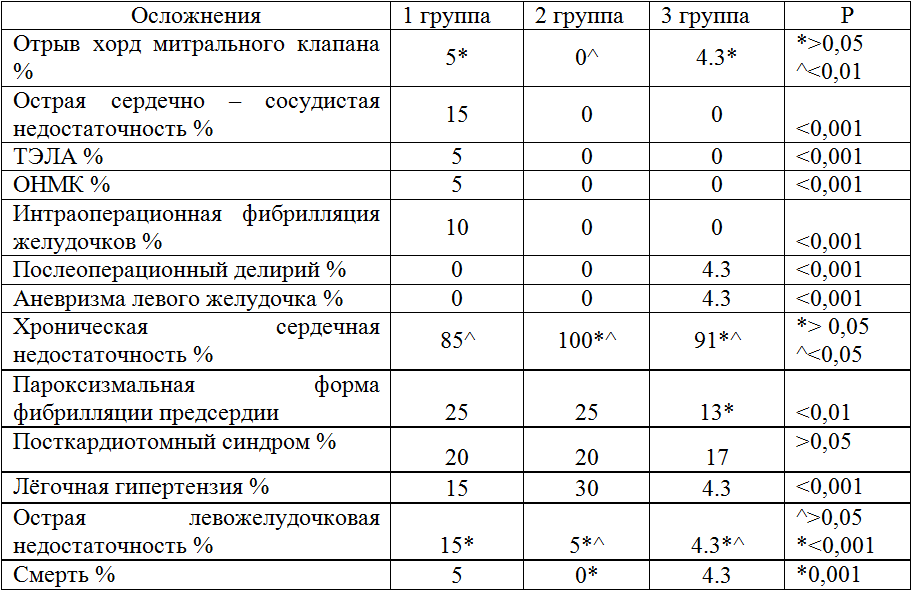
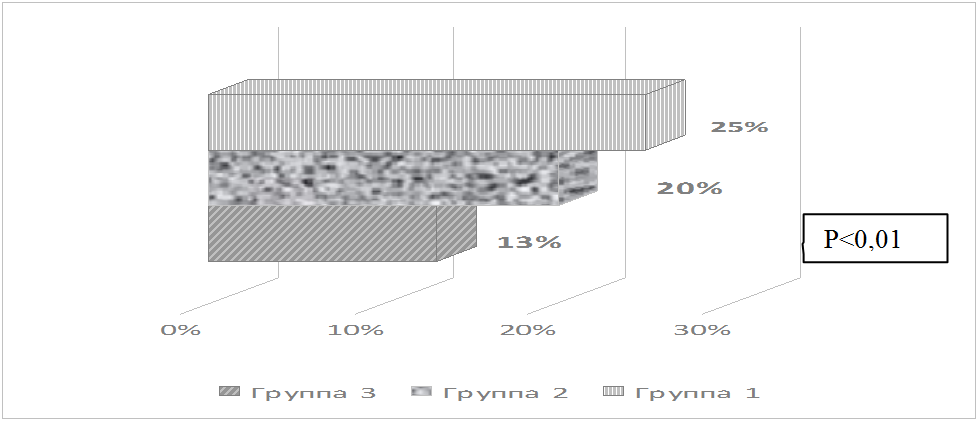
Таким образом, пароксизмальная фибрилляция предсердий после АКШ наблюдалась у 5(25%)пациентов в 1 группе и у 4(20%) пациентов во 2 группе. В 3 группе у 3(13%) пациентов.
Рис.3. Послеоперационная фибрилляция предсердий
- Отрыв хорд митрального клапана и смерть выявлены в группах 1 и 3.
- Острая сердечно-сосудистая недостаточность, ТЭЛА, ОНМК, а также интраоперационная фибрилляция желудочков - только в группе 1.
- Послеоперационный делирий и аневризма ЛЖ – только в группе 3.
- Острая левожелудочковая недостаточность с развитием отёка лёгких во всех 3 группах.
- ОНМК в нашем исследовании зарегистрировано у 1 пациента первой группы. Оно же и стала непосредственной причиной смерти.
- Послеоперационный делирий наблюдался в 3 группе у 1 из 23 пациентов.
- Инфицирование стернальной раны с несостоятельностью швов зарегистрировано во 2 группе у пациентки страдающей сахарным диабетом 2 типа, на фоне ожирения 1 степени (ИМТ=31.16 кг/м2) и бронхиальной астмы. Операция у нее была выполнена с применением АИК (длительность АИК=54 мин., пережатие аорты - 37 мин.). Поскольку в этом случае продолжительность применения АИК и пережатия аорты невелики, вероятнее всего, развитие инфекционного процесса связано с наличием СД и ХОБЛ.
- Хроническая сердечная недостаточность, посткардиотомный синдром, лёгочная гипертензия, острая левожелудочковая недостаточность выявлены во всех трёх группах, с разными степенями встречаемости.
Выводы:
- В 1 группе пациентов АКШ чаще всего (95%), проводилось с АИК, однако ее длительность, а также длительность пережатия аорты наименьшее. Несмотря на это в этой группе наиболее часто встречаются жизне - угрожающие периоперационные осложнения: ТЭЛА, ОНМК, острая сердечно-сосудистая недостаточность, чаще возникает фибрилляция желудочков, интроперационный ОИМ. При этом в дальнейшем пациентов с хронической сердечной недостаточностью меньше чем в 2 и 3 группе.
- . Во 2 группе количество пациентов с АИК наименьшее 56%, а 44% операций проводится без АИК. В этой группе зарегистрированы отёк лёгких и инфицирование стернальной раны и, хотя летальных исходов не отмечалось, тем не менее, все пациенты страдали в дальнейшем хронической сердечной недостаточностью.
- В 3 группе чаще всего возникают когнитивные нарушения и делириозный синдром, по видимому за счет длительного периода искусственного кровообращения, но меньше количество случаев пароксизмальной фибрилляции предсердий и легочной гипертензии.
- Риск развития послеоперационных инфекций увеличивается на фоне ХОБЛ, сахарного диабета, ожирения и при длительном применении АИК.
Литература
- Alam M., Siddiqui S., Lee V. et al., “Isolated coronary artery bypass grafting in obese individuals: a propensity matched analysis of outcomes,” Circulation Journal, vol. 75, no. 6, pp. 1378–1385, 2011.
- Ho P. M., Arciniegas D. B., Grigsby J. et al., “Predictors of cognitive decline following coronary artery bypass graft surgery,” Annals of Thoracic Surgery, vol. 77, no. 2, pp. 597–603, 2004.
- Mangano C. M., Diamondstone L. S., Ramsay J.G., “Renal dysfunction after myocardial revascularization: risk factors, adverse outcomes, and hospital resource utilization,” Annals of Internal Medicine, vol. 128, no. 3, pp. 194–203, 1998.
- Mariscalco G., Klersy C., Zanobini M. et al., “Atrial fibrillation after isolated coronary surgery affects late survival,” Circulation, vol. 118, no. 16, pp. 1612–1618, 2008.
- Roach G. W., Kanchuger M., Mangano C. M. et al., “Multicenter study of perioperative ischemia research group and the ischemia research and education foundation investigators. Adverse cerebral outcomes after coronary bypass surgery,” The New England Journal of Medicine, vol. 335, pp. 1857–1863, 1996.