Когнитивные нарушения, связанные с COVID-19: систематический обзор
Когнитивные нарушения, связанные с COVID-19: систематический обзор
Аннотация
Важность изучения особенностей заболевания COVID-19 обосновывается непосредственно клиническими значимыми симптомами, как для отдельного человека, так и для человечества в целом, а именно: уровнем работоспособности, снижением когнитивных способностей человека, влияющим как следствие на качество жизни человечества. Самыми распространёнными симптомами и пост-симптомами заболевания COVID-19 являются усталость, нарушения когнитивных функций, нарушение памяти и внимания, причем данная клиническая картина возникает, как и в течение самого заболевания, так и в постреабилитационный период. В статье освещены актуальные проблемы заболевания, выраженные нарушением когнитивных функций в период восстановления после COVID-19; проведена характеристика функциональных последствий вирусного воспалительного заболевания; проведен систематический поиск и определена доля людей, обладающих постоянным снижением памяти, мышления, внимания и восприятия не меньше 3 месяцев после определения и постановки диагноза COVID-19. Исследования были проведены по пяти электронным библиографическим базам данных: MEDLINE через Ebsco, Cochrane Central Register of Controlled Trials (CENTRAL), база данных Excerpta Medica (EMBASE), SCOPUS и здравоохранение Латинской Америки и Карибского бассейна научная литература (LILACS), с момента создания до 30 марта 2021 года.
1. Введение
В ноябре 2019 года вспышка пневмонии неизвестной причины в Ухане, провинция Хубэй, Китай, привлекла внимание китайских органов здравоохранения. COVID-19 был объявлен пандемией Всемирной организацией здравоохранения 11 марта 2020 года, с высоким уровнем заражения и смертности в Китае, Италии и Испании, а затем и в других странах. COVID-19 имеет широкий спектр клинических проявлений . Следует отметить, что неврологические проявления у пациентов с COVID-19 были продемонстрированы во время пандемии. В исследовании, проведенном в Ухане провинции Хубэй, у 36,4% пациентов наблюдались те или иные неврологические проявления, причем центральное вовлечение было более распространенным (головокружение, головная боль, измененный уровень сознания, инсульт, атаксия и эпилепсия). Кроме того, у пациентов с тяжелым заболеванием была большая вероятность развития неврологических расстройств, особенно расстройств сознания, острых цереброваскулярных заболеваний и заболеваний опорно-двигательного аппарата.
Помимо общих неврологических проявлений, у пациентов с COVID-19 оценивались когнитивные нарушения. В китайском исследовании оценивались когнитивные способности 29 пациентов с COVID-19 с использованием цифровых анкет, связывающих когнитивные жалобы с высоким уровнем С-реактивного белка во время острой фазы заболевания. В другом исследовании оценивались когнитивные нарушения у амбулаторных пациентов с использованием мини-оценки психического состояния (MMSE) и Монреальской когнитивной оценки (MoCA), Шкала оценки депрессии по Гамильтону и показатель функциональной независимости (FIM), обнаруживающий 80% когнитивных нарушений . Более того, были описаны различные когнитивные проявления, такие как энцефалопатия, связанная с тяжелыми состояниями и акинетический мутизм, связанный с лобным гипометаболизмом .
Относительно патофизиологии когнитивных проявлений и более тяжелых неврологических проявлений у пациентов был описан аллель APOE 4 аполипопротеина E. Эта ассоциация значима, поскольку один и тот же аллель повышает риск спорадической болезни Альцгеймера (AD).
Растущее старение населения за последние несколько десятилетий было связано с увеличением числа когнитивных расстройств. Данные международного отчета по болезни Альцгеймера (ADI) 46,8 миллион человек, живущих с деменцией во всем мире в 2015 году. По оценкам, в 2030 году это число составит около 74,5 миллионов, и 131,5 миллиона в 2050 году. Болезнь Альцгеймера является наиболее распространенной формой деменции и составляет 50-70% случаев слабоумия. Распространенность умеренных когнитивных нарушений (MCI) составляет 12-18% среди взрослых старше 65 лет, и ежегодные темпы прогрессирования от MCI до AD составляют 10-15% . Невропатологические изменения амнестического MCI являются промежуточными между нормальными людьми и лицами с болезнью Альцгеймера, включающая нейрофибриллярные клубки с тау-белком, отложения бета-амилоида и нейродегенерацию. Кроме того, незначительное бремя травм возникает, когда MCI представляет собой стадию до AD, которая теоретически восприимчива к медикаментозному воздействию. Помимо этих состояний, субъективное снижение когнитивных способностей является состоянием, предшествующим MCI, и возможным предшественником деменции. В нем представлены лица с когнитивными жалобами без объективных признаков когнитивных нарушений. Поэтому крайне важно определить, связаны ли возможные неврологические поражения, вызванные COVID-19, с более значительными когнитивными нарушениями.
Это исследование было направлено на определение какой-либо взаимосвязи между COVID-19 и когнитивных жалоб, такие как деменция, умеренные когнитивные нарушения (MCI) или субъективное снижение когнитивных способностей (SCD).
2. Материал и методы исследования
Мы провели систематический обзор наблюдательных исследований, основанный на рекомендации Кокрейновского сотрудничества .
Стратегия поиска
Стратегия поиска будет реализована для повышения методологической прозрачности и улучшения воспроизводимости результатов в соответствии с контрольным списком PRISMA. Это систематическое обзорное исследование включало шесть этапов:
1) формулирование центрального исследовательского вопроса (определение темы);
2) определение критериев включения и исключения и поиск литературы;
3) категоризация первичных исследований (определение данных, которые будут извлечены из выбранных исследований);
4) оценка включенных исследований;
5) интерпретация результатов;
6) выполнение обобщения знаний о результатах, полученных в результате оцененных исследований .
Кроме того, мы использовали метод PICo (Популяция; Интерес; Контекст) аббревиатура, где «P» – исследуемая популяция (пациенты с подтвержденным COVID-19); «I» – оцениваемый интерес (когнитивные нарушения); и «Co» – контекст (риск развития когнитивных нарушений). Затем мы разработали руководящий вопрос этого обзора, чтобы обеспечить систематический поиск научной литературы: «Развиваются ли у пациентов с COVID-19 более серьезные когнитивные нарушения?».
Прежде всего, мы определили наличие индекса конкретных тематических рубрик в каждой базе данных (таких, как термины MeSH, термины Emtree и дескрипторы DeCS-HealthScience) и их синонимы (ключевые слова). Естественный язык использовался с контролируемым языком (дескрипторы) для расширения результатов поиска . Поисковые запросы были объединены с использованием логических операторов «И» и «ИЛИ».
Выбор исследования
Мы включили исследования с пациентами с COVID-19, подтвержденными серологией или ПЦР, у которых развились новые когнитивные нарушения или ухудшились предыдущие когнитивные нарушения после заражения. Не было никаких ограничений в отношении возраста, предшествующего заболевания, пола или этнической принадлежности. Критериями включения были статьи на английском языке, и COVID-19, подтвержденный серологией или ПЦР, с новыми или ухудшившимися когнитивными нарушениями с детальной когнитивной оценкой. Критериями исключения были исследования, посвященные психиатрическим проявлениям, руководящим принципам и институциональным протоколам. Что касается дизайна исследования, мы включили проспективные или ретроспективные и перекрестные исследования. Этот систематический обзор не имел никаких ограничений, касающихся условий жизни целевой группы населения.
Скрининг и извлечение данных
Первоначально исследователи независимо провели поиск в базе данных и отправили его справочному менеджеру Mendeley для исключения дубликатов документов. После исключения дубликатов проверили исследования на основе их названий и информации в аннотациях. Полученные данные в результате исследования были оценены в соответствии с критериями приемлемости. Затем статьи были прочитаны полностью, используя ту же предыдущую процедуру. Результаты отбора исследований были представлены с использованием блок-схемы PRISMA. Стандартизированная форма была использована для извлечения данных после достижения консенсуса по отдельным исследованиям. Извлеченная информация включала страну, автора, год, цели, дизайн исследования, распространенность когнитивных нарушений в отдельных исследованиях, первичные результаты, средний возраст, размер и тип выборки, время оценки с момента начала COVID-19, а также инструменты когнитивной и функциональной оценки, используемые для постановки диагноза.
Качественный синтез
Для качественного обобщения систематического обзора анализы будут проводиться в три этапа:
1) предварительный анализ включенных исследований, основанный на определении их характеристик, клинического контекста, инструментов, используемых для измерения снижения когнитивных функций, и найденных когнитивных результатов;
2) изучение взаимосвязей между данными исследования, выявление тех, которые работают с аналогичными инструментами и результатами или даже с разными инструментами, имеющими дело с аналогичными результатами;
3) оценка о надежности синтеза, который включает критику методологического качества включенных исследований и того, как это качество влияет на результаты первичных исследований.
Кроме того, мы разделили исследования на те, которые включали пациентов в острой и подострой фазах (<12 недель с момента начала COVID-19) от тех, кто оценивал когнитивные ухудшение после этой фазы (>12 недель от начала COVID-19), чтобы дифференцировать острое и подострое воздействие COVID-19 на когнитивные способности от хронического.
В конце процесса обобщения анализ взаимосвязей внутри описанных исследований и между ними привел к общей оценке достоверности имеющихся фактических данных, позволяющих сделать выводы на основе обобщения описаний.
Риск предвзятости в отдельных исследованиях
Инструмент «Риск предвзятости» Кокрановского сотрудничества был использован для классификации риска предвзятости включенных исследований с учетом следующих областей: неадекватный отбор пациентов и включение в исследование; контроль за смешивающими факторами; ослепление исследователей и оценщиков результатов; неполные результаты данных. Таким образом, риск предвзятости был классифицирован как низкий, высокий или неизвестный.
3. Результаты исследования и их обсуждение
На рис. 1 показана блок-схема процесса отбора для исследования в соответствии с руководящими принципами PRISMA. В общей сложности было извлечено и прочитано 3520 статей. Для нашего обзора было отобрано двадцать два исследования. Шестнадцать исследований включали пациентов в острой и подострой фазах COVID-19, а в 6 были включены только пациенты после 12 недели от начала заболевания.
Размеры выборки варьировались от 14 до 195 участников. Исследования проводились в 10 странах, и большинство из них были из Италии (27,7%) и Германии (18,8%). Средний возраст колебался в пределах 36,2 лет (SD = 11,7) до 67,23 лет (SD = 12,89) . Что касается типа найденных исследований, то 63,6% были когортными, 31,9% – поперечными и 4,5% – случайными.
Были обнаружены различные типы образцов. Большинство из них касались госпитализированных или выписанных пациентов (81,8%), в то время как другие оценивали только амбулаторных пациентов, никогда не госпитализированных из-за COVID19 (18,1%).
Не во всех исследованиях указывалась частота когнитивных нарушений. В некоторых исследованиях, когнитивные нарушения варьировались от 2,6% до 81%. В исследованиях через 12 недель когнитивные нарушения варьировались от 21% до 65%.
Был использован широкий спектр инструментов когнитивной оценки (n = 25). Следует отметить, что наиболее часто использовалась Монреальская когнитивная оценка (MoCA) (50,0%). Кроме того, метод фронтальной оценки и мини-обследование психического состояния (MMSE) использовались только в 2 исследованиях каждое. В случае MMSE в одном из исследований использовалась телефонная версия. Другой метод, исследования был с использованием телефона, это было модифицированное телефонное интервью для определения когнитивного статуса (TICS-M). Исследования, в которых подробно описывалось образование, показали участников с высшим образованием, и только в одном из них были пациенты с менее чем восьмилетним сроком обучения. Важно отметить, что подробная информация об образовании пациентов не была доступна в более 40,9% исследований.
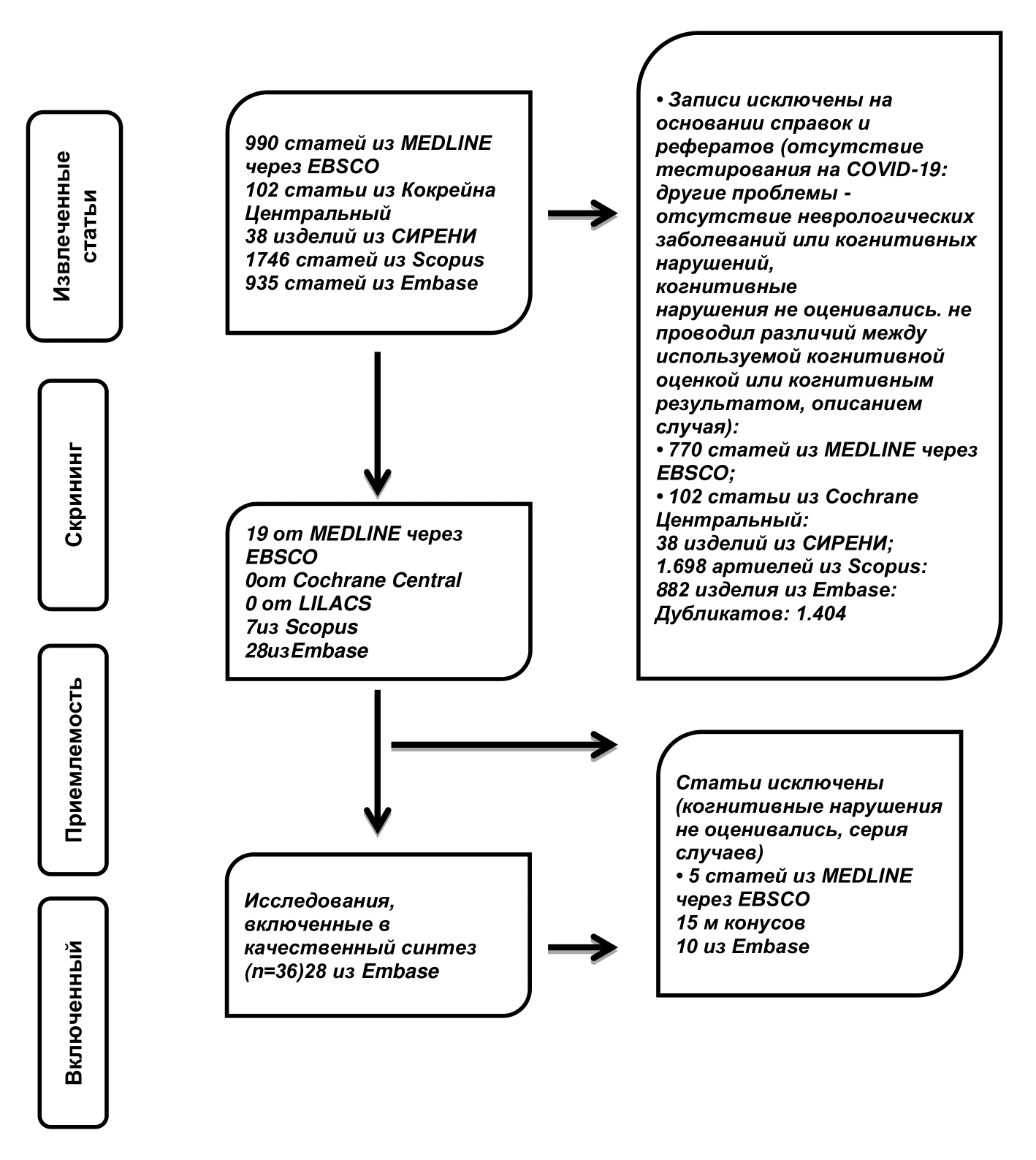
Рисунок 1 - Блок-схема процесса отбора на исследование
Что касается исследований, в которых оценивались пациенты в острой/подострой фазах, то во всех них оценивались пациенты, которые все еще находились в больнице или ранее были госпитализированы. Для сравнения, в исследованиях, которые оценивали пациентов только через 12 недель, 50% включали только амбулаторных пациентов. Кроме того, что касается различий в выборках, в 75% исследований были включены пациенты, которые в какой-то момент находились в отделении интенсивной терапии, тогда как только в 16,6% исследований пациенты были госпитализированы в отделение интенсивной терапии в какой-то момент. Кроме того, что касается основных целей, то 50% обследований имели в качестве основной цели оценку когнитивных нарушений, вызванных заболеванием, в то время как 66,6% исследований было направлено на оценку когнитивных нарушений после 12 недель болезни.
Исследования не выявили специфических изменений при обследовании структурной нейровизуализации (компьютерная томография головного мозга или магнитно-резонансная томография). В двух из отобранных исследованиях оценивали пациентов в острой фазе с помощью позитронно-эмиссионной томографии черепа, обнаружили лобно-теменной гипометаболизм у пациентов с энцефалопатией .
Все статьи были отправлены на оценку риска предвзятости (рис. 2). Общий риск предвзятого отбора был высок в 20 исследованиях, в то время как риск контроля за смешивающими факторами и отсевом был низким в 16 и 18 исследованиях, соответственно. В свою очередь, риск предвзятости в отношении производительности и обнаружения был высок в 10 исследованиях в каждом.
4. Обсуждение
Мы провели критический обзор когнитивных нарушений у пациентов с подтвержденным COVID-19. Наши результаты выявили возможность когнитивных нарушений даже у пациентов с умеренными симптомами через шесть месяцев после начала заболевания . Важность этого систематического обзора показала возможную взаимосвязь между инфекцией SARS-Cov 2 и развитием или ухудшением жалоб и когнитивных нарушений. Более того, когнитивные нарушения возникают не только в тяжелых случаях, но и в острой фазе заболевания.
Неврологические симптомы могут сохраняться в подострой фазе и представлять собой синдром «длительного Covid» . Из-за этого, а также для того, чтобы дифференцировать когнитивные нарушения во время острой или подострой фазе от хронической фазы, мы разделили исследования в соответствии с фазой заболевания при оценке пациентов. Когнитивные нарушения все еще наблюдались через 12 недель после начала заболевания. Однако нам все еще нужно больше данных, чтобы определить, является ли это когнитивное нарушение, когда оно возникает, длительным или улучшается через определенный период времени.
Когнитивные нарушения были обнаружены после других инфекций, включая коронавирусные инфекции. Кроме того, поскольку COVID-19 может вызывать критические заболевания у некоторых пациентов, могут возникнуть ОРДС и делирий, которые ранее были связаны с когнитивными нарушениями . Так, Расс и др. показали когнитивные нарушения у 23% пациентов с COVID-19 (в тяжелой 29% пациентов с COVID-19, 30% с умеренной и 3% с легкой степенью тяжести). Кроме того, ожидается заболевание, приводящее к гипоксемии с последствиями для памяти, поскольку гиппокамп чувствителен к низкой концентрации кислорода.
В большинстве отобранных исследований оценивались ранее госпитализированные пациенты или даже сами госпитализированные пациенты. Мы не можем исключить, что когнитивные нарушения были вызваны травмами, связанными с госпитализацией, бредом или даже оставшейся острой фазой заболевания или гипоксемией. Кроме того, Маклафлин и соавторы, оценили группу пациентов с COVID-19 с делирием и сравнил его с лицами без делирия в острой фазе. Все пациенты, участвовавшие в этом исследовании, были оценены четыре недели спустя с помощью шкалы TICS по телефону. Не было обнаружено существенных различий в отношении применяемого инструмента между группами. Другой возможной причиной, которая еще не нашла подтверждения в медицинской литературе, было прямое действие вируса. Такая прямая роль вируса не дает убедительных доказательств в исследованиях общих неврологических проявлений, оценивающих спинномозговую жидкость, или исследованиях вскрытия.
И наоборот, Дель Брутто и его коллеги оценивали только амбулаторных пациентов без предыдущей госпитализации и с легкой формой заболевания . В этом исследовании у пациентов была легкая форма COVID-19, не требующая госпитализации. До пандемии они наблюдались амбулаторно и регулярно проходили когнитивную оценку. Авторы оценили пациентов через шесть месяцев после появления симптомов в контрольной группе и выявили снижение на 4 пункта в MoCA, применявшемся к пациентам до пандемии.
Другие исследования указали на возможные причины COVID-19 связанных с этим когнитивных нарушений. Чжоу и др. оценивали выписанных пациентов с помощью шкал, применяемых с помощью цифровых устройств, выявляя снижение внимания пациентов, также связывая такие результаты с высокими маркерами воспаления. Это последнее открытие интересно, поскольку предыдущие данные указывают на возможную причинную роль воспаления микроглии и более позднего возникновения болезни Альцгеймера. Другой возможной причиной когнитивных нарушений ассоциированными с COVID-19 являются ишемические изменения, связанные с COVID-19, поскольку изменения в мозге указывают на риск когнитивных нарушений и деменции. Кроме того, повреждения эндотелия, описанные при COVID-19, могут ухудшать выведение метаболитов мозга, включая бета-амилоидные пептиды, которые участвуют в развитии болезни Альцгеймера.
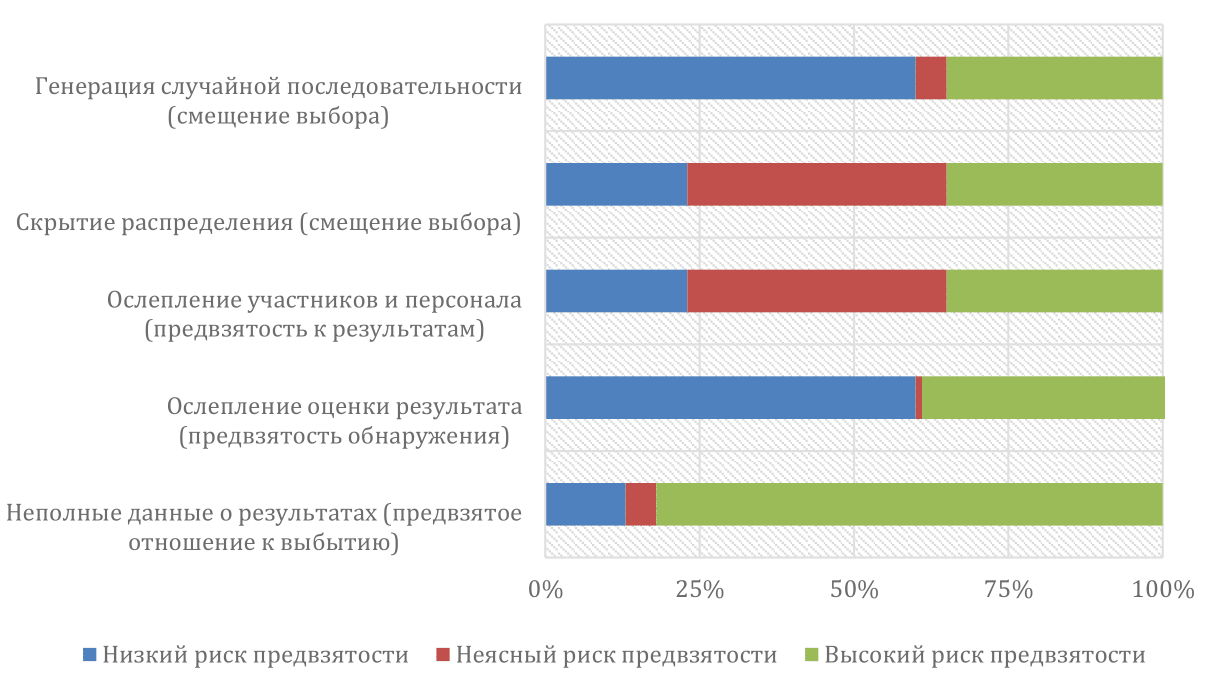
Рисунок 2 - График риска предвзятости
Примечание: просмотрите суждения авторов о каждом элементе риска предвзятости, представленные в процентах по всем включенным исследованиям
Это обзорное исследование имеет некоторые важные ограничения. Во-первых, в некоторых исследованиях не упоминается распространенность когнитивных нарушений. Кроме того, почти во всех исследованиях не проводились предыдущие когнитивные оценки пациентов. Кроме того, почти во всех исследованиях отсутствовала информация о подтипе когнитивных нарушений (например, MCI, AD, другие нейродегенеративные заболевания). Еще одним предостережением является то, что в большинстве исследований не было контрольных групп, что исключает прямое сравнение. Кроме того, не было возможности сравнить наиболее затронутые когнитивные области между исследованиями до и после 12 недель инфекции Covid-19. Другим потенциальным ограничением этого систематического обзора было широкое разнообразие используемых инструментов когнитивной оценки, влияющих на внешнюю валидность. Наконец, ни в одном исследовании, включенном в этот обзор, не использовалась полная когнитивная нейропсихологическая оценка, метод оценки «золотого стандарта». Эти ограничения сделали невозможным проведение мета-анализа.
С другой стороны, сильной стороной этого систематического обзора является его воспроизводимая и прозрачная процедура систематического обзора литературы. При публикации исследования протокол необходим для демонстрации ясности стратегии и снижения риска предвзятости. Эти результаты предоставляют доказательства для информирования, поддержки и настройки совместного принятия решений поставщиками медицинских услуг, заинтересованными сторонами и правительством. В этом смысле этот систематический обзор предоставляет соответствующие данные о влиянии COVID-19 на когнитивные функции пациентов для решения восполнить пробел в литературе и руководствоваться основными стратегиями, выявлять пациентов с когнитивными нарушениями (SCD, MCI и деменция) с назначением надлежащего лечения, когнитивной реабилитации и психообразования. Возможность когнитивных нарушений после заражения еще больше подчеркивает важность профилактических мер в отношении COVID-19.
Что касается будущих направлений, важно проводить клинические исследования с использованием контрольных групп, используя обширную нейропсихологическую оценку для определения наиболее затронутых когнитивных областей, используя визуализацию и биомаркеры спинномозговой жидкости (ликвора) для выявления нейродегенеративных заболеваний, таких как Болезнь Альцгеймера, чтобы выяснить специфические патофизиологические изменения, вызванные COVID-19. В идеале, люди с предшествующим нейрокогнитивным наблюдением, включая биомаркеры и предварительную когнитивную оценку, должны быть включены в будущие исследования. Аналогичным образом, включение пациентов с предшествующими когнитивными нарушениями имеет важное значение для оценки эволюции этих пациентов. Другой важной группой, подлежащей оценке, являются пациенты с низким уровнем образования, для чего необходимо собрать психометрические данные из этой популяции и оценить, оказывает ли низкое образование из-за низкого когнитивного резерва негативное влияние на когнитивные способности после заболевания COVID-19.
5. Заключение
В этом обзоре подчеркивается высокая частота когнитивных нарушений после COVID - 19 инфекции. Однако мы не смогли определить, соответствовали ли обнаруженные когнитивные нарушения умеренным когнитивным нарушениям или деменции с помощью данных отдельных исследований, и этот вопрос служит одной из целей будущих исследований, которые будут рассмотрены по этой теме.
