НОВАЯ ТЕХНОЛОГИЯ ПОЛУЧЕНИЯ [18F] ФЛЮМАЗЕНИЛА, РАДИОФАРМПРЕПАРАТА ДЛЯ РЕЦЕПТОРНЫХ ИССЛЕДОВАНИЙ МОЗГА МЕТОДОМ ПЭТ
Насирзадех М.1, Ваулина Д.Д.2 , Гомзина Н.А.3
1ORCID: 0000-0003-3486-2787, аспирант, Санкт-Петербургский государственный университет, Институт химии, 2ORCID: 0000-0003-1088-2396, младший научный сотрудник, 3ORCID: 0000-0002-4554-6125, кандидат химических наук, старший научный сотрудник, 2,3Федеральное государственное бюджетное учреждение науки Институт мозга человека им. Н.П. Бехтеревой Российской академии наук (ИМЧ РАН)
НОВАЯ ТЕХНОЛОГИЯ ПОЛУЧЕНИЯ [18F] ФЛЮМАЗЕНИЛА, РАДИОФАРМПРЕПАРАТА ДЛЯ РЕЦЕПТОРНЫХ ИССЛЕДОВАНИЙ МОЗГА МЕТОДОМ ПЭТ
Аннотация
Впервые показана принципиальная возможность использования метода твердофазной экстракции (ТФЭ) для получения [18F]флюмазенила ([18F]ФМЗ), радиолиганда для визуализации ГАМКА рецепторов методом позитронной эмиссионной томографии (ПЭТ). Проведено сравнение эффективности использования для выделения [18F]ФМЗ экспресс-метода ТФЭ на одноразовых картриджах и традиционной полупрепаративной ВЭЖХ. Разработана новая радиохимическая автоматизированная технология, которая позволяет получить в одном синтезе (53 мин) 2-5 клинических дозы [18F]ФМЗ с удельной активностью > 185 ГБк/мкмоль, с радиохимической чистотой >98 % и химическими примесями (нитромазенил)≤4 мкг/мл. Полученный препарат отвечает всем требованиям, предъявляемым Фармакопеей, и может быть рекомендован для использования в клинических ПЭТ исследованиях.
Ключевые слова: позитронная эмиссионная томография, радиофармпрепараты, радиолиганды, ГАМКА рецепторы, фтор-18, автоматизированный модуль синтеза, [18F]флюмазенил ([18F]ФМЗ), твердофазная экстракция.
Nasirzadeh М.1, Vaulina D.D.2 , Gomzina N.А.3
1ORCID: 0000-0003-3486-2787, Postgraduate Student, Saint-Petersburg State University, Institute of Chemistry, 2ORCID: 0000-0003-1088-2396, Junior researcher, 3ORCID: 0000-0002-4554-6125, PhD in Chemistry, Senior researcher, 2,3N. P. Bechtereva Institute of Human Brain, Russian Academy of Sciences, (IHB RAS)
A NOVEL TECHNOLOGY FOR PRODUCING OF [18F]FLUMAZENIL, RADIOPHARMACEUTICAL FOR BRAIN RECEPTORS STUDIES BY PET
Abstract
For the first time an express method of solid phase extraction (SPE) was proposed for producing of [18F]flumazenil ([18F]FMZ), a radioligand for visualization GABAA receptors by positron emission tomography (PET). Efficiencies of [18F]FMZ extraction by SPE on commercially available cartridges and by traditional semi-preparative HPLC were compared. Application of novel radiochemical automated technology allowed to obtain 2-5 clinical doses of radioligand in one production run (53 minutes). [18F]FMZ was produced with specific activity >185 GBq/µM, radiochemical purity >98 % and ≤ 4 µg/ml of nitromazenil residual amounts. The obtained preparation meets all Pharmacopoeia requirements and can be recommended for PET clinical applications.
Keywords: positron emission tomography, radiopharmaceuticals, radioligands, GABA receptors, fluorine-18, automated synthesis module, [18F] flumazenil ([18F] FMZ), solid-phase extraction.
Позитронная эмиссионная томография (ПЭТ) – метод ядерной медицины, позволяющий при использовании соответствующих радиофармпрепаратов (РФП) и фармакокинетических моделей их поведения в организме, количественно измерить параметры многих физиологических и биохимических процессов in vivo (перфузия, метаболизм, рецепторные и нейротрансмиттерные взаимодействия), обеспечивая тем самым точную диагностику онкологических, кардиологических, неврологических и психических заболеваний на ранних этапах. В качестве РФП используют биологически активные соединения, меченные короткоживущими радионуклидами с позитронным типом распада: 18F (Т ½ =109.7 мин),11C (Т ½ =20.4 мин) и др. При изучении нейрохимических процессов в центральной нервной системе (ЦНС) методом ПЭТ используют меченые соединения, специфично связывающиеся с отдельными типами рецепторов ЦНС (рецепторные радиолиганды). С помощью этих соединений получают ценную информацию о механизмах рецепторных взаимодействий и о плотности и распределении самих рецепторов в различных отделах мозга [1-4]. Большой интерес вызывают ПЭТ исследования ГАМК-эргической системы, реализующей биохимическое действие ГАМК (гамма-аминомасляной кислоты), основного тормозного нейромедиатора ЦНС [2,4]. Бензодиазепиновыми рецепторами (БЗР) называют участки (сайты) ГАМКА-рецепторов для связывания c бензодиазепинами. БЗР локализованы на мембранах нервных клеток и входят в состав ГАМКА-бензодиазепин-ионофорного комплекса, действие которого направлено на изменение устойчивости нервных клеток к возбуждающим сигналам. В частности, бензодиазепины, связываясь с БЗР, усиливают процессы торможения в ЦНС. Седативное действие бензодиазепинов нашло широкое применение в виде транквилизаторов, релаксантов, антиконвульсантов и снотворных препаратов. Центральные БЗР (цБЗР) играют ключевую роль в таких заболеваниях, как: эпилепсия, тревожные состояния, деменции, алкоголизм и др.
В ПЭТ в качестве РФП для определения плотности цБЗР используют меченые аналоги лекарственного средства флюмазенил (8-фтор-имидазо[1,5-a][1,4]бензодиазепин-3-карбоксил этиловый эфир), (рис. 1а). Флюмазенил обладает высокой аффинностью к цБЗР (Kd<5nM), является их полным антагонистом и применяется для снятия наркоза, вызываемого действием препаратов на основе бензодиазепинов [4]. В ИМЧ РАН в 2005 г был разработан метод получения [18F]флюмазенила ([18F]ФМЗ) (2, рис. 1б), меченного фтором-18 в нативную позицию молекулы флюмазенила, путем замещения на [18F]фторид нитрогруппы в молекуле нитромазенила (этил-5,6-дигидро-5-метил-8-нитро-6-оксо-4H-имидазо[1,5a][1,4]бензодиазепин-3-карбоксилат) (1) в условиях межфазного катализа криптандом К 2.2.2 (4,7,13,16,21,24-гексаоксо-1,10-диазабицикло [8.8.8]гексакозан) [5].
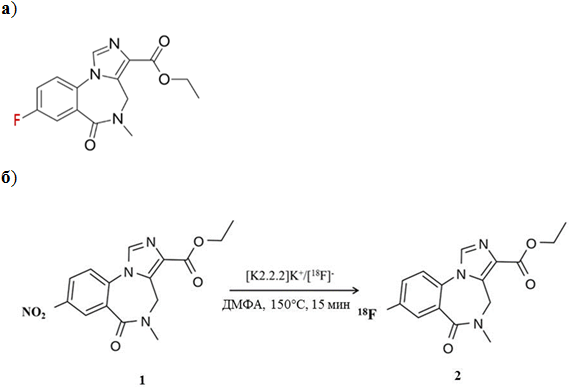
Рис. 1 – Получение [18F]ФМЗ по методу [5]
Радионуклид фтор-18 получают в циклотроне по ядерной реакции 18O(p,n)18F при облучении протонами мишени, заполненной водой, обогащенной по изотопу кислород-18 ([18O]H2O). Полученный фтор-18 стабилизируется в химической форме 18F-фторид-иона, который выделяют из мишенного материала сорбцией на анион-обменной смоле с последующим элюированием раствором, содержащим комплекс К 2.2.2 со щелочным металлом ([К 2.2.2]К+), для перевода в апротонный растворитель ДМФА, где и происходит реакция нуклеофильного замещения.
По методу [5] [18F]ФМЗ получают без добавления носителя, т.е. с очень высокой удельной активностью (> 37 ГБк/мкМоль), которая является одним из обязательных параметров радиолиганда для рецепторных исследований мозга. Поскольку при связывании с активными центрами рецептора носитель конкурирует с радиолигандом, это сказывается на качестве ПЭТ томограмм, а насыщение рецепторов может привести к нежелательным фармакологическим и даже нейротоксическим эффектам. Например, для полного насыщения цБЗР достаточно 15 мкг флюмазенила на 1 кг массы тела [6]. В случае «безносительного» [18F]ФМЗ необходимо контролировать оставшееся количество нитромазенила (1), поскольку и радиолиганд и предшественник имеют близкие физико-химические свойства и сродство к цБЗР.
До настоящего времени для выделения из реакционной смеси и последующей очистки [18F]ФМЗ для клинических исследований использовали метод полупрепаративной радио-ВЭЖХ. Длительная (30—40 мин) и трудоемкая ВЭЖХ процедура сопряжена с большими потерями радиоактивного продукта, радиохимический выход (РХВ) [18F]ФМЗ, выделенного из реакционной смеси с помощью ВЭЖХ, варьировал от 10 [7] до 0.4—1.1% [8] (с поправкой на распад). Столкнувшись с этой проблемой при разработке новой технологии получения [18F]ФМЗ, мы предложили использовать для ее решения альтернативный метод твердофазной экстракции (ТФЭ). В основу нового подхода была положена сорбция [18F]ФМЗ и 1 на микроколонке Oasis HLB 6cc («Waters»), заполненной сополимером N-винилпирролидона и дивинилбензола, с последующим разделением радиолиганда и более липофильного 1 путем фракционного элюирования водно-этанольными растворами возрастающей концентрации. Результаты показали, что неоптимизированный РХВ радиолиганда составил 8% (с поправкой на распад) при сокращении времени процедуры (по сравнению с ВЭЖХ) в 1.5 раза. [18F]ФМЗ был получен с удельной активностью > 37 ГБк/мкмоль, радиохимической чистотой > 97% и содержанием 1 ~ 1мкг/мл [9]. Эти исследования были выполнены на полуавтоматической экспериментальной системе синтеза (модуле), сконструированном в ИМЧ РАН, с начальной активностью [18F]фторида < 3.7 ГБк (100 мКи), поэтому активности препарата было недостаточно даже для одного рецепторного исследования мозга (0.2 ГБк). Для того чтобы добиться воспроизводимого выхода продукта, стандартизировать все этапы синтеза и полностью автоматизировать всю процедуру, а также избежать облучения персонала при работе с высокими уровнями активности фтора-18, необходимо было выбранный метод интегрировать в современные модули для получения РФП для ПЭТ. Одним из них является Tracerlab FX N Pro (GE Healthcare) – модуль для получения РФП путем нуклеофильного радиофторирования.
Для того, чтобы сравнить эффективность методов ВЭЖХ и ТФЭ в технологии получения [18F]ФМЗ, мы проводили на Tracerlab FX N Pro синтезы препарата с двумя разными схемами очистки (рис. 2), начиная при этом с одинаковой активности [18F]фторида (~ 30 ГБк). Значения параметров радиолиганда, полученного с использованием этих схем, представлены в таблице 1, значения, регламентированные Фармакопеей [10], приведены в скобках.
Таблица 1 - Сравнение методов выделения [18F]ФМЗ
| Параметры* | ТФЭ (n=7) | ВЭЖХ (n=3) |
| Радиохимический выход c поправкой на распад, % | 8.6±1 | 3-3.3 |
| Радиохимическая чистота (≥95), % | 98.6±1.1 | 99.5±0.5 |
| Общее время синтеза, мин | 53 | 80 |
| Удельная активность (≥30), ГБк/мкМ | 185-555 | 370-740 |
| Примесь нитромазенила, мкг/мл | 3.1±0.9 | ≤0.5 |
*- Контроль качества [18F]ФМЗ выполняли методом ВЭЖХ хроматографии: Dionex ВЭЖХ система с детекторами по радиоактивности (гамма-счетчик) и УФ (λ=254 nm), колонка ACE C-18 HL (250×4.6 мм) (Aberdeen). Элюент: 0.01 M H3PO4/MeCN (v/v=3/1), скорость подачи: 1.5 мл/мин.
Как видно из рисунка 2, перед введением реакционной смеси в петлю ВЭЖХ-колонки проводили предварительную очистку на картридже с кремнийорганическим сорбентом (С18) для удаления гидрофильных радиоактивных примесей. После ВЭЖХ процедуры для удаления органического растворителя (ацетонитрила) из фракции, содержащей продукт, использовали сорбцию [18F]ФМЗ на втором картридже С18 с
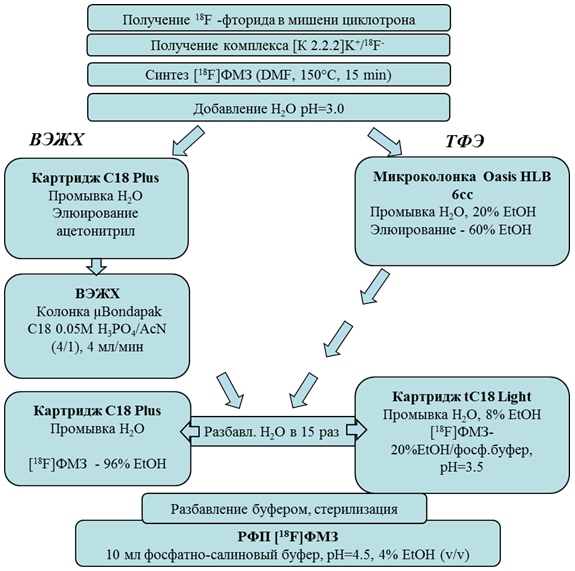
Рис. 2 – Технологическая схема получения [18F]ФМЗ с выделением и очисткой методами а) ВЭЖХ и б) ТФЭ
последующим элюированием этанолом. Видно, что метод ВЭЖХ является трехступенчатой длительной процедурой, с большими потерями активности на ВЭЖХ-колонке; РХВ [18F]ФМЗ составил ~ 3% с поправкой на распад, общее время синтеза – 80 мин (таблица 1). Активность продукта была невысока – около 370 MБк, но вполне достаточна для одной клинической дозы (180 МБк). При этом продукт был получен с высокой удельной активностью, с радиохимической чистотой ~100% и с ничтожно малым содержанием 1. В синтезах с ТФЭ методом выделения целевого продукта РХВ составил 8-10 % (с поправкой на распад), а активности радиолиганда (750-1100 МБк) хватило для получения 2-5 клинических доз. Значения параметров качества радиолиганда при этом отвечали фармакопейным требованиям.
Однако содержание 1 (2-4 мкг/мл) было в несколько раз больше, чем в опытах с использованием ВЭЖХ процедуры (<0.5 мкг/мл). Поскольку фармакопейных норм для остаточного количества 1 в препарате [18F]ФМЗ нет, то для доказательства допустимой нормы нитромазенила ≤4мкг/мл мы воспользовались результатами доклинических исследований на безопасность РФП [18F]ФМЗ для ПЭТ, проведенными вместе с Научно-исследовательским Институтом гриппа МЗ РФ на группах аутбредных крыс (30 самок и 30 самцов). Исследования показали, что однократное введение [18F]ФМЗ в дозе эквивалентной человеческой и в 30 раз её превышающей, не вызвало изменений в состоянии опытных животных в течение 14 дней. Структура поведенческого паттерна «открытое поле» у животных из всех экспериментальных групп соответствовала таковой у здоровых белых крыс. У всех опытных животных отмечалась положительная динамика массы тела, значения температуры тела не выходили за пределы физиологической нормы. Достоверные различия в величине внутренних органов и головного мозга опытных и контрольных животных не были выявлены. Гистологические исследования также не выявили признаков изменений во внутренних органах крыс самцов и самок, получавших как плацебо, так и препарат.
Метод твердофазной экстракции был положен в основу создания новой технологии получения флюмазенила, меченного 18F, первого в России радиолиганда для рецепторных исследований мозга методом ПЭТ.
Список литературы / References
- Ametamey, S.M. Molecular imaging with PET/ S. M. Ametamey, M. Honer, P.A. Schubiger // Chem.Rev. – 2008. – V. 108. – P.1501–1516.
- Sigel, E. Structure, function and modulation of GABAAreceptors / E.Sigel, M.E. Steinmann // J. Biol. Chem. - 2012. – V.287. – P.40224-40231.
- Chakravarty, R. Positronemissiontomographyimage-guideddrugdelivery: current statusand future perspectives / R.Chakravarty, H.Hong, W.Cai // Mol. Pharmaceutics. – 2014. – V. 11. – P. 3777−3797.
- Andersson, J.D. PET radioligands targeting the brain GABAA/benzodiazepine receptor complex / J. D. Andersson, C. Halldin//J. Label Compd. Radiopharm. – 2013. – V. 56 –P.196–206.
- Ryzhikov, N. Preparation of high specific radioactivity [18F]flumazenil and its evaluation in cynomolgus monkey by positron emission tomography / N.N. Ryzhikov, N. Seneca, R.N. Krasikova [et al.] // Nucl. Med. Biol. – 2005. –V. 32. –P. 109-116.
- Delforge, J. Quantitation of Benzodiazepine Receptors in Human Brain Using the Partial Saturation Method / J. Delforge, L. Spelle, B. Bendriem [et al.] // J. Nucl. Med. – 1996. – V. 37. – P. 5-11.
- Odano, I. [18F]Flumazenil binding to central benzodiazepine receptor studies by PET - Quantitative analysis and comparisons with [11C]flumazenil/ I. Odano, C. Halldin, P. Karlsson [et al.] // Neuroimage. – 2009.– V. 45. – P. 891-902.
- Moon, B. S. Facile aromatic radiofluorination of [18F]flumazenil from diaryliodonium salts with evaluation of their stability and selectivity / B. S. Moon, H. S. Kil, J. H. Park [et al.] // Org. Biomol. Chem. – 2011. – V. 9. – P. 8346-8355.
- Nasirzadeh, M. A novel approach to the synthesis of [18F]flumazenil, a radioligand for PET imaging of central benzodiazepine receptors / M. Nasirzadeh, D. D. Vaulina, O. F. Kuznetsova, N. A. Gomzina // Russ. Chem. Bull. Int. Ed.- 2016 – V. 65. – P. 794-800.
- Radiopharmaceutical preparation, in: European Pharmacopoeia. 8.0, European Directorate for the Quality of the Medicines; Strasbourg, 2014, pp. 759-763.
