РАННЯЯ ДИАГНОСТИКА ВНУТРИБРЮШНЫХ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ В ЭКСПЕРИМЕНТАЛЬНОЙ ХИРУРГИИ
РАННЯЯ ДИАГНОСТИКА ВНУТРИБРЮШНЫХ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ В ЭКСПЕРИМЕНТАЛЬНОЙ ХИРУРГИИ
Аннотация
Целью данного исследования является разработка способа ранней диагностики внутрибрюшных послеоперационных осложнений у лабораторных животных в эксперименте.
Проведено экспериментальное исследование на крысах линии «Стандарт» (n=24, масса 500 г). Разработано устройство для ранней диагностики внутрибрюшных послеоперационных осложнений, содержащее силиконовый катетер с дренирующим просветом и блок регистрации. В дистальной части катетера расположены перфорационные отверстия, белый светодиод (400–700 нм) и кремниевый фотодиод под углом 45° к продольной оси. Блок регистрации включает микроконтроллер и три светодиодных индикатора (зелёный — норма, жёлтый — снижение фототока на 25–40%, красный — снижение более 40%). Катетер имплантировали в брюшную полость после лапаротомии, проводили индивидуальную калибровку (2–3 минуты). Моделировали осложнения введением 2,5 мл патологического содержимого (кровь, жёлчь, кишечные массы). Контрольная группа получала физиологический раствор. Наблюдение составляло 72 часа с последующим гистологическим исследованием.
Устройство обеспечило регистрацию снижения фототока при попадании патологического содержимого в зону оптической оси за 35–50 минут до появления клинических признаков перитонита (тахикардия, снижение артериального давления, вялость). Пороги детекции составили: кровь — 0,1 мл/100 мл, жёлчь — 0,05 мл/100 мл, кишечное содержимое — 0,2 мл/100 мл. Жёлтый индикатор активировался при снижении фототока на 25–40%, красный — при снижении более 40%. В контрольной группе ложноположительных срабатываний не зафиксировано (изменения фототока <5%). Дренирующая функция катетера сохранялась на всём протяжении эксперимента.
Разработанный способ позволяет осуществлять раннюю диагностику внутрибрюшных послеоперационных осложнений у лабораторных животных за 35–50 минут до манифестации клинических симптомов. Цветовая индикация обеспечивает дифференциацию степени загрязнения брюшной полости. Устройство обладает высокой специфичностью, не реагируя на оптически прозрачные жидкости, и сохраняет дренирующую функцию, что делает его пригодным для одновременного мониторинга и дренирования в экспериментальной хирургии.
1. Введение
Осложнения послеоперационного периода в абдоминальной хирургии остаются одной из наиболее актуальных проблем современной медицины, значительно влияющих на показатели летальности и качество жизни пациентов . Согласно классификации Clavien-Dindo, тяжелые внутрибрюшные осложнения, такие как несостоятельность анастомозов, перитонит и внутрибрюшные абсцессы, требуют своевременной коррекции, поскольку задержка в диагностике неизбежно ведет к прогрессированию системного воспалительного ответа и полиорганной недостаточности . В экспериментальной хирургии моделирование данных патологических процессов на лабораторных животных является ключевым этапом для отработки новых лечебно-диагностических алгоритмов перед их внедрением в клиническую практику . Однако проведение экспериментов сопряжено с этическими обязательствами по минимизации страданий животных (принципы 3R), что требует разработки высокочувствительных методов мониторинга, позволяющих выявлять осложнения на доклинической стадии без необходимости преждевременного усыпления подопытных особей . Традиционные методы наблюдения, включающие визуальную оценку поведения и веса, обладают низкой специфичностью и часто позволяют диагностировать патологию лишь на терминальных стадиях, что искажает результаты исследования и повышает вариабельность данных .
Для ранней диагностики внутрибрюшных послеоперационных осложнений в текущей практике используют комплексный подход, который включает клинический осмотр, лабораторные анализы и инструментальные методы. Важно своевременно выявить осложнения, так как несвоевременная диагностика может привести к промедлению с повторным вмешательством.
В литературе описан способ экспресс-диагностики рецидива гастродуоденального кровотечения (ГДК) , основанный на установке пациенту назогастрального зонда и исследовании желудочного содержимого. Методика предполагает приготовление серий разведений содержимого желудка с дистиллированной водой (1:1, 1:2 и 1:3) и последовательное пропускание их через проточный электрод джоульметрического прибора. При подаче тока 0,01 мА в течение менее 6 секунд строятся графики зависимости изменения потенциала во времени, по которым оценивается динамика вольтамперных характеристик. Диагностическим критерием служит показатель работы тока: значение более 20 Дж свидетельствует об отсутствии рецидива ГДК, тогда как 20 Дж и менее указывает на его наличие.
Однако данный способ обладает рядом существенных ограничений, снижающих его клиническую применимость, особенно в эксперименте. Инвазивная процедура установки назогастрального зонда сопряжена с риском аспирации и дополнительным стрессом для животного, что недопустимо согласно современным биоэтическим нормам . Многоэтапная подготовка образца делает метод трудоёмким и не соответствующим заявленному «экспресс»-статусу. Критически важным недостатком является отсутствие физиологического обоснования порогового значения 20 Дж, а также игнорирование влияния рН биологических сред, слизи и лекарственных препаратов на электропроводность, что может приводить к ложноположительным и ложноотрицательным результатам. Способ не позволяет локализовать источник патологии и не имеет подтверждённых данных о чувствительности и специфичности в сравнении с «золотым стандартом» визуализации .
Известен также способ ранней диагностики рецидива желудочно-кишечного кровотечения с помощью зонда-детектора , который предполагает использование оптической системы внутри желудочного катетера, регистрирующей помутнение среды при появлении крови. Однако данный способ неприменим для диагностики внутрибрюшных осложнений в эксперименте, поскольку патологическое содержимое (экссудат, гной, кровь) в перитонеальной полости распределяется диффузно и не может быть надёжно детектировано отражательной оптической схемой, рассчитанной на локальную среду полого органа. Кроме того, конструкция зонда-детектора не совмещает дренирующую функцию с возможностью мониторинга, что ограничивает её использование в послеоперационном периоде после лапаротомных вмешательств у мелких лабораторных животных.
Таким образом, анализ существующих методов показывает отсутствие универсального, малоинвазивного и высокочувствительного инструмента для мониторинга состояния брюшной полости в экспериментальной хирургии. Существующие решения адаптированы преимущественно для клинической практики на человеке и не учитывают анатомо-физиологические особенности лабораторных животных, а также специфические требования к послеоперационному ведению в условиях вивария. Несовершенство методов контроля качества эксперимента приводит к росту отсева животных и снижению воспроизводимости научных данных.
В связи с этим целью исследования стала разработка способа ранней диагностики внутрибрюшных послеоперационных осложнений у лабораторных животных в эксперименте, который позволит повысить точность мониторинга, снизить летальность подопытных животных и оптимизировать использование биологических моделей в хирургических исследованиях.
2. Методы и принципы исследования
Проведенное авторским коллективом экспериментальное исследование осуществляли помощью разработанного авторами устройства для ранней диагностики внутрибрюшных послеоперационных осложнений , которое содержит силиконовый катетер с дренирующим просветом и блок регистрации (см. рис. 1). В стенках катетера выполнены перфорационные отверстия со стороны дистальной части (напротив друг друга по три перфорационных отверстия), после которых, напротив друг друга, установлены белый светодиод (с длиной волны излучения 400–700 нм) и кремниевый фотодиод под углом 45° к продольной оси катетера, обеспечивая пересечение световым потоком дренирующего просвета в области перфорационных отверстий. Белый светодиод (400–700 нм) был выбран на основании предварительных спектрофотометрических исследований in vitro. Проведено сравнение монохроматических источников (синий 450 нм, зелёный 525 нм, красный 650 нм) с белым светодиодом при детекции крови, жёлчи и кишечного содержимого. Белый спектр обеспечил наибольшую чувствительность за счёт одновременной регистрации поглощения в синей области (билирубин) и рассеяния на форменных элементах (гемоглобин, взвешенные частицы). Разница в чувствительности составила 15–20% в пользу белого источника (p<0,05). Технические характеристики оптической системы: Белый светодиод: мощность 20 мВт, длина волны 400-700 нм, угол излучения 120°. Кремниевый фотодиод: модель BPW34 (или укажите фактическую), чувствительность 0,6 А/Вт при 550 нм, площадь активной зоны 7,5 мм², темновой ток <2 нА. Расстояние между излучателем и детектором: 8 мм. Угол установки фотодиода: 45° к продольной оси катетера. Белый светодиод и кремниевый фотодиод подключены гибкими проводниками, через герметичный узел вывода проводников 6 в проксимальной части катетера к блоку регистрации.
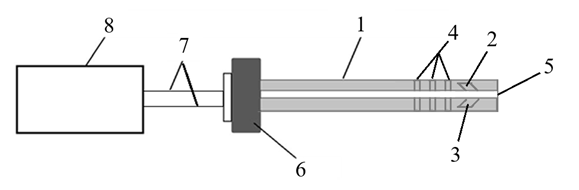
Рисунок 1 - Устройство, с помощью которого осуществляется способ:
1 – катетер; 2 – белый светодиод; 3 – кремниевый фотодиод; 4 – перфорационные отверстия; 5 – дренирующий просвет; 6 – герметичный узел вывода проводников; 7 – гибкий проводник; 8 – блок регистрации
Примечание:
Катетер изготавливают из платинового силикона методом литья под давлением с формированием дренирующего просвета. Перфорационные отверстия расположены с шагом 5 мм.
Катетер устанавливают в брюшную полость после операции на органах брюшной полости у лабораторных животных. Исследователь активирует устройство и в течение 2–3 минут кремниевый фотодиод фиксирует базовый уровень фототока от белого светодиода при отсутствии патологического содержимого; этот уровень сохраняется в памяти микроконтроллера и служит индивидуальной калибровочной точкой для данного животного. После завершения калибровки зелёный индикатор блока регистрации загорается, подтверждая нормальное состояние системы и отсутствие патологического содержимого в брюшной полости. В дальнейшем при проникновении в брюшную полость даже минимальных объёмов патологического содержимого (крови, жёлчи или кишечных масс) оно поступает через перфорационные отверстия непосредственно в зону оптической оси, вызывая рассеяние и поглощение света за счёт изменения оптической плотности среды; кремниевый фотодиод фиксирует снижение интенсивности светового потока, при снижении фототока на 25–40% активируется жёлтый индикатор (указывающий на умеренное загрязнение брюшной полости), при снижении более 40% — красный индикатор (указывающий на сильное загрязнение брюшной полости), требующий немедленного вмешательства. При этом зелёный индикатор гаснет, визуально сигнализируя об отклонении от нормы.
Катетер удаляют из брюшной полости после выявления патологического содержимого и принятия мер по устранению осложнений.
Для демонстрации работоспособности устройства, крысам линии «Стандарт» (n=24) устанавливали катетер на период проведения эксперимента.
Время нахождения катетера в организме животного определялось продолжительностью эксперимента. В данном случае катетер находился 72 часа и потом был взят материал для гистологического исследования, что достаточно по клиническим рекомендациям и для человека, и этого достаточно для: калибровки устройства; моделирования осложнения (введения патологического содержимого); фиксации срабатывания индикаторов; подтверждения биосовместимости материалов.
2.1. Алгоритм работы устройства в эксперименте
Катетер имплантируют в брюшную полость крысы под наркозом через прокол брюшной стенки. Перфорационные отверстия ориентируют в сторону брюшной полости.
В первые 2–3 минуты после установки активируют устройство. Микроконтроллер фиксирует базовый уровень фототока и сохраняет его как калибровочную точку, после чего зелёный индикатор блока регистрации активируется, подтверждая нормальное состояние системы у животного.
Далее в брюшную полость вводят патологическое содержимое (кровь, жёлчь или кишечное содержимое (массы)) в контролируемых объёмах. Устройство фиксирует снижение фототока и активирует соответствующий индикатор: при снижении на 25–40% загорается жёлтый индикатор, при снижении более 40% – красный, при этом зелёный индикатор гаснет.
После фиксации всех параметров и забора биоматериала для гистологического исследования катетер извлекают, животное эвтаназируют в соответствии с этическими стандартами.
3. Основные результаты
В рамках исследования, была проведена экспериментальная апробация на лабораторных животных (крысы линии «Стандарт», n = 24), которая показала, что использование заявляемого устройства обеспечивает регистрацию снижения фототока, соответствующего попаданию патологического содержимого в зону оптической оси за 35–50 минут до появления клинических признаков, характерных для перитонита (увеличение объёма свободной жидкости в брюшной полости, снижение артериального давления, тахикардия, вялость и снижение двигательной активности у лабораторных животных). Дренирующая функция устройства сохранялась на всём протяжении эксперимента.
3.1. Примеры осуществления способа
Примечание: в экспериментах использовались лабораторные животные – крысы, породы стандарт, массой 500 г.
Стандартная доза инстилляции во всех экспериментальных группах составляла 2,5 мл жидкости — объём, соответствующий 50% от максимально допустимого, согласно учебному пособию Титовой А.А. , где на стр. 41-42 в таблице 6 прописаны максимально допустимые объемы введения экспериментальных веществ лабораторным животным, конкретно внутрибрюшинно — 10 мл/кг, соответственно для крысы массой 500 г (0,5 кг) максимальный объём = 10 мл/кг × 0,5 кг = 5,0 мл. Вводимая доза также согласуется с учебно-методическим пособием Онищенко Г.Г. , где прописано, что «Внутрибрюшинно можно вводить крысам до 5 мл жидкости».
Примечание: концентрации патологического содержимого для первых трех экспериментов — получены при калибровочных испытаниях в стеклянных фотометрических кюветах объёмом 100 мл и адаптированы для эксперимента in vivo путём приготовления инстиллята с сохранением пропорций. Абсолютные объёмы патологического содержимого в 2,5 мл инстиллята составляли: кровь — 0,0025 мл, жёлчь — 0,00125 мл, кишечное содержимое — 0,005 мл. Таким образом, калибровочные испытания in vitro в стандартных стеклянных фотометрических кюветах подтвердили возможность надёжной детекции крови при концентрации от 0,1 мл на 100 мл физиологического раствора, жёлчи — от 0,05 мл на 100 мл (что обусловлено высоким коэффициентом поглощения билирубина в синей области спектра), кишечного содержимого — от 0,2 мл на 100 мл (обусловлено рассеянием света на взвешенных частицах).
3.1.1. Пример 1
Методика эксперимента. Катетер имплантировали в брюшную полость крысы линии «Стандарт» через прокол брюшной стенки под наркозом. Перфорационные отверстия ориентировали в сторону брюшной полости. В течение первых 2 минут после установки устройство автоматически фиксировало базовый уровень фототока от белого светодиода и сохраняло его в памяти микроконтроллера как индивидуальную калибровочную точку, после чего зелёный индикатор блока регистрации 8 активировался, подтверждая нормальное состояние системы.
Моделирование осложнения. В брюшную полость вводили 2,5 мл жидкости, содержащей кровь в концентрации 0,1 мл на 100 мл физиологического раствора (что соответствует порогу детекции, установленному при калибровочных испытаниях in vitro в фотометрических кюветах). Физический механизм детекции: комбинированный эффект поглощения света гемоглобином и рассеяния на форменных элементах крови.
Результаты. Кремниевый фотодиод зафиксировал снижение интенсивности светового потока на 30% после поступления крови через перфорационные отверстия в зону оптической оси. Снижение фототока находилось в диапазоне 25–40%, что привело к активации жёлтого индикатора (умеренное загрязнение), при этом зелёный индикатор гаснет, визуально подтверждая отклонение от нормы. Клинические признаки перитонита (снижение артериального давления, тахикардия, вялость) появились через 42 минуты после регистрации снижения фототока. Дренирующая функция катетера сохранялась в полном объёме.
3.1.2. Пример 2
Методика эксперимента. Катетер устанавливали в брюшную полость крысы линии «Стандарт» аналогичным образом. В течение первых 2,5 минут после установки устройство автоматически фиксировало базовый уровень фототока от белого светодиода и сохраняло его в памяти микроконтроллера как индивидуальную калибровочную точку, после чего зелёный индикатор блока регистрации 8 активировался.
Моделирование осложнения. В брюшную полость вводили 2,5 мл жидкости, содержащей жёлчь в концентрации 0,05 мл на 100 мл физиологического раствора, что соответствует порогу детекции, обусловленному высоким коэффициентом поглощения билирубина в синей области спектра белого светодиода.
Результаты. При поступлении жёлчи через перфорационные отверстия в зону оптической оси кремниевый фотодиод зафиксировал снижение фототока на 46% вследствие интенсивного поглощения света билирубином. Данное снижение превысило порог в 40%, что привело к активации красного индикатора, требующего немедленного вмешательства, при этом зелёный индикатор гаснет. Сигнал о наличии патологического содержимого был зарегистрирован за 38 минут до появления объективных клинических признаков перитонита. Дренирующая функция устройства сохранялась в полном объёме.
3.1.3. Пример 3
Методика эксперимента. Катетер имплантировали в брюшную полость крысы линии «Стандарт» через прокол брюшной стенки. Базовый уровень фототока фиксировали в течение первых 3 минут работы устройства и сохраняли в памяти микроконтроллера, после чего зелёный индикатор блока регистрации 8 активировался.
Моделирование осложнения. В брюшную полость вводили 2,5 мл жидкости, содержащей кишечное содержимое в концентрации 0,2 мл на 100 мл физиологического раствора, что соответствует минимальному порогу детекции, обусловленному рассеянием света на взвешенных частицах.
Результаты. При проникновении кишечных масс через перфорационные отверстия в зону оптической оси кремниевый фотодиод зафиксировал снижение интенсивности светового потока на 37% вследствие рассеяния света на взвешенных частицах. Снижение фототока находилось в диапазоне 25–40%, что привело к активации жёлтого индикатора (умеренное загрязнение), при этом зелёный индикатор гаснет. Регистрация патологического содержимого произошла за 45 минут до появления клинических признаков перитонита (увеличение объёма свободной жидкости в брюшной полости, снижение артериального давления, тахикардия, вялость). Дренирующая функция катетера сохранялась на всём протяжении эксперимента.
3.2. Общее заключение по экспериментальным примерам
Во всех трёх случаях устройство продемонстрировало способность к ранней детекции патологического содержимого в брюшной полости за 35–50 минут до появления клинических признаков перитонита. Активация цветовых индикаторов (жёлтого при снижении фототока на 25–40%, красного при снижении более 40%) позволяла дифференцировать степень загрязнения и своевременно принимать решение о необходимости хирургического вмешательства, при этом зелёный индикатор гаснет, подтверждая отклонение от нормы. Дренирующая функция катетера сохранялась на всём протяжении наблюдения, что подтверждает его пригодность для одновременной диагностики и дренирования брюшной полости.
3.3. Пример 4. Контрольный эксперимент: введение физиологического раствора (отсутствие патологического загрязнения)
Методика эксперимента. Катетер имплантировали в брюшную полость крысы линии «Стандарт» через прокол брюшной стенки под наркозом. Перфорационные отверстия ориентировали в сторону брюшной полости. В течение первых 3 минут после установки устройство фиксировало базовый уровень фототока от белого светодиода и сохраняло его в памяти микроконтроллера как индивидуальную калибровочную точку, после чего зелёный индикатор блока регистрации 8 активировался, подтверждая нормальное состояние системы. Базовый уровень устанавливался в условиях прозрачной серозной жидкости брюшной полости, оптические свойства которой близки к физиологическому раствору.
Моделирование контрольной ситуации. В брюшную полость вводили 2,5 мл стерильного физиологического раствора (объём, эквивалентный объёмам патологических жидкостей в основных экспериментальных группах). Физиологический раствор представляет собой прозрачную среду без взвешенных частиц и хромофоров, не вызывающую значимого рассеяния или поглощения света в видимом спектре.
Результаты. При поступлении физиологического раствора через перфорационные отверстия в зону оптической оси кремниевый фотодиод не зафиксировал статистически значимого снижения интенсивности светового потока. Изменения фототока не превышали 5% от базового уровня, что соответствует фоновому шуму измерительной системы. Цветовые индикаторы (жёлтый и красный) не активировались на всём протяжении наблюдения, при этом зелёный индикатор продолжал гореть, подтверждая отсутствие патологического содержимого. Клинические признаки перитонита в течение 72 часов наблюдения не развивались.
Физическое обоснование. Физиологический раствор (0,9% NaCl) является оптически прозрачной средой с низким коэффициентом рассеяния и отсутствием хромофоров в видимом диапазоне спектра. В отличие от крови (поглощение гемоглобином), жёлчи (поглощение билирубином) и кишечного содержимого (рассеяние на взвешенных частицах), физиологический раствор не изменяет оптическую плотность среды в измеримой степени, что подтверждает специфичность работы устройства — оно реагирует именно на патологическое содержимое, а не на любую интраабдоминальную жидкость.
Таким образом, контрольный эксперимент подтвердил отсутствие ложноположительных срабатываний устройства при поступлении в брюшную полость оптически прозрачной жидкости, что свидетельствует о высокой специфичности метода детекции патологического содержимого. В контрольной группе зелёный индикатор продолжал гореть на протяжении всего наблюдения, подтверждая отсутствие отклонений от нормы.
4. Обсуждение
Полученные в ходе экспериментального исследования данные свидетельствуют о принципиальной возможности и высокой эффективности предложенного устройства для ранней диагностики внутрибрюшных послеоперационных осложнений. Ключевым результатом работы стало подтверждение способности оптической системы регистрировать появление патологического содержимого в брюшной полости за 35–50 минут до манифестации клинических признаков перитонита. Этот временной интервал имеет критическое значение в хирургии, так как позволяет инициировать терапевтические или хирургические вмешательства на этапе локального воспаления, предотвращая развитие системного воспалительного ответа и полиорганной недостаточности, которые традиционно ассоциированы с высокой летальностью.
В сравнении с существующими методами мониторинга, предложенное устройство демонстрирует ряд существенных преимуществ. Во-первых, в отличие от традиционного клинического наблюдения, которое фиксирует осложнения лишь на стадии декомпенсации (вялость, гемодинамические сдвиги), непрерывный оптический контроль обеспечивает объективизацию данных в реальном времени. Во-вторых, по сравнению с описанными в литературе методами экспресс-диагностики, такими как джоульметрия желудочного содержимого , , разработанная методика менее инвазивна в контексте экспериментальной модели. Установка катетера производится одномоментно с основной операцией, что исключает дополнительный стресс для животного, связанный с повторными манипуляциями (например, установкой назогастрального зонда), и соответствует принципам биоэтики (3R — Reduction, Refinement, Replacement) , .
Важным аспектом является специфичность метода, подтвержденная в контрольном эксперименте. Отсутствие ложноположительных срабатываний при введении физиологического раствора доказывает, что устройство реагирует именно на изменение оптической плотности среды, обусловленное наличием хромофоров (гемоглобин, билирубин) или взвешенных частиц (кишечное содержимое, гной), а не на оптически прозрачные физиологические жидкости (серозный выпот, физиологический раствор). Устройство может реагировать на любые среды с изменённой оптической плотностью, включая гной, фибриновые наложения, геморрагический экссудат. Дальнейшие исследования требуются для оценки реакции на другие патологические жидкости. Это решает проблему дифференциации послеоперационного серозного выпота от патологического экссудата, что является частой диагностической дилеммой в послеоперационном периоде. Цветовая индикация (зеленый/желтый/красный) упрощает интерпретацию данных персоналом вивария, снижая влияние человеческого фактора и позволяя быстро принимать решения о необходимости эвтаназии или спасительной операции, что повышает воспроизводимость научных данных.
5. Заключение
Таким образом, проведённые эксперименты на крысах линии «Стандарт» доказали, что способ ранней диагностики внутрибрюшных послеоперационных осложнений у лабораторных животных обеспечивает раннюю детекцию патологического содержимого (крови, жёлчи или кишечных масс) в брюшной полости за 35-50 минут до появления клинических признаков перитонита, дифференцирует степень изменения оптических свойств перитонеальной жидкости посредством цветовой индикации (жёлтый индикатор при снижении фототока на 25–40%, красный — при снижении более 40%), при этом зелёный индикатор гаснет, визуально подтверждая отклонение от нормы. Система сохраняет дренирующую функцию на всём протяжении наблюдения и обладает высокой специфичностью, не реагируя на оптически прозрачные жидкости (физиологический раствор), что подтверждается сохранением горящего зелёного индикатора в контрольных условиях.
