ИССЛЕДОВАНИЕ ОКИСЛИТЕЛЬНЫХ МОДИФИКАЦИЙ БЕЛКОВ В ТКАНЯХ МОЗГА КРЫС В УСЛОВИЯХ СТРЕСС-ИНДУЦИРОВАННОЙ ДЕПРЕССИИ
ИССЛЕДОВАНИЕ ОКИСЛИТЕЛЬНЫХ МОДИФИКАЦИЙ БЕЛКОВ В ТКАНЯХ МОЗГА КРЫС В УСЛОВИЯХ СТРЕСС-ИНДУЦИРОВАННОЙ ДЕПРЕССИИ
Аннотация
В настоящее время депрессивное расстройство диагностируется у более чем у 350 миллионов человек по всему миру, а хронический стресс рассматривается как одна из ведущих причин его формирования. Стресс нарушает окислительно-восстановительный баланс клетки, что приводит к возникновению оксидативного стресса. Мозг, благодаря своей функциональной и метаболической активности, особенно подвержен влиянию оксидативного стресса. Окислительная модификация белков считается одним из ранних и надёжных маркеров оксидативного стресса.
Цель нашего исследования — изучение окислительных модификаций белков в тканях мозга крыс в условиях стресс-индуцированной депрессии. Работа проводилась на 60 крысах-самцах линии Wistar шестимесячного возраста. Для моделирования депрессивного состояния у животных использовали модель «социального» стресса. Все животные были разделены поровну по принципу рандомизации на 2 группы: 1 группа — интактные животные; 2 группа — животные, у которых моделировали депрессивное состояние. Количественное определение окислительных модификаций белков в тканях мозга крыс проводили методом иммуноферментного анализа с помощью готовых наборов реагентов Rat AOPP ELISA Kit (Cusabio, Китай). Продукты реакции регистрировали на двух длинах волн 270 нм и 363 нм, что соответствует карбонильным производным белков с гидрофильными и гидрофобными аминокислотными остатками. Цифровой материал всех экспериментов подвергали статистической обработке с помощью параметрических и непараметрических методов анализа.
Установлено, что крысы-агрессоры и жертвы характеризуются разной концентрацией окисленных модификаций белков в различных структурах мозга. Исследование процессов свободнорадикального окисления белков в различных структурах мозга в комплексе с оценкой поведенческих реакций вносит вклад в понимание патогенеза депрессии через нарушение нейронной сигнализации, пластичности и метаболического баланса.
1. Введение
Депрессивное расстройство диагностируется у более чем у 350 миллионов человек по всему миру, хронический стресс рассматривается как одна из ведущих причин его формирования , . Известно, что стресс нарушает окислительно-восстановительный баланс клетки и это приводит к возникновению оксидативного стресса, сопровождающего различные патологические состояния, в том числе расстройства психики, способствующего ускоренному старению и деструктивным изменениям различных систем организма, в том числе нервной системы . С другой стороны, оксидативный стресс можно рассматривать как участника адаптивных процессов организма к стрессорным условиям, так как он активирует пролиферацию, дифференциацию и апоптоз клеток .
Мозг, благодаря своей функциональной и метаболической активности, особенно подвержен влиянию оксидативного стресса. Установлено, что оксидативный стресс играет важную роль в нейродегенеративных психопатологиях и, в частности, в посттравматическом стрессовом расстройстве и депрессии . Изучение окислительно-восстановительных в тканях мозга является важным для оценки дальнейшего развития патологий и предупреждения нейродегенеративных заболеваний при воздействии стресса.
Как правило, при изучении функционирования прооксидантных и антиоксидантных систем в тканях исследуются процессы перекисного окисления липидов, а не окислительная модификации белков (ОМБ), хотя это один из ранних и надёжных маркеров окислительного стресса .
Белкам и продуктам их метаболизма, в частности продуктам свободнорадикального окисления принадлежит центральная роль в работе сигнальных систем клетки. Свободнорадикальное окисление белков можно рассматривать как механизм внутренней модуляции и передачи информации как от внешней среды к внутриклеточным системам и обратно .
Многочисленные исследования демонстрируют, что при большинстве патологических состояний именно белки выступают более эффективными ловушками активных форм кислорода, чем липиды и нуклеиновые кислоты, и их окислительная модификация считается одним из ранних и надёжных маркеров оксидативного стресса, так как продукты окисления белков в тканях проявляются раньше, и более стабильны, по сравнению с продуктами перекисного окисления липидов .
В связи с этим цель исследования — изучение окислительных модификаций белков в тканях мозга крыс в условиях стресс-индуцированной депрессии.
2. Методы и принципы исследования
Работа проводилась на 60 крысах-самцах линии Wistar шестимесячного возраста. Для моделирования депрессивного состояния у животных использовали модель «социального» стресса , при котором у крыс формируется агрессивный и субмиссивный характер поведения. Все животные были разделены поровну по принципу рандомизации на 2 группы: 1 группа — интактные животные; 2 группа — животные, у которых моделировали депрессивное состояние.
Для определения окислительных модификаций белков, крыс убивали в соответствии с этическими нормами и из черепной коробки извлекали мозг, из которого выделяли неокортекс, стриатум, гиппокамп и гипоталамус. Затем готовили из тканей 10% гомогенат в 0,1 М фосфатном буфере (рН=7,4), гомогенат центрифугировали при 10000 g, t=+4 °С в течение 40 мин для удаления клеточного дебриса. В гомогенате определяли спонтанную и индуцированную реактивом Фентона ОМБ методом иммуноферментного анализа с помощью готовых наборов реагентов Rat AOPP ELISA Kit (Cusabio, Китай). Продукты реакции регистрировали на двух длинах волн 270 нм и 363 нм, что соответствует карбонильным производным белков с гидрофильными и гидрофобными аминокислотными остатками.
Количество продуктов ОМБ выражали в единицах оптической плотности, рассчитанной на 1 мг белка. Для оценки Фентон-индуцированного окисления белков использовали величину приращения ОМБ, вычитая из значений оптической плотности, полученной в пробе после индукции реактивом Фентона, значения оптической плотности спонтанного ОМБ. Оптическую плотность растворов измеряли фотоэлектроколориметром КФК-3-01 ЗОМЗ (Россия).
Цифровой материал всех экспериментов подвергали статистической обработке с помощью пакета программ STATISTICA Application 10.0.1011.0. (США).
3. Основные результаты
Результаты исследования уровня спонтанного и Фентон-индуцируемого окисления гидрофильных и гидрофобных аминокислотных остатков (АКО) в тканях мозга крыс представлены на рисунках 1–4.
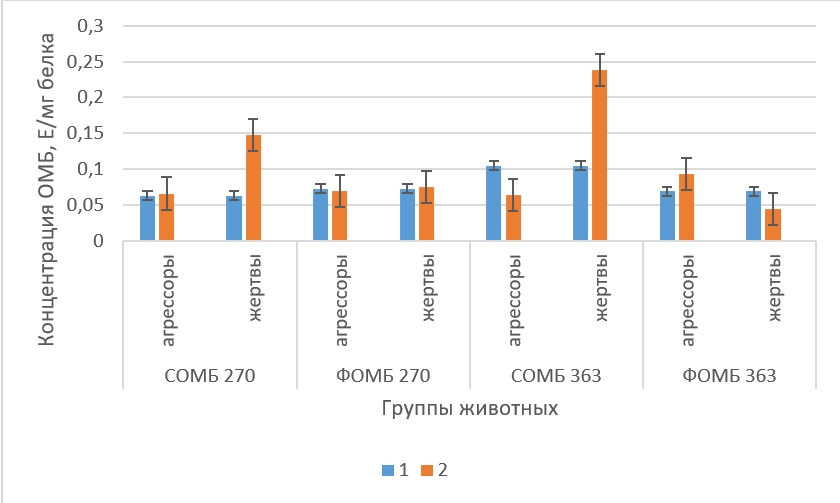
Концентрация ОМБ в неокортексе крыс в норме и в состоянии депрессии
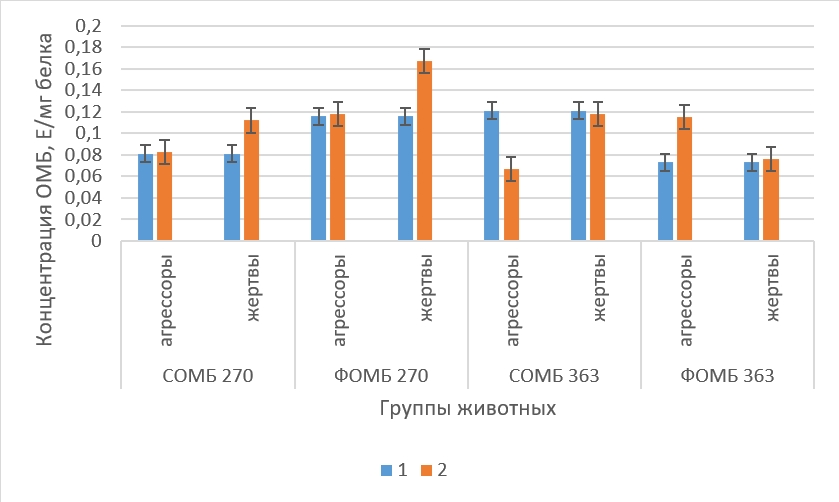
Рисунок 2 - Концентрация ОМБ в гипоталамусе крыс в норме и в состоянии депрессии
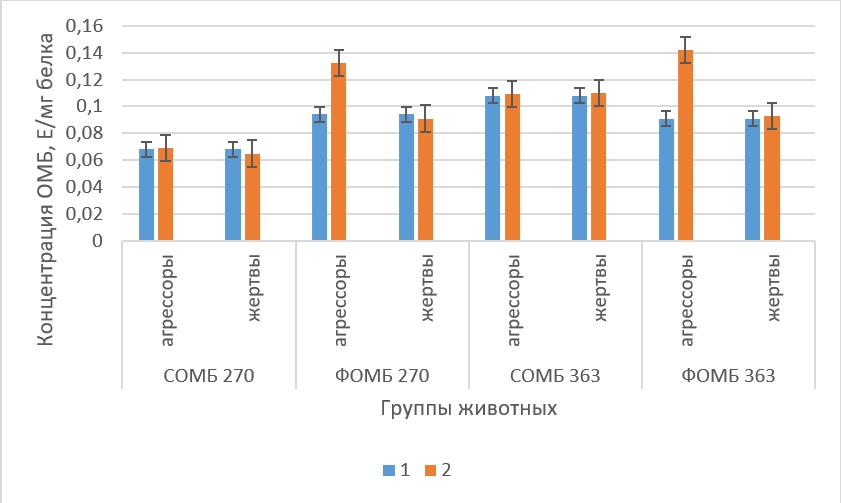
Рисунок 3 - Концентрация ОМБ в гиппокампе крыс в норме и в состоянии депрессии
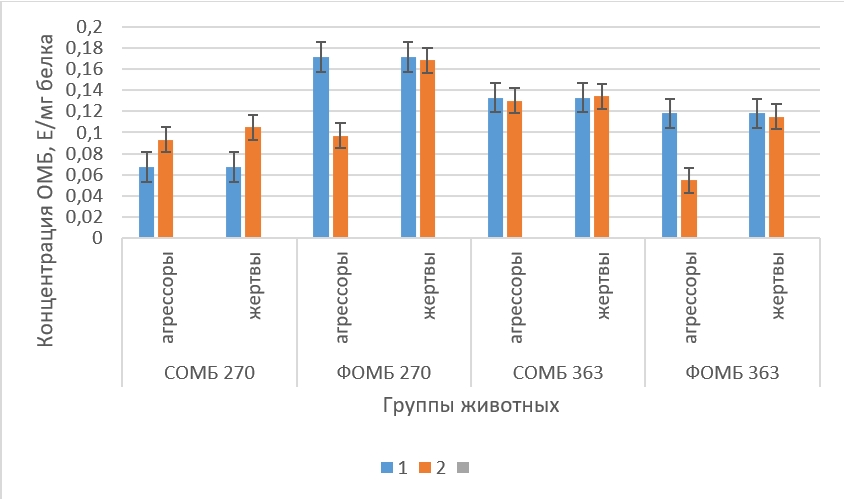
Рисунок 4 - Концентрация ОМБ в стриатуме крыс в норме и в состоянии депрессии
4. Обсуждение результатов
В целом спонтанное окисление белков в тканях представляет собой естественный физиологический процесс, происходящий без внешних стрессоров и сопровождающийся непреднамеренными химическими модификациями аминокислотных остатков (например, атаками свободных радикалов на серин, лизин, цистеин; образованием окисленных функциональных групп и карбоно-/нуклеофильными изменениями). В результате возникает умеренное число окисленных белковых остатков, что в целом влияет на структуру белков, их активность и склонность к полимеризации. Базальная ОМБ отражает баланс между продукцией активных форм кислорода и антиоксидантной защитой организма и обычно функционирует как регуляторный механизм: модификации белков могут менять их активность или взаимодействие с другими клеточными компонентами. Изменения физиологического уровня спонтанного окисления белков могут сигнализировать о дисбалансе редокс-потенциала ткани и предвещать риск возрастных или патологических состояний
.Индуцируемая ОМБ обычно возникает под влиянием внешних факторов или патологических состояний, например, при ультрафиолетовом облучении, поступлении токсических агентов, активации воспалительных медиаторов, гипоксии или усиленной активности свободных радикалов. Она характеризуется резким ростом концентрации окисленных остатков в тканях и образованием продуктов перекисного окисления липидов, связанных с белками (например, малоновый диальдегид и другие).
Индуцируемая ОМБ служит индикатором того, как организм справляется со стрессом: чем выше порог чувствительности организма к стрессу и чем эффективнее антиоксидантная защита, тем меньше вероятность чрезмерной индуцированной модификации белков. Низкая устойчивость тканей к переокислению проявляется быстрым ростом индуцированной модификации белков под действием стимулов и коррелирует с повышенным риском окислительного повреждения клеток и тканей
, .Совокупный анализ обоих видов ОМБ позволяет всесторонне оценить редокс-потенциал ткани, риск повреждений и эффективность антиоксидантной терапии, а также служит маркером динамики патологических состояний и ответов на лечение.
Таким образом, по результатам эксперимента установлено, что при моделировании депрессивного состояния у крыс агрессоров и жертв наблюдаются разнонаправленные изменения ОМБ в различных структурах мозга. Повышение концентрации СОМБ и ФОМБ гидрофильных и гидрофобных АКО свидетельствует о интенсивном окислительном стрессе в тканях, ухудшении редокс-гомеостаза и повреждении белков клеточных мембран, а снижение концентрации СОМБ и ФОМБ гидрофильных и гидрофобных АКО свидетельствует об эффективной работе антиоксидантной системы организма.
5. Заключение
На фоне депрессивного состояния у крыс агрессоров и жертв наблюдаются разнонаправленные изменения ОМБ в различных структурах мозга и дестабилизация их редокс-потенциала. Повышение концентрации ФОМБ гидрофобных АКО характеризует повреждение клеточных мембран в структурах мозга и интенсивный локальный окислительный стресс. Повышение концентрации СОМБ гидрофильных АКО отражает интенсификацию цитозольных источников активных форм кислорода. Исследование процессов свободнорадикального окисления белков в различных структурах мозга вносит вклад в понимание патогенеза депрессии через оценку нарушений нейронной сигнализации, пластичности и метаболического баланса.
