Клинико-гематологические маркеры адаптации у глубоко недоношенных детей, перенесших гипоксию: региональный опыт катамнестического наблюдения
Клинико-гематологические маркеры адаптации у глубоко недоношенных детей, перенесших гипоксию: региональный опыт катамнестического наблюдения
Аннотация
Статья посвящена комплексному анализу динамики гематологических показателей у глубоко недоношенных детей с экстремально низкой (ЭНМТ) и очень низкой массой тела (ОНМТ) в течение первого года жизни. Исследование основано на ретроспективном анализе 75 медицинских карт катамнестического наблюдения, разделенных на основную группу (ЭНМТ, n=25), группу сравнения (ОНМТ, n=25) и контрольную группу (здоровые доношенные новорожденные, n=25).
В ходе работы выявлена тесная связь гематологического профиля детей с патологическим течением антенатального периода у матерей, характеризующегося высокой частотой маточно-плацентарной недостаточности (до 60%), анемии (до 60%) и угроз прерывания беременности. Установлено, что для детей с ЭНМТ и ОНМТ характерны достоверно более низкие уровни гемоглобина, эритроцитов и нейтрофилов при рождении по сравнению с доношенными сверстниками. Доказано, что стабилизация уровня гемоглобина у детей с ЭНМТ происходит лишь к 6-месячному возрасту, что сопровождается реактивным тромбоцитозом к 3-му месяцу жизни как признаком истощения депо железа.
На основании полученных данных авторами сформулированы конкретные практические рекомендации по ведению данной категории пациентов. Обоснована необходимость раннего назначения препаратов железа и фолиевой кислоты с 3–4-й недели жизни, а также важность оптимизации нутритивной поддержки (использование фортификаторов грудного молока, контроль потребления белка до 3,5-4 г/кг/сут). Акцентировано внимание на важности регулярного лабораторного мониторинга (не реже 1 раза в 2 недели в стационаре) и минимизации ятрогенных кровопотерь. Предложенный комплекс мероприятий направлен на стимуляцию нормобластического типа кроветворения и снижение риска тяжелых форм анемии недоношенных на этапе катамнестического наблюдения.
1. Введение
1.1. Актуальность темы
В современной неонатологии и педиатрии проблема выхаживания и эффективной реабилитации детей, родившихся с экстремально низкой (ЭНМТ) и очень низкой массой тела (ОНМТ), занимает одно из центральных мест. Успехи перинатальных технологий позволили значительно повысить выживаемость глубоко недоношенных младенцев, что является общероссийской тенденцией в структуре детского здравоохранения , , однако это требует постоянной актуализации протоколов выхаживания на этапе катамнестического наблюдения , . Так в Республике Мордовия за 2024 отчетный год младенческая смертность составила 1,2 промилле, в данном году за год умерло всего 6 детей до 1 года и наш регион вышел на первое ранговое место в Российской Федерации, однако это привело к росту частоты специфических осложнений, среди которых нарушения гематологической адаптации и анемия недоношенных играют ведущую роль. Особую значимость данная проблема приобретает в региональном аспекте (на примере Республики Мордовия), где структура заболеваемости и особенности катамнестического наблюдения требуют постоянного мониторинга и уточнения прогностических критериев. И несомненно важным является интеграция таких детей в общество.
Гематологический профиль новорожденных с ЭНМТ и ОНМТ характеризуется выраженной незрелостью всех ростков кроветворения, что требует глубокой клинической интерпретации лабораторных данных , . Процессы эритро-, лейко- и тромбоцитопоэза у данной категории пациентов протекают в условиях глубокой гипоксии, инфекционно-воспалительного стресса и истощения антенатальных депо микроэлементов. Существующие литературные данные указывают на то, что ранняя анемия недоношенных развивается уже к 3–4-й неделе жизни, однако вопросы долгосрочной динамики гемограммы (до года жизни) и её сопряженности с акушерским фоном матери остаются недостаточно освещенными в комплексных исследованиях. При этом тактика ведения таких пациентов должна опираться на современные международные рекомендации по коррекции железодефицитных состояний .
Цель исследования заключалась в комплексной оценке динамики основных гематологических показателей (гемоглобина, эритроцитов, тромбоцитов и лейкоцитарной формулы) у детей с ЭНМТ и ОНМТ в течение первого года жизни для научного обоснования стратегии ранней профилактики и коррекции выявленных нарушений.
1.2. Научная новизна
В ходе работы впервые для регионального здравоохранения Республики Мордовия установлены специфические закономерности гематологической адаптации глубоко недоношенных детей. Выявлено, что у новорожденных с ЭНМТ нормализация уровня гемоглобина наступает существенно позже (к 6 месяцам жизни) по сравнению с детьми с ОНМТ. Впервые показана взаимосвязь между критическим снижением уровней нейтрофилов (до 35,5%) при рождении и тяжестью перенесенной антенатальной патологии (хроническая плацентарная недостаточность, анемия матери). Установлен характер реактивного тромбоцитоза в возрасте 3 месяцев как индикатора формирования латентного дефицита железа у данной категории пациентов.
1.3. Теоретическая значимость
Теоретическая значимость исследования заключается в расширении представлений о патогенезе анемии и особенностях миелопоэза у детей с массой тела при рождении менее 1000 г и менее 1500 г. Обосновано влияние «кислородного комфорта» и нутритивной поддержки на интенсивность эритропоэза, что дополняет существующие теории физиологической и патологической адаптации недоношенных детей.
1.4. Практическая значимость
На основании полученных результатов сформулированы конкретные рекомендации для врачей-неонатологов и педиатров кабинетов катамнеза. Обоснована необходимость старта профилактического приема препаратов железа и фолиевой кислоты с 3–4-й недели жизни вне зависимости от исходных показателей крови. Предложенный алгоритм лабораторного мониторинга и принципы нутритивной поддержки (использование фортификаторов грудного молока, расчет белка до 3,5 г/кг/сут) позволяют минимизировать риск развития тяжелых форм анемии и оптимизировать темпы психомоторного развития детей на первом году жизни.
2. Методы и принципы исследования
В ретроспективное исследование включено 75 новорожденных, распределенных на три группы: I группа (основная) — 25 детей с ЭНМТ (масса <1000 г), II группа (сравнения) — 25 детей с ОНМТ (масса 1000–1500 г), III группа (контрольная) — 25 здоровых доношенных детей.
Критерии включения: срок гестации <32 недель для I и II групп; наличие информированного согласия родителей; катамнестическое наблюдение в течение 12 месяцев. Критерии исключения: врожденные пороки развития; гемолитическая болезнь новорожденных; острые инфекционные заболевания на момент первичного забора крови; неполные данные медицинских карт.
2.1. Статистическая обработка
Анализ данных проводился с использованием пакета Statistica 12.0 и MS Excel 2019. Количественные показатели представлены в виде средней арифметической и ошибки средней (M±m). Для оценки значимости межгрупповых различий использовался t-критерий Стьюдента (при нормальном распределении) и U-критерий Манна-Уитни. Различия считались статистически значимыми при p < 0,05. Для оценки связи признаков применялся корреляционный анализ Спирмена (r).
3. Результаты и их обсуждение
Работа состояла из двух этапов. На первой ступени исследования были проанализированы данные выписок из родительного дома и перинатального центра. По полученным данным, большая часть детей 1-й группы (92%) и все дети 2-й группы (100%) родились путем кесарева сечения. В контрольной группе доношенных выше был процент рожденных естественным путем (68%), путем кесарева сечения родились на свет 8 малышей (32%).
При изучении акушерского анамнеза внимание привлек высокий процент акушерской патологии. По данным авторов, у беременных матерей 1-й (56%) и 2-й группы (60%) достоверно выше, чем в контрольной группе (40%) регистрировалась маточно-плацентарная недостаточность. Также достоверно выше, чем в контроле, в обеих группах настоящая беременность осложнялась угрозой прерывания (52% и 36% соответственно против 0%).
Среди экстрагенитальной патологии у матерей, родивших детей с экстремально низкой массой тела и очень низкой массой тела, на первом месте стояла анемия (60% и 28% против 20% в контроле), на втором месте — хронический пиелонефрит (20% и 8% против 4% в контроле), обращает на себя внимание наличие в анамнезе артериальной гипертензии 2–3 степени в 3-х исследуемых группах (20% и 24% соответственно против 4%).
Все новорожденные с ЭНМТ имели гипоксическое поражение ЦНС — церебральную ишемию II–III степени (100%), в группе детей с ОНМТ данный показатель составил так же 100%, но по степени тяжести чаще встречалась церебральная ишемия I–II степени, в контрольной группе данный результат был равен 0%. Достоверно в 1-й и 2-й группах диагностировалась врожденная пневмония (88% и 92% против 0%), респираторный дистресс-синдром и/или бронхолегочная дисплазия (68% и 80%, 92% и 36% соответственно против 0% в контроле), анемия (92% и 72% против 20% в контроле), была диагностирована ретинопатия новорожденных (78% и 16%, 5 новорожденных с ОНМТ составили группу риска по возникновению данной патологии (20%), против 0%).
На втором этапе исследования авторами были изучены показатели периферической крови у детей исследуемых групп. По полученным данным было выявлено, что у недоношенных новорожденных 1-й и 2-й групп уровень гемоглобина при рождении был ниже (160,8 г/л и 184 г/л соответственно), чем у доношенных новорожденных (194,08 г/л) (рис. 1). В 1 месяц жизни отмечалось снижение гемоглобина во всех группах. Современные зарубежные исследования подтверждают, что у детей с ЭНМТ этот процесс протекает наиболее агрессивно из-за незрелости рецепторного аппарата к эритропоэтину и высокого уровня ятрогенных потерь . Согласно литературным данным, это связано со сменой гипоксии на гипероксию, что приводит к уменьшению выработки эритропоэтина — гликопротеина, принадлежащего к семейству цитокинов, ведущий, в свою очередь, к снижению интенсивности эритропоэза и гемоглобина , , . У доношенных новорожденных показатели гемоглобина в течение первого года жизни находились в пределах нормальных значений (145–110 г/л). При этом у детей 1-й и 2-й группы данный показатель крови колебался на протяжении 12 мес. У детей с ОНМТ отмечается наибольшее снижение гемоглобина в 1 мес. (107,12 г/л), чем у детей с ЭНМТ (100,6 г/л). Следует отметить, что в патогенезе ранней анемии у недоношенных детей значительное влияние оказывают сочетание нескольких факторов: укороченная продолжительность жизни эритроцитов; пролонгированная циркуляция и поздняя смена фетального гемоглобина; инфекционные агенты, в том числе грамотрицательная флора, для жизнедеятельности которой необходимо активное потребление железа , . В три месяца у малышей двух первых двух группы уровень гемоглобина также находился ниже возрастной нормы (109,2 г/л и 106,76 г/л соответственно). Данное состояние расценивается как поздняя анемия недоношенных, развивающаяся в данном периоде (на 3–4-м мес. жизни), являясь в большинстве случаев железодефицитной анемией , . Наиболее активное поступление железа от матери к плоду осуществляется в последние два месяца беременности, поэтому недоношенность в 4–8 недель может привести к сокращению запасов железа в 1,5–3 раза по сравнению с доношенными , . Если запасов железа недостаточно, происходит дальнейшее снижение гемоглобина, и анемия становится железодефицитной.
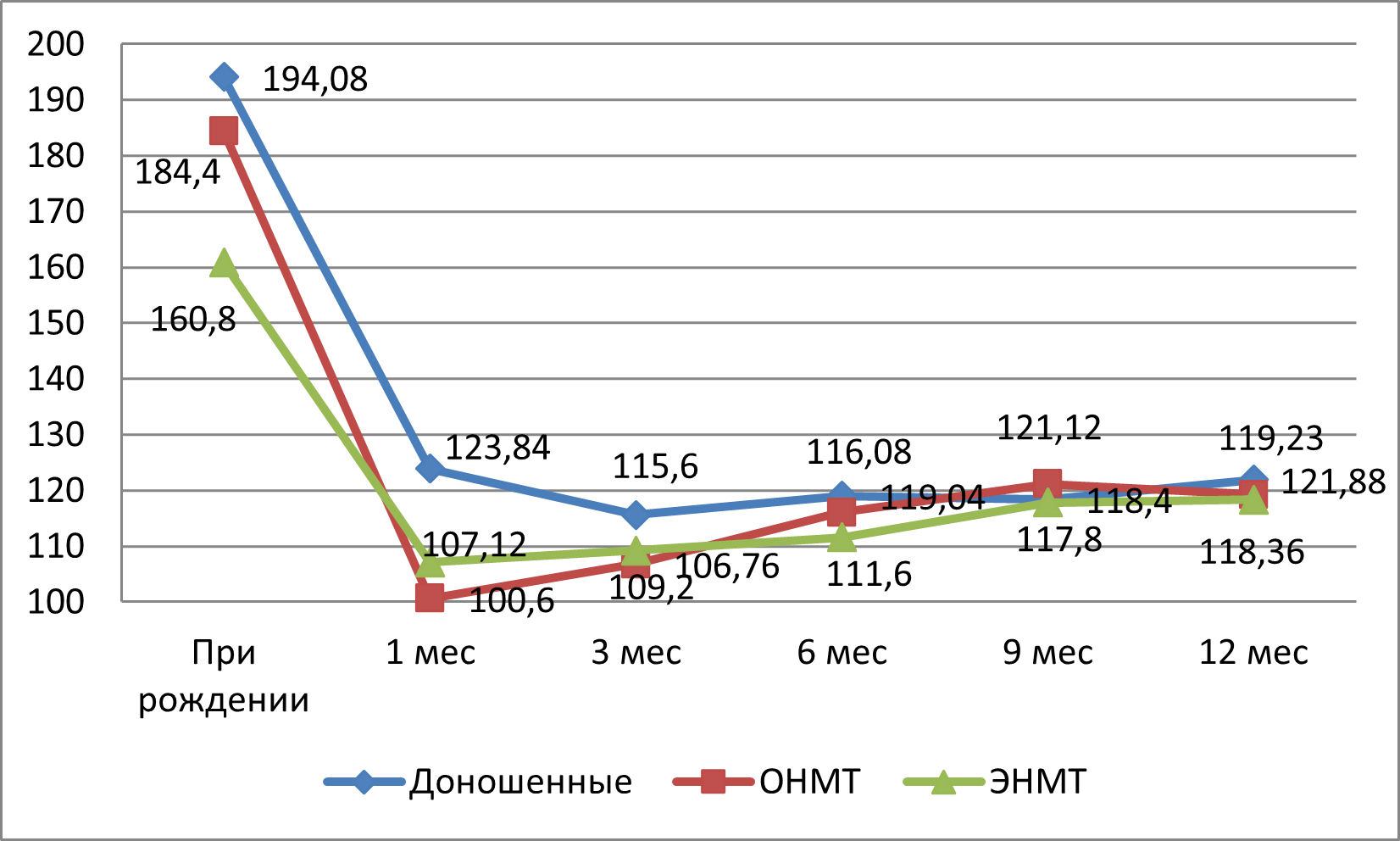
Динамика уровня гемоглобина у детей трех групп в первый год жизни
составлен авторами
Полученные нами данные согласуются с результатами международных исследований, указывающих на критическую роль истощения депо железа у детей с массой тела менее 1000 г к 8–12 неделе жизни . При этом сохранение высоких концентраций эритропоэтина на фоне анемии у пациентов основной группы свидетельствует о напряженности компенсаторных механизмов эритропоэза в ответ на пролонгированную тканевую гипоксию . Подобная гематологическая картина диктует необходимость пересмотра стандартных протоколов и инициации ферротерапии в более ранние сроки, что коррелирует с современными подходами к ведению детей с экстремально низкой массой тела в катамнезе .
Количество эритроцитов в периферической крови при рождении было выше у доношенных новорожденных (5,62*1012/л), чем у детей 1-й и 2-й групп (4,6*10 12/л и 5,1*1012/л) (рис. 2). К первому месяцу жизни количество эритроцитов значительно снижается во всех группах, но более значительно у детей с ЭНМТ — до 3,78*1012/л, это связано с тем, что у недоношенных детей процесс разрушения эритроцитов протекает быстрее из-за более короткой продолжительности жизни этих клеток , . К трем месяцам жизни количество эритроцитов повысилось, достигая почти равных значений. Однако, в последующие месяцы жизни у детей первых двух групп можно заметить, что содержание показателей эритроцитов повышалось в сравнении со стабильными показателями в группе доношенных детей. Вероятнее всего, наблюдаемое изменение обусловлено повышенной активностью эритропоэза, возникающей как адаптация к внеутробной жизни на фоне выраженной гипоксии у недоношенных младенцев , .
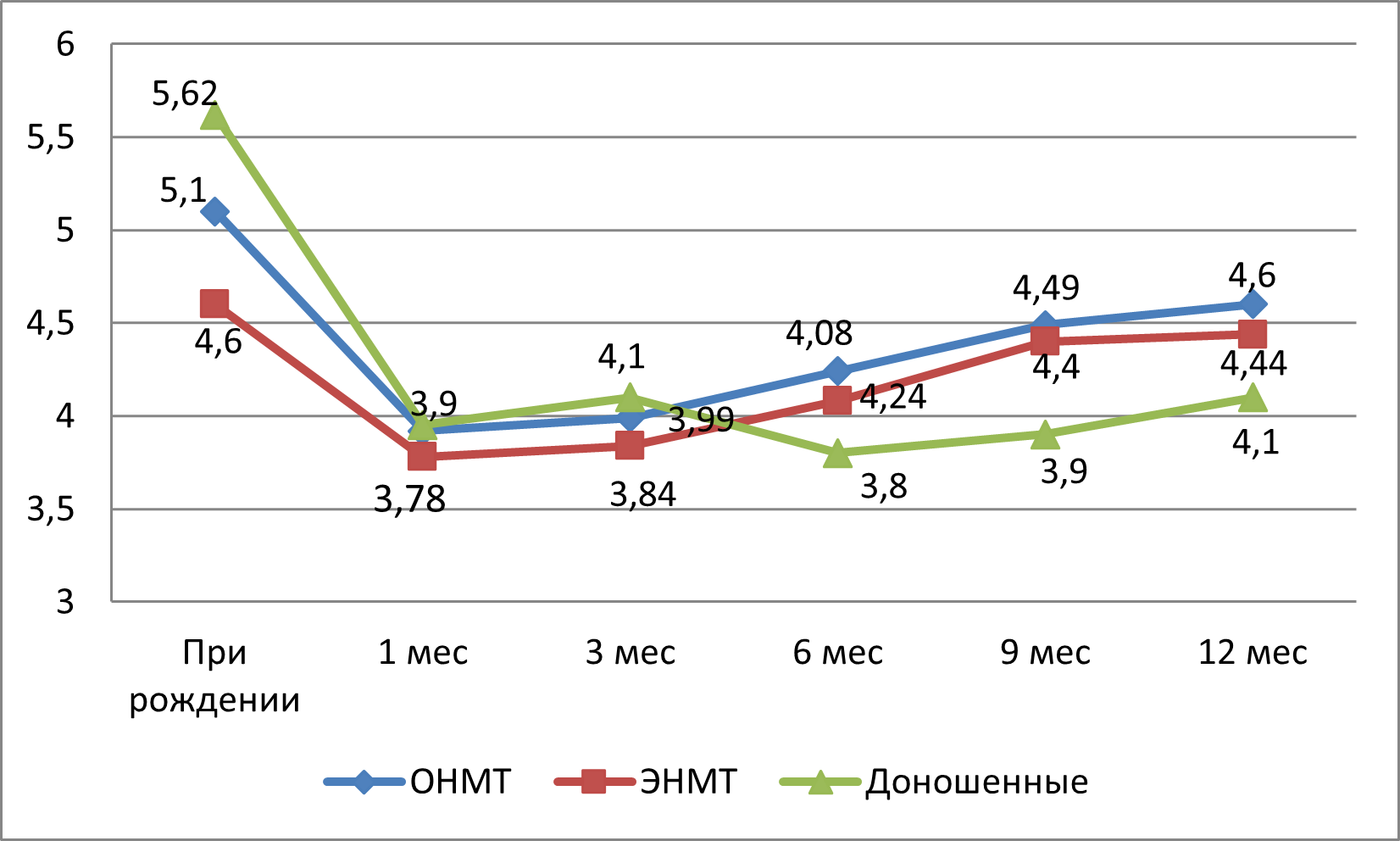
Динамика уровня эритроцитов у трех групп
составлен авторами
Установлено, что уровень гемоглобина у детей с ЭНМТ в возрасте 3 месяцев был достоверно ниже (94,2±3,1 г/л), чем в контрольной группе (118,5±4,2 г/л), (p < 0,001). Выявленный реактивный тромбоцитоз в основной группе коррелировал с дефицитом железа (r = -0,64; p < 0,05), что подтверждает необходимость раннего старта ферротерапии.
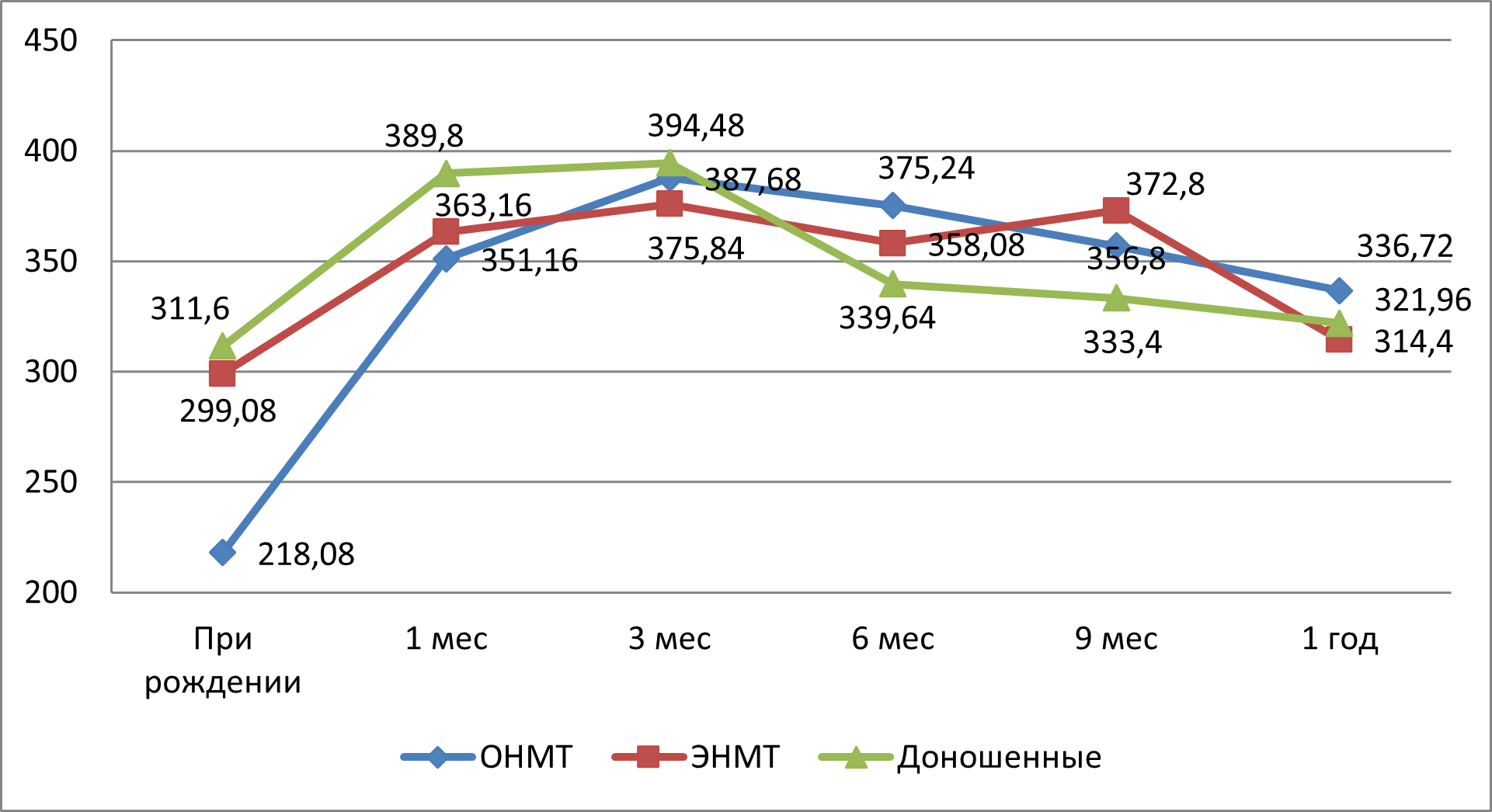
Динамика уровня тромбоцитов у трех групп
составлен авторами
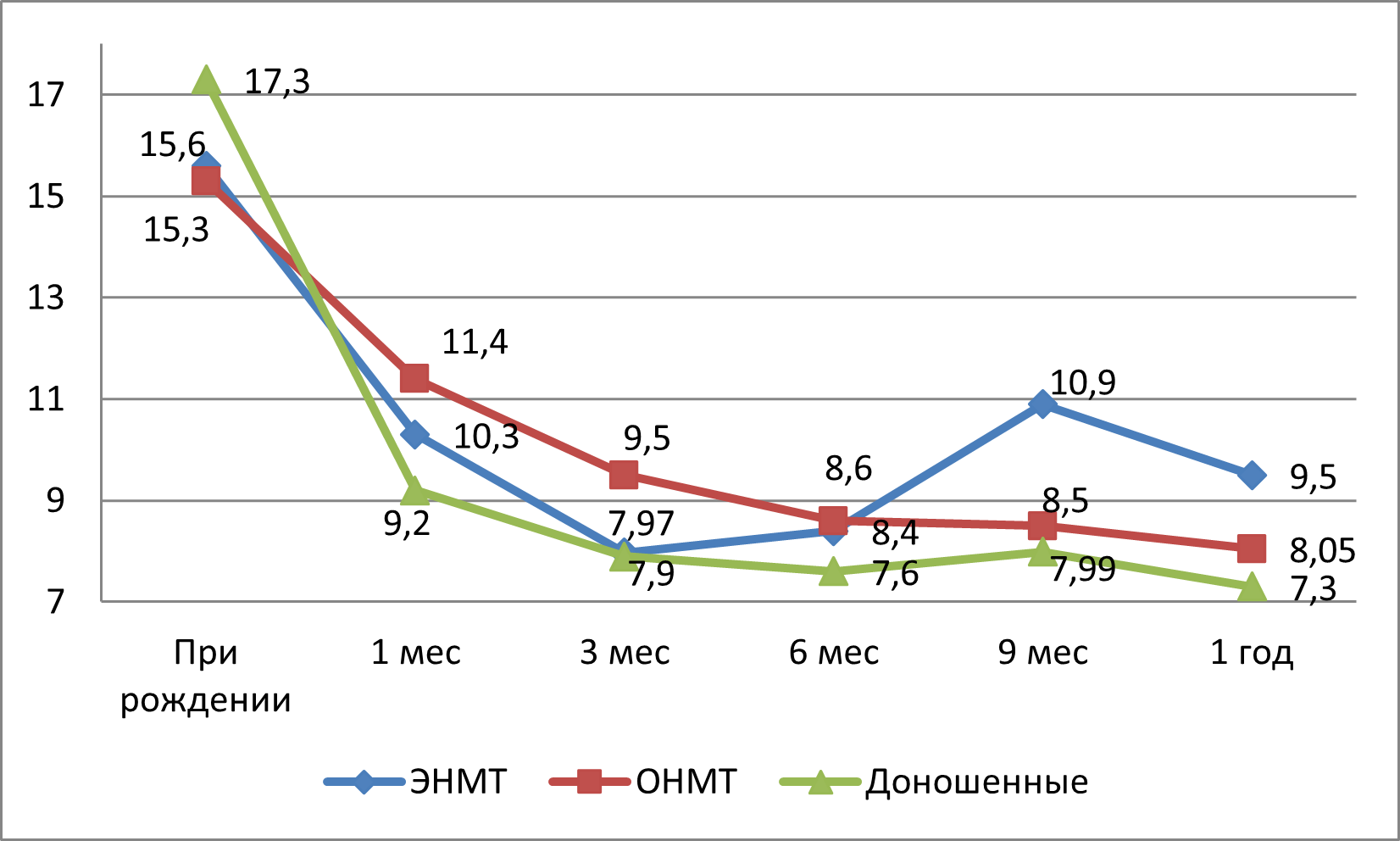
Динамика уровня лейкоцитов у трех групп
составлен авторами
4. Практические рекомендации
Учитывая выявленные особенности гемограммы (исходно низкие показатели эритроцитов и гемоглобина, позднюю стабилизацию показателей к 6 месяцам) и высокий риск развития анемии у глубоконедоношенных детей, рекомендуется следующий комплекс профилактических мероприятий:
· Раннее начало назначения препаратов железа: всем глубоконедоношенным детям, находящимся на естественном или искусственном вскармливании, профилактический прием препаратов железа (в форме гидроксид-полимальтозного комплекса или сульфата железа) необходимо начинать с 3–4-й недели жизни, независимо от уровня гемоглобина при рождении. Последние систематические обзоры указывают на целесообразность индивидуализации доз железа (от 2 до 6 мг/кг/сут) в зависимости от уровня сывороточного ферритина на этапе выписки из стационара .
· Контроль обеспеченности витаминами и микроэлементами: фолиевую кислоту необходимо назначать с 3–4-й недели жизни в дозе 0.5–1 мг/кг/сутки на протяжении первых 2–3 месяцев жизни для стимуляции нормобластического типа кроветворения.
· Оптимизация нутритивной поддержки: обеспечить максимально раннее поступление белка (3.5 г/кг/сутки) для построения гемоглобина и эритропоэтина. При невозможности полноценного энтерального питания (первые недели жизни) обязательно назначение парентерального питания, обогащенного железом и аминокислотами. При вскармливании грудным молоком обязательно использование фортификаторов грудного молока, так как в нативном грудном молоке содержание железа и микронутриентов является недостаточным для недоношенного ребенка.
· Лабораторный мониторинг: проводить контроль клинического анализа крови с определением уровня ретикулоцитов не реже 1 раза в 2 недели в стационаре и ежемесячно после выписки до достижения шестимесячного возраста.
· Обеспечить адекватный «кислородный комфорт» (своевременная санация очагов инфекции, профилактика апноэ), так как гипоксия угнетает эритропоэз.
· Минимизировать ятрогенные кровопотери (частые заборы крови для анализов) путем использования микролабораторных методик.
5. Заключение
На основании проведенного исследования установлено, что гематологический профиль глубоконедоношенных детей при рождении характеризуется исходно более низкими уровнями гемоглобина, эритроцитов, лейкоцитов и нейтрофилов по сравнению с доношенными сверстниками. Динамическое наблюдение в течение первого года жизни показало, что у младенцев с экстремально низкой массой тела (ЭНМТ) физиологическая стабилизация показателей красной крови наступает лишь к 6-месячному возрасту. Этот процесс протекает на фоне компенсаторной активации эритропоэза и транзиторного реактивного тромбоцитоза в возрасте 3 месяцев, что является специфическим индикатором истощения антенатальных депо железа.
Ключевым модифицирующим фактором, определяющим характер гематологической адаптации, выступает тяжесть перенесенной перинатальной патологии. Выраженность отклонений в гемограмме новорожденных находится в прямой зависимости от наличия у матери хронической плацентарной недостаточности, анемии, инфекционных заболеваний мочевыводящих путей и угрозы прерывания беременности. Полученные результаты диктуют необходимость ранней (с 3–4-й недели жизни) медикаментозной и нутритивной коррекции гематологических нарушений у детей с ЭНМТ и ОНМТ для предотвращения формирования тяжелых дефицитных состояний на этапе катамнестического наблюдения.
