Возможности прогнозирования развития острого повреждения почек при инфаркте миокарда у мужчин молодого и среднего возраста с помощью диагностического алгоритма
Возможности прогнозирования развития острого повреждения почек при инфаркте миокарда у мужчин молодого и среднего возраста с помощью диагностического алгоритма
Аннотация
Актуальность. Острое повреждение почек (ОПП) при инфаркте миокарда (ИМ) ухудшает прогноз и увеличивает сроки лечения пациентов.
Цель. Оценить значимость клинических, инструментальных и лабораторных предикторов развития ОПП при ИМ у мужчин моложе 60 лет для моделирования прогноза риска развития этого осложнения с помощью диагностического алгоритма и улучшения профилактики.
Материалы и методы. В исследование включены мужчины 32-60 лет с ИМ I типа. Пациенты разделены на две сравнимые по возрасту группы: I – исследуемую, с ОПП – 25 больных; II – контрольную, без нее – 166 пациентов. Методом Хи-квадрат Пирсона оценены абсолютный (АР) и относительный (ОР) риски развития ОПП при воздействии различных факторов. Выполнено математическое моделирование риска развития этого осложнения методом деревьев классификации.
Результаты. Среди предикторов ОПП при ИМ у обследованных выделены: стресс (АР: 15,9%; р=0,01), зимний период года (АР: 21,8%; ОР: 3,1; р=0,003), гипертриглицеридемия (≥1,8 ммоль/л) (АР: 23,0%; р=0,007) и язвенная болезнь (АР: 25,8; ОР: 2,5; р=002). Для дерева-решений наиболее значимыми оказались: зимний период года и величина систолического (сист) артериального давления (АД) пациента в первые часы ИМ. С помощью дерева-решений выделено четыре класса риска. Самый высокий уровень риска (30,2%; объем группы = 53) – у пациентов с ИМ в зимний период и АДсист ≥130 мм рт.ст. Наименьший уровень риска (0,0%, объем группы = 45) развития ОПП наблюдали для ИМ в весенний, летний и осенний периоды и АДсист ˂135,0 мм рт.ст. При АДсист≥135 мм рт.ст. в эти периоды риск развития ОПП увеличивается до 11,6% (69 пациентов). В зимний период при снижении АДсист ˂130 мм рт.ст. риск развития ОПП уменьшается до 4,2% (24 человека). Чувствительность модели составила 94,1%; специфичность – 70,9%; эффективность – 82,5%.
Выводы. Добавочными предикторам развития ОПП при ИМ у мужчин моложе 60 лет оказались: зимний период года, стресс, гипертриглицеридемия в первые часы ИМ (≥1,8 ммоль/л) и наличие язвенной болезни в анамнезе. На основе сочетания показателей АД и зимнего периода года построена модель оценки риска развития этого осложнения. Она позволяет выделить среди пациентов с ИМ группу риска развития ОПП для последующего наблюдения и проведения своевременных профилактических и лечебных мероприятий.
1. Введение
Проблема острого повреждения почек (ОПП) при инфаркте миокарда (ИМ) далека от разрешения: прогноз и качество жизни пациента при развитии этого осложнения резко ухудшаются, экономические затраты на лечение возрастают, а эффективные методы лечения и профилактики установлены не для всех случаев , , . В то же время проблемы ИМ и его осложнений у мужчин молодого и среднего возраста сохраняют свою остроту из-за стабильно высоких показателей смертности и инвалидизации в этой группе, а также связанных с ними медико-социальных проблем , , . Поэтому изучение вопросов раннего выявления и профилактики ОПП у мужчин моложе 60 лет с ИМ признается крайне важным.
Цель исследования. Оценить значимость различных факторов риска развития ОПП при ИМ у мужчин моложе 60 лет. Разработать модель прогнозирования риска развития этого осложнения в виде пригодного к применению диагностического алгоритма для улучшения раннего его выявления, повышения эффективности профилактики и улучшения исходов.
2. Методы и принципы исследования
Изучены результаты обследования и лечения 191 мужчины, жителей Санкт-Петербурга, 32-60, лет по поводу ИМ I типа (по IV универсальному определению этого заболевания) и скоростью клубочковой фильтрации (CKD-EPI) 30 и более мл/мин/1,73 м2 . Исследование одобрено независимым этическим комитетом Федерального государственного бюджетного военного образовательного учреждения высшего образования «Военно-медицинская академия имени С.М. Кирова» Министерства обороны Российской Федерации 27.04.2021 г., протокол № 229. От всех участников перед началом процедур получено письменное информированное согласие на включение.
Пациентов разделили на две группы в зависимости от развития ОПП. Исследуемую группу сформировали из больных с ИМ и ОПП – 25 мужчин (средний возраст 50,6±5,3 лет). Контрольная группа составлена из больных ИМ без ОПП – 166 человек (51,0±6,7 лет, p=0,4). Диагностический и лечебный алгоритмы соответствовали стандартам на момент госпитализации. ОПП диагностировали на основании критериев KDIGO (2012) при увеличении уровня креатинина на 26,5 мкмоль/л на протяжении не менее двух суток (и/или в 1,5 раза в течение семи суток) по сравнению с его исходным уровнем в первые 48 часов ИМ или по почасовому диурезу в этот период .
Выделенные группы не отличались по проводимому лечению. Так, пациенты не получали статины до развития изучаемого случая ИМ. В период исследования и в течение двух недель до него пациенты не принимали антибактериальные препараты. Коронарография с реваскуляризацией выполнены у 16,0% пациентов исследуемой группы и – 17,1% в контрольной (р=0,8). У пациентов исследуемой группы патология почек отсутствовала до развития изучаемого случая ИМ. Исследование включало прицельную оценку частоты наблюдения основных и дополнительных факторов риска кардиоваскулярных заболеваний, сопутствующей патологии и состояний, провоцирующих возникновение ИМ . Артериальную гипертензию (АГ) оценивали по рекомендациям Российского кардиологического общества . Массу тела – по ее индексу Кетле (ИМТ). Избыточной считали ситуации с ИМТ 25,0 кг/м2 и выше. Периферические ангиопатии у пациентов верифицировали по клиническим показаниям. Подагру диагностировали согласно критериям EULAR/ACR (2016) . Определение сезонных особенностей заболевания выполняли распределением случаев по климатическим периодам, длительность и границы которых выделяли для каждого года с помощью дат устойчивого перехода среднесуточной температуры воздуха через реперные точки в 0 и 150С . Верификацию стресса и его связи с ИМ выполняли с помощью опросников Копиной О.С., Ридера Л. и соответствию дополнительному перечню распространенных стрессовых ситуаций по Бальсевичу В.К. . Клинические фенотипы ИМ распределяли по известным вариантам проявлений заболевания и его осложнений . Последние объединяли в группы по В.Н. Ардашеву на связанные с электрической нестабильностью миокарда (ЭН), сократительной его недостаточностью (СкН) и механической несостоятельностью (МН) . Прогноз летальности оценивали по индексу R. Norris . Среди параметров липидного обмена изучали триглицериды (ТГ). При комплексной эхокардиографии определяли диастолический размер правого желудочка (КДР ПЖ), толщину межжелудочковой перегородки (МЖП), индексы (конечных систолического (КСО/S)) и диастолического (КДО/S) объемов левого желудочка (ЛЖ), ударный (УИ), скорости раннего (Ve) и позднего (Va) диастолического наполнения ЛЖ и их соотношение (Ve/Va). Показатели систолической функции ЛЖ оценивали по J.S. Simpson . Индексацию проводили к площади поверхности тела (S) . Среднее давление в легочной артерии (СДЛА) определяли эхокардиографически (A. Kitabatake) . Величины среднего артериального давления (АДср) общих периферического (ОПС) и легочного сопротивления (ОЛС) рассчитывали по Ю. Н. Шишмареву .
На первом этапе методом анализа рисков применением критерия Хи-квадрат Пирсона из сформированной аналитической базы данных (более 300 анамнестических, клинико-лабораторных и инструментальных показателей течения ИМ) отобраны факторы, оказывавшие значимое влияние на абсолютный (АР) и относительный (ОР) риски развития ОПП у обследованных. На втором этапе, используя полученные факторы, выполняли математическое моделирование риска развития этого осложнения методом деревьев классификации. Прогнозное качество деревьев-решений оценивали ROC-анализом. Количественные параметры определяли в первые 48 часов ИМ. Их сравнивали по критерию Манна-Уитни.
3. Основные результаты
Результаты оценки методом анализа рисков влияния основных и дополнительных факторов риска кардиоваскулярных заболеваний на возможность развития ОПП у обследованных представлено в таблице 1.
Таблица 1 - Влияние факторов риска кардиоваскулярных заболеваний на риск развития ОПП у обследованных
Факторы кардиоваскулярного риска | Частота ОПП при ИМ: (абсолютный риск, %; изменение риска, % (95% ДИ)) | Относительный риск (95% ДИ) | P |
Операции реваскуляризации коронарных артерий в анамнезе | 46,2; 35,60 (8,1; 63,1) | 4,37 (2,12; 9,03) | 0,0002 |
Избыточная масса тела менее 10 лет | 23,1; 16,99 (6,7; 27,3) | 3,79 (1,66; 8,65) | 0,0006 |
ИМ в зимний период | 21,8; 14,84 (4,6; 25,1) | 3,13 (1,42; 6,90) | 0,003 |
Масса тела ≥ 81,8 кг | 18,8; 13,81 (5,2; 22,4) | 3,8 (1,36; 10,64) | 0,005 |
Периферические ангиопатии | 18,9; 12,99 (4,0; 22,0) | 3,21 (1,26; 8,19) | 0,008 |
ХНМК | 19,8; 12,78 (3,2; 22,4) | 2,83 (1,24; 6,45) | 0,009 |
Психо-эмоциональный стресс | 15,9; 15,9 | - | 0,01 |
Кризовое течение АГ | 15,9; 15,9 | - | 0,01 |
Изменения метеофакторов | 15,9; 15,9 | - | 0,01 |
Нестабильная стенокардия в анамнезе | 19,8; 11,72 (1,7; 21,7) | 2,46 (1,14; 5,28) | 0,02 |
Курение ≥20 лет | 16,4; 12,65 (4,7; 20,7) | 4,35 (1,06; 17,83) | 0,02 |
Возраст ˂53 лет | 18,6; 11,27 (1,9; 20,6) | 2,54 (1,11; 5,81) | 0,02 |
Язвенная болезнь | 25,8; 15,31 (-0,8; 31,4) | 2,46 (1,16; 5,19) | 0,02 |
АГ ≥ семи лет | 21,4; 11,94 (0,1; 23,8) | 2,26 (1,10; 4,64) | 0,03 |
Мочекаменная болезнь & подагра | 50,0; 37,83 (-11,4; 87,1) | 4,11 (1,43; 11,77) | 0,03 |
Курение как в настоящем, так и в анамнезе | 15,8; 11,50 (3,2; 19,8) | 3,7 (0,91; 15,12) | 0,04 |
Примечание: P – критерий достоверности
Как видно из таблицы 1, среди изученных основных факторов кардиоваскулярного риска наиболее значимыми для развития ОПП у обследованных оказались: избыточная масса тела в анамнезе (≥81,8 кг) с коротким анамнезом, курение, возраст, АГ с кризовым течением давностью семь и более лет. Из дополнительных: операции реваскуляризации в анамнезе; зимний период ИМ; периферические ангиопатии, в том числе – хроническая недостаточность мозгового кровообращения (ХНМК); психоэмоциональный стресс, изменения метеофакторов как причина ИМ; нестабильная стенокардия; наличие язвенной болезни желудка и/или 12-перстной кишки, а также подагры в сочетании с мочекаменной болезнью в анамнезе (табл. 1).
Достоверное влияние параметров клинического течения ИМ на риск развития ОПП, полученное методом анализа рисков, представлено в таблице 2.
Таблица 2 - Влияние параметров клинического течения ИМ на риск развития ОПП у обследованных
Параметры клинического течения заболевания | Частота ОПП при ИМ: (абсолютный риск, %; изменение риска, % (95% ДИ)) | Относительный риск (95% ДИ) | P |
СкН & МН | 28,6; 13,26 (3,2; 23,3) | 2,77 (1,32; 5,80) | 0,008 |
Сердечная астма | 23,3; 13,26 (-0,3; 26,8) | 2,33 (1,13; 4,80) | 0,03 |
Индекс Norris ≥ 4,6 ≤ 11,7 | 16,4; 11,33 (2,9; 19,7) | 3,23 (1,01; 10,37) | 0,03 |
Общее состояние средней тяжести, тяжелое и крайне тяжелое в первые 48 часов ИМ | 14,97; 14,97 | - | 0,04 |
Примечание: P – критерий достоверности
Как видно из таблицы 2, риск развития ОПП возрастал при: сочетании осложнений групп СкН и МН, наличии сердечной астмы среди осложнений ИМ, значениях индекса R. Norris 4,9-11,66 и общем состоянии пациента в первые 48 часов ИМ средней тяжести, тяжелым или крайне тяжелым (табл. 2).
Результаты оценки взаимосвязей параметров центральной гемодинамики и риска развития ОПП у обследованных представлены в таблице 3.
Таблица 3 - Влияние параметров центральной гемодинамики на риск развития ОПП у обследованных
Параметры гемодинамики | Частота ОПП при ИМ: (абсолютный риск, %; изменение риска, % (95% ДИ)) | Относительный риск (95% ДИ) | P |
МЖП≥12 мм | 18,4; 15,30 (7,0; 23,6) | 5,89 (1,43; 24,33) | 0,004 |
СДЛА<30,4 мм рт.ст. | 19,3; 14,39 (5,6; 23,1) | 3,95 (1,41; 11,06) | 0,004 |
КДО/SI≥72,2 мл/м2 | 21,3; 14,12 (3,5; 24,7) | 2,96 (1,28; 6,82) | 0,007 |
КДР ПЖ < 26,0 мм | 25,0; 20,74 (0,9; 40,6) | 5,88 (1,24; 27,79) | 0,01 |
УИ ≥ 30,89 мл/м2 | 19,2; 12,45 (3,1; 21,8) | 2,85 (1,19; 6,81) | 0,01 |
ОЛС˂622,8 дин×с×см-5 | 16,8; 14,58 (6,7; 22,4) | 7,56 (1,05; 54,59) | 0,01 |
Ve/Va | 21,6; 15,37 (3,8; 27,0) | 3,46 (1,06; 11,24) | 0,02 |
КСО/S 38,8 мл/м2 | 20,0; 11,75 (1,2; 22,3) | 2,43 (1,09; 5,42) | 0,02 |
Примечание: P – критерий достоверности
При рассмотрении воздействия параметров центральной гемодинамики на риск развития ОПП у обследованных достоверные взаимосвязи получены для: толщины МЖП (≥12 мм), СДЛА (˂30,4 мм рт.ст), КДО/S (≥72,2 мл/м2), КДР ПЖ (˂26 мм), УИ (≥30,9 мл/м2), ОЛС (˂622,8 дин×с×см-5), Ve/Va (˂0,88) и КСО/S (≥38,8 мл/м2) (табл. 3).
Результаты оценки взаимосвязей показателей периферической гемодинамики и риска развития ОПП у обследованных представлены в таблице 4.
Таблица 4 - Влияние параметров периферической гемодинамики на риск развития ОПП у обследованных
Параметры гемодинамики | Частота ОПП при ИМ: (абсолютный риск, %; изменение риска, % (95% ДИ)) | Относительный риск (95% ДИ) | P |
АДср≥106,7 мм рт.ст. | 22,6; 18,50 (9,1; 27,9) | 5,53 (1,97; 15,51) | 0,0002 |
АДд≥90 мм рт.ст. | 20,4; 15,84 (6,9; 24,8) | 4,49 (1,60; 12,57) | 0,001 |
АДс≥140 мм рт.ст. | 18,8; 13,46 (4,8; 22,1) | 3,7 (1,32; 10,37) | 0,006 |
ОПС ≥ 1 780,7 дин×с×см-5 | 17,5; 10,48 (0,9; 20,1) | 2,49 (0,96; 6,43) | 0,047 |
Примечание: P – критерий достоверности
Как видно из таблицы 4, риск развития ОПП у обследованных значимо повышался при АГ с уровнями АДср≥106,7 мм рт.ст., диастолического≥90 мм рт.ст., систолического (АДсист)≥140 мм рт.ст. и ОПС≥1780,7 дин×с×см-5 (табл. 4).
Результаты оценки взаимосвязей параметров обмена веществ и риска развития ОПП у обследованных представлены в таблице 5.
Таблица 5 - Влияние параметров обмена веществ на риск развития ОПП у обследованных
Параметры гемодинамики | Частота ОПП при ИМ: (абсолютный риск, %; изменение риска, % (95% ДИ)) | Относительный риск (95% ДИ) | P |
Kалий<4,75 ммоль/л | 17,2; 17,2 | - | 0,003 |
ТГ≥1,88 ммоль/л | 22,95; 22,95% | - | 0,007 |
Натрий≥140 ммоль/л | 18,2; 13,18 (1,9; 24,4) | 3,64 (1,20; 11,01) | 0,01 |
Хлориды≥104,2 ммоль/л | 22,6; 3,64 (1,20; 11,01) | 3,67 (1,16; 11,61) | 0,02 |
Примечание: P – критерий достоверности
Как видно из таблицы 5, риск развития ОПП у обследованных увеличивался при: уровнях калия менее 4,75 ммоль/л, ТГ≥1,88 ммоль/л, натрия≥140,0 ммоль/л, хлоридов≥104,2 ммоль/л (табл. 5).
На следующем этапе исследования методом деревьев классификации на основе двух наиболее влияющих предикторов: периода года и уровня АДсист1≥130 мм рт.ст. построена модель прогноза развития ОПП (табл. 6).
Таблица 6 - Дерево решений для риска развития острого повреждения почек при инфаркте миокарда у обследованных
Определение класса | Объем группы | Доля класса, % | Риск, % |
Время года (Зима) & АДсист, мм рт.ст. ≥ 130,0 | 53 | 27,7 | 30,2 |
Время года (Весна, Лето, Осень) & АДсист, мм рт.ст. ≥ 135,0 | 69 | 36,1 | 11,6 |
Время года (Зима) & АДсист, мм рт.ст. < 130,0 | 24 | 12,6 | 4,2 |
Время года (Весна, Лето, Осень) & АДсист, мм рт.ст. < 135,0 | 45 | 23,6 | 0 |
Диаграмма дерева решений для оценки риска развития ОПП при ИМ у обследованных представлена на рис. 1.
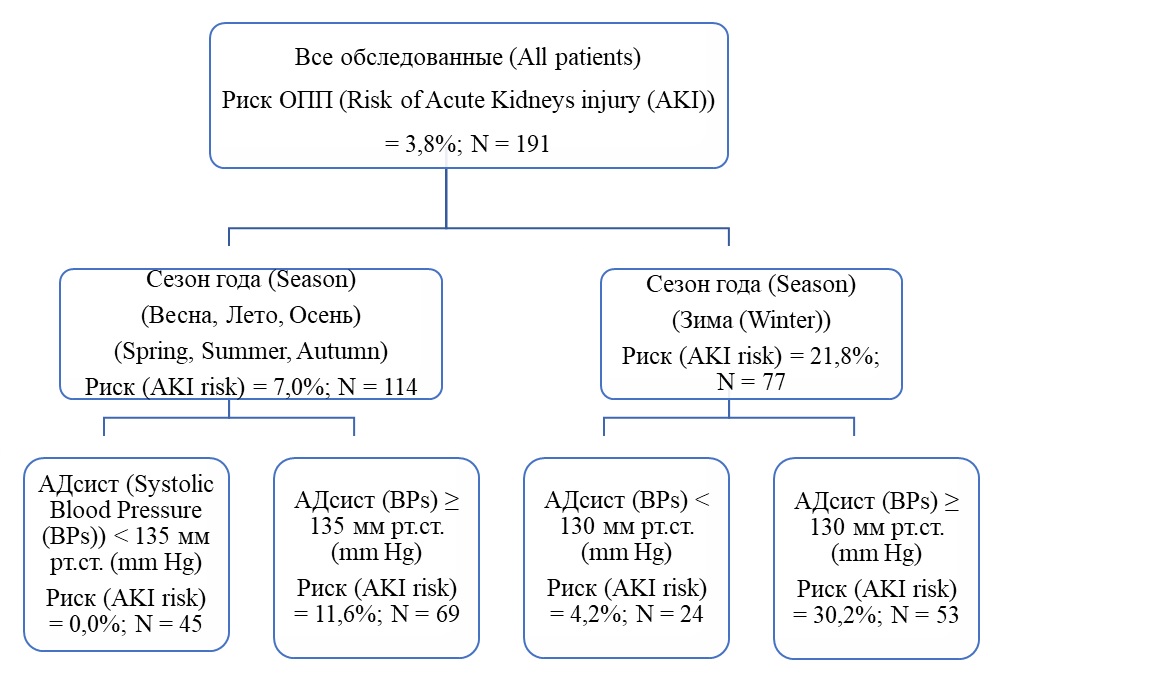
Рисунок 1 - Дерево решений для оценки риска развития острого повреждения почек при инфаркте миокарда у обследованных.
Как видно из таблицы 6, максимальный уровень риска (30,2%; объем группы 53 пациента) – у пациентов с ИМ в зимний период и АДс≥130 мм рт.ст. Минимальный уровень риска (0,0%; 45 пациентов, соответственно) развития ОПП получен для ИМ в весенний, летний и осенний периоды и АДс˂135,0 мм рт.ст. При АДс≥135 мм рт.ст. в эти периоды риск развития ОПП повышается до 11,6% (объем группы 69). В зимний период при снижении АДсист1 менее 130 мм рт.ст. риск развития ОПП уменьшается до 4,2% (объем выборки 24 случая).
Результаты ROC-анализа и прогнозные показатели качества построенного дерева-решений представлены в таблице 7. Точка отсечения (11,6%) представляет собой оптимальную границу отделения положительного прогноза от отрицательного.
Таблица 7 - Прогнозные показатели качества дерева-решений
Показатель | Значение |
Точка отсечения, % | 11,6 |
AuROC | 0,85 |
Чувствительность, % | 94,1 |
Специфичность, % | 70,9 |
Эффективность, % | 82,5 |
Значение AuROC (0,85) свидетельствует о высоком прогнозном качестве полученной модели, что позволяет рекомендовать ее к практическому применению.
На основании моделирования к группе высокого риска развития ЛГ после ИМ относятся пациенты с расчетным (согласно модели) риском в 11,6% и выше. Этим пациентам показано наблюдение с целью раннего выявления ОПП и быстрого проведения комплекса диагностических и лечебных мероприятий. С учетом параметров модели ее целесообразно использовать в сочетании с другими методами диагностики ОПП или при невозможности и или затруднении своевременного их выполнения.
4. Обсуждение
В настоящее время связанными с ОПП состояниями признаются: АГ (при нефросклерозе), анемия, сахарный диабет, двусторонний стеноз почечных артерий, хроническая болезнь почек и хроническая сердечная недостаточность , , . Помимо этого, к ним также относят нарушения липидного обмена, метаболический синдром и рак , , . Потенциально модифицируемыми факторами риска развития ОПП рассматриваются: дегидратация, гипотония, нефротоксические лекарственные препараты, безнатриевая диета и выполнение рентгенконтрастных исследований , , . К немодифицируемым – пожилой (≥65 лет) возраст, мужской пол, женский пол при кардиохирургических операциях и рентгенконтрастных исследованиях, негроидная раса , , .
В настоящем исследовании выявлены дополнительные предикторы ОПП при ИМ в дополнение к установленным факторам риска ее развития. Среди них необходимо отметить психологический стресс, климатический зимний период, гипертриглицеридемию (≥1,88 ммоль/л) и язвенную болезнь в анамнезе. Выявленные особенности факторов риска ОПП связаны с конкретной клинической ситуацией (ИМ), ограничениями анализируемой группы по возрасту, полу, геолокации. Взаимосвязь поражения почек и зимнего периода года описана ранее для мужчин моложе 60 лет с ИМ . Значение ассоциированной с хеликобактерозом язвенной болезни для развития атеросклероза и связанных с ним осложнений у этой категории пациентов рядом исследователей считается вполне закономерным , . Однако эта гипотеза признается не всеми авторами и требует более обоснованных доказательств . Гипертриглицеридемия указывает на выраженность метаболических нарушений при изученной критической ситуации. Последнее подтверждается полученным в настоящем исследовании достоверным значением стрессовой ситуации для развития ОПП.
Необходимо уточнить, что внедрение концепции ОПП выглядит существенным достижением из-за повышения частоты выявления поражения почек у стационарных пациентов почти в семь раз при ее применении , , . Однако требующей решения проблемой остается ранняя диагностика ОПП из-за того, что при утвержденном в рекомендательных документах способе ее верификации, основанном на определении креатинина в сыворотке крови, теряется от 12 до 24 часов возможного «терапевтического окна» , , . В то же время внедрение рутинного скрининг-тестирования ОПП с помощью лабораторных его маркеров (NGAL (neutrophil gelatinase-associated lipocalin)), KIM-1 (kidney injury molecule-1) цистатин С и др. и дополнительных показателей для дифференциальной диагностики патогенетического типа ОПП (осмолярность мочи, экскреция креатинина, мочевины, натрия и хлоридов мочой, мочевые индексы), урологическое обследование ограничено с одной стороны, их дороговизной и технологическими трудностями, с другой – невысокой частотой этого осложнения , , . Полученный алгоритм позволяет на более ранних стадиях заболевания выделить среди пациентов с ИМ группу высокого риска развития ОПП (11,6%), которым показано дополнительное обследование и лечение.
5. Заключение
Таким образом, существующие в настоящее время методы прогноза развития ОПП разнообразны, но не всегда применимы у мужчин молодого и среднего возраста при ИМ.
Прогностический алгоритм, полученный с помощью метода дерева решений, включающий три класса риска (от 4,2 до 30,0%) на основе измерения АД в первые часы ИМ и сезона года имеет характеристики, позволяющие рекомендовать его применение в повседневной клинической практике в качестве дополнения к существующим стандартам для оценки вероятности развития ОПП при ИМ у обследованных.
Использование полученного алгоритма для прогнозирования появления ОПП в начальные периоды ИМ с целью выделения группы риска его развития позволит в более ранние сроки заподозрить появление этого осложнения, провести необходимые дополнительные методы обследования и выбрать подходящее лечение.
