ПОКАЗАТЕЛИ КРОВИ КРЫС ПРИ ХРОНИЧЕСКОМ ВВЕДЕНИИ НОВЫХ ЧАСТИЧНО ГИДРИРОВАННЫХ ПИРИДИНОВ, ПРОИЗВОДНЫХ α-ЦИАНОТИОАЦЕТАМИДА
ПОКАЗАТЕЛИ КРОВИ КРЫС ПРИ ХРОНИЧЕСКОМ ВВЕДЕНИИ НОВЫХ ЧАСТИЧНО ГИДРИРОВАННЫХ ПИРИДИНОВ, ПРОИЗВОДНЫХ α-ЦИАНОТИОАЦЕТАМИДА
Аннотация
Кровь является одним из важнейших показателей общего состояния организма, по которому возможно оценить адаптационные и патологические изменения на фоне длительного воздействия различных ксенобиотиков. На базе научно-исследовательской лаборатории ФГБОУ ВО ЛГМУ им. Свт. Луки Минздрава России реализовано экспериментальное исследование. Целью исследования стал биохимический анализ крови крыс с целью определения гематотоксичности новых опытных образцов. Эксперимент проведен на 120 беспородных лабораторных животных — половозрелых крысах-самцах. Препараты сравнения — метамизол натрия (7 мг/кг) и мефенаминовая кислота (5 мг/кг). Биохимический анализ реализован с помощью анализатора Solar PM2111 с использованием требуемых реактивов. Наивысший уровень гемоглобина зарегистрирован в группе крыс, получавших соединение с шифромcv-099. Наименьший результат с предполагаемыми проявлениями лейкопении зарегистрирован в группе, получавшей препарат сравнения метамизол натрия — 4,99±0,41 х 109/л. Далее следует результат, полученный в группе животных, получавших мефенаминовую кислоту — 6,71±0,41 х 109/л. Наименьшее количество тромбоцитов зафиксировано у крыс, получавших внутрижелудочно метамизол натрия — 568,13±4,12 х 109/л. В остальных опытных группах результаты стабильны и сопоставимы с данными в контрольной группе. По показателю скорости оседания эритроцитов (СОЭ) в ходе лабораторного исследования не зафиксированы относительные отклонения от значений интактной и контрольной групп. В ходе эксперимента был также исследован показатель С-реактивного белка и во всех опытных группах получен отрицательный результат. В ходе реализованного экспериментального исследования гематотоксичности новых образцов, производных α-ЦТА, установлено, что соединения cv-091, cv-095, cv-099, cv-142 не влияют на уровень гемоглобина в крови, не вызывают выраженных проявлений лейкопении, тромбоцитопении.
1. Введение
Потребление лекарственных препаратов пациентами имеет тенденцию к неуклонному росту. Согласно информации, изложенной в базе данных «Аудит розничных продаж лекарственных препаратов в России» аналитической компании RNC Pharma, каждый житель Российской Федерации в 2024 году приобрел 33,4 упаковки лекарств . Хроническое и бесконтрольное использование лекарственных препаратов — актуальная проблема современной фармакологии. Полипрагмазия, сочетанное применение препаратов, самолечение не проходят для организма человека бесследно. Каждый препарат обладает определенным спектром нежелательных фармакологических явлений (побочных эффектов) , , которые в той или иной степени проявляются, оказывая значительное действие на органы-мишени и могут варьироваться в зависимости от возраста пациента, пола, а также тяжести основных и сопутствующих заболеваний, острых состояний и хронических патологий .
В связи с этим актуальным является реализация научных исследований в области поиска новых эффективных и безопасных биологически активных компонентов. Особый интерес для исследователей представляет α-цианотиоацетамид и его производные, которые в схожих экспериментальных опытах показали себя как активные и относительно безопасные полифункциональные химические структуры , , , . В ходе данного исследования реализовано изучение влияния производных α-цианотиоацетамида на гемостаз и сердечно-сосудистую систему лабораторных крыс, основанном на биохимическом анализе крови. Кровь является одним из важнейших показателей общего состояния организма, по которому возможно оценить адаптационные и патологические изменения на фоне длительного воздействия различных ксенобиотиков, что имеет значимую роль в доклинических испытаниях новых лекарственных средств и позволяет определить ранние признаки токсического действия препаратов , , .
2. Методы и принципы исследования
Экспериментальные исследования проводились на базе научно-исследовательской лаборатории ФГБОУ ВО ЛГМУ им. Свт. Луки Минздрава России (Российская Федерация, Луганская народная республика, г. Луганск, кв. 50-летия Обороны Луганска, д. 1г). В качестве опытных животных использованы белые беспородные крысы-самцы, полученные из специализированного вивария учебного заведения. Животные на протяжении исследования содержались в соответствии с руководством ARRIVE, правилами работы с лабораторными животными на основе положений Хельсинской декларации и рекомендаций, содержащихся в Директиве ЕС 86/609ЕСС и Конвенции Совета Европы по защите позвоночных животных, используемых для экспериментальных и других научных целей, а также иных актов, соответствующих современным требованиям по реализации доклинических исследований на животных. Исследования одобрены комиссией по биоэтике ФГБОУ ВО ЛГМУ им. Свт. Луки Минздрава России (протокол заседания № 5 от 10.12.2022 г.).
Во время эксперимента опытные животные содержались на стандартном пищевом рационе с соблюдением питьевого режима и постоянным доступом к воде. На протяжении экспериментальной части работы все исследования реализовывались в соответствии с Федеральным законом «Об ответственном обращении с животными и о внесении изменений в отдельные законодательные акты Российской Федерации» от 27.12.2018 № 498-ФЗ; Федеральным законом «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ; ГОСТ 33216-2014 «Правила работы с лабораторными грызунами и кроликами» (принят Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 22 декабря 2014 г. № 73-П)), учитывающий положения Европейской конвенции о защите позвоночных животных, используемых в экспериментах и в других научных целях (European Convention for the protection of Vertebrate animals used for experimental and other scientific purposes (EST № 123)), а также в соответствии с иными соответствующими нормативно-правовыми актами.
До начала эксперимента все животные были тщательно осмотрены и отобраны согласно следующим критериям: масса тела, состояние кожного и шерстистого покрова, состояние слизистых, отсутствие видимой травматизации животного и нагноений кожных покровов, отсутствие повреждения зоны вибрисс, передних и задних конечностей, хвоста. Помимо вышеуказанного, оценивалась общая двигательная и поведенческая активность животного. Согласно данным критериям, для участия в экспериментальном исследовании отобрано 120 животных, которые распределены на 12 опытных групп рандомизированным методом «конвертов». Общий дизайн исследования сформирован в виде схемы (см. рис. 1).
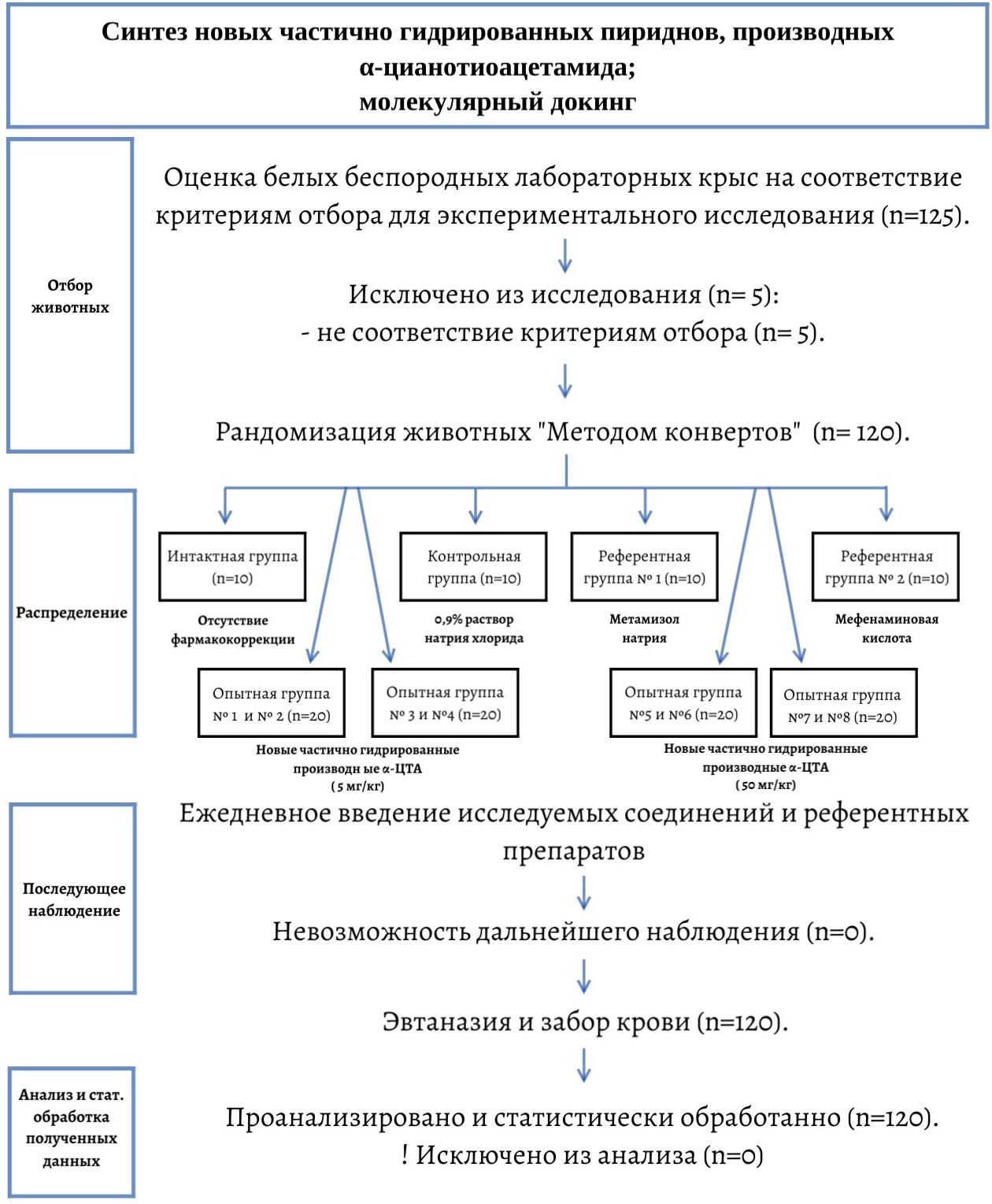
Рисунок 1 - Дизайн исследования хронической токсичности новых частично гидрированных пиридинов, производных α-ЦТА
Опытные образцы, частично гидрированные пиридины, производные α-цианотиоацетамида (см. рис. 2), синтезированы и предоставлены для исследований научно-исследовательской лабораторией «ХимЭкс» ФГБОУ ВО ЛГУ им. В. Даля, под руководством д.х.н., проф. С.Г. Кривоколыско.
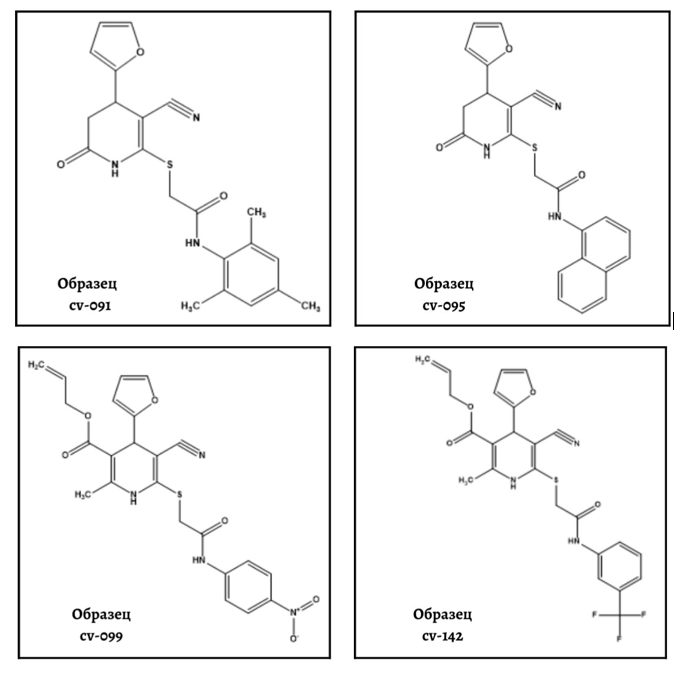
Химическая структура новых частично гидрированных пиридинов, производных α-ЦТА
В исследованиях по определению биологической активности производные α-цианотиоацетамида показали значимые результаты в опытах по исследованию анальгетической, противовоспалительной и жаропонижающей активности , , .
Фармакокоррекция осуществлялась в соответствующих условиях: группа сравнения № 1 получала метамизол натрия (производное пиразолона, неопиоидный анальгетик) в дозировке 7 мг/кг массы тела; группа сравнения № 2 получала мефенаминовую кислоту (фенамат, производное антраниловой кислоты) в дозировке 5 мг/кг; опытные группы № 1 (cv-091), № 2 (cv-095), № 3 (cv-099), № 4 (cv-142) получали образцы новых частично гидрированных пиридинов, производных α-ЦТА, в дозировке 5 мг/кг; опытные группы № 5 (cv-091), № 6 (cv-095), № 7 (cv-099), № 8 (cv-142) получали образцы новых частично гидрированных пиридинов, производных α-ЦТА, в дозировке 50 мг/кг.
Путь введения — внутригастральный, с помощью желудочного зонда. В интактной группе отсутствовала фармакокоррекция. В группе контроля животные на протяжении всего экспериментального исследования получали внутрижелудочно 0,9% раствор натрия хлорида. Растворителем во всех случаях являлась вода очищенная (aqua destillata).
Хроническое воздействие на организм животного смоделировано ежедневным введением препаратов на протяжении 14-ти календарных дней с принудительным голоданием в течение 16 часов до введения суспензии согласно методическим рекомендациям . На пятнадцатые сутки произведена эвтаназия животных с забором крови. Биохимический анализ реализован с помощью анализатора Solar PM2111 с использованием требуемых реактивов.
Статистическая обработка полученных результатов проведена с применением программ Microsoft Excel 2019, а также Statistica 10.0 для Windows. Ввиду ненормального характера распределения выборки беспородных лабораторных крыс, использован непараметрический метод обработки данных с помощью Т-критерия Уилкоксона и расчета коэффициентов вариации. Изменчивость ряда принято считать незначительной в случае, если коэффициент вариации менее 10% .
3. Основные результаты
Одним из ключевых показателей состояния кровеносной системы является гемоглобин (Hb) — железосодержащий белок, находящийся внутри эритроцитов. Согласно полученным результатам (см. табл. 1), можно сделать вывод о том, что наименьшие значения гемоглобина, согласно данным биохимического анализа, зафиксированы в референтной группе № 1, получавшей метамизол натрия.
Таблица 1 - Результаты биохимического анализа крови по показателю гемоглобин
Опытная группа | а, ед/л | Ме, ед/л | σ | σ2 | К, % | p |
Интактная | 134,88 ±0,95 | 135,0 | 2,70 | 7,27 | 2,0% | - |
Контрольная (0,9% NaCl) | 135,63 ±0,84 | 136,5 | 2,39 | 5,70 | 1,76% | *0,595 |
Референтная 1 (метамизол натрия) | 108,13 ±2,18 | 106,5 | 6,17 | 38,13 | 5,70% | **0,0009 |
Референтная 2 (мефенаминовая кислота) | 114,63 ±1,05 | 114,5 | 2,97 | 8,84 | 2,60% | **0,00089 |
cv-091 | 132,75 ±1,23 | 133,0 | 3,24 | 10,5 | 2,40% | **0,0788 |
cv-095 | 131,75 ±0,92 | 131,0 | 2,60 | 6,79 | 1,98% | **0,00733 |
cv-099 | 135,0 ±0,6 | 135,0 | 1,69 | 2,86 | 1,25% | **0,556 |
cv-142 | 132,88 ±1,30 | 132,0 | 3,68 | 13,55 | 2,77% | **0,062 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Стоит отметить, что относительно среднего показателя, полученного в интактной группе, который составил 134,88±0,95 г/л и в контрольной группе 135,63±0,84 г/л, в группе сравнения № 1 наблюдаются первичные признаки анемии. В группе сравнения № 2 результат также отличается от данных интактной и контрольной групп и составляет 114,63±1,05. Опытные группы показывают удовлетворяющий результат. Наивысший уровень гемоглобина зарегистрирован в группе, получавших соединение с шифром cv-099. Из всех опытных соединений наименьший результат по данному показателю у группы cv-142. В группах cv-095 и cv-091 данные стабильны, с минимальным разбросом относительно контрольной группы. В результате статистической обработки определено, что зафиксированные отклонения статистически значимы, различия достоверны.
Снижение уровня гемоглобина в крови крыс можно связать с потенциальным воздействием нестероидных противовоспалительных средств на желудочно-кишечный тракт, в частности, на слизистую оболочку кишечника, что влияет на всасываемость железа.
Хроническое потребление НПВС также зачастую сопряжено с воздействием на уровень лейкоцитов в крови. Снижение количества лейкоцитов приводит к ослаблению иммунной реакции организма и возрастанию риска развития инфекций в организме. В ходе исследования, в интактной группе был получен следующий показатель содержания лейкоцитов — 8,26±0,1 х 109/л, а в группе контроля — 8,26±0,098 х 109/л. Остальные группы в порядке возрастания имеют следующую тенденцию (см. табл. 2).
Таблица 2 - Концентрация лейкоцитов в периферической крови крыс, получавших новые производные α-ЦТА
Опытная группа | а, × 10⁹/л | Ме, × 10⁹/л | σ | σ2 | К, % | p |
Интактная | 8,26 ±0,100 | 8,25 | 0,28 | 0,08 | 3,42% | - |
Контрольная (0,9% NaCl) | 8,26 ±0,098 | 8,25 | 0,28 | 0,78 | 3,36% | *0,563 |
Референтная 1 (метамизол натрия) | 4,99 ±0,145 | 4,90 | 0,40 | 0,16 | 8,12% | **0,00046 |
Референтная 2 (мефенаминовая кислота) | 6,71 ±0,146 | 6,75 | 0,41 | 0,17 | 6,14% | **0,00047 |
cv-091 | 8,39 ±0,104 | 8,35 | 0,29 | 0,087 | 3,51% | **0,525 |
cv-095 | 8,50 ±0,146 | 8,50 | 0,34 | 0,17 | 4,87% | **0,246 |
cv-099 | 8,59 ±0,32 | 8,50 | 0,44 | 0,169 | 4,84% | **0,225 |
cv-142 | 7,96 ±0,131 | 7,95 | 0,37 | 0,137 | 4,65% | **0,161 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Наименьший результат с предполагаемыми проявлениями лейкопении зарегистрирован в группе, получавшей препарат сравнения метамизол натрия, и составляет 4,99±0,145 х 109/л. Затем следует результат, полученный в группе, получавшей мефенаминовую кислоту — 6,71±0,146 х 109/л. Среди новых образцов, производных α-ЦТА, умеренно стабильный результат относительно контрольной группы был получен в группах cv-091, cv-095, cv-099. В опытной группе cv-142 у животных зафиксирован результат, превышающий данные референтных групп, однако уступающий результатам группы контроля. В ходе исследования отсутствовала возможность исследования развернутой лейкоцитарной формулы, данные показатели требуют дальнейшего детального изучения.
Хроническое потребление ксенобиотиков может влиять на количество тромбоцитов в крови, воздействовать на функцию тромбоцитов, особенно в сочетании с иными факторами риска. В ходе исследования изучены показатели количества тромбоцитов в крови животных (см. табл. 3).
Таблица 3 - Концентрация тромбоцитов в периферической крови крыс, получавших новые производные α-ЦТА
Опытная группа | а, × 10⁹/л | Ме, × 10⁹/л | σ | σ2 | К, % | p |
Интактная | 620,63 ±2,51 | 621,5 | 7,09 | 50,27 | 1,14% | - |
Контрольная (0,9% NaCl) | 623,0 ±4,35 | 626,0 | 12,31 | 151,43 | 1,98% | *0,4420 |
Референтная 1 (метамизол натрия) | 568,13 ±1,46 | 569,5 | 4,12 | 16,9 | 0,73% | **0,00016 |
Референтная 2 (мефенаминовая кислота) | 581,75 ±1,36 | 580 | 3,85 | 14,79 | 0,66% | **0,00093 |
cv-091 | 613,75 ±1,78 | 612,5 | 5,04 | 25,36 | 0,82% | **0,0736 |
cv-095 | 620,0 ±3,78 | 618,5 | 3,78 | 14,29 | 0,61% | **0,2470 |
cv-099 | 614,75 ±1,50 | 614,0 | 4,23 | 17,90 | 0,69% | **0,0910 |
cv-142 | 612,63 ±5,18 | 619,0 | 14,65 | 214,55 | 2,39% | **0,0570 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Наименьшее количество тромбоцитов зафиксировано в группе животных, получавших внутрижелудочно метамизол натрия — 568,13±1,46 х 109/л. Однако стоит отметить, что в группе животных, получавших мефенаминовую кислоту, зафиксирован результат с относительно минимальным разбросом — 581,75±1,36 х 109/л, что может свидетельствовать о начальных проявлениях тромбоцитопении в данных группах. В остальных опытных группах результаты стабильны и сопоставимы с данными, полученными в контрольной группе.
По показателю скорости оседания эритроцитов (СОЭ), в ходе лабораторного исследования, не зафиксированы относительные отклонения от интактной и контрольной групп. Данные стабильны с минимальным разбросом (см. табл. 4).
Таблица 4 - Результаты биохимического анализа крови по показателю скорости оседания эритроцитов (СОЭ)
Опытная группа | а, мм/ч | Ме, мм/ч | σ | σ2 | К, % | p |
Интактная | 2,10 ±0,020 | 2,10 | 0,060 | 0,0030 | 2,73% | - |
Контрольная (0,9% NaCl) | 2,11 ±0,018 | 2,11 | 0,047 | 0,0022 | 2,24% | *0,816 |
Референтная 1 (метамизол натрия) | 1,97 ±0,027 | 1,97 | 0,078 | 0,0060 | 3,94% | **0,0062 |
Референтная 2 (мефенаминовая кислота) | 1,98 ±0,026 | 2,0 | 0,073 | 0,0053 | 3,66% | **0,0091 |
cv-091 | 2,11 ±0,040 | 2,11 | 0,038 | 0,0015 | 1,84% | **0,955 |
cv-095 | 2,13 ±0,030 | 2,14 | 0,038 | 0,0014 | 1,77% | **0,281 |
cv-099 | 2,08 ±0,030 | 2,08 | 0,033 | 0,0011 | 1,59% | **0,162 |
cv-142 | 2,11 ±0,020 | 2,11 | 0,023 | 0,0005 | 1,10% | **0,769 |
Примечание: *р – достоверно в отношении группы без фармакокоррекции (при p≥0,05); **р – достоверно в отношении контрольной группы (при p≥0,05)
Показатель СОЭ является относительным маркером воспалительных реакций, протекающих в организме животного, однако зависит от многих факторов и не имеет тенденции к неуклонному снижению.
В ходе эксперимента был также исследован показатель С-реактивного белка и во всех опытных группах получен отрицательный результат.
Биохимические показатели крови крыс, получавших внутрижелудочно новые соединения — частично гидрированные пиридины, производные α-цианотиоацетамида, в дозировке 50 мг/кг представлены в таблице 5.
Таблица 5 - Результаты биохимического анализа крови животных, получавших, производные α-ЦТА, в дозе 50 мг/кг
Опытная группа | Показатель гемоглобина, ед/л | Концентрация лейкоцитов, × 10⁹/л | Концентрация тромбоцитов, × 10⁹/л |
cv-091 | 133,63 ± 0,91 **p = 0,1970 | 8,43 ± 0,11 **р = 0,3620 | 613,75 ± 1,78 **p = 0,2340 |
cv-095 | 132,08 ± 0,74 **p = 0,1370 | 8,37 ± 0,20 **p = 0,4290 | 625,85 ± 2,64 **p = 0,1547 |
cv-099 | 133,20 ± 1,03 **p = 0,2350 | 8,46 ± 0,25 **p = 0,4680 | 617,88 ± 2,11 **p = 0,1880 |
cv-142 | 133,12 ± 0,72 **p = 0,2790 | 8,01 ± 0,17 **p = 0,1370 | 614,93 ± 4,07 **p = 0,1720 |
Примечание: **р – достоверно в отношении контрольной группы (при p≥0,05)
Показатель скорости оседания эритроцитов в группах, получавших опытные соединения в дозе 50 мг/кг стабилен и не имел значимых отклонений от данных, полученных в интактной и контрольной группе. Зафиксированные различия не имели статистической значимости.
Также стоит отметить, что введение десятикратной дозировки (50 мг/кг) синтезированных соединений не повлияло на поведенческую активность лабораторных животных, было зафиксировано нормальное состояние глаз и слизистых оболочек, их цвет оставался неизменным, рефлексы и реакции на болевые, световые, звуковые и тактильные раздражения в норме.
4. Заключение
В результате реализованного экспериментального исследования гематотоксичности новых частично гидрированных пиридинов, производных α-цианотиоацетамида, с лабораторными шифрами cv-091, cv-095, cv-099, cv-142 в дозировках 5 мг/кг и 50 мг/кг установлено, что опытные образцы не влияют на уровень гемоглобина в крови, не вызывают выраженных проявлений лейкопении и тромбоцитопении.
В ходе доклинических исследований фармакологической активности исследуемых образцов, установлена выраженная анальгетическая активность, противовоспалительные и жаропонижающие свойства, что делает данные образцы перспективными для дальнейших исследований их безопасности с увеличением числа экспериментальных животных.
