Клиническое течение дилатационной кардиомиопатии у подростка: от манифестации до ортотопической трансплантации сердца
Клиническое течение дилатационной кардиомиопатии у подростка: от манифестации до ортотопической трансплантации сердца
Аннотация
Дилатационная кардиомиопатия (ДКМП) в детском возрасте остается одной из самых серьезных проблем кардиологии, являясь частой причиной сердечной недостаточности и наиболее частым показанием к трансплантации сердца у подростков. Распространённость ДКМП у детей оценивается в пределах 0,57–1,13 случая на 100 000 человек, что составляет около половины всех кардиомиопатий, выявляемых в детском возрасте
. В данной научной работе представлен подробный разбор сложного клинического случая пациентки 16 лет с ДКМП, сопровождающейся тяжелой сердечной недостаточностью и выявленным вторичным дефектом межпредсердной перегородки. Освещена динамика состояния больной от момента первичной диагностики до выполнения ортотопической трансплантации сердца, ставшей ключевым этапом радикальной терапии. Данное клиническое наблюдение подчеркивает необходимость мультидисциплинарного подхода и тщательного мониторинга в детской кардиологии.Цель исследования — проанализировать клиническое течение дилатационной кардиомиопатии у подростка, включая ответ на консервативную терапию и результаты трансплантации сердца.
1. Введение
Дилатационная кардиомиопатия в педиатрической практике представляет собой патологию миокарда, патогномоничными признаками которой являются расширение полостей обоих желудочков и предсердий, а также выраженное угнетение систолической функции и сократимости . Данная патология относится к категории критических состояний, при которых трансплантация сердца выступает в качестве наиболее радикального и эффективного метода лечения как в педиатрической, так и во взрослой практике. Внедрение методов трансплантологии позволило существенно увеличить показатели выживаемости и продолжительность жизни детей с данным диагнозом. Высокая летальность в течение первого года после верификации диагноза зачастую обусловлена поздней манифестацией заболевания, когда возможности консервативной терапии уже исчерпаны . Своевременная диагностика ДКМП является глобальной задачей здравоохранения, поскольку ранняя верификация позволяет своевременно оптимизировать терапевтическую поддержку.
Кардиомиопатии, подразделяющиеся на первичные (генетические или приобретенные) и вторичные (связанные с системными заболеваниями), являются важной причиной сердечной недостаточности и показанием к трансплантации сердца . Этиологические факторы включают миокардит различной вирусной природы (парвовирус B19, грипп, ВИЧ, Коксаки, герпес, аденовирусы), нервно-мышечные расстройства (мышечная дистрофия Дюшенна/Беккера) и ятрогенное воздействие (антрациклины) . Генетическая этиология играет существенную роль, с преобладанием аутосомно-доминантного типа наследования, но также встречаются аутосомно-рецессивные, Х-сцепленные и митохондриальные формы (20-48% случаев) . Следовательно, ключевыми причинами миокардиальной дисфункции, прогрессирующей до ДКМП, являются: персистенция вирусных агентов в миокарде после инфекционного эпизода; аутоиммунные реакции, приводящие к лимфоцитарному миокардиту; или генетические дефекты структурных белков. Последние не только вызывают непосредственную дисфункцию миокарда, но и могут быть причиной нарушений проводимости.
Патогенез ДКМП инициируется повреждением кардиомиоцитов под воздействием различных этиологических факторов, что приводит к уменьшению пула функциональных мышечных элементов. Это вызывает развитие сердечной недостаточности, характеризующейся выраженным снижением сократительной способности миокарда (систолическая дисфункция желудочков) и быстрой дилатацией всех камер сердца . Прогрессирование заболевания приводит к критическому ухудшению насосной функции, росту конечно-диастолического давления в желудочках и миогенной дилатации полостей, что обусловливает относительную недостаточность митрального и трехстворчатого клапанов. Одновременно активируются нейрогормональные системы (симпатоадреналовая и ренин-ангиотензин-альдостероновая системы), которые, несмотря на компенсаторный характер, способствуют дальнейшему повреждению кардиомиоцитов, снижению сердечного выброса и повышению периферического сопротивления. Это приводит к развитию застойной сердечной недостаточности в обоих кругах кровообращения. Также наблюдается дисбаланс в системе гемостаза, предрасполагающий к образованию внутрисердечных тромбов и системным тромбоэмболиям .
Клиническая картина ДКМП у пациентов характеризуется симптомами сердечной недостаточности, такими как потливость, одышка, ортопноэ и снижение толерантности к физическим нагрузкам. У детей младшего возраста часто наблюдаются снижение аппетита и кахексия. Характер болевого синдрома отличается значительной вариабельностью: пациенты могут описывать ощущения как колющие, ноющие, а в ряде случаев — как сжимающие или давящие боли. У части больных интенсивность болевых ощущений остается низкой, проявляясь лишь субъективным чувством дискомфорта в грудной клетке. При вовлечении в патологический процесс заднедиафрагмальных отделов левого желудочка возможна атипичная локализация, в виде болей в эпигастральной области, сопровождающихся диспептическими расстройствами, такими как тошнота и рвота. При объективном осмотре выявляются синусовая тахикардия, набухание яремных вен, бледность и гепатомегалия. Поздние признаки включают периферические отеки и асцит. Аускультативно может определяться шум митральной регургитации. Инструментально ДКМП характеризуется кардиомегалией, дилатацией левого желудочка (часто бивентрикулярной), систолической дисфункцией ЛЖ (с истончением стенок и глобальной гипокинезией) и диастолической дисфункцией ЛЖ . Снижение сердечного выброса приводит к усталости, кахексии, узкому пульсовому давлению, дикротическому пульсу, одышке, похолоданию конечностей, а также к когнитивной дисфункции и почечной недостаточности вследствие гипоперфузии органов. Диастолическая дисфункция ЛЖ является непосредственной причиной одышки и ортопноэ. К осложнениям ДКМП относятся аритмии (например, фибрилляция предсердий) и тромбоэмболические события (например, тромбоз стенок левого желудочка), которые могут привести к внезапной сердечной смерти .
Определение оптимальной тактики ведения пациентов с кардиомиопатиями требует проведения комплексного обследования. Индикатором повреждения и деструкции кардиомиоцитов служит повышение концентрации в крови ряда биохимических маркеров. К ним относятся: МВ-фракция креатинфосфокиназы (МВ-КФК), изоферменты лактатдегидрогеназы (ЛДГ 1+2), NT-proBNP - мозговой натрийуретический пептид, а также кардиальные тропонины I и Т .
Электрокардиография (ЭКГ) у пациентов с кардиомиопатией может выявлять ряд характерных изменений. К ним относятся умеренно выраженные признаки гипертрофии левого желудочка и левого предсердия. Часто регистрируются нарушения внутрижелудочковой проводимости, такие как блокада левой ножки пучка Гиса или ее передневерхней ветви. Кроме того, ЭКГ может отражать различные нарушения сердечного ритма, в частности, мерцательную аритмию (фибрилляцию предсердий) и желудочковые аритмии , .
Эхокардиография (ЭхоКГ) является ключевым и общедоступным методом для выявления ряда характерных изменений, свидетельствующих о ДКМП. К ним относятся: значительное расширение полостей сердца, в первую очередь левого желудочка и левого предсердия, при относительно небольшой толщине их стенок. Наблюдается существенное увеличение конечного диастолического объема левого желудочка, а также выраженное нарушение его сократимости, проявляющееся гипокинезией задней стенки ЛЖ и межжелудочковой перегородки, что приводит к резкому снижению фракции выброса (менее 30–40%) .
Эндомиокардиальная биопсия выявляет комплекс морфологических изменений, характерных для ДКМП. Отмечается обширная (более 30%) необратимая альтерация миокарда с замещающим склерозом, при этом выраженность компенсаторной гипертрофии остается относительно низкой, а признаки активной воспалительной реакции (экссудативные и пролиферативные проявления) отсутствуют. Дополнительно наблюдается атрофия более 50% жизнеспособных сократительных кардиомиоцитов. Характерным является также универсальное поражение ядерного аппарата, проявляющееся полиморфизмом и аморфностью ядер сократительных кардиомиоцитов, а также индукцией формирования в них ядрышкового аппарата .
Высокотехнологичные методы визуализации играют ключевую роль в детальной оценке характера изменений в миокарде. К ним относятся магнитно-резонансная томография (МРТ) с контрастированием парамагнитными препаратами, а также томосцинтиграфия миокарда , . Данный метод позволяет детально оценить степень дилатации желудочковых камер, морфологические изменения миокарда, наличие фиброза, а также функциональное состояние сердца, включая насосную функцию и показатели деформации желудочков. Кроме того, МРТ может способствовать идентификации источника нарушений сердечного ритма, что имеет решающее значение для дифференциальной диагностики, определения типа и тяжести кардиомиопатии, а также для исключения аритмогенной правожелудочковой кардиомиопатии. Использование гадолиниевого контрастного вещества в МРТ сердца открывает возможности для количественной оценки степени фиброза миокарда и анализа качества сердечной ткани . У пациентов с ДКМП степень фиброза и выраженность задержки контрастирования гадолинием являются важными прогностическими факторами, коррелирующими с риском смертности.
Основными целями медикаментозного лечения ДКМП являются купирование симптомов сердечной недостаточности с низкой фракцией выброса левого желудочка. Современная базисная медикаментозная «Квадри терапия» включает применение ингибиторов ангиотензинпревращающего фермента (иАПФ), бета-адреноблокаторов, антагонистов минералокортикоидных рецепторов (АМКР) и ингибиторов натрийзависимого котранспортера глюкозы 2-го типа (иНГЛТ-2) , . В качестве замены иАПФ у пациентов с хронической сердечной недостаточностью (ХСН) и сниженной фракцией выброса для снижения риска смерти и госпитализации используют сакубитрил/валсартан . Базисную терапию при ХСН следует назначать максимально быстро и все классы препаратов назначаются и титруются параллельно. Согласно рекомендациям Американской кардиологической ассоциации, иНГЛТ-2 показаны для применения в фармакотерапии сердечной недостаточности у пациентов со всеми категориями фракции выброса: низкой (ФВ — менее 40%), умеренно низкой (ФВ — от 41% до 49%) и сохраненной (ФВ — 50% и более) . В педиатрической практике карведилол, альфа- и бета-адреноблокатор с дополнительным вазодилатирующим эффектом, зарекомендовал себя как препарат с высоким профилем безопасности и минимальным количеством побочных эффектов. Рекомендуется применение ивабрадина, селективного ингибитора If-каналов синусового узла, у пациентов с синусовым ритмом, получающих оптимальную терапию бета-адреноблокаторами, при недостаточном контроле частоты сердечных сокращений . При наличии нарушений возбудимости и сократимости миокарда, а также симптоматических аритмий, может быть рассмотрено применение амиодарона — антиаритмического препарата III поколения, пролонгирующего потенциал действия. Рекомендовано назначение поддерживающих доз дигоксина с ХСН и ФВ <40% в сочетании с иАПФ, бета-адреноблокаторами, АМКР и диуретиками для улучшения симптомов ХСН. В педиатрической практике при прогрессирующей ХСН и нарушениях внутрижелудочковой проводимости может быть показана сердечная ресинхронизирующая терапия. В случаях тяжелого и критического течения заболевания трансплантация сердца является основным и наиболее эффективным радикальным методом лечения.
От пациента получено письменное информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
2. Клиническое наблюдение
Пациентка, 16 лет, экстренно поступила в ГБУЗ СК «КДКБ» г. Ставрополь. При поступлении предъявляла жалобы на выраженную общую слабость, адинамию, одышку смешанного характера при минимальной физической активности, чувство нехватки воздуха (затрудненное дыхание), а также сухой навязчивый кашель, усиливающийся в горизонтальном положении.
2.1. Анамнез жизни
Ребенок от первой физиологически протекавшей беременности, первых срочных родов. Масса тела при рождении — 3500 г, длина — 52 см. Ранний неонатальный период осложнился аспирацией околоплодных вод, окрашенных меконием. Требовалась искусственная вентиляция лёгких в течение 5 суток. Выписана из родильного стационара на 14-е сутки жизни в удовлетворительном состоянии. Генеалогический анамнез: по материнской линии — дедушка перенёс инсульт в 68 лет; по отцовской линии — бабушка страдала желчнокаменной болезнью. Нервно‑психическое развитие не нарушено. Перенесённые заболевания: бронхит в 2 месяца жизни; в дошкольном возрасте — частые острые респираторные вирусные инфекции; ветряная оспа. Профилактические прививки выполнены по индивидуальному календарю. Аллергологический анамнез: пищевая аллергия — на коровье молоко (реакция в виде кашля и спазма) и на цитрусовые (крапивница).
2.2. Анамнез заболевания
Пациентка ранее считалась практически здоровой, активно занималась танцами с 5-летнего возраста, хорошо переносила высокие физические нагрузки. В январе и феврале 2025 года дважды перенесла ОРВИ. Несмотря на симптомы (кашель, гипертермия до 38,5°С), она продолжала ежедневные интенсивные физические нагрузки (занятия танцами). В терапии применялись осельтамивир, бромгексин и тимьяна ползучего травы экстракт + калия бромид. В начале марта 2025 года после танцев состояние резко ухудшилось: появились боли в груди, выраженная слабость и одышка при минимальной нагрузке (подъем на 1 этаж). Обратились в поликлинику к участковому педиатру. Как отметила мать, ранее ЭхоКГ не проводилось, а у кардиолога они не наблюдались. При первичном обследовании по результатам ЭхоКГ были выявлены признаки критического снижения сократительной способности миокарда, диастолическая функция левого желудочка была снижена, фракция выброса составила 17% (рис. 4). Отмечалась выраженная дилатация левого желудочка и предсердия, а также умеренная дилатация правого предсердия и желудочка (рис. 1) В тот же день, после обращения в поликлинику и выявления критических изменений на ЭхоКГ, пациентка была экстренно госпитализирована в ГБУЗ СК «КДКБ» г. Ставрополь. На амбулаторном этапе терапия, направленная на лечение сердечной недостаточности, не проводилась.
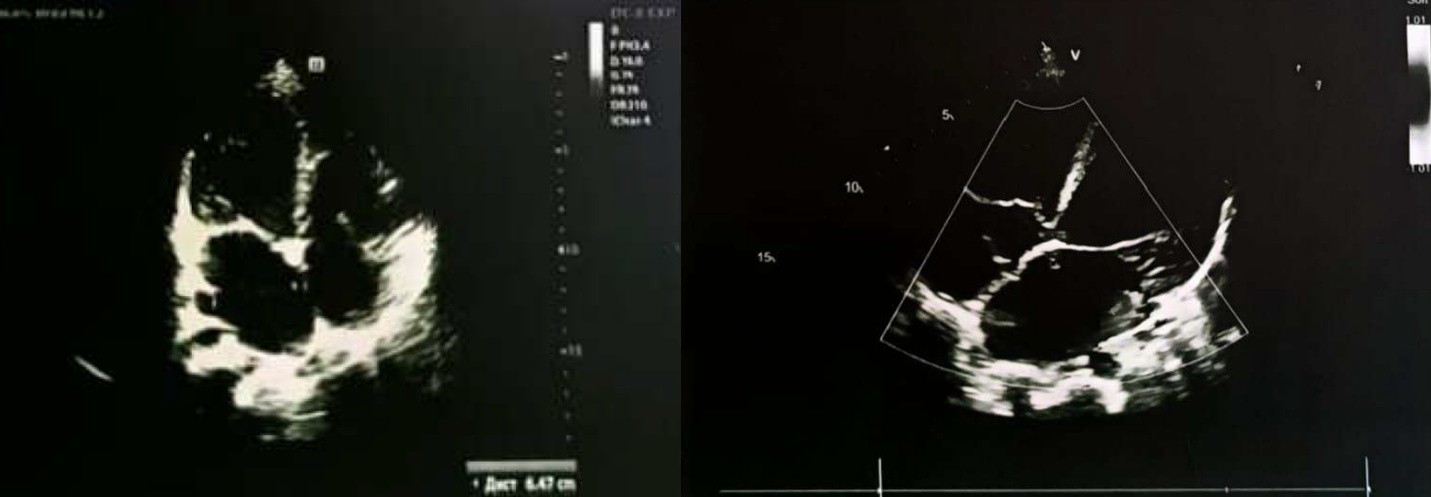
Рисунок 1 - Эхокардиографическое исследование Пациентки на догоспитальном этапе: визуализация выраженной дилатации полостей сердца
На базе ГБУЗ СК «КДКБ» г. Ставрополь было проведено комплексное лабораторно-инструментальное обследование Пациентки.
Анализ биохимических показателей выявил повышенное значение тропонина Т (20 нг/л при норме до 14 нг/л), что свидетельствует о продолжающемся цитолизе кардиомиоцитов. Особого внимания заслуживает уровень NT-proBNP, составивший 7291 пг/мл, что в 22,7 раза превышает верхнюю границу референсного диапазона (320 пг/мл) и коррелирует с клиническими признаками выраженной сердечной недостаточности.
При эхокардиографическом исследовании перикард без особенностей; перикардиальная жидкость в физиологическом объёме, сепарация листков перикарда до 2,0 мм. Отмечается выраженная дилатация полости левого желудочка и левого предсердия, умеренная дилатация правых отделов сердца. Фракция выброса ЛЖ по Teicholz составила 36% (норма — более 60%), по методу Simpson — 24% (норма — более 55%) (рис. 4). Выраженное снижение глобальной сократительной способности миокарда левого желудочка. Выявлен вторичный дефект межпредсердной перегородки диаметром 7,0 мм с перекрестным шунтом. Митральная регургитация III степени; трикуспидальная регургитация — умеренная. Отмечается повышенная трабекулярность стенок ЛЖ и диффузные изменения миокарда левого желудочка и межжелудочковой перегородки. Незначительная лёгочная гипертензия (рСДЛА — 37,0 мм/Hg).
По данным компьютерной томографии органов грудной клетки очаговых и инфильтративных изменений в паренхиме легких не выявлено. Отмечается некоторое усиление легочного рисунка за счет перибронховаскулярного компонента и наличие участков тяжистого пневмофиброза в базальных отделах левого легкого. Свободная жидкость в плевральных полостях отсутствует. Подтверждены признаки кардиомегалии: поперечник тени сердца расширен, кардиоторакальный индекс (КТИ) составил 0,59. В полости перикарда визуализируется минимальный объем выпота (плотностью от -6 до +10 HU), что соответствует транссудату. Также выявлены двусторонние плевро-диафрагмальные спайки.
Результаты суточного мониторирования ЭКГ. За период наблюдения регистрировался синусовый ритм, чередующийся с предсердным примерно равные по продолжительности отрезки времени, а также миграция водителя ритма по предсердиям. Зарегистрировано преходящее нарушение желудочковой проводимости по типу WPW-синдрома (рис. 2), полиморфная желудочковая экстрасистолия (рис. 3), в том числе ритмированная, преходящее ишемическое смещение сегмента ST на фоне брадикардии и удлинение корригированного интервала QT.
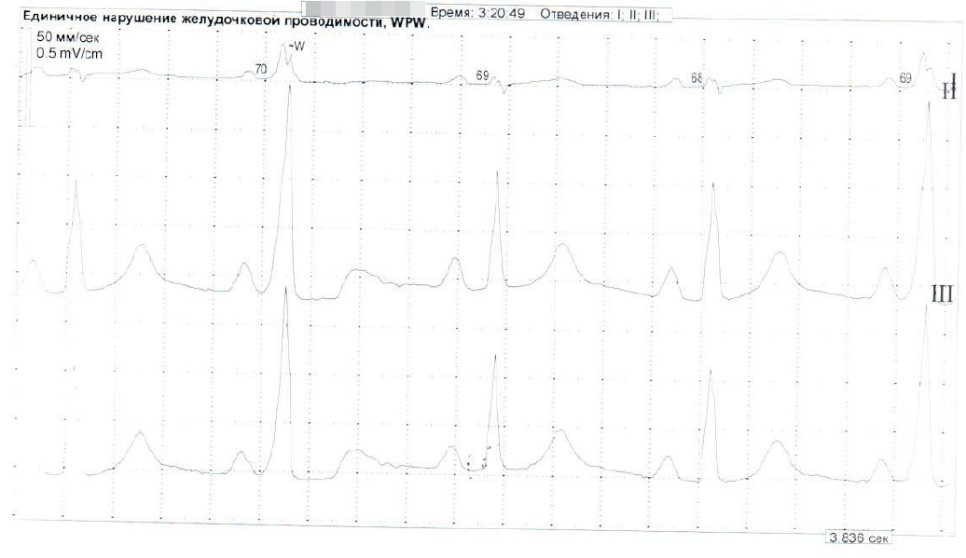
Рисунок 2 - Фрагмент суточного мониторирования ЭКГ по Холтеру
Примечание: регистрация преходящего нарушения внутрижелудочковой проводимости по типу феномена Вольфа-Паркинсона-Уайта (WPW-синдром)
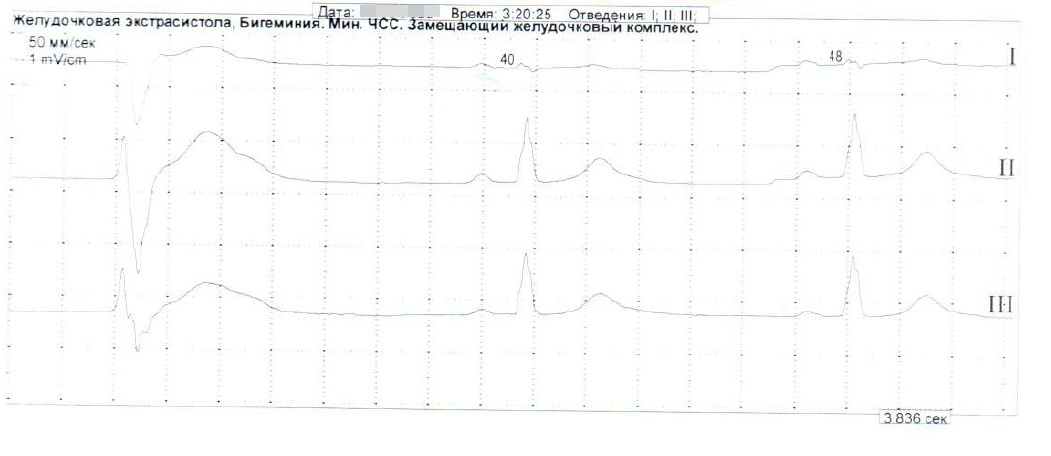
Рисунок 3 - Фрагмент суточного мониторирования ЭКГ по Холтеру
Примечание: регистрация желудочковой экстрасистолии
На фоне стартовой терапии (эналаприл по 5мг 2 раза в день, бисопролол по 1,25мг 1 раз в день утром, спиронолактон по 25мг 2 раза в день, дигоксин по 0,25мг 2 раза в день, фуросемид по 20 мг 2 раза в день внутривенно, фосфокреатин по 1г 1 раз в день внутривенно) удалось добиться временной стабилизации состояния и повышения фракции выброса по Simpson до 43% (рис. 4). Отмечалось незначительное уменьшение одышки при минимальной нагрузке, снижение выраженности отеков нижних конечностей, улучшение общего самочувствия. Объективно: ЧСС снизилась до 90-95 уд/мин, артериальное давление стабилизировалось на уровне 100/60 мм рт.ст. Документы ребенка были направлены по телемедицинской консультации в ФГАУ НМИЦ здоровья детей МЗ РФ для решения вопроса о необходимости госпитализации для дальнейшего обследования и определения тактики ведения пациента.
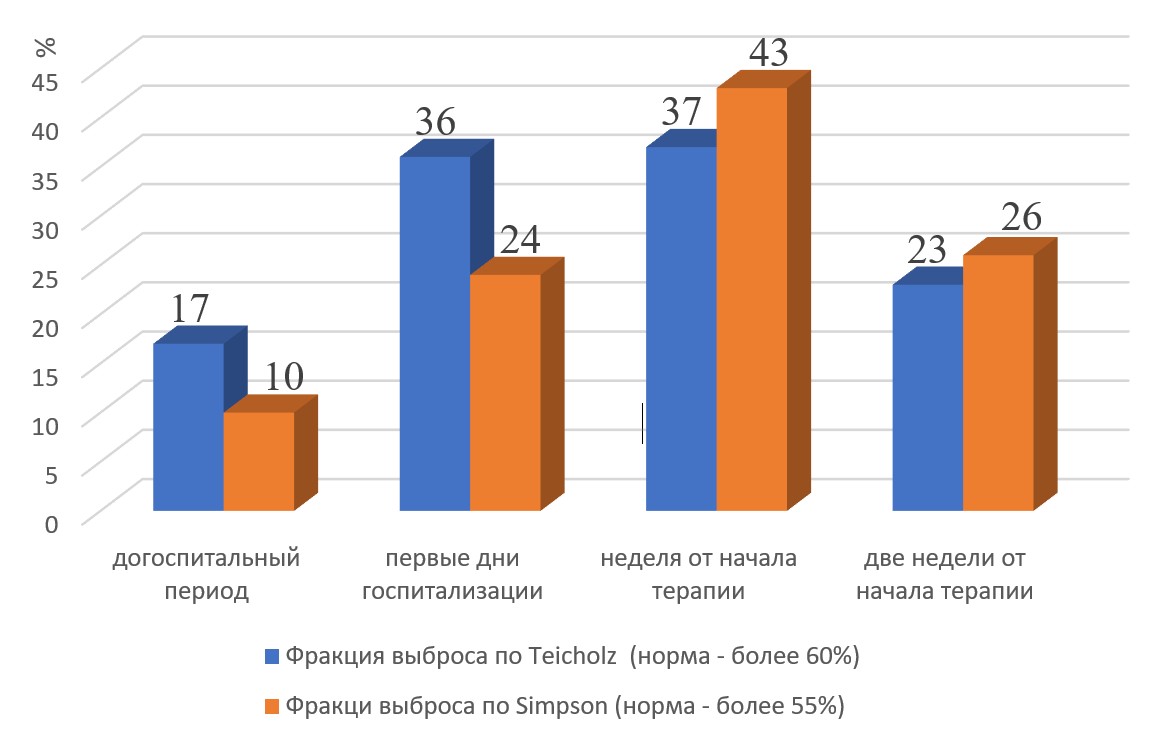
Рисунок 4 - Сравнительная динамика показателей фракции выброса левого желудочка (оценка по методам Teicholz и Simpson) на различных этапах госпитального наблюдения и проводимой терапии
1. Ограничен общий объём жидкости (энтерально и парентерально) до 800 мл в сутки.
2. Коррекция терапии сердечной недостаточности: дигоксин по 0,0625 мг в сутки, эналаприл по 2,5мг 2 раза в день, бисопролол по 0,625 мг 2 раза в день, спиронолактон по 25 мг в сутки, омепразол по 40мг в сутки, фуросемид по 40 мг 2 раза в день перорально, ацетилсалициловая кислота по 150 мг 3 раза в день, ацетазоламид 125 мг 1 раз в неделю утром вместе с фуросемидом, дапаглифлозин по 10 мг в сутки.
После коррекции терапии по рекомендации ТМК, несмотря на попытки оптимизации доз препаратов, состояние пациентки продолжало ухудшаться. Отмечалось нарастание одышки, вновь появились отеки, усилилась общая слабость. При назначении дигоксина в дозе 0,0625 мг/сутки и попытках увеличить дозу бисопролола выше 1,25 мг/сутки отмечалось резкое снижение ЧСС до 40 уд/мин утром и до 50 уд/мин в течение дня с выраженными эпизодами бигеминии. Дигоксин был отменен. Увеличение дозы эналаприла выше 5 мг/сутки приводило к выраженной гипотонии до 70/40 мм рт. ст. На фоне проводимой терапии наблюдалась отрицательная динамика: снижение фракции выброса по Simpson до 26%, повышение NT-proBNP до 8451 пг/мл, что свидетельствовало о прогрессировании систолической дисфункции левого желудочка и нарастания сердечной недостаточности.
Учитывая возраст, тяжесть состояния и характер заболевания документы ребенка были направлены на обсуждение по ТМК в НМИЦ трансплантологии и искусственных органов имени академика В.И. Шумакова для решения вопроса о необходимости хирургического лечения. Прогрессирующее ухудшение состояния пациентки, отсутствие адекватного ответа на медикаментозную терапию, критическое снижение фракции выброса левого желудочка и нарастание симптомов сердечной недостаточности, было принято решение о необходимости хирургического лечения — ортотопической трансплантации сердца. Показаниями к трансплантации сердца послужили: терминальная стадия дилатационной кардиомиопатии, сердечная недостаточность, рефрактерная к консервативной терапии, высокий риск внезапной сердечной смерти и отсутствие других эффективных методов лечения.
В мае 2025 года Пациентке была выполнена ортотопическая трансплантация сердца по бикавальной методике. Ранний послеоперационный период протекал без грубых хирургических осложнений. При контрольном осмотре в июле 2025 года (через два месяца после трансплантации) наблюдалась значительная положительная динамика. Симптомы сердечной недостаточности, такие как одышка в покое и при минимальной нагрузке, ортопноэ, периферические отеки и генерализованная слабость, в большей степени нивелировались. Пациентка стала активной, отмечалось значительное улучшение толерантности к физическим нагрузкам. Объективно: общее состояние удовлетворительное, кожные покровы чистые, обычной окраски, акроцианоз отсутствовал. При аускультации тоны сердца ясные, ритмичные, шумы не выслушивались. Частота сердечных сокращений в пределах 80–90 уд/мин, артериальное давление стабильное 110/70 мм рт.ст. Размеры печени в норме, отеков нижних конечностей не наблюдалось. Параметры ЭхоКГ соответствовали норме, фракция выброса левого желудочка составляла 75%, полости сердца не расширены. Пациентка находится под динамическим наблюдением, получает иммуносупрессивную терапию, качество жизни значительно улучшилось.
3. Заключение
Представленный клинический случай 16-летней пациентки с дилатационной кардиомиопатией (ДКМП) демонстрирует высокую вариабельность и агрессивность течения данного заболевания в педиатрической популяции. Несмотря на применение современных стандартов медикаментозной терапии сердечной недостаточности с низкой фракцией выброса, включая ингибиторы ангиотензинпревращающего фермента, бета-адреноблокаторы, антагонисты минералокортикоидных рецепторов и ингибиторы натрийзависимого котранспортера глюкозы 2-го типа, у пациентки отмечалась прогрессирующая дисфункция миокарда и снижение фракции выброса левого желудочка. Несмотря на достигнутую временную стабилизацию состояния и частичное восстановление насосной функции миокарда на фоне медикаментозной терапии, дальнейшее прогрессирование заболевания и отсутствие перспектив для полного восстановления функции левого желудочка обусловили необходимость радикального лечения — ортотопической трансплантации сердца.
Данное клиническое наблюдение подчеркивает важность раннего выявления пациентов с ДКМП и тщательной оценки степени тяжести заболевания и прогноза, а также применения комплексного подхода к лечению сердечной недостаточности, с индивидуальным подбором препаратов и титрованием доз.
Кроме того, данный случай акцентирует внимание на необходимости широкого просвещения населения, особенно подростков и их родителей, о значимости соблюдения постельного режима и ограничения физических нагрузок во время острых инфекционных заболеваний для предотвращения развития и прогрессирования постинфекционных поражений миокарда, способных привести к дилатационной кардиомиопатии.
