КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА С УЗЛОВЫМ АТОМОМ АЗОТА — НОВЫЕ ПЕРСПЕКТИВНЫЕ ПРОТИВООПУХОЛЕВЫЕ АГЕНТЫ
КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА С УЗЛОВЫМ АТОМОМ АЗОТА — НОВЫЕ ПЕРСПЕКТИВНЫЕ ПРОТИВООПУХОЛЕВЫЕ АГЕНТЫ
Аннотация
Осуществлен синтез ряда 24 моно-, ди-, три- и тетразамещенных производных конденсированного бензимидазола с узловым атомом азота. Изучена цитотоксичность полученных веществ в отношении двух линий клеток опухолевого происхождения — аденокарциномы легкого человека (A549) и аденокарциномы молочной железы (MCF-7). Для сравнения селективности действия полученных конденсированных производных бензимидазола на нормальные и опухолевые клетки также использовалась линия клеток нормального происхождения из эмбриональной почки человека (HEK-293). Все синтезированные соединения обладали более сильной цитотоксической активностью в отношении линий раковых клеток по сравнению с клетками нормального происхождения.
1. Введение
Рак — это гетерогенные и многофакторные заболевания, при которых серия геномных/молекулярных изменений вызывает неконтролируемый рост и пролиферацию клеток, вызывая быстрое увеличение массы тканей в пораженных частях тела. Раковые клетки растут, используя кислород и питательные вещества организма, лишая другие клетки регулярных питательных веществ и факторов роста , . Эти клетки могут изменять микросреду в свою пользу, обманывать иммунную систему организма и использовать физиологию других клеток для обеспечения своей жизнедеятельности , , , . Для обозначения этой категории заболеваний используются также термины «злокачественные опухоли» и «новообразования».
Рак — вторая по значимости причина смерти в мире, на долю которой приходится каждая шестая смерть. Рак лёгких, предстательной железы, толстой кишки, желудка и печени — наиболее распространённые виды рака у мужчин, в то время как рак молочной железы, толстой кишки, лёгких, шейки матки и щитовидной железы — наиболее распространённые у женщин.
В современной медицине существует много вариантов лечения различных онкологических заболеваний в зависимости от стадий злокачественного процесса. Важнейшее значение среди них, несмотря на имеющиеся недостатки, имеет химиотерапия , , , . Химиотерапия основана на применении специальных медикаментов — цитостатиков, способных воздействовать на опухолевые клетки и препятствовать их росту и размножению , .
Перспективными соединениями для создания новых химиотерапевтических препаратов являются производные бензимидазола. Так, в работе было показано, что исследуемый потенциальный лекарственный агент на основе бензимидазола снижал жизнеспособность клеточной линии аденокарциномы молочной железы и ингибировал образование колоний MCF-7 (аденокарциномы), что обусловлено его способностью вызывать окислительный стресс в клетках. На клеточной линии гистиоцитарной лимфомы человека U937 в исследовании был показан аналогичный механизм цитотоксического действия другого производного бензимидазола. Прооксидантная активность была обнаружена ещё для некоторых бензимидазолов, приводящих в клетках глиомы к значительному увеличению продукции активных форм кислорода (АФК) и потере мембранного потенциала митохондрий по сравнению с контролем, что, в свою очередь, сопровождалось повышением уровня цитозольного цитохрома С и индукцией митохондриального пути апоптоза . В работе была синтезирована серия низкомолекулярных замещенных 1-бензил-1Н-бензимидазолов и исследована их противоопухолевая активность. Гибель опухолевых клеток была вызвана дозозависимым увеличением уровня АФК.
Поэтому в данном исследовании был получен ряд конденсированных производных с узловым атомом азота и изучена их цитотоксичность в отношении линий клеток опухолевого происхождения.
2. Методы и принципы исследования
Синтез и функционализацию конденсированных производных бензимидазола проводили по следующей схеме:
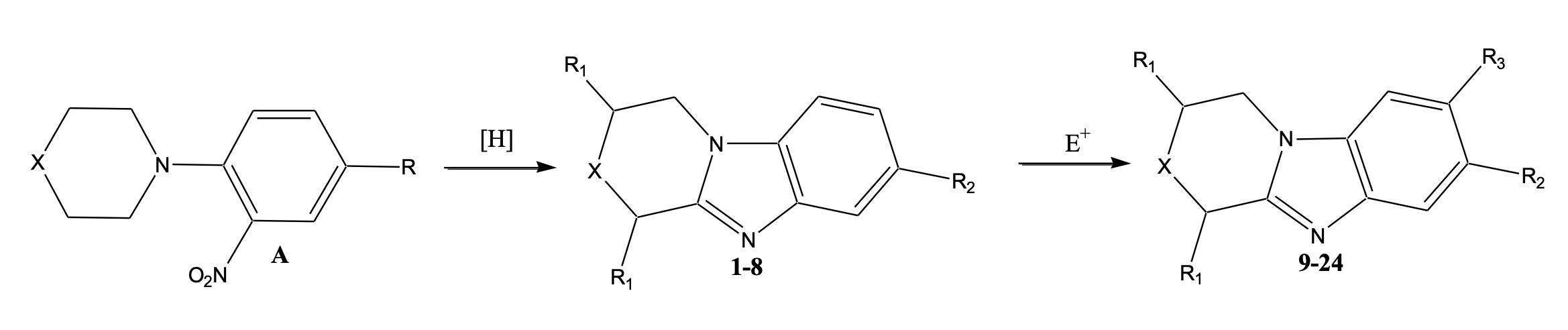
Рисунок 1 - Схема синтеза конденсированных производных бензимидазола
Структура всех полученных 24 соединений была определена с помощью 1Н, 13С ЯМР спектроскопии и масс-спектрометрии высокого разрешения. Отнесение сигналов протонов сделано на основании данных 2D 1H-1H NOESY спектроскопии. Методики синтеза и описание спектров веществ приведены в наших статьях ,
, .Для изучения цитотоксичности (степень, с которой вещество деструктивно действует на отдельные клетки) синтезированных производных бензимидазола 1–24 использовали клетки аденокарциномы легкого человека A549 и карциномы молочной железы MCF-7. Для оценки селективности действия данных соединений на клетки опухолевого и нормального происхождения в исследовании также применялись нормальные клетки из эмбриональной почки человека HEK-293.
Для определения цитотоксического действия синтезированных молекул был использован МТТ-тест . В основе данного метода лежит реакция восстановления соли тетразолия (3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-тетразолиум бромид) митохондриальными дегидрогеназами живых клеток до нерастворимых в воде кристаллов формазана.
В качестве показателей эффективности были определены величины IC50 цитотоксического эффекта, представляющие собой концентрации соединения, приводящие к гибели 50% клеток в пробе. Чем меньшее значение IC50 имели исследуемые соединения, тем выше была их цитотоксичность.
Подробные методики проведения цитотоксических исследований приведены в работе .
Статистическую обработку проводили методами описательной и математической статистики с применением пакета прикладных программ Statistica 10.0 (StatSoftInc., USA) и GraphPad Prism 5.0 (GraphPad Software, США). Количественные данные представлены в виде среднего значения (Mean) и стандартного отклонения (SD).
3. Основные результаты
В таблице 1 представлены значения IC50 конденсированных производных бензимидазола (рис. 2) в отношении клеток нормального и опухолевого происхождения.
Таблица 1 - Значения IC50 (мкм) цитотоксического эффекта конденсированных соединений ряда бензимидазола
№ | А549 | МСF-7 | Hek-293 |
1 | 76,86 ± 0,19 | 73,90 ± 0,31 | ≥100 |
2 | 73,38 ± 0,21 | 62,02 ± 0,19 | ≥100 |
3 | 68,72 ± 0,21 | 57,14 ± 0,63 | 91,37 ± 0,52 |
4 | 86,81 ± 0,64 | 83,35 ± 0,32 | ≥100 |
5 | 73,09 ± 1,80 | 69,32 ± 1,51 | ≥100 |
6 | 59,09 ± 0,79 | 57,16 ± 0,56 | 89,81 ± 0,64 |
7 | 46,78 ± 0,63 | 44,24 ± 0,43 | 86,09 ± 0,33 |
8 | 74,09 ± 0,64 | 69,41 ± 0,32 | ≥100 |
9 | 69,21 ± 0,79 | 71,32 ± 0,94 | ≥100 |
10 | 57,23 ± 0,84 | 56,32 ± 0,93 | 92,83 ± 0,42 |
11 | 47,11 ± 0,72 | 41,22 ± 0,54 | 89,59 ± 0,34 |
12 | 71,68 ± 0,75 | 68,71 ± 0,42 | ≥100 |
13 | 73,52 ± 0,38 | 67,22 ± 0,61 | 95,58 ± 0,41 |
14 | 56,39 ± 0,27 | 54,82 ± 0,43 | 91,31 ± 0,76 |
15 | 48,24 ± 0,64 | 43,36 ± 0,51 | 89,27 ± 0,58 |
16 | 69,83 ± 0,51 | 66,42 ± 0,51 | ≥100 |
17 | 67,24 ± 0,24 | 65,89 ± 0,38 | ≥100 |
18 | 56,98 ± 0,63 | 53,72 ± 0,47 | 92,78 ± 0,58 |
19 | 47,59 ± 0,31 | 39,81 ± 0,28 | 84,33 ± 0,72 |
20 | 75,11 ± 0,32 | 67,98 ± 0,37 | ≥100 |
21 | 66,24 ± 0,36 | 61,53 ± 0,44 | 89,34 ± 0,61 |
22 | 41,37 ± 0,49 | 26,33 ± 0,59 | 84,91 ± 0,32 |
23 | 12,41 ± 0,28 | 8,33 ± 0,85 | 81,37 ± 0,42 |
24 | 67,29 ± 0,42 | 60,73 ± 0,87 | ≥100 |
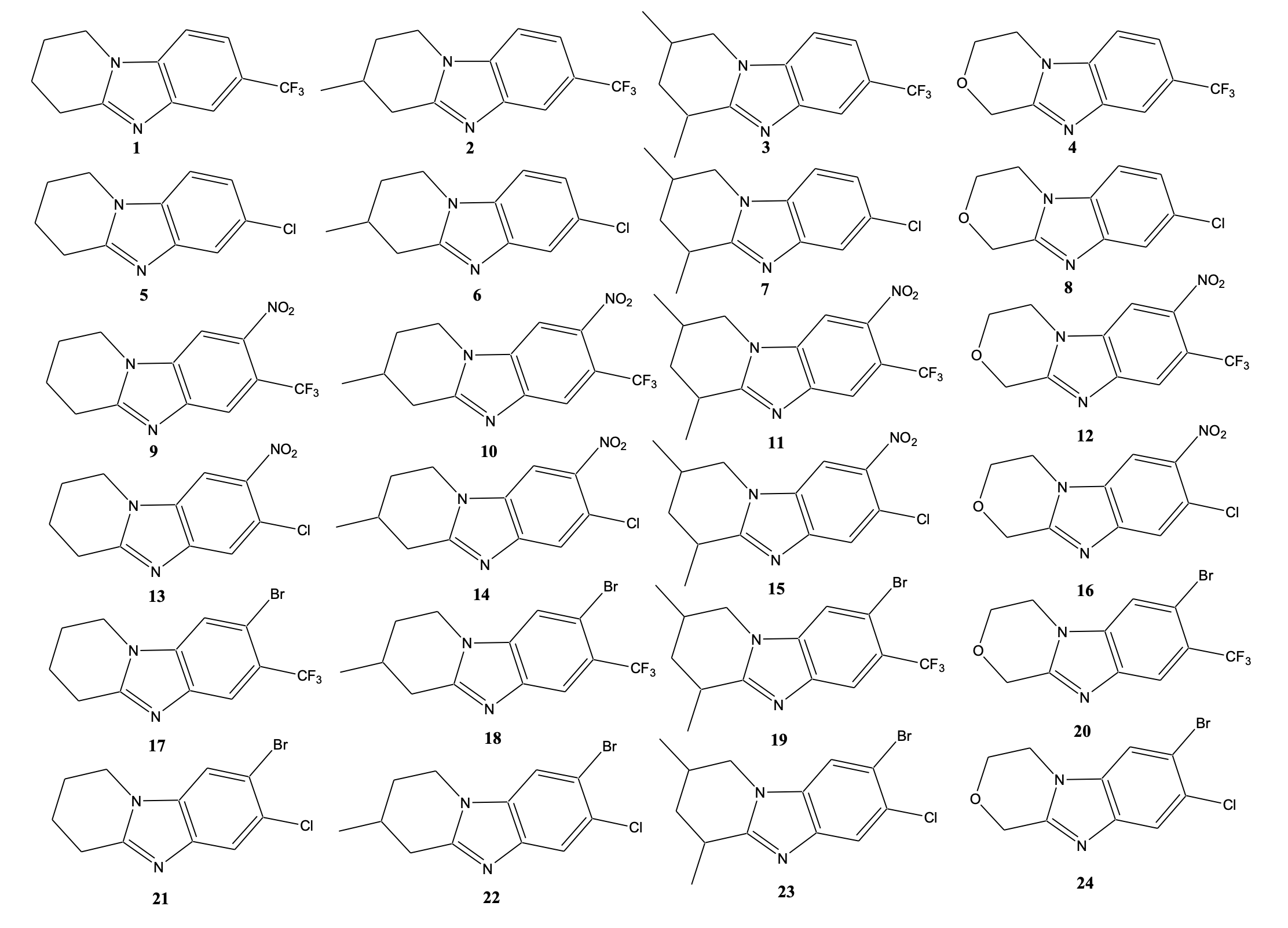
Рисунок 2 - Структуры исследуемых конденсированных производных бензимидазола
4. Обсуждение
Анализ данных таблицы позволил сделать следующие выводы:
– все полученные производные бензимидазола 1–24 проявляли цитотоксичность в отношении линий клеток опухолевого происхождения;
– производные бензимидазола 9–24, содержащие два заместителя в бензольном кольце, имели больший цитотоксический эффект, чем монозамещенные соединения 1–8, из которых они были получены;
– структура аннелированного к имидазолу предельного гетероцикла (Х=О или Х=СН2) не оказывала сильного влияния на цитотоксичность исследуемых веществ;
– в большей степени цитотоксический эффект зависел от природы заместителей в конденсированном бензимидазоле. Наличие двух атомов галогенов (структуры 21–24), непосредственно связанных с бензольным кольцом, способствовало значительному увеличению цитотоксичности;
– в еще большей степени на цитотоксичность веществ влияло наличие метильных (СН3) групп в предельном гетероцикле. Известно, что алкильные заместители увеличивают липофильность молекулы, что облегчает ее проникновение в клетку через липидную мембрану;
– из двух использованных линий клеток опухолевого происхождения клетки карциномы молочной железы МСF-7 были менее устойчивы к действию синтезированных гетероциклов;
– по отношению к клеткам нормального происхождения все исследуемые соединения проявляли значительно меньший цитотоксический эффект по сравнению с раковыми клетками;
– из всех исследованных соединений наибольший интерес вызывали бензимидазолы 22 и 23, содержащие алкильные заместители в предельном гетероцикле и два атома галогена в бензольном кольце. Данные соединения были наиболее цитотоксичны в отношении линий клеток МСF-7, при этом не оказывая существенного цитотоксического эффекта в отношении нормальных клеток. Цитотоксичность соединения 23 была почти в 10 раз больше для опухолевых клеток по сравнению с нормальными.
5. Заключение
Таким образом, синтезированные конденсированные производные бензимидазола обладали цитотоксичностью в отношении клеточных линий опухолевого происхождения — аденокарциномы легкого (A549) и аденокарциномы молочной железы (MCF-7). При этом они были значительно менее токсичны для клеток нормального происхождения. Эти данные свидетельствовали о перспективности поиска селективных цитотоксических агентов среди конденсированных производных бензимидазола.
