In-silico исследование профиля биологической активности, путей химической модификации и фармацевтического воздействия йодантипирина
In-silico исследование профиля биологической активности, путей химической модификации и фармацевтического воздействия йодантипирина
Аннотация
Разработана эффективная методика выделения йодантипирина. Доказательством структуры и чистоты служили: температура плавления 161,2–164,6°C, характерные ИК-полосы поглощения (C=O при 1650 см-1, C-I при 607 см-1) и УФ-спектр с максимумами при 224 нм и 267 нм (ε = 1,83⋅103 л·моль-1·см-1). In silico анализ выявил высокую вероятность противовирусной (Pa = 0,787) и противовоспалительной (Pa = 0,744) активности исходной молекулы. Среди синтезированных in silico аналогов наилучшие результаты показали производные с заменой бензольного кольца: пиридиновый аналог (1e) проявил жаропонижающую активность (Pa = 0,860), а тиофеновый аналог (1f) — еще более высокую антипиретическую активность (Pa = 0,879) при полном отсутствии прогнозируемых серьезных побочных эффектов.
1. Введение
Йодантипирин (4-йод-1,5-диметил-2-фенил-1,2-дигидро-3H-пиразол-3-он) — препарат, широко применяемый в России для профилактики и лечения вирусного клещевого энцефалита (см. рис. 1) .
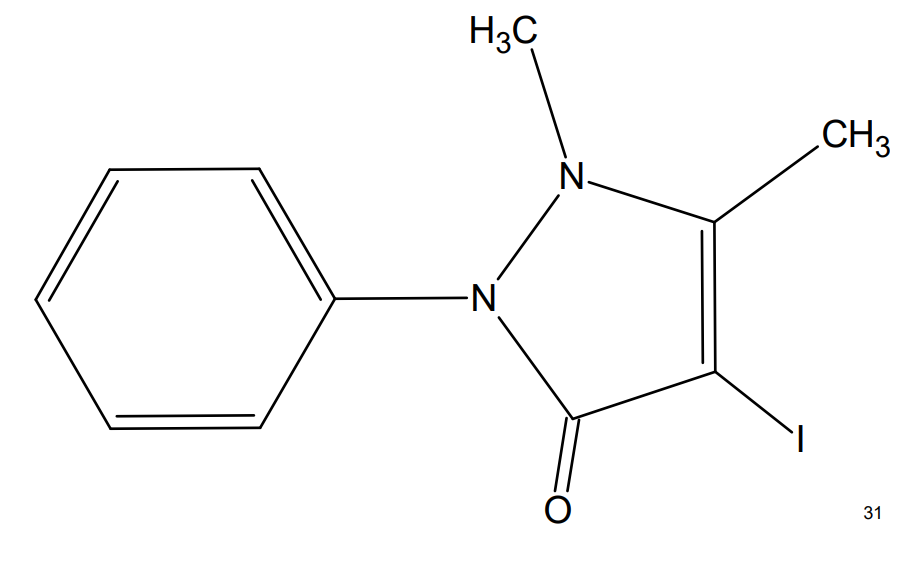
Рисунок 1 - Структура 4-йод-1,5-диметил-2-фенил-1,2-дигидро-3H-пиразол-3-она
Несмотря на высокую безопасность данного лекарственного препарата , отмечаемую многими исследователями, существуют сомнения и пробелы в области селективности действия данного препарата : конкретные молекулярные мишени для данного препарата практически не описаны в современной литературе. Разработка методики выделения действующего вещества йодантипирина из лекарственной матрицы необходима для проведения дальнейших исследований препарата: способов идентификации и распознавания фальсифицированных лекарств , высокие требования к чистоте также важны при проведении in vitro тестов на клеточных культурах и при определении полумаксимальных эффективных концентраций , при применении хроматографических методов анализа (ВЭЖХ) и т.д.
Таким образом, целью данного исследования является разработка методики выделения и идентификации йодантипирина и оценка перспектив дальнейшей модификации действующего вещества, присутствующего в рассматриваемом лекарственном препарате.
2. Методы и принципы исследования
Спектры выделенного действующего вещества записывали на спектрофотометре ПЭ 5400 УФ компании «ЭКРОСХИМ» и на ИК-спектрометре Spectrum 65 (Perkin Elmer) методом нарушенного полного внутреннего отражения, температура плавления измерена с помощью прибора Stuart SMP10. Оценка вероятности биологической активности проводилась с помощью программного комплекса PASS Online .
В работе использован лекарственный препарат Йодантипирин (АО «ТАТХИМФАРМПРЕПАРАТЫ») следующего состава: йодофеназон — 100,0 мг, крахмал картофельный — 26,0 мг, декстрозы моногидрат — 29,0 мг, повидон К17 — 5,0 мг, стеариновая кислота — 1,0 мг.
3. Методика выделения действующего вещества йодантипирина из лекарственной матрицы
3 таблетки йодантипирина по 100 мг растирали в фарфоровой ступке до порошкообразного состояния. Полученный порошок переместили в химический стакан объемом 25 мл и залили 15 мл этилового спирта 96%, затем перемешивали на магнитной мешалке в течение 5 минут до образования гомогенной массы, которую отфильтровывали. Фильтрат медленно упаривали на плитке при температуре 50-60 оС, не допуская перегрева. Сухой остаток промыли этилацетатом от остаточных количеств поливинилпирролидона и стеариновой кислоты, после чего декантировали. Выделенное действующее вещество поставили сушиться в шкаф при температуре 50 оС на 1 час. Выход составил 68% (масса сухого остатка — 204 мг).
4. Основная часть
C целью идентификации и подтверждения выделения 4-йод-1,5-диметил-2-фенил-1,2-дигидро-3H-пиразол-3-она измерен диапазон температур плавления, который составил 161,2-164,6 оС (Т=3,4 оС), что соответствует данным из ГФ РФ .
Измерен электронный спектр (см. рис. 2) выделенного действующего вещества (растворитель – дистиллированная вода): обнаружены 2 типа π→π* переходов бензольного (λmax1=224 нм) и пиразолонового кольца (λmax2=267 нм). Молярный коэффициент экстинкции соединения составил ε = 1,83⋅103 л·моль-1·см-1.
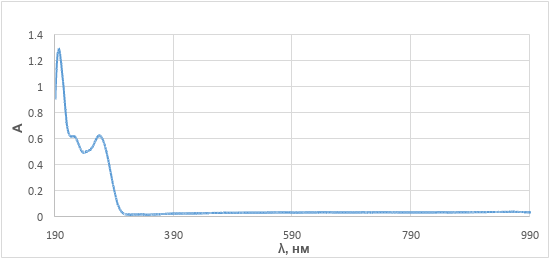
Рисунок 2 - Электронный спектр йодантипирина
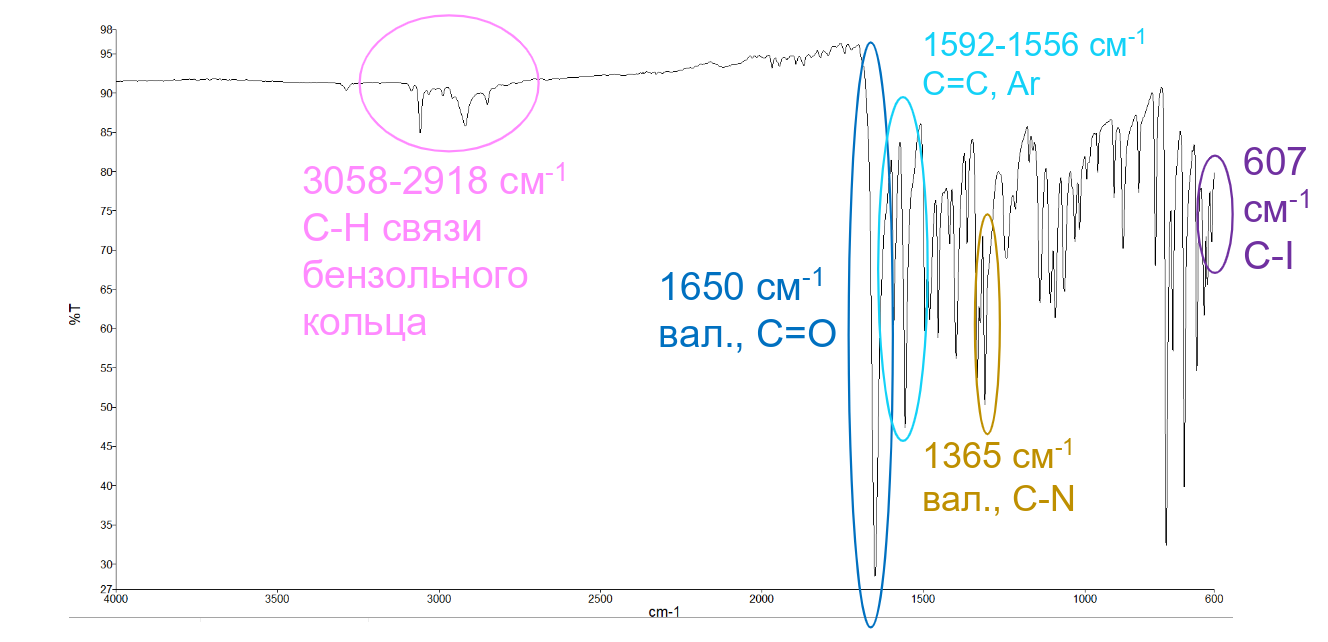
Рисунок 3 - ИК-спектр выделенного действующего вещества йодантипирина
Таблица 1 - Полосы поглощения, присутствующие на ИК-спектре йодантипирина
Волновое число, см-1 | Интенсивность, %T | Группировки атомов |
3058,01 | 84,97 | C-H, валентное |
2918,40 | 85,82 | CH3, симметричное валентное |
1650,12 | 28,50 | C=O валентное |
1592,20 | 60,50 | С=C, C=N; валентное |
1556,94 | 47,38 | C=N, валентное |
1494,66 | 58,37 | C=C, валентное |
1481,36 | 61,17 | C=C, валентное |
1454,89 | 58,82 | -CH3, асимметричное, деформационное |
1419,11 | 70,80 | деформационное, –CH3 |
1365,17 | 70,86 | С-N, валентное |
1242,61 | 68,99 | С-O, валентное |
1215,21 | 75,25 | С-N, валентное |
1106,82 | 63,28 | N-N, валентное |
1063,41 | 64,73 | -CH3, качательное |
1030,88 | 71,09 | -CH3, качательное |
909,85 | 76,68 | Ароматическое C-H, внеплоскостное |
727,61 | 57,14 | Ароматическое C-C-C, внеплоскостное |
607,22 | 71,11 | C-I, валентное |
В программном комплексе PASS Online изучена вероятность биологической активности и нежелательных побочных эффектов для йодантипирина (см. табл. 2). Исходное лекарственное вещество (см. рис. 1) имеет высокую противовирусную (0,787), противовоспалительную (0,744) активность и может применяться в качестве обезболивающего (0,724). С Ра>0,7 присутствует лишь 2 типа побочных эффектов: синдром Свита и подергивание, что подтверждает опытные данные о безопасности данного препарата.
Таблица 2 - Вероятность биологического воздействия йодантипирина
Pa | Pi | Активность |
0,787 | 0,003 | Противовирусный (пикорнавирус) |
0,744 | 0,011 | Противовоспалительное средство |
0,724 | 0,008 | Обезболивающее |
0,863 | 0,009 | Нейтрофильный дерматоз (синдром Свита) |
0,720 | 0,088 | Подергивание |
Был проведен ряд биоизостерических замен для препарата. Последовательная замена функциональных групп в сравнении с исходным препаратом отражена на рис. 4.
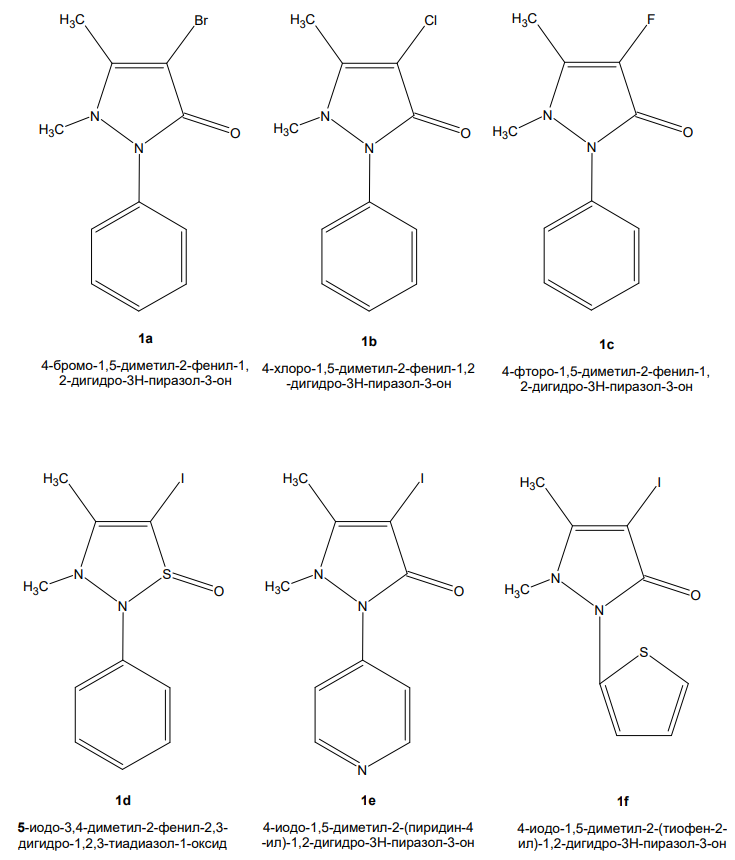
Рисунок 4 - Структуры — производные йодантипирина, полученные путем биоизостерических замен
Таблица 3 - Вероятность биологического воздействия соединения 1а
Pa | Pi | Активность |
0,790 | 0,005 | Обезболивающее |
0,781 | 0,004 | Антигипоксическое |
0,771 | 0,005 | Неопиоидный анальгетик |
0,706 | 0,015 | Противовоспалительное средство |
0,863 | 0,009 | Нейтрофильный дерматоз (синдром Свита) |
Замена галогена на хлор в 4-м положении (структура 1b; см. табл. 4) понизила противовирусное воздействие на 10,54%, увеличила токсичность (4 побочных эффекта вместо 2), в том числе серьезные (полиорганная недостаточность и др.); возросла вероятность возникновения 2-х исходных (синдром Свита и подергивание).
Таблица 4 - Вероятность биологического воздействия соединения 1b
Pa | Pi | Активность |
0,704 | 0,005 | Противовирусный (пикорнавирус) |
0,702 | 0,008 | Антигипоксическое |
0,907 | 0,004 | Нейтрофильный дерматоз (синдром Свита) |
0,790 | 0,047 | Подергивание |
0,742 | 0,021 | Полиорганная недостаточность |
0,733 | 0,017 | Желудочно-кишечное кровотечение |
Замена на фтор (структура 1c; см. табл. 5) сопровождалась ростом на 11,83% противовоспалительного воздействия, на 14,75% — обезболивающего; появились как антигипоксический эффект (0,747), так и возможность лечения ревматоидного артрита (0,721).
Таблица 5 - Вероятность биологического воздействия соединения 1с
Pa | Pi | Активность |
0,832 | 0,005 | Противовоспалительное средство |
0,831 | 0,005 | Обезболивающее |
0,815 | 0,005 | Анальгетик, неопиоидный |
0,747 | 0,005 | Антигипоксическое |
0,721 | 0,004 | Лечение ревматоидного артрита |
0,897 | 0,005 | Нейтрофильный дерматоз (синдром Свита) |
0,803 | 0,006 | Ингибитор тромбоцитопоэза |
0,783 | 0,009 | Желудочно-кишечное кровотечение |
0,743 | 0,028 | Фибрилляция предсердий |
0,756 | 0,067 | Подергивание |
Таким образом, в ряду галогенов токсичность (оцениваемая по вероятности проявления синдрома Свита, что также соотносилось с количеством, ущербом для здоровья и вероятностью проявления остальных побочных эффектов) возрастала в ряду: -I ≈ -Br < -F < -Cl.
Замена карбонильной группы пиразолонового кольца на биоизостерическую сульфоксидную (структура 1d, см. табл. 6) группу привела к исчезновению всех видов фармацевтического воздействия при Ра>0,7, в то время как побочные эффекты оставались (вероятность возникновения существенно не изменилась; см. табл. 5).
Таблица 6 - Вероятность биологического воздействия соединения 1d
Pa | Pi | Активность |
0,859 | 0,010 | Нейтрофильный дерматоз (синдром Свита) |
0,712 | 0,028 | Полиорганная недостаточность |
0,740 | 0,076 | Подергивание |
Наиболее перспективными оказались замены фенильного радикала на пиридиновое кольцо (1е) и тиофен (1f) — см. табл. 7 и 8 соответственно. В первом случае вероятность возникновения синдрома Свита в сравнении с исходной молекулой уменьшилась, но крайне незначительно (на 0,46%). Появилось жаропонижающее действие (0,860), но противовирусное понизилось на 8,25%.
Таблица 7 - Вероятность биологического воздействия соединения 1е
Pa | Pi | Активность |
0,860 | 0,003 | Жаропонижающее |
0,722 | 0,005 | Противовирусный (пикорнавирус) |
0,736 | 0,023 | Изменение цвета ногтей |
0,748 | 0,037 | Нейтрофильный дерматоз (синдром Свита) |
Во втором — побочных эффектов при Ра>0,7 вообще не наблюдается, при этом жаропонижающее действие еще выше, чем у предыдущего соединения (0,879 против 0,860), что делает указанные молекулы перспективными для синтеза в качестве потенциальных препаратов-антипиретиков.
Таблица 8 - Вероятность биологического воздействия соединения 1f
Pa | Pi | Активность |
0,879 | 0,003 | Жаропонижающее |
0,740 | 0,054 | Убихинол-ингибитор цитохром-с-редуктазы |
Более того, полученные в ходе анализа закономерности «структура-свойство» данные можно интерпретировать следующим образом: предполагаемым фармакофором в йодантипирине является пиразолоновое кольцо, которое оказывает противовирусное и противовоспалительное действие. Данный тезис также подтверждает то, что при любой попытке замены карбонильной группы, являющейся неотъемлемой части пиразолонового кольца, терапевтического эффекта при Ра>0,7 не наблюдалось.
5. Заключение
Разработана и апробирована методика выделения йодантипирина из лекарственной формы, подтвержденная данными, полученными с помощью физико-химических методов анализа. Ключевыми доказательствами чистоты и идентичности вещества являются: УФ-спектр с λmax1=224 нм, λmax2=267 нм, а также ИК-спектр, показавший наличие всех характерных группировок, включая карбонильную (1650 см-1) и связь C-I (607 см-1). Производное 1f (замена фенила на тиофен) продемонстрировало наивысшую жаропонижающую активность (Pa = 0,879) и полное отсутствие прогнозируемых побочных эффектов с вероятностью Pa > 0,7, что делает его самым перспективным кандидатом. Производное 1c (замена йода на фтор) показало значительное усиление противовоспалительной (Pa = 0,832, +11,83%) и обезболивающей (Pa = 0,831, +14,75%) активности по сравнению с исходной молекулой. Таким образом, работа предоставляет экспериментальную основу для целенаправленного синтеза новых производных йодантипирина с улучшенными физиологическими свойствами.
